Дисметаболическая нефропатия у детей что это такое: Дисметаболическая нефропатия у детей: признаки, лечение
Дисметаболическая нефропатия у детей: симптомы и лечение
Дисметаболическая нефропатия у детей – распространенное заболевание почек, которое диагностируется у каждого третьего ребенка. В структуре органа начинают происходить изменения, его функции ухудшаются, в результате чего появляются болезненные ощущения, отечность и повышается риск возникновения нефрита, отложения почечных камней.
Виды патологий и их проявления
 В зависимости от причин, вызвавших болезнь, дисметаболические нефропатии делятся на первичные и вторичные. Первичные развиваются вследствие нарушений функциональности почек, мочекаменной болезни и ряда других хронических процессов в организме. Значительную роль при этом играет наследственность.
В зависимости от причин, вызвавших болезнь, дисметаболические нефропатии делятся на первичные и вторичные. Первичные развиваются вследствие нарушений функциональности почек, мочекаменной болезни и ряда других хронических процессов в организме. Значительную роль при этом играет наследственность.
Вторичные виды дисметаболических нефропатий развиваются на фоне нарушений обмена веществ в организме. Такое нередко происходит из-за нерационального питания или продолжительного приема определенных медицинских препаратов. Причем чаще всего основной причиной дисметаболической нефропатии становится нарушение кальциевого метаболизма. По составу солей, которые выявляются в моче в ходе диагностики, различают следующие виды нефропатии:
- оксалатно-кальциевая;
- фосфатная;
- уратная;
- цистиновая;
- смешанная.
В 85-90% всех случаев у больных фиксируется именно оксалатно-кальциевая форма заболевания.
Причины возникновения
Обменная форма нефропатии возникает при воздействии целого комплекса факторов. К примеру, первичная форма заболевания нередко развивается по причине нарушений обменных процессов у родителей ребенка. Накопленные генетические мутации провоцируют ухудшение метаболизма, что затрудняет предстоящее лечение.
Среди общих причин, приводящих к дисметаболической нефропатии, выделяют:
- интоксикацию;
- чрезмерные физические нагрузки;
- продолжительное применение медикаментов;
- монодефицитные диеты.
Вторичная обменная нефропатия развивается по причине передозировки определенными веществами или из-за замедления их вывода из организма. В норме моча должна содержать растворенные соли. Однако при воздействии ряда причин они кристаллизуются и выпадают в осадок.
К таким факторам относят:
- жаркий и сухой климат;
- недостаток витаминов;
- жесткая вода;
- профицит протеинов, щавелевой кислоты, пуринов;
- алкоголизм;
- лечение диуретиками, цитостатиками и сульфаниламидами;
- частые походы в сауну.
Выделяют также внутренние факторы:
- врожденные нарушения почек и мочеточников;
- сбои в гормональном фоне;
- инфекции мочевыводящих путей;
- продолжительное соблюдение постельного режима;
- иммобилизация;
- наследственные нарушения метаболизма.

соли в моче
Данные факторы приводят к формированию солей и их скоплению в почечных тканях. В результате запускается воспалительный процесс. Местное отложение кристаллов провоцирует появление камней в почках.
Нередко возникновение дисметаболической нефропатии у детей, страдающих нервно-артрическим диатезом. На развитие болезни могут повлиять осложнения во время беременности матери, в том числе токсикоз на поздних сроках, гипоксия плода.
Кроме того, выделяют множество частных причин дисметаболической нефропатии, которые связаны непосредственно с видом заболевания. Оксалатная форма обуславливается нарушением метаболизма оксалатов: солей, кальция, щавелевой кислоты. Провоцирующим фактором для развития патологии становится недостаток витаминов А, Е, В6 и избыток витамином D вследствие лечения рахита, нехватка калия и магния, а также профицит оксалатов из-за определенных продуктов. Часто заболевание диагностируется у детей, больных колитом, сахарным диабетом, хроническим панкреатитом, пиелонефритом и дискинезией желчевыводящих путей, энтеритом.
При уратной форме дисметаболической нефропатии в почках откладываются ураты – соли натрия, которые также выделяются с мочой. Первичная форма болезни поражает детей, страдающих синдромом Леша-Найхана, вторичная протекают на фоне миеломы, пиелонефрита, гемолитической анемии, эритремии. Уратная нефропатия почек может быть спровоцирована приемом цитостатических средств, тиазидовых диуретиков, сциклоспорина А, салицилатов.
Фосфатурию провоцируют хронические инфекции мочевых путей, гиперпаратиреоз, поражения центральной нервной системы. Цистинурия развивается на фоне цистиноза и характеризуется отложением кристаллов цистина в кровяных клетках, лимфатических узлах, печени, селезенке, тканях мышц и нервов, костном мозге, почках. Вторичная форма цистинурии развивается при наличии пиелонефрита и тубулярного интерстициального нефрита.
Симптоматика болезни
Признаки оксалатной формы дисметаболической нефропатии могут диагностироваться сразу после рождения, но чаще всего такое заболевание протекает бессимптомно в течение продолжительного времени. По статистике у большинства больных детей есть родственники страдающие подагрой, мочекаменной и желчнокаменной болезнями, спондилезом, артропатией, сахарным диабетом.
 Факт кристаллизации обычно диагностируется в возрасте 5–7 лет, причем происходит это случайно по результатам стандартного исследования мочи. Однако родители могут заметить изменения в моче ребенка самостоятельно – она становится мутной, выпадает осадок, а на стенках горшка образуется стойкий налет.
Факт кристаллизации обычно диагностируется в возрасте 5–7 лет, причем происходит это случайно по результатам стандартного исследования мочи. Однако родители могут заметить изменения в моче ребенка самостоятельно – она становится мутной, выпадает осадок, а на стенках горшка образуется стойкий налет.
При внимательном отношении к детям дисметаболическую нефропатию можно диагностировать на ранних стадиях, что облегчит лечение в дальнейшем.
Кроме того, дети, страдающие данной патологией, подвержены ряду болезней, среди которых присутствуют:
- кожные аллергические высыпания;
- диспепсия;
- головные боли;
- вегето-сосудистая дистония;
- энурез;
- ожирение;
- мышечная гипотония;
- зуд и покраснение в паховой области.
У ребенка страдающего дисметаболической нефропатией наблюдаются следующие симптомы:
- быстрая утомляемость;
- колющие боли в спине;
- вздутие живота;
- частые позывы в туалет;
- болезненность мочеиспускания;
- субфебрильная температура тела.
Диагностика заболевания
Чтобы назначить адекватное лечение дисметаболической нефропатии, врачу необходимо провести обследование, главной целью которой является обнаружение кристаллизации. Все процедуры проходят под наблюдением педиатра, детского уролога и нефролога.
Кристаллизация выявляется по результатам УЗИ почек и мочевого пузыря. Обнаруженные кристаллы свидетельствуют о присутствии песка или конкрементов. Проводится анализ мочи на биохимические показатели, определяющий увеличенное содержание солей. Дополнительно берутся функциональные пробы мочи, проводится анализ ее микрофлоры.
Способы лечения
 Лечение дисметаболической нефропатии проводится комплексно с использованием следующих методов:
Лечение дисметаболической нефропатии проводится комплексно с использованием следующих методов:
- восстановление нормального метаболизма;
- диета;
- активизация выведения солей;
- ликвидация условий для кристаллизации.
Альтернативные варианты лечения дисметаболической нефропатии предполагают использование средств гомеопатии под наблюдением профильного специалиста. Дополнительно назначают прием витамина E в качестве антиоксиданта и мембранотропных препаратов – Димефосфона, Ксидифона.
Диета при дисметаболической нефропатии подразумевает отказ от мясных бульонов, морковки, свеклы, какао и шоколада, щавеля и шпината.
Очень важно увеличить потребление жидкости. Для больных детей суточная норма воды равняется 1,5 л, для взрослых – около 3 л. Рекомендуется пить свежевыжатые яблочные и тыквенные соки, разбавленные водой, морсы, чаи с травами, лечебные отвары.
Диета при уратной формы дисметаболической нефропатии требует исключения продуктов с высоким содержанием пуринов – фасоли, почек, печени. Питание должно основываться на молоке, кисломолочных продуктах и пище растительного происхождения. Чтобы снизить выработку мочевой кислоты, дополнительно назначают медикаменты: цистон, никотинамид, аллопуринол, фитолизин.
Диета при цистинозе почек — исключает продукты с высоким содержанием аминокислот и метионина. Эти вещества присутствуют в рыбе, яйцах, твороге. В обязательном порядке проводят подщелачивание мочи щелочной минералкой и гидрокарбонатом натрия. Для профилактики отложения кристаллов цистина назначают пеницилламин и купренил.
Такое заболевание, как фосфатная дисметаболическая нефропатия, накладывает табу на фосфорсодержащие продукты питания: печень, курицу, шоколад, бобовые, сыр. Для подкисления мочи используют минералку, витамин C и цистенал.
Профилактика и прогноз
Если строго соблюдается диета и проводится медикаментозное лечение, прогноз исхода дисметаболической нефропатии благоприятный. В таком случае биохимические показатели мочи приходят в норму, и этот результат сохраняется в течение продолжительного времени.
При игнорировании врачебных рекомендаций дисметаболическая нефропатия прогрессирует, в результате чего возникает пиелонефрит, откладываются камни в почках. Если развивается цистиноз, единственным действенным способом лечения остается пересадка органа.
Но спустя некоторое время после операции кристаллики цистина могут появиться и в трансплантате. Такое явление часто становится причиной смерти подростков от 15 до 19 лет.
Для профилактики осложнений дисметаболической нефропатии в рамках диспансера ведется наблюдение больных нефрологом и педиатром. Основными мерами профилактики являются:
- медобследование детей, входящих в группу риска;
- исключение влияния провоцирующих факторов;
- своевременное лечение сопутствующих патологий;
- особый питьевой режим;
При адекватной терапии, если соблюдается диета и исполняются профилактические мероприятия, дисметаболическая нефропатия у детей излечивается.
Дисметаболические нефропатии в практике педиатра | #01/19
Диcметаболические нефропатии (ДН) — гетерогенная группа заболеваний с различной этиологией и патогенезом, которые характеризуются поражением тубулоинтерстициального аппарата почек вследствие нарушения обмена веществ [1, 2, 9].
Проблема ДН является достаточно актуальной в педиатрии и детской нефрологии. Это обусловлено высокой частотой ДН в популяции, а также возможностью их прогрессирования вплоть до развития мочекаменной болезни и/или тубулоинтерстициального нефрита. В структуре заболеваемости мочевыделительной системы у детей ДН составляет от 27% до 64%, а в повседневной практике врача-педиатра синдром обменных нарушений в моче встречается практически у каждого третьего больного [8]. Параллельно отмечается увеличение частоты мочекаменной болезни (МКБ) в популяции в целом, которая в возрастной группе 65–69 лет у мужчин достигает 8,8%, у женщин — 5,6%, а в более молодом возрасте — 3,7% у мужчин и 2,8% у женщин [11]. Одной из причин повсеместного роста частоты МКБ является реализация во взрослом возрасте обменных нарушений, возникших в детстве. По данным эпидемиологического исследования, проведенного V. Romero (2010), частота уролитиаза в таких странах, как США, Италия, Германия, Испания, Япония, за последние 20 лет удвоилась, а в последние годы наблюдается наиболее драматический рост этого показателя [14].
В зависимости от причины выделяют первичные и вторичные ДН. Первичные ДН развиваются в рамках системных наследственно-обусловленных нарушений обмена, характеризуются прогрессирующим течением, ранним развитием уролитиаза и хронической почечной недостаточности. К ним относятся первичная наследственная гипероксалурия (оксалоз), синдром Леша–Нихана, цистиноз, цистинурия и некоторые другие заболевания. Первичные дефекты обмена встречаются достаточно редко, поэтому в данной статье в основном речь пойдет о вторичных ДН.
Вторичные ДН представляют собой вторичные тубулярные синдромы, иначе называемые дисметаболическими расстройствами (диатезами) с кристаллуриями, которые могут быть полигенно-наследуемыми или мультифакториальными. Тубулопатии с кристаллуриями, развивающиеся вследствие генетической предрасположенности, М. С. Игнатовой и Ю. Е. Вельтищевым (1992) были объединены термином «дисметаболические диатезы и нефропатии». Однако причиной вторичных ДН может быть также повышенное поступление определенных веществ в организм, нарушение их метаболизма в связи с поражением других органов и систем (например, желудочно-кишечного тракта), лекарственной терапией, нестабильностью цитомембран канальцев, дегидратацией и др. [1, 2, 8, 9, 11, 14].
В зависимости от типа нарушений обмена при дисметаболических диатезах выделяют оксалатный (щавелевокислый), уратный (мочекислый), цистиновый и другие диатезы.
Любые ДН, вне зависимости от причины, характеризуются мочевым синдромом в виде кристаллурии. В большинстве случаев именно первичная нестабильность мембран канальцевого эпителия является одной из причин кристаллурии. Вследствие генетической предрасположенности или токсического и гипоксического воздействия нарушаются процессы перекисного окисления липидов с образованием свободных радикалов, токсических форм кислорода, что приводит к накоплению вторичных токсических продуктов перекисного окисления липидов, в частности, малонового диальдегида. Параллельно активации процессов перекисного окисления липидов отмечается снижение активности ферментов антиоксидантных защитных систем, в том числе супероксиддисмутазы, активность которой может снижаться до четырех раз. Активное течение свободно-радикальных реакций на мембранах клеток в условиях снижения антиоксидантной защиты приводит к канальцевой мембранопатии, клеточной деструкции, вторичной кристаллурии.
Течение мембранопатологических процессов с развитием иммунного воспаления, циркуляторных нарушений может привести к формированию метаболического тубулоинтерстициального нефрита, представляющего собой острое или хроническое неспецифическое, абактериальное, недеструктивное воспаление интерстициальной ткани почек, сопровождающееся вовлечением в патологический процесс канальцев, кровеносных и лимфатических сосудов почечной стромы.
Персистирующая кристаллурия также может приводить к отложению кристаллов в ткани почки, а также к их адгезии, «слипанию» друг с другом, что служит основой формирования камня и развитию МКБ [12].
Наиболее часто в основе кристаллурии и МКБ лежат нарушения обмена кальция, щавелевой кислоты (оксалатов), мочевой кислоты (уратов), фосфатов, цистина и др. Подавляющее большинство кристаллурий и выявляемых камней связано с кальцием (от 70 до 90%), около 85–90% из них — с оксалатами (в виде оксалата кальция), остальные с фосфатами (фосфаты кальция — 3–10%) или являются смешанными — оксалатно-(фосфатно)-уратными. Уратная кристаллурия и литиаз составляют около 5%, цистиновая — до 3%. В 5–15% выявляются трипельфосфаты — фосфатные кристаллы, содержащие ион аммония, магний и кальций.
На кристаллообразование влияют три основных фактора: 1) перенасыщение канальцевой жидкости сверх пределов ее стабильности; 2) снижение активности ингибиторов перенасыщения; 3) активаторы преципитации.
Для образования кристалла необходимо наличие ионной пары — аниона и катиона (например, иона кальция и иона оксалата). Перенасыщение мочи различными видами ионов в конечном итоге приводит к их преципитации в виде кристаллов, к последующему их росту, кульминацией чего является образование камня [5, 6].
Кроме степени насыщения на растворимость ионов влияет ионная сила, способность к комплексообразованию, рН мочи и скорость ее тока. рН мочи также является важным фактором растворимости. Например, при кислых значениях рН мочевая кислота практически не диссоциирует и легко преципитирует; тогда как фосфатные соли (фосфат кальция), наоборот, малорастворимы при щелочных значениях рН мочи. Нарушение тока мочи также будет способствовать выпадению кристаллов, свидетельством чему является повторное образование камней в условиях частичной обструкции на фоне аномалий развития.
Довольно часто при перенасыщении мочи не выявляется кристаллурии. По всей видимости, это связано с действием ингибиторов перенасыщения — веществ, которые повышают способность мочи удерживать кристаллоиды в растворенном состоянии. Важными ингибиторами образования фосфатно-кальциевых кристаллов и камней являются пирофосфаты, цитрат, магний и низкомолекулярные вещества, а оксалатно-кальциевых — пирофосфаты и высокомолекулярные вещества.
Важными активаторами кристаллообразования является инфекция мочевой системы и рН мочи. Так, трипельфосфаты образуются только вследствие действия уреазоактивной флоры и являются свидетельством инфекции мочевой системы. Стойкое изменение рН мочи вследствие тех или иных заболеваний также может провоцировать кристаллообразование и рост камней. Например, при некоторых заболеваниях желудочно-кишечного тракта (ЖКТ) рН мочи постоянно сдвинут в кислую сторону, что приводит к образованию мочекислых камней из-за снижения растворимости мочевой кислоты в кислой среде [5, 6, 12].
Следует отметить, что понятия «дисметаболическая нефропатия» и «кристаллурия» не являются синонимами. Кристаллурия может носить транзиторный характер, выявляясь, например, на фоне интеркуррентных заболеваний, таких как респираторные вирусные инфекции. Дисметаболическая нефропатия, в свою очередь, не всегда сопровождается кристаллурией (например, после курса терапии и/или на фоне соблюдения диеты).
Оксалатно-кальциевая кристаллурия
Одной из наиболее распространенных кристаллурий в детском возрасте к настоящему времени остается оксалатно-кальциевая кристаллурия.
У большинства больных с оксалатно-кальциевой кристаллурией нет выраженного нарушения метаболизма оксалатов или повышения их экскреции с мочой, но выявляется гиперкальциурия. Однако кристаллы оксалата кальция могут образовываться и при нормальном уровне кальция в моче, вследствие повышения содержания оксалатов. Таким образом, патогенез оксалатно-кальциевой кристаллурии может быть связан как с нарушением обмена кальция, так и с нарушением обмена оксалатов. Так как все оксалатные кристаллы содержат кальций, термины «оксалатная нефропатия» и «оксалатно-кальциевая нефропатия» употребляются как синонимы.
Оксалаты являются конечным метаболическим продуктом в организме, поэтому все они должны экскретироваться. Оксалаты попадают в организм экзогенно с пищей и всасываются в кишечнике или образуются эндогенно. Оксалаты полностью фильтруются в клубочках, затем реабсорбируются и секретируются в канальцах. Даже при небольшом повышении количества оксалатов в моче вследствие их высокой ионной силы высока вероятность выпадения кристаллов оксалата кальция, которые практически нерастворимы.
Гипероксалурические состояния возникают при увеличении всасывания оксалатов в кишечнике либо при повышении их эндогенного образования (табл.).
Избыточное всасывание оксалата в кишечнике при питании продуктами, содержащими большие количества щавелевой кислоты (ревень, шпинат, шоколад, крепкий чай, избыток аскорбиновой кислоты и др.) может возникать при увеличенном потреблении с пищей предшественников оксалата, таких как аскорбиновая кислота и этиленгликоль, либо при авитаминозе В
В генезе гипероксалурий играет важную роль нарушение почечных цитомембран. Причины мембранопатий разнообразны. Лабильность фосфолипидного слоя цитомембран может приводить к кальцифилаксии — нарушению гомеостаза внутриклеточного кальция, приводящего к патологической кальцификации. Нестабильность цитомембран может быть результатом повышенной активности процессов перекисного окисления липидов, как вследствие окислительного стресса, так и снижения факторов антиоксидантной защиты. Все это будет приводить к ускоренному метаболизму мембранных фосфолипидов, вследствие активации фосфолипаз, и высвобождению компонентов липидной оболочки — фосфатидилэтаноламина, фосфатидилсерина, которые через этаноламин и серин будут метаболизироваться в оксалат [3, 5, 6].
Первые симптомы заболевания могут проявиться в любом возрасте, однако чаще отмечаются у детей 5–7 лет в виде лабораторных изменений. Клинически, как правило, данное заболевание себя никак не проявляет. Ввиду отсутствия специфических признаков самочувствие детей, как и общее состояние, чаще всего не страдают. Как правило, это дети, склонные к аллергическим реакциям, к ожирению, дети с синдромом вегетативной дистонии по симпатико-тоническому типу [16]. Иногда отмечаются жалобы на дизурические явления, особенно при присоединении инфекции мочевой системы.
Что касается лабораторных изменений, то мочевой синдром представлен оксалатно-кальциевой или фосфатно-кальциевой кристаллурией, гематурией разной степени выраженности, незначительной протеинурией, абактериальной лейкоцитурией. Также отмечено снижение антикристаллообразующей способности мочи, выявляется фосфолипидурия и повышение фосфолипазной активности мочи. Характерна гиперстенурия.
Морфологически выявляется деструкция апикальных поверхностей эпителия канальцев почек, лимфогистиоцитарная инфильтрация интерстиция. В просветах канальцев и интерстиции обнаруживаются кристаллы оксалата кальция. При прогрессировании заболевания отмечаются явления склероза, вовлечение гломерул.
В случае прогрессирующего течения заболевания, учитывая особенности патогенеза, возможно развитие тубулоинтерстициального нефрита, мочекаменной болезни, рецидивирующего течения пиелонефрита.
Фосфатная кристаллурия
Чаще всего фосфатурия встречается при хроническом течении инфекции мочевой системы, что является основной причиной фосфатурии. Особенное значение для этого имеют микроорганизмы с уреазной активностью. Уреаза разлагает мочевину с ощелачиванием мочи, что приводит к перенасыщению мочи фосфатами магния и аммония (струвит). Соединение струвита с углекислым аппатитом в различных количествах приводит к образованию трипельфосфатных кристаллов. Для кристаллизации трипельфосфатов и дальнейшего формирования камней необходима щелочная реакция мочи. Истинная фосфатурия (или первичная) встречается при заболеваниях центральной нервной системы.
Часто фосфатно-кальциевая кристаллурия сопровождает оксалатно-кальциевую, но выражена при этом в меньшей степени. Фосфатурия также может развиваться вследствие нарушения кальциевого обмена при гиперкальциуриях, при этом кристаллы будут представлены в основном фосфатом кальция.
Нарушения обмена мочевой кислоты
Уратная (подагрическая) нефропатия — патология почек, возникающая вследствие нарушения обмена пуринов или избыточного выведения солей мочевой кислоты почками, приводящая в уратному нефролитиазу или тубулоинтерстициальному нефриту.
Уратные нефропатии в зависимости от происхождения могут быть первичными и вторичными. Первичные уратные нефропатии обусловлены наследственными нарушениями метаболизма мочевой кислоты (подагра, синдром Леша–Нигана). Вторичные возникают как осложнения других заболеваний (эритремии, миеломной болезни, хронической гемолитической анемии, алкоголизма и др.), являются следствием применения некоторых препаратов (тиазидные диуретики, цитостатики, салицилаты, циклоспорин А и др.) или нарушения функции канальцев почек и физико-химических свойств мочи (при пиелонефрите, тубулоинтерстициальном нефрите и др.) [1, 2, 4, 9].
Мочевая кислота (урат) является конечным продуктом обмена пуринов. Следовательно, количество образующейся мочевой кислоты определяется количеством пуринов, поступивших с пищей, эндогенной продукцией и интенсивностью их перехода в мочевую кислоту. Большинство свободных пуриновых оснований утилизируется для ресинтеза пуриновых нуклеотидов.
На кристаллизацию мочевой кислоты влияют рН мочи, суточная экскреция мочевой кислоты и объем мочи. При повышении рН мочи растворимость мочевой кислоты резко возрастает (при изменении рН от 5 до 6 концентрация недиссоциированной формы снижается в 6 раз). В ночное время суток (во время сна) повышается экскреция уратов, снижается количество мочи, а также отсутствует подщелачивание мочи, что усугубляет риск выпадения кристаллов уратов [5, 12].
У больных с уратной нефропатией выявляется дефект почечной экскреции аммония, приводящий к избыточной экскреции титруемых кислот и снижению рН мочи. Причинами экскреции постоянно кислой мочи могут быть заболевания ЖКТ, сопровождающиеся диареей, вследствие дегидратации и/или потери бикарбонатов, а также при илеостоме, лекарственно-индуцированной ацидификации.
Уратурия, как причина, обусловившая поражение почек, выявляется у 14–26% больных. Уратные нефропатии (интерстициальный нефрит на фоне уратурии) представляют собой хронически протекающие заболевания, характеризующиеся умеренной протеинурией, микрогематурией и мочекислой кристаллурией. Результаты обследования детей с уратурией и их родственников выявили обменные нарушения, носящие семейный характер. Очень информативным оказался генеалогический анализ родословных, что позволяет выявлять определенный спектр почечной и внепочечной патологии среди родственников. Так, развитие уратной нефропатии на фоне ожирения, гиперлипидемиии, инсулинрезистентного сахарного диабета рассматривается как клиническое проявление метаболического синдрома, который носит семейный характер. Первые проявления синдрома отмечаются уже в подростковом возрасте. Другая причина развития гиперурикозурии — медикаментозная (диуретики, анальгетики, цитостатики). Экскреция мочевой кислоты с мочой считается превышающей норму при уровне более 1 мг на 1 мл, когда возникает опасность повреждения интерстициальной ткани почек, сосудов и камнеобразования. Что касается клинических проявлений, то при уратной нефропатии могут появиться жалобы на дизурические явления, рецидивирующие боли в животе, боли в поясничной области, в случае уролитиаза (у 5–41%) развивается почечная колика, в тяжелых случаях появляются клинические проявления подагры [4].
Нарушения обмена цистина
Цистин является продуктом метаболизма метионина и представляет собой наименее растворимую из встречаемых в природе аминокислот. Кристаллы цистина выпадают при превышении порога растворимости (более 400 мг/л) и при кислой реакции мочи [1, 2, 5, 9].
Можно выделить две основные причины повышения концентрации цистина в моче: избыточное накопление цистина в клетках почки и нарушение обратного всасывания цистина в почечных канальцах.
Однако наиболее часто кристаллы цистина выявляются при нефропатиях с преимущественным поражением канальцевого аппарата почек (пиелонефрит, тубулоинтерстициальный нефрит), и такая цистинурия носит вторичный характер. Если кристаллы оксалатов, уратов, фосфатов могут появляться эпизодически и при различных колебаниях в диете, то наличие цистина в моче — всегда признак патологии.
Диагноз цистинурии может быть заподозрен у любого пациента при наличии в анамнезе камней в почках, с текущими явлениями уролитиаза, отягощенным семейным анамнезом по мочекаменной болезни и специфическим янтарным окрасом камней.
Диагностические критерии ДН у детей
Постановка диагноза ДН включает в себя комплексную оценку образа жизни ребенка, характер его питания, генеалогический анамнез, результаты лабораторно-инструментальных методов исследования. Скудность клинических проявлений компенсируется характерными лабораторными и инструментальными признаками заболеваний.
Лабораторно-инструментальная диагностика ДН основывается на выявлении кристаллурии в общем анализе мочи, повышении концентрации тех или иных солей в биохимическом исследовании мочи, исследовании антикристаллобразующей способности мочи (АКОСМ) и тестов на кальцифилаксию и перекиси в моче, ультразвуковом исследовании (УЗИ) почек и мочевыводящих путей.
Выявление кристаллов солей только в общих анализах мочи не является основанием для постановки диагноза ДН. Следует иметь в виду, что кристаллурия у детей часто бывает транзиторной и не связанной с патологией обмена и нестабильностью почечных цитомембран. Особенно это касается кристаллурии, выявляемой на высоте лихорадки, после перенесенных инфекций, диареи, а также у детей в периоде новорожденности при развитии «мочекислого инфаркта».
Для подтверждения диагноза ДН при выявлении кристаллурии в общем анализе мочи проводится биохимическое исследование мочи, где следует обратить внимание на концентрацию солей (оксалаты, мочевая кислота, кальций, фосфор и др.) и показатели функции канальцев (глюкоза, титруемая кислотность, аммиак, рН и др.), что позволяет выявить не только повышение экскреции тех или иных веществ, но и оценить условия для кристаллообразования, степень вовлеченности тубулярного аппарата в патологический процесс.
Повышение экскреции солей по данным биохимического исследования мочи при нормальных общих анализах мочи и отсутствии изменений при УЗИ почек также не может в полной мере свидетельствовать о ДН у ребенка, однако позволяет вынести полученные изменения в диагноз, например: гипероксалурия, гиперуратурия и т. д.
При подозрении на ДН отсутствие кристаллурии и повышенной экскреции солей с мочой у ребенка в данный момент не позволяет достоверно исключить этот диагноз. Нормальные показатели в общем и биохимическом анализах мочи могут быть обусловлены, например, правильной диетой и режимом жизни ребенка в данный период, тогда как предпосылки к тем или иным обменным нарушениям сохраняются.
Поэтому важно определить способность мочи растворять различные соли. Для этой цели проводится анализ на АКОСМ к оксалатам кальция, фосфатам кальция и трипельфосфатам, наиболее часто встречаемым при кристаллуриях у детей. В нормальной моче способность растворять эти соли и предотвращать кристаллообразование сохранна за счет наличия ингибиторов кристаллообразования и отсутствия или малой активности активаторов (промоторов) кристаллообразования. При ДН АКОСМ снижена в различной степени за счет повышения концентрации этих солей в растворенном виде и/или нарушения баланса ингибиторов и активаторов.
Тест на кальфилаксию позволят выявить нарушение клеточного гомеостаза кальция, приводящее к патологической кальцификации клеток и тканей. Тест на перекиси в моче отражает активность процессов перекисного окисления липидов цитомембран, повышение уровня перекисей будет являться признаком нестабильности цитомембран.
Ценность методов исследования мочи на АКОСМ, кальцифилаксию и перекиси заключается в возможности доклинического выявления патологии даже при отсутствии каких-либо других лабораторных признаков и в использовании их для контроля эффективности проводимой терапии [3].
Изменения, выявляемые при ультразвуковом исследовании почек, как правило, малоспецифичны и заключаются в очаговом или диффузном повышении эхогенности паренхимы почек за счет отложения кристаллов. Показанием к проведению более углубленного, в частности рентгенологического обследования, является обнаружение в почке при проведении УЗИ микролитов или включений, дающих эффект эхонегативной дорожки.
Общие подходы к лечению ДН
С учетом особенностей этиопатогенеза комплексное лечение ДН предполагает проведение мероприятий неспецифического (нормализация образа жизни, исключение гиподинамии, повышенный питьевой режим) и специфического характера (диета, коррекция метаболических нарушений медикаментозной терапией).
Нормализация образа жизни, физическое и психическое здоровье являются важным условием для достижения положительного эффекта в терапии ДН. Выраженные и длительные нарушения этих составляющих в конечном счете реализуются в микроциркуляторных отклонениях, ведущих к гипоксии, и/или в непосредственном повреждающем воздействии на клетки. Все это активизирует и/или усугубляет нарушения клеточного обмена, интенсивность перекисного окисления липидов мембран, их нестабильность и т. д.
Прием большого количества жидкости является универсальным способом лечения любой ДН, так как способствует уменьшению концентрации растворимых веществ в моче. Также важно время приема жидкости, особенно в периоды максимальной суточной концентрации мочи, т. е. во время сна. Поэтому одной из целей лечения является никтурия, что достигается приемом жидкости перед сном. Предпочтение следует отдавать простой или минеральной воде, поскольку длительный прием жидкостей, например, подкисляющих мочу или содержащих углеводы, может вызвать увеличение экскреции кальция [5].
Диета позволяет в значительной степени снизить метаболическую нагрузку на тубулярный аппарат.
При лечении больных с оксалатной нефропатией назначается картофельно-капустная диета, при которой снижается поступление оксалатов с пищей и нагрузка на тубулярный аппарат. Применение картофельно-капустной диеты в течение 2–3 недель сопровождается статистически достоверным снижением экскреции оксалатов, что сочетается с улучшением мочевого синдрома. Картофельно-капустная диета назначается на 3 недели с трехнедельными перерывами, во время которых ребенок получает диету № 5 по Певзнеру.
Также необходимо исключить экстрактивные мясные блюда, богатые оксалатами щавель, шпинат, клюкву, свеклу, морковь, какао, шоколад и др. «Подщелачивающий» эффект оказывают курага, чернослив, груши.
Из минеральных вод используются такие, как «Славяновская» и «Смирновская», по 3–5 мл/кг/сут в 3 приема курсом 1 мес 2–3 раза в год.
При лечении уратной нефропатии диета предусматривает исключение богатых пуриновыми основаниями продуктов (печень, почки, мясные бульоны, горох, фасоль, орехи, какао и др.). Преимущество должно отдаваться продуктам молочного и растительного происхождения. Важным условием успешной терапии является достаточное употребление жидкости — от 1 до 2 л в сутки. Предпочтение следует отдавать слабощелочным и слабоминерализованным водам, отварам трав (хвощ полевой, укроп, лист березы, брусничный лист, клевер пашенный, спорыш и др.), отвару овса. Для поддержания рН мочи в пределах 6,2–6,6 можно использовать цитратные смеси (Уралит-У, Блемарен, Магурлит, Солимок и др.), которые обладают значительной буферной емкостью [1, 4, 5, 9, 10].
Специфическая терапия должна быть направлена на предупреждение кристаллообразования, выведение солей, нормализацию обменных и энергетических процессов. Поскольку в большинстве случаев мембранопатия у детей является одним из звеньев патогенеза ДН, основной акцент делается на антиоксидантную и мембраностабилизирующую терапию.
Медикаментозная терапия включает мембранотропные препараты и антиоксиданты [5, 6, 9]. Лечение должно быть длительным и курсовым для достижения пролонгированного эффекта.
Пиридоксин (витамин В6) назначается в дозе 1–3 мг/кг/сут (до 400 мг/сут) в течение 1 мес ежеквартально. Витамин В6 оказывает мембраностабилизирующее действие за счет участия в обмене жиров в качестве антиоксиданта и обмене аминокислот. Целесообразно также назначение препарата Магне В6 из расчета 5–10 мг/кг/сут курсом в течение 2 мес 3 раза в год.
Мембраностабилизирующее действие оказывает витамин А, который встраивается в билипидный слой и нормализует взаимодействие белков и липидов мембраны. Суточная доза витамина А 1000 МЕ на год жизни ребенка, курсом 1 мес ежеквартально.
Токоферола ацетат (витамин Е) является мощным антиоксидантом, который поступает в организм извне и вырабатывается эндогенно. Необходимо помнить, что экзогенное введение витамина Е может тормозить его эндогенную продукцию по механизму отрицательной обратной связи. Витамин Е укрепляет белково-липидные связи клеточных мембран, участвует в процессах акцепции электронов при свободно-радикальных реакциях на мембранах. Назначается с витамином А в дозе 1–1,5 мг/кг массы в сутки.
В качестве мембраностабилизаторов также используются Димефосфон и Ксидифон. Димефосфон восстанавливает связь между окислением и фосфорилированием в клеточном дыхании, разобщенность которого наблюдается при нестабильности митохондриальных мембран, прерывая каскадные процессы перекисного окисления липидов. Применяется в дозе 1 мл 15% раствора на каждые 5 кг веса, 3 приема в сутки. Курс — 1 мес, 3 раза в год.
Ксидифон является комплексообразующим препаратом, который облегчает включение кальция в митохондрии и предупреждает отложение его нерастворимых солей. Назначается в дозе 10 мг/кг/сут 2% раствора в 3 приема. Курс — 1 мес, 2 раза в год.
В лечении детей с оксалатно-кальциевой кристаллурией широко применяется фитотерапия. Из комбинированных фитопрепаратов рекомендуется применение Цистона, Фитолизина и Канефрона. Цистон назначается в дозе 1–2 таблетки 2–3 раза в день курсом от 3 до 6 мес. Канефрон у взрослых применяется в форме драже и капель: по 2 драже 3 раза в день (или по 50 капель 3 раза в день). Для детей доза уменьшается в 2–3 раза в зависимости от возраста: по 11–25 капель или по 1 драже 3 раза в день в течение 6–8 недель [3].
Помимо этого, назначается окись магния, особенно при первичной гипероксалурии, в дозе 0,15–0,2 г/сут. При первичной гипероксалурии следует иметь в виду, что любая терапия является паллиативной. Радикальным методом лечения оксалоза является трансплантация печени, что устраняет дефект отсутствия аланин-глиоксилаттрансферазы и восстанавливает нормальный обмен оксалатов.
При гиперурикемии важно уменьшить концентрацию мочевой кислоты до 6 мг/100 мл и менее. Для этого используются средства, снижающие синтез мочевой кислоты, — ингибиторы ксантиноксидазы. Применение в педиатрии аллопуринола ограничено из-за возможных осложнений — гепатит, эпидермальный некроз, алопеция, лейко- и тромбоцитопения, повышение уровня ксантина в крови. Под строгим контролем аллопуринол назначают в дозе 0,2–0,3 г/сут в 2–3 приема в течение 2–3 нед, затем доза снижается. Длительность общего курса — до 6 мес. Никотинамид является более слабым ингибитором активности ксантиноксидазы, чем аллопуринол, но лучше переносится; назначается в дозе 0,005–0,025 г 2–3 раза в сутки по 1–2 мес повторными курсами. Колхицин снижает транспорт пуриновых оснований и скорость их обмена. Назначается в дозе 0,5–2 мг/сут сроком от 18 мес до нескольких лет.
Урикозурическим эффектом также обладают оротовая кислота, Цистон, Этомид, Цистенал, Фитолизин и др. Калия оротата таблетки назначаются в дозе 10 мг/кг в сут в 2–3 приема в течение 1 мес. Урикозурическим и урикозостатическим действием обладает также бензбромарон, который применяют по 50–100 мг/сут 2–3 раза в сочетании с салуретиками и цитратом натрия [5, 6, 9].
Лечение при фосфатной кристаллурии должно быть направлено на подкисление мочи (минеральные воды: «Нарзан», «Арзни», «Дзау-суар» и др.; препараты: Цистенал, аскорбиновая кислота, метионин). Назначается диета с ограничением продуктов, богатых фосфором (сыр, печень, икра, курица, бобовые, шоколад и др.). При выраженной экскреции фосфата кальция необходимо добиться снижения всасывания фосфора и кальция в кишечнике (например, назначением Альмагеля). Обязательным компонентом лечения при наличии трипельфосфатов является антибактериальная терапия и санация хронической инфекции мочевой системы [9].
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию, направленную на подщелачивание мочи и повышение растворимости цистина [2, 4–6].
Цель диетотерапии — предотвратить избыточное поступление в организм ребенка предшественника цистина — метионина и других серосодержащих кислот. Для этого также исключают (или резко ограничивают) из рациона питания ребенка богатые метионином и серосодержащими аминокислотами продукты — творог, рыбу, яйца, мясо и др. Поступление метионина при таких диетических мероприятиях сокращается до 0,7 г/сут. Поскольку метионин необходим растущему организму ребенка для пластических процессов, длительное применение строгой диеты невозможно, поэтому через 4 нед от начала диетотерапии рацион ребенка расширяется и приближается к обычному, но характеризуется строгим исключением рыбы, творога и яиц.
Количество жидкости, употребляемой ребенком, должно быть не менее 2 л/сут, особенно важно принимать жидкость перед сном. Для подщелачивания мочи используется цитратная смесь, растворы гидрокарбоната натрия, Блемарен, щелочные минеральные воды. Это позволяет добиться повышения рН мочи до 7,5–8,0. Снижению концентрации цистина и повышению рН мочи будут также способствовать ингибиторы карбоангидразы (Диакарб) и Гипотиазид.
Для повышения растворимости цистина и предупреждения кристаллизации назначается пеницилламин, с целью активации тиолзависимых ферментов. Пеницилламин обладает некоторой токсичностью и антиметаболическим действием на пиридоксин, поэтому в начале терапии назначаются невысокие дозы препарата — 10 мг/кг/сут в 4–5 приемов, далее доза увеличивается в течение недели до 30 мг/кг/сут, а при цистинозе — до 50 мг/кг/сут. Лечение пеницилламином должно проводиться под контролем содержания цистина в лейкоцитах и/или цианиднитропруссидного теста (проба на цистин в моче, где концентрация цистина должна составлять до 150–200 мг/л). При достижении этих показателей доза пеницилламина снижается до 10–12 мг/кг/сут. Лечение пеницилламином проводится длительно, годами. Поскольку пеницилламин инактивирует пиридоксин, параллельно назначается витамин В6 (пиридоксин) в дозе 1–3 мг/кг/сут в течение 2–3 мес с повторными курсами. Для стабилизации мембран почечных канальцев назначаются витамин А (6600 МЕ/сут) и витамин Е (токоферол, 1 капля на 1 год жизни 5% раствора в сутки) в течение 4–5 нед с повторными курсами. Имеются данные о положительном эффекте применения вместо пеницилламина менее токсичного его аналога — Купренила в уменьшенной дозе в сочетании с Ксидифоном и другими мембраностабилизаторами [1, 9].
При цистинозе успешно используется трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности (ХПН). Трансплантация почки позволяет значительно увеличить срок жизни больных — до 15–19 лет, однако отложение кристаллов цистина наблюдается и в трансплантате с преимущественным поражением интерстиция и мезангиума, что в конечном итоге приводит к развитию интерстициального фиброза и склерозированию в пересаженной почке и ХПН.
При развитии на фоне ДН и МКБ хронического пиелонефрита необходимо включение в комплексную терапию наряду с антибиотиками иммунокорригирующих препаратов, повышающих эффективность антибиотикотерапии, особенно учитывая часто наблюдающуюся у таких больных поливалентную антибиотикорезистентность. С этой целью могут использоваться различные препараты (Уро-Ваксом, Иммунал, Имунофан, левамизол, Ликопид и др.) [6].
Прогноз при вторичной ДН в целом благоприятен. В большинстве случаев при соответствующем режиме, диете и медикаментозной терапии удается добиться стойкой нормализации соответствующих показателей в моче. В отсутствие лечения или при его неэффективности наиболее естественными исходами ДН являются МКБ и тубулоинтерстициальный нефрит.
Диспансерное наблюдение и профилактика
Диспансерное наблюдение включает в себя ежегодное обследование по плану. При необходимости биохимическое исследование мочи проводят 1 раз в 3–6 месяцев. Основные профилактические мероприятия направлены на сбалансированное питание ребенка и профилактику осложнений (инфекция мочевой системы, мочекаменная болезнь, тубулоинтерстициальный нефрит).
Литература
- Вельтищев Ю. В., Игнатова М. С. Наследственные и врожденные болезни почек и мочевыводящих путей. В кн.: Наследственная патология человека / Под ред. Ю. В. Вельтищева, Н. П. Бочкова. М., 1992. Т. 2. С. 3–71.
- Возианов А. Ф., Майданник В. Г., Бидный В. Г., Багдасарова И. В. Основы нефрологии детского возраста. Киев: Книга плюс, 2002. С. 214–225.
- Длин В. В., Османов И. М., Юрьева Э. А. Обменные нефропатии. М.: Оверлей, 2009. 128 с.
- Игнатова М. С. Наследственные и врожденные нефропатии. В кн.: Нефрология / Под ред. И. Е. Тареевой. М.: Медицина, 2000. С. 337–371.
- Малкоч А. В. Дисметаболические нефропатии и мочекаменная болезнь. В кн.: Нефрология детского возраста: Практическое руководство по детским болезням. М.: Медпрактика, 2005. Т. 6. С. 472–516.
- Малкоч А. В., Бельмер С. В. Мочекаменная болезнь у детей // Лечащий Врач. 2005, № 7. [Электронный ресурс: URS https://www.lvrach.ru/2005/07/4532751/, дата обращения: 17.08.2018].
- Малкоч А. В., Бельмер С. В. Нефропатии при целиакии // Лечащий Врач. 2012, № 8. [Электронный ресурс]. URL: https://www.lvrach.ru/2012/08/15435496/ (дата обращения: 17.08.2018).
- Рычкова С. В. Дисметаболические нефропатии в педиатрической практике // Лечащий Врач. 2010, № 8. [Электронный ресурс]. URL: https://www.lvrach.ru/2010/08/15392892/ (дата обращения: 17.08.2018).
- Юрьева Э. А., Длин В. В. Диагностический справочник нефролога. Клиническая и лабораторная диагностика. М.: Изд. «Медпрактика-М», 2007. 352 с.
- Cameron J. S., Moro F., Simmonds H. A. Gout, uric acid andpurine metabolism in paediatric nephrology // Pediatr. Nephrol. 1993; 7: 105–118.
- Indridason O. S., Birgisson S., Edvardsson V. O., Sigvaldason H., Sigfusson N., Palsson R. Epidemiology of kidney stones in Iceland: a population-based study // Scand. J. Urol. Nephrol. 2009. Vol. 40, № 3. P. 215–220.
- Jobs K., Rakowska M., Paturej A. Urolithiasis in the pediatric population — current opinion on epidemiology, patophysiology, diagnostic evaluation and treatment // Dev Period Med. 2018; 22 (2): 201–208.
- John C. Lieske Probiotics for prevention of urinary stones [Электронный ресурс]. URL: http://dx.doi.org/10.21037/atm.2016.11.86 (дата обращения: 17.08.2018).
- Romero V., Akpinar H., Assimos D. G. Kidney Stones: A Global Picture of Prevalence, Incidence, and Associated Risk Factors // Rev Urol. 2010. Vol. 12, № 2–3. P. 86–96.
- Sadaf H., Raza S. I., Hassan S. W. Role of gut microbiota against calcium oxalate. // Microb Pathog. 2017 Aug; 109: 287–291.
- Sakhaee K., Capolongo G., Maalouf N. M., Pasch A., Moe O. W., Poindexter J. et al. Metabolic syndrome and the risk of calcium stones // Nephrol Dial Transplant. 2012. № 8. Р. 3201–3209.
А. В. Малкоч*, 1, кандидат медицинских наук, профессор
Е. Г. Куликова**
Ю. Б. Юрасова***, доктор медицинских наук, профессор
* ФГБОУ ДПО РМАНПО, Москва
** ГБУЗ МО МОКДЦД, Мытищи
*** ФГБОУ ВО МГУПП, Москва
1 Контактная информация: [email protected]
Дисметаболические нефропатии в практике педиатра/ А. В. Малкоч, Е. Г. Куликова, Ю. Б. Юрасова
Для цитирования: Лечащий врач № 1/2019; Номера страниц в выпуске: 34-39
Теги: диета, водно-питьевой режим, энерготропные препараты
Купить номер с этой статьей в pdf
Что такое нефропатия у ребенка? Симптомы и лечение нефропатии у детей
Содержание:
Часто при самом рядовом обследовании в анализе мочи обнаруживаются соли. Врачи-педиатры часто не обращают особенного внимания на них, считая наличие солей вариантом нормы. Однако это не всегда верно.

Действительно — единичный анализ, показавший незначительный солевой осадок, может считаться непоказательным при условии, что нет других отклонений. Но если он значителен, кристаллы крупные и соли появляются с завидным постоянством (в каждом или почти каждом анализе) — это повод направить малыша на консультацию к специалисту — детскому нефрологу или урологу. Возможно, у ребенка дисметаболическая (солевая) нефропатия. Вот о ней мы подробно и поговорим — чем она так опасна, как ее выявлять и как лечить.
Дисметаболическая нефропатия — (от латинского dis — нарушение работы, metabolismum — обмен веществ, nefros — почка, pathos — патология, болезнь) — это группа заболеваний, нарушения работы почек, развивающиеся в результате нарушения метаболизма, расстройства солевого обмена в организме. Чаще всего у детей встречаются нарушения обмена веществ, которые приводят к повышенному выведению с мочой различных солей — оксалатов, уратов, фосфатов и др.
Моча — это сложный раствор продуктов обмена организма ребенка, она постоянно вырабатывается почками в процессе жизни организма. В моче у детей нередко обнаруживаются кристаллы. Но признаком патологии они могут быть лишь при наличии симптомов нарушения мочевыделения и воспалительного процесса. Наибольшую ценность в плане диагностики представляет ночная моча — ее состав и объем отражают пищевую и энергетическую нагрузки ребенка за предыдущий день и объективно отражают работу почек.
Образование кристаллов происходит в ткани почки, спустя 5 минут они попадают в лоханку, а из нее в течение 5-10 минут оказываются в мочевом пузыре, в котором могут находиться около 3-6 часов. Если время их нахождения в любом из отделов увеличивается, это приводит к увеличению размеров кристаллов, их задержке в мочевыводящей системе и как результат — к повреждению ее тканей. Немаловажную роль в образовании солей играет и реакция (или рН) мочи. В норме она должна быть слабокислой, резкие колебания (как в сторону кислотности, так и в сторону ощелачивания) приводят к выпадению солей в осадок.
Причины развития нефропатии
Нет четкой, конкретной причины, которая бы в ста процентах случаев вызывала метаболические нарушения в почках. Обычно врачи считают, что основой патологии является семейная, наследственная предрасположенность к почечным и обменным проблемам. В результате малыш наследует особенности обмена веществ, которые формируют усиленное всасывание некоторых солей в кишечнике, а также различные дефекты микростроения почки, которые и формируют избыточное выделение солей с мочой. Этим нарушениям способствуют токсикозы, инфекции и патологическое течение беременности, загрязнение окружающей среды, проживание в неблагоприятных районах, плохое качество питьевой воды (жесткая вода), употребление в пищу продуктов с химическими добавками, а также наследственные факторы.
Однако не у всех детей особенности строения почек и нечастое наличие солей в моче трансформируются в нефропатию, чаще всего это состояние формируется под воздействием провоцирующих факторов — дефицита витаминов группы В (особенно В1 и В6), витаминов А и Е, бактериальных токсинов при тяжелых инфекциях, например, при ангинах, при гипоксии (недостатке кислорода), при передозировке кальция и витамина Д, при оперативных вмешательствах на кишечник и др.
Дети с обменными нефропатиями в дальнейшем имеют высокий риск образования мочевых камней и формирования мочекаменной болезни, поэтому важно распознать патологию на ранних этапах и правильно построить лечебные и диетические мероприятия. В дальнейшем это позволит сохранить здоровье почек и всей мочевыделительной системы в целом.
При этой группе заболеваний происходит повреждение ткани почки ребенка кристаллами солей, отло-жение солей в структуре почечной ткани. В результате формируются очаги воспаления, нарушается нормальное функционирование почек и развиваются пиелонефриты (воспаление почечной лоханки), нефриты (воспаление всей ткани почки), формируются камни почек и даже может развиться почечная недостаточность.
Все нефропатии разделяются на оксалатные (бывают двух типов, первичные и вторичные), уратные и очень редко фосфатные. В основу классификации положен тип солевого осадка мочи. Но соли в моче могут появляться в как осложнение при различных почечных и внепочечных заболеваниях.
Медикаментозное лечение оксалатной нефропатии
В детской нефрологии они встречаются чаще других нефропатий, их возникновение связано с нарушением обмена щавелевой кислоты и кальция в организме. У малышей с этим видом патологии в кишечнике происходит усиленное всасывание щавелевой кислоты, ее избыток в виде соли (оксалата кальция) выводится с мочой в растворенном виде. Однако, помня школьный курс органической химии, мы знаем, что оксалаты растворимы только в слабощелочной и нейтральной среде, при сдвиге мочи в кислую сторону, их растворимость снижается, и они выпадают в осадок в виде кристаллов. Учитывая тип питания и реакцию мочи детей — это у них не редкость.
Кристаллы оксалата кальция белого цвета, жесткие на ощупь и чаще других солей повреждают мочевыводящие пути, что сопровождается появлением эритроцитов в моче и болевыми ощущениями. Кристаллы повреждают нежную ткань почки малыша, и в моче могут появиться фрагменты мембран почечных клеток (мембранные фосфолипиды).
В развитии оксалатной нефропатии немаловажную роль играют также и дефицит витаминов группы В, которые участвуют в метаболизме щавелевой кислоты, способствуя ее утилизации, витамины А и Е, защищающие оболочки почечных клеток от повреждения оксалатными кристаллами. Оказывают негативное влияние и бактериальные инфекции, нарушающие кислотно-щелочную среду мочи, и гипервитаминоз Д, который усиливает выведение кальция с мочой и связывание его с щавелевой кислотой. Предрасполагающим к солеобразованию является прием продуктов, богатых аскорбиновой и щавелевой кислотами — щавель, спаржа, шпинат, свекла, клубника, чай, какао, шоколад, бобы, грецкие орехи, перец. Немаловажна и наследственность: у таких детей в роду есть больные мочекаменной болезнью, заболеваниями желудка и кишечника, аллергиями. Риск возникновения нефропатии повышается в условиях сухого жаркого климата, так как при недостаточном потреблении воды при ее активных потерях происходит концентрирование мочи и перенасыщение ее солями.
Обычно у таких малышей обнаруживаются периодические боли в животе неясного происхождения и неточной локализации, они никак не связаны с приемами пищи, усиливаются после физических нагрузок. Помимо этого родители могут отмечать редкие мочеиспускания, выделение небольших порций мочи, уменьшение общего суточного ее количества, склонность к большему отделению мочи в ночное время (так называемая никтурия), в отстоявшейся моче может выявляться беловатый, как бы меловой, осадок. Внешне такие детки обычно медлительны. Могут иметь несколько повышенную массу тела, у них отмечаются нарушения вегетативной нервной системы — потливость, мраморность, похолодание конечностей, нарушение терморегуляции в виде субфебрильной температуры — до 37-37.2 градуса С, часто бывают расстройства желудочно-кишечного тракта. Иногда оксалатная нефропатия может прояв-ляться исключительно нарушениями, отмечаемыми в анализах мочи, при общем удовлетворительном состоянии ребенка.
Проявления возникают обычно раннем и дошкольном возрастах. В анализе мочи будет отмечаться наличие эритроцитов, небольшое количество белка, наличие лейкоцитов, при отсутствии бактерий — так называемое неинфекционное воспаление. Обязательным является наличие в моче кристаллов и высокая удельная плотность мочи — до 1030 и выше.
Главной задачей лечения оксалатной нефропатии — подбор адекватной диеты. Рацион малыша должен состоять из разнообразных пищевых продуктов растительного и животного происхождения, соотноше-ние белков, жиров и углеводов в питании при этом — 1:1:5. Содержание витаминов группы В должно превышать нормативы в два раза, а витамина В6 не менее чем в четыре раза.
В диете при оксалурии разрешаются брюссельская, цветная, белокочанная капуста, абрикосы, бананы, бахчевые, груши, тыква, огурцы, горох, все виды круп, белый хлеб, растительное масло. Периодически — картофельно-капустная диета.
Ограничиваются — морковь, зеленая стручковая фасоль, лук, помидоры, крепкий чай, говядина, курица, заливное, печень, треска, смородина, антоновские яблоки, редис.
Исключаются — шоколад, свекла, сельдерей, шпинат, щавель, ревень, петрушка, экстрактивные вещества (бульоны).
Обогащение диеты витаминами группы В и магнием можно достигнуть путем включения в рацион пшеничных отрубей и блюд из гречневой, овсяной, пшеничной крупы, кураги, пекарских дрожжей. Отвар из пшеничных отрубей рекомендуется ежедневно добавлять к различным блюдам. В связи с тем, что наименьшее количество солей выпадает в осадок при рН 6.5-6.6, то кислотность мочи регулируется специальным подбором пищевых продуктов, уравновешивающих в диете содержание кислых и щелочных компонентов, для этого в рацион вводится повышенное количество картофеля, овощей и фруктов.
Для обеспечения нормального количества мочи препятствующего выпадению солей в осадок, дети получают дополнительно к рациону отвары из сухофруктов, отвары трав, обладающих мочегонным действием (зверобой, толокнянка, тысячелистник) и минеральные воды без газа.
Медикаментозное лечение назначается при высоком содержании оксалатов в моче или выпадении солевого осадка. Применяют пиридоксин (витамин В6), который снижает образование в организме и всасывание из пищи щавелевой кислоты, витамины А и Е, предохраняющие клетки почечной ткани от повреждения, окись магния — она действует в кишечнике, образуя труднорастворимые соли щавелевой кислоты и не давая, таким образом, ей всасываться. Длительность таких курсов составляет от 3 месяцев до полутора лет, обычно делая 3-4 недели перерыв и контролируя анализы мочи. Естественно, лечение должно проходить под контролем врача.
Кроме того, в комплекс лечебных мероприятий входит достаточный питьевой режим и двигательный режим, лечебная физкультура.

Лечение уратной нефропатии у детей
Этот вид нефропатий развиваются реже. Обычно уратные соли в моче обнаруживаются на фоне различных заболеваний, хотя возможно развитие уратной нефропатии как самостоятельного заболевания. Появление осадка кирпично-красного цвета в свежевыпущенной моче говорит о выделении мочевой кислоты и ее солей. Возникает патология при нарушении обмена пуринов (определенных участков ДНК, РНК и белков). Входит в состав так называемого нервно-артритического диатеза. У детей с такой патологией имеются определенные ферментативные дефекты, формирующие нарушения обмена не только мочевой кислоты и ее солей, но еще и углеводов и жиров. В результате может формироваться еще и ацетонемический синдром с рвотами и болями в животе. К тому же эти дети еще и имеют особенности работы нервной системы.
Мальчики болеют в 2.5 раза чаще девочек, а в семьях у таких детей часто отмечаются патологии почек, мочекаменная болезнь, подагра, артриты, гипертонии и ишемическая болезнь сердца, сахарный диабет, заболевания желудка и кишечника, желчного пузыря. Часто особенности обмена наследуются от роди-телей или близкой родни вместе с аллергиями. Наиболее ярко проявляются симптомы с началом посещения садика или школы, когда чаще возникают стрессы. Усугубляется течение нефропатии при инфекциях, при погрешностях в питании и потреблении жирной и высокобелковой пищи. Очень заметно и влияние окружающей среды — провоцирующим фактором могут стать резкие колебания температур, нахождение на открытом солнце, некачественная питьевая вода с большим количеством солей кальция (жесткая вода), дефицит фтора и йода.
Клинически нефропатия проявляется в виде изменений мочи — высокое содержание уратов, вплоть до кирпично-красного окрашивания мочи, высокие уровни аммиака и ацетона в моче, небольшое количество белка. В моче появляются лейкоциты, которые свидетельствуют о воспалении в такни почки, эритроциты, характеризующие повреждение ткани почки кристаллами и изменение рН в кислую сторону (что способствует снижению растворимости уратов и образованию камней).
У таких детей отмечается неврастенический синдром в виде эмоциональной неустойчивости, раздражительности, изменчивости поведения — упрямство, негативизм, агрессивность. Реже возникают ночные страхи, различные тики, заикание и энурез. Дети, имеющие нервно-артритичекую конституцию и уратные соли часто имеют дефицит массы тела более 10% на фоне сниженного аппетита, различные аллергические сыпи, приступообразные боли в животе. У большинства из них при обследовании выявляются заболевания желудка с повышением кислотности, кишечные расстройства, дискинезии желчевыводящих путей, нарушения мочеиспускания, и возникают ацетонемические кризы. У подростков могут возникать и повышения артериального давления.
Лечение уратных нефропатий проводится по тем же принципам, что и оксалатных. На первом месте в лечении стоит корректировка диеты. Объем уратных солей, выделяемых с мочой, зависит от массы тела малыша и содержания пуринов в пище. В связи с этим рекомендуется поддержание стабильного веса за счет ограничения белков животного происхождения и жиров, а также ограничение продуктов, содержащих много пуринов. Разрешаются — молочные продукты в первую половину дня, картофельно-капустная диета. Цветная и белокочанная капуста, крупы (гречневая, овсяная, пшенная, рис), фрукты, курага, чернослив, морская капуста, пшеничные отруби, сливочное и растительное масло, хлеб пшеничный, ржаной из муки грубого помола. Нежирное мясо и рыба —3 раза в неделю по 150 г. старшим детям в отварном виде в первую половину дня. Ограничиваются — горох, бобы, говядина, курица, кролик. Исключаются — крепкий чай, какао, кофе, шоколад, сардины, печень животных, почки, мозги, чечевица, свинина, субпродукты, жирная рыба, мясные и рыбные бульоны.
В диету вводятся продукты, содержащие белки растительного происхождения, а также способствующие ощелачиванию мочи (овощи, особенно картофель, фрукты с большим содержанием клетчатки). Почти не содержат пуринов крупы, яйца, рис, молоко. В качестве разгрузочных диет при избытке солей наиболее показаны фруктовые, картофельные и молочные. Лимон может быть использован в пищу для растворения камней в комплексе со щелочным питьем.
Лечение нефропатий при нарушении обмена пуринов включает обязательное воздействие на обменные процессы. Поскольку растворимость кислот в значительной степени связана с рН среды, что регулируется объемом воды, то для увеличения растворимости уратов необходимо увеличивать объем суточной мочи, при низкой плотности мочи (1010 и менее) кристаллов не выпадает в осадок совсем. Поэтому детям показано обильное питье с целью увеличения диуреза (количества мочи). Причем распределение жидкости в течение суток должно быть равномерным и соотнесено с количеством принимаемой пищи. Примерно рассчитывается объем питья — не менее 120 мл на кг тела в сутки. Объем выпиваемой жидкости важно поддерживать и ночью, когда моча более концентрированная, что создает предпосылки для кристаллизации солей.
Кроме питьевого режима и диеты лечащие врачи назначают препараты, влияющие на метаболизм солей. Лечение продолжают длительно — от полутора до месяцев, под контролем рН мочи с помощью специальных тест-полосок. Назначаются и щелочные минеральные воды. Для активного отделения мочи и профилактики застоя назначают достаточный двигательный режим и лечебную физкультуру.
Диета при фосфатной нефропатии у ребенка
Характеризуется патологическим выделением фосфатов с мочой. Все виды заболевания подразделяют на истинную и ложную фосфатурию (выделение фосфатов с мочой). Ложная фосфатурия (наличие фосфатов в моче) возникает на фоне переизбытка в питании фосфоросодержащих продуктов — сыра, икры, говяжьей печени, овсянки, перловки, творога, шоколада, гороха, яиц и речки, а также на фоне болезней паращитовидных желез, отеков, рахита, отравлений.
Истинная фосфатная нефропатия бывает наследственной и приобретенной. Первый вид приобретается от родителей, причем чаще всего по материнской линии. Это довольно тяжелое обменное заболевание, и ранее именовалось фосфатным диабетом, потому что помимо солей в моче у пациентов наблюдаются жажда и полиурия (выделение очень больших объемов мочи), что очень сходно с первыми признаками сахарного диабета. Нарушения возникают из-за тяжелого поражения почечной ткани, которая не может нормально фильтровать мочу, и кроме солей фосфора в мочу уходят и многие другие вещества, особенно кальций, что нарушает еще и строение скелета. Клиника может напоминать выраженный рахит, но изменения в моче помогают врачу поставить верный диагноз. К счастью, такое состояние встречается очень редко.
В большинстве случаев фосфаты в моче обнаруживаются у малышей с наличием инфекции в мочевых путях, вызванной особыми организмами, способными разлагать мочевину — стафилококком, протеем, синегнойной палочкой, клебсиеллой. Поэтому наличие в моче малыша этих солей должно настроить врача и родителей на более углубленное обследование мочевой системы малыша, даже если признаков инфекции нет. Эти микроорганизмы разлагают в мочевом тракте мочевину на угольную кислоту и ам-моний. За счет этого происходит ощелачивание мочи и выпадение фосфатов в осадок. Поэтому появление в моче трипельфосфатов, аморфных фосфатов и щелочная реакция мочи являются индикатором инфекции мочевого тракта.
Лечение аналогично предыдущим нефропатиям. Немаловажную роль играет диета. Причем диетические лечебные мероприятия направлены не только на ограничение пищевых продуктов, богатых фосфатами, но и назначение пищи, тормозящей секрецию желудочного сока, и ограничение введения кальция. При фосфатурии на фоне инфекции мочевого тракта используется подкисляющая молочно-мясная диета.
Разрешаются — масло сливочное, растительное, рис, манная крупа, макароны, мука высшего и первого сорта, картофель, капуста, морковь, огурцы, свекла, томаты, абрикосы, арбуз, груши, сливы, клубника, вишня. Ограничиваются — говядина, свинина, колбаса вареная, яйцо, крупа кукурузная, мука второго сорта, молоко, сметана. Исключаются — сыр, творог, печень говяжья, мясо куриное, рыба, икра, фасоль, горох, шоколад, крупа овсяная, перловая, гречневая, пшенная. При сочетанных метаболических нару-шениях (т.е. когда есть несколько видов солей) диета назначается индивидуально.
В комплекс лечебных мероприятий входят лекарственные средства, назначенные врачом, витамины А и Е.
Как осуществляется наблюдение за детьми с нефропатией?
Наблюдение за малышами со всеми типами нефропатий в поликлинике осуществляют педиатр и нефролог. Госпитализация в стационар требуется только в случае наличия осложнений — пиелонефрита, инфекции мочевых путей, камнеобразования, либо в случае детального обследования с целью выяснения причины и уточнения диагноза.
Детям с дисметаболической нефропатией в зависимости от состояния устанавливают группу здоровья от IIб до IV. Педиатром такие малыши осматриваются ежемесячно в течение первого года наблюдения, далее один раз в три месяца, а нефрологом — раз в полгода.
Малыши сдают необходимые анализы и проходят обследования — анализ мочи контролируется ежемесячно. Причем желательно определять характер мочевого осадка, размер кристаллов солей. Проводится проба по Зимницкому, которая дает понятие о концентрационной способности почек, делают УЗИ почек и мочевого пузыря. Если потребуется, врач может назначить и рентгенологическое исследование с применением контрастных веществ.
Иногда врач просит родителей контролировать рН мочи дома специальными тест-полосками и записывать результаты. Эти данные дают возможность проводить коррекцию диеты и дозировки препаратов.
Диспансерное наблюдение осуществляют до перевода ребенка во взрослую поликлинику.
Реабилитация и профилактика нефропатии у детей
При стационарном лечении врач при выписке назначает различные виды реабилитации — ЛФК, специальные курсы гимнастики, питьевой режим и диету. Но за процессом восстановления будет следить участковый врач.
Профилактика дисметаболических нарушений включает в себя строгое соблюдение назначенной диеты, обеспечение повышенного питьевого режима (особенно летом), курсы минеральных вод (причем лучше в условиях специализированного санатория), применение курса витаминов и метаболической терапии, активная профилактика инфекций мочевой системы и ОРВИ, которые негативно влияют на течение нефропатии.
Противорецидивное (направленное на устранение обострений, предупреждающее осложнения) лечение следует проводить 2-3 раза в год, при этом нужно чередовать курсы лечения различными препаратами, чтобы к ним не возникало привыкания организма. Особо хорошо себя зарекомендовали себя курсы фитотерапии — прием травяных чаев, обладающих мочегонным, солевыводящим и общеукрепляющим, тонизирующим действием. Рекомендуются активные занятия с крохой, обеспечивающие ему достаточный объем движений.
При правильном питании и выполнении рекомендаций врача риск развития осложнений при наличии у ребенка дисметаболической нефропатии можно свести к минимуму, а у многих детей с возрастом метаболические нарушения проходят совсем. Важно заложить с детства привычку правильно питаться, вести определенный образ жизни при этом заболевании. И тогда уже во взрослом возрасте ребенок сможет избежать проблем с мочевыделительной системой.
Дисметаболическая нефропатия у детей — симптомы болезни, профилактика и лечение Дисметаболической нефропатии у детей, причины заболевания и его диагностика на EUROLAB
Что такое Дисметаболическая нефропатия у детей —
Дисметаболическая нефропатия у детей – это почечное заболевание, которое делится на виды, возникает в связи с нарушением обмена веществ.
Болезнь проявляется общими симптомами нарушения обмена веществ и изменениями в моче. Последние проявляются наличием примесей соли, белка, эритроцитов, лейкоцитов. Если вовремя не провести терапию, в некоторых случаях появляются мочекаменная болезнь, нефрит или пиелонефрит, цистит у детей и подростков.
Распространенные виды дисметаболической нефропатии:
- оксалурия (выделение оксалатов с мочой)
- уратурия (выделение уратов с мочой)
Что провоцирует / Причины Дисметаболической нефропатии у детей:
Причины дисметаболической нефропатии у ребенка:
— инфекции мочевыводящих путей
— нарушения обмена веществ (щавелевой кислоты, кальция, фосфатов, цистина, мочевой кислоты)
— эндокринные болезни
— застой мочи
— онкологические проблемы
— болезни ЖКТ (лямблиоз, глисты)
— лучевая терапия
— влияние некоторых лекарств
Причины оксалурии:
- повышенное поступление оксалатов с пищей
- наследственные дефекты некоторых ферментов
- перенесенные операции на кишечнике
- воспалительные заболевания кишечника
- язвенный колит
- болезнь Крона
- избыточное потребление аскорбиновой кислоты
- дефицит витамина В6
Причины уратурии у детей:
- повышенное потребление мясных продуктов
- наследственные причины (дефект почечных канальцев, усиленные обмен пуринов)
- длительный прием фуросемида
- лечение химиопрепаратами
Две группы предрасполагающих факторов:
— экзогенные
— эндогенные
Экзогенные факторы:
- питьевая вода высокой жесткости
- сухой и жаркий климат
- содержание микро- и макроэлементов во внешней среде (избыток кальция, недостаток магния и пр.)
- уровень солнечной радиации
- гипервитаминоз D
- дефицит витаминов А, В6, РР
- избыточное употребление продуктов с высоким содержанием пуринов, белка, щавелевой кислоты
- недостаточность питьевого режима
- недостаточное употребление продуктов с ненасыщенными жирными кислотами
- прием алкогольных напитков
- частое посещение сауны
- прием диуретиков, сульфаниламидов, цитостатиков
Эндогенные факторы:
- воспалительные процессы в почках и по ходу мочевых путей
- врожденные аномалии почек и мочевыводящих путей
- повышенные потери воды при экстраренальных потерях, физических нагрузках высокой интенсивности
- нарушение водно-солевого обмена при гиперпаратиреозе
- наследственные варианты нарушения обмена веществ
- увеличение всасывания кальция и оксалатов при повышенной проницаемости кишечной стенки
- нарушение обмена кальция у пациентов, лечение которых включает длительный постельный режим
Патогенез (что происходит?) во время Дисметаболической нефропатии у детей:
Защитные факторы заключаются в действии веществ, которые удерживают соли растворенными. Часто их называют защитными коллоидами. Такие вещества находятся в плазме крови, фильтруются в первичную и окончательную мочу, секретируются канальциевым эпителием. Если ферменты защиты недостаточны и есть предрасполагающие факторы, описанные выше, соли образую кристаллы.
При обменной нефропатии у детей кристаллы откладываются в собирательных трубочках, канальцах и интерстиции почек. Сначала развивается неспецифический воспалительный процесс, далее может развиться иммунокомплексный воспалительный процесс, который поражает разные отделы нефрона. В зависимости от того, насколько поражен нефрон, заболевание протекает в таких вариантах (которые проявляются разными симптомами):
- тубуло-интерстициальный нефрит
- острая почечная недостаточность
- мочекислый диатез
- бессимптомное течение
- уролитиаз
Дисметаболические нарушения, которые длятся долго, вызывают фиброн интерстиция, снижение канальциевых функций, что, в свою очередь, вызывает нарушение концентрационной функции почек.
Первичная оксалурия – довольно редкий вариант заболевания. У детей чаще встречается вторичная оксалурия. Большинство оксалатов, выводимых с мочой, образуются в процессе обмена веществ из аминокислот. Оксалаты могут локально формироваться в почках по причине разрушения фосфолипидов клеточных мембран. Как результат – образуются предшественники оксалатов, с которыми кальций формирует нерастворимые соли.
Мембраны распадаются по причине воздействия мембранотоксических соединений, бактериальных фосфолипаз при воспалительных процессах в почках. Морфологически выявляется выраженная деструкция щеточных каемок проксимальных и дистальных канальцев.
Симптомы Дисметаболической нефропатии у детей:
Оксалатно-кальциевая нефропатия
Этому заболеванию более всего подвержены дети. Причиной его возникновения могут являться нарушения обмена оксалатов (соли щавелевой кислоты) и обмена кальция. Оксалаты вырабатывает организм, или они могут попасть в организм с едой.
Причины, по которым могут образовываться оксалаты
- Кишечник, пораженный язвенным колитом, кишечными анастомозами, болезнью Крона.
- Повышенное синтезирование организмом.
- Чрезмерное употребление пищи с оксалатами.
Оксалатная нефропатия у детей
Заболевание может быть вызвано многими факторами. Как полагают некоторые авторы, наследственность проявляется в 70–75% случаев. Кроме того, огромную роль играют такие факторы, как: стресс, неблагоприятная экологическая обстановка, питание и т.п.
Впервые болезнь может проявиться в любом возрасте, даже у новорожденных. Но наиболее часто они проявляются в 5-7 лет. При общем анализе мочи обнаруживаются незначительное содержание белка, эритроцитов, лейкоцитов, кристаллов оксалатов. Кроме того, повышается удельная плотность мочи.
Дети, больные оксалатной нефропатией страдают от аллергии, вегетативно-сосудистой дистонии с тенденцией к гипотонии (пониженному артериальному давлению), головных болей. Но общее развитие при этом не нарушается. В период полового созревания (10-14 лет) болезнь обостряется. Скорее всего, это связано с перестройкой гормональной системы. Если оксалатная нефропатия прогрессирует, у больного может развиться мочекаменная болезнь, воспаление почек, а также бактериальная инфекция.
Фосфатная нефропатия у детей
При заболеваниях, которые сопровождаются нарушениями кальциевого и фосфорного обменов, встречается довольно часто. Но основной причиной фосфатурии является хроническое инфицирование мочевой системы. Фосфатно-кальциевая нефропатия очень часто сопутствует оксалатно-кальциевой, но выражается в гораздо меньшей степени.
Уратная нефропатия (нарушения обмена мочевой кислоты)
В сутки организм вырабатывает 570–1000 мг мочевой кислоты, треть которой секретируется в кишечник, в котором и разрушается бактериями. Оставшиеся две трети фильтруются почками. Большая часть всасывается обратно, а 6-12% профильтрованной кислоты выводятся с мочой. Первичные уратные нефропатии связаны с нарушениями обмена мочевой кислоты, вызванными наследственностью.
Вторичные уратные нефропатии являются осложнениями иных болезней, таких как хроническая гемолитическая анемия, эритремия, миеломная болезнь и др. Кроме того, могут быть вызваны применением определенных препаратов: циклоспорина А, цитостатиков, салицилатов, тиазидовых диуретиков и др. еще одной причиной могут стать нарушения физико-химических свойств мочи (при воспалении почек, например) или функции канальцев почек. Кристаллы уратов могут откладываться в почках, что становится причиной развития воспаления и снижает почечные функции.
Первые симптомы нередки уже в раннем возрасте, но чаще всего длительное время процесс протекает скрыто. В общем анализе мочи выявляют небольшое количество эритроцитов и белка, ураты. Если количество уратов большое, моча становится кирпичного цвета.
Нарушения обмена цистина у детей
Цистин – продукт обмена аминокислоты метионина. В моче цистин концентрируется по двум причинам.
1. Нарушено обратное всасывание цистина в почечных канальцах.
2. Чрезмерное накопление цистина в почках.
Накопление цистина в клетках является результатом генетической патологии фермента цистинредуктазы. Такое нарушение обмена имеет системный характер и носит название цистиноз. Внеклеточное и внутриклеточное накопление кристаллов цистина обнаруживается не только в канальцах и интерстиции почки, но и в других органах: мышечной ткани, лимфоузлах, нервной системе, печени, костном мозге, клетках периферической крови.
Обратное всасывание цистина в канальцах почек может быть нарушено в результате генетического дефекта транспортировки через стенки клеток аминокислот – орнитина, цистина, лизина, аргинина.
Диагностика Дисметаболической нефропатии у детей:
Для диагностики используют не только данные анамнеза. Обязательной является лабораторно-инструментальная диагностика. Выявляют повышение концентрации солей, проводят биохимическое исследование мочи. В общем анализе мочи у детей ищут кристаллы соли. Проводят исследование антикристаллообразующей способности мочи, тесты на кальцифилаксию и перекиси в моче, а также ультразвуковую диагностику почек.
Если кристаллы соли обнаружены только в общем анализе мочи, дисметаболическую нефропатию у детей еще не диагностируют. Иногда такое явление проходит само по себе, не требуя лечения. Чтобы подтвердить диагноз, необходимо биохимическое исследование мочи. При УЗИ можно выявить микрокамушки или включения, но эти изменения нельзя назвать специфическими именно для рассматриваемой болезни.
Лечение Дисметаболической нефропатии у детей:
Терапия дисметаболической нефропатии у детей базируется на таких принципах:
- правильный питьевой режим
- нормализация образа жизни
- специфические методы терапии
- диетотерапия
Чтобы уменьшить концентрацию растворимых веществ в моче, необходим прием большого количества жидкости. Нужно увеличить большой объем мочеиспускания, для этого ребенку дают достаточно жидкости прямо перед сном. В качестве жидкости выбирают обычную или минеральную воду (лучше – без газа). Снижение солевой нагрузки на почки снижается при помощи специальной диеты.
Лечение оксалатной нефропатии у детей
Основные принципы диетотерапии:
1. Из рациона исключают такие продукты
- крепкие мясные бульоны
- холодцы
- шпинат
- щавель
- свекла
- клюква
- морковь
- какао, шоколад, продукты с содержанием какао
2. Диета должна быть картофельно-капустной, что снижает поступление оксалатов с пищей.
3. В рацион вводят минеральные воды, чернослив, курагу и груши.
Медикаментозное лечение оксалатной нефропатии
— витамин В6
— пиридоксин
— витамин А
— токоферола ацетат (витамин Е)
— мембраностабилизаторы: ксидифон и димефосфон
— цистон (эффективен при кристаллурии)
— окись магния в дозе 0,15–0,2 г/сут
Лечение уратной нефропатии у детей
Принципы построения диеты:
— включать в рацион продукты молочные и растительные
— исключают из диеты почки, печень, бульоны на мясе, фасоль и горох, все виды орехов, какао и прочие продукты с пуриновыми основаниями
— ребенок должен пить 1-2 литра воды в сутки: минеральные воды, отвар овса, отвар укропа, полевого хвоща, брусничного или березового листа, спорыша, клевера и т.д.
Ребенку дают цитратные смеси:
Средства для снижения синтеза мочевой кислоты:
- никотинамид
- аллопуринол
- цистон
- оротовая кислота
- цистенал
- этамид
- фитолизин
Лечение фосфатной нефропатии у детей
— подкисление мочи при помощи минеральных вод и приема препаратов: метионин, аскорбиновая кислота, цистенал
— в рационе ограничивают продукты с высоким содержанием фосфора: печень, сыр, курицу, икру, бобовые, шоколад и т.п.
Лечение цистиноза и цистинурии у ребенка
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию. В рационе ограничивают рыбу, творог, мясо, яйца. Такого рациона придерживаются 4 недели, а потом расширяют, приближая к нормальному. Но всё же продолжают не давать ребенку творог, рыбу и яйца. Ребенок должен пить 2 литра жидкости в сутки, особенно перед отходом ко сну.
Медикаментозная терапия цистиноза и цистинурии:
- растворы гидрокарбоната натрия
- цитратная смесь
- блемарен
- пеницилламин или купренил в сочетании с ксидифоном и другими мембраностабилизаторами
- витамин А
При цистинозе у детей может понадобиться трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности. Этот метод увеличивает продолжительность жизни пациента на 15-19 лет.
Фитотерапия дисметаболической нефропатии у детей:
— петрушка
— можжевельник
— хвощ полевой
— листья березы
— толокнянка
— листья брусники
— зверобой
— ромашка
— пол-пола
— тысячелистник
— василек
— почечный чай
— марена красильная
Прогноз при дисметаболической нефропатии у детей
Прогноз благоприятный в большинстве случаев. Показатели в моче нормализируются, если введена выше описанная диета, проведена адекватная лекарственная терапия. Если лечение неэффективно, возникают мочекаменная болезнь и воспаление почек. Частым осложнением является пиелонефрит.
Профилактика Дисметаболической нефропатии у детей:
Чтобы ребенку не поставили диагноз «дисметаболическая нефропатия», особое внимание нужно уделить лечению и профилактике инфекций мочевой системы. Чтобы предотвратить рецидивы болезни, проводят профилактические курсы антимикробной терапии с помощью уросептиков и фитоуросептиков. Фитотерапия, которая была описана выше, применяется не только для лечения, но и в качестве профилактики рецидивов болезни. Врачи могут назначить такой препарат как канефрон.
Диетотерапия как профилактический метод
Диета назначается индивидуально. Исследователи сегодня говорят о том, что строгие диетические ограничения не рекомендованы. При составлении рациона обращают внимание в первую очередь на содержание в продуктах питания метаболитов литогенных веществ.
Для оксалатной нефропатии важен учет содержания щавелевой кислоты в продуктах питания. Щавелевой кислоты меньше всего в таких продуктах:
— рис, яичная лапша, макароны, спагетти
— сливочное масло, маргарин, сыр молоко
— говядина, курица, яйца куриные, баранина, морская рыба
— авокадо, арбуз, дыни, бананы, ананас, вишня
— брюссельская капуста, белокачанная капуста, картоефель, брокколи, редис, цветная капуста, огурцы, лук зеленый
— фруктовое желе, некоторые виды джемов и мармелада
— соки: грейпфрутовый, ананасовый, яблочный, апельсиновый
— лимонад, пепси-кола
При профилактике оксалурии в построении диеты нужно опираться на принципы диеты № 5. Исключают облигатные пищевые аллергены. Врачи могут назначить в качестве профилактической меры препараты кальция. Некоторые исследователи настаивают, что ребенку для профилактики оксалурии нужно принимать продукты, в которых содержится магний:
- тыквенные семеяки
- миндаль
- арбуз
- гречневая крупы
- овсяная крупа
- фундук
- пшеничный хлеб
- кальмары
- рисовая крупа
- печень трески
- брюссельская капуста и пр.
Увеличивают количество витаминов в рационе, особенно А и В6.
Содержание витамина В6 в продуктах
| Продукты | Содержание В6, мг/100 г |
| Грецкие орехи | 0,80 |
| Дрожжи | 0,58 |
| Ячневая крупа | 0,54 |
|
Курица |
0,52 |
| Банан | 0,38 |
| Яйцо куриное | 0,37 |
| Пшеничный, зерновой хлеб | 0,30 |
| Баранина | 0,30 |
| Картофель | 0,30 |
| Овсяная крупа | 0,27 |
Содержание витамина А в продуктах
| Продукты | Содержание витамина и провитамина А, мг на 100 г |
| Рыбий жир | 19 |
| Красный сладкий перец | 10 |
| Морковь | 9 |
| Абрикосы | 2 |
| Яйца | 0,7 |
| Сливочное масло | 0,6 |
| Сметана | 0,3 |
Для профилактики уратной дисметаболической нефропатии у детей нужно минимизировать в рационе продукты с пуринами:
- какао
- чай
- кофе
- шоколад
- селедка
- чечевица
- печень
- свинина
- карп
- бобы
- телячье и говяжье мясо
- кролик
- куриное мясо и т.д.
Животные белки врачи советуют кушать до 16 часов, из расчета 100–150 г/сутки не чаще 3 р в неделю. Лучше не давать ребенку жареные и копченые мясные блюда. Отдают предпочтение вареным продуктам. Из рациона исключают субпродукты, колбасы, холодцы, фаршевые мясопродукты, мясо молодых животных и консервы. Для профилактики уратной нефропатии ребенку дают груши, яблоки, виноград, сливы и различные цитрусовые. Среди овощей полезным действием в данном случаев обладают капуста белокачанная, картофель, морковь, свекла, огурцы и кабачки.
Для профилактики фосфатной дисметаболической нефропатии в диете ребенка ограничивают продукты с кальцием, применяют продукты с преобладанием кислотных валентностей. К таким продуктам относят:
- незрелые фрукты
- чернослив
- лук
- сухие бобы
- тыкву
- грибы
- овощи с содержанием крохмала
- сливочное масло
- кисломолочные продукты
- арахис
- соки с сахаром
- какао
- маргарин
- варенья и джемы
- мясо и рыбу
Для профилактики фосфатной дисметаболической нефропатии ребенку дают как можно меньше:
- грейпфрутов
- лимонов
- арбузов
- крыжовника
- слив
- томатов
- свеклы
К каким докторам следует обращаться если у Вас Дисметаболическая нефропатия у детей:
Педиатр
Гастроэнтеролог
Нефропатолог
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Дисметаболической нефропатии у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Если Вами ранее были выполнены какие-либо исследования, обязательно возьмите их результаты на консультацию к врачу. Если исследования выполнены не были, мы сделаем все необходимое в нашей клинике или у наших коллег в других клиниках.
У Вас ? Необходимо очень тщательно подходить к состоянию Вашего здоровья в целом. Люди уделяют недостаточно внимания симптомам заболеваний и не осознают, что эти болезни могут быть жизненно опасными. Есть много болезней, которые по началу никак не проявляют себя в нашем организме, но в итоге оказывается, что, к сожалению, их уже лечить слишком поздно. Каждое заболевание имеет свои определенные признаки, характерные внешние проявления – так называемые симптомы болезни. Определение симптомов – первый шаг в диагностике заболеваний в целом. Для этого просто необходимо по несколько раз в год проходить обследование у врача, чтобы не только предотвратить страшную болезнь, но и поддерживать здоровый дух в теле и организме в целом.
Если Вы хотите задать вопрос врачу – воспользуйтесь разделом онлайн консультации, возможно Вы найдете там ответы на свои вопросы и прочитаете советы по уходу за собой. Если Вас интересуют отзывы о клиниках и врачах – попробуйте найти нужную Вам информацию в разделе Вся медицина. Также зарегистрируйтесь на медицинском портале Eurolab, чтобы быть постоянно в курсе последних новостей и обновлений информации на сайте, которые будут автоматически высылаться Вам на почту.
Другие заболевания из группы Болезни ребенка (педиатрия):
Если Вас интересуют еще какие-нибудь виды болезней и группы заболеваний человека или у Вас есть какие-либо другие вопросы и предложения – напишите нам, мы обязательно постараемся Вам помочь.Дисметаболическая нефропатия у детей — симптомы болезни, профилактика и лечение Дисметаболической нефропатии у детей, причины заболевания и его диагностика на EUROLAB
Автор На чтение 31 мин. Опубликовано
Виды патологий и их проявления
В зависимости от причин, вызвавших болезнь, дисметаболические нефропатии делятся на первичные и вторичные. Первичные развиваются вследствие нарушений функциональности почек, мочекаменной болезни и ряда других хронических процессов в организме. Значительную роль при этом играет наследственность.
Вторичные виды дисметаболических нефропатий развиваются на фоне нарушений обмена веществ в организме. Такое нередко происходит из-за нерационального питания или продолжительного приема определенных медицинских препаратов. Причем чаще всего основной причиной дисметаболической нефропатии становится нарушение кальциевого метаболизма. По составу солей, которые выявляются в моче в ходе диагностики, различают следующие виды нефропатии:
- оксалатно-кальциевая;
- фосфатная;
- уратная;
- цистиновая;
- смешанная.
В 85-90% всех случаев у больных фиксируется именно оксалатно-кальциевая форма заболевания.
Описание и классификация
Что такое дисметаболическая нефропатия? Этим вопросом задается каждый пациент, услышав подобный диагноз. Дисметаболическая нефропатия – это собирательное название, включающее множество метаболических нарушений, которые в конечном итоге приводят к серьезным нарушениям в работе почек.
Дисметаболическая нефропатия у детей чаще бывает наследственным заболеванием. Опасно, так как приводит к серьезным осложнениям за короткий промежуток времени. У взрослых нефропатия, связанная с нарушением обменных процессов в организме, возникает в результате негативного воздействия внутренних и внешних факторов.
В зависимости от содержания веществ в урине, нефропатия у ребенка и взрослого может быть:
- Оксалатной – характеризуется повышенной концентрацией оксалатов в моче, является наиболее часто диагностируемым видом.
- Уратной – при повышенном уровне мочевой кислоты.
- Фосфатной – в ходе клинических исследований обнаруживается рост фосфатов.
- Цистиновой – развивается в результате нарушения обмена метионина, что приводит к повышению цистина.
- Смешанная – в моче повышается одновременно уровень оксалатов, уратов, фосфатов и цистина.
Причины возникновения
Основной причиной нефропатии является нарушение обменных процессов в организме из-за врожденных и приобретенных патологий мочевыделительных органов. К нарушению метаболизма приводит уролитиаз, воспалительные процессы в мочеполовых органах, аномальное строение и расположение органов мочевыделительной системы, из-за которого происходит обратный заброс мочи и ее застой.


Негативное воздействие на обмен веществ во взрослом и детском организме оказывает длительное лечение гормональными препаратами и некоторыми другими видами лекарств, радиационное и лучевое облучение, отравление токсическими соединениями.
Так как общие моменты возникновения нефропатии уже разобрали выше, необходимо по классификации определить конкретные причины развития. В частном порядке можно разобрать некоторые виды нарушений обмена веществ в составе дисметаболической нефропатии.
Патология с выявлением оксалатов (солей щавелевой кислоты) развивается в связи с нарушением обмена самой кислоты и солей кальция. В формировании оксалатной нефропатии играет значительную роль дефицит некоторых витаминов и минералов (ретинол, альфа-токоферол, пиридоксин, магний, калий). Данное состояние может наблюдаться во время лечения рахита, когда имеет место передозировка витамином Д. Также часто у детей наблюдается оксалатная нефропатия при нарушении правильного питания (избыточное поступление оксалатов с пищей).
Наибольшая концентрация оксалатов (щавелевой кислоты) достигается в следующих продуктах: какао, щавель, петрушка, ревень, свёкла.
Важно помнить, что нефропатия может развиваться не только экзогенным путём, а также и эндогенным. Нарушение обмена щавелевой кислоты часто сочетается с другой патологией. Чаще это заболевания желудочно-кишечного тракта (болезнь Крона, колит, энтерит, панкреатит, дисфункция желчевыводящей системы), но также могут быть и эндокринные патологии (сахарный диабет).
Уратная нефропатия
Другой составляющей дисметаболической патологии является уратная нефропатия. Такое состояние характеризуется отложением мочевой кислоты в почках, а также их обнаружение в осадке мочи. Уратная нефропатия может носить как первичный (наследственный) характер, так и вторичный (приобретённый). Наследственное заболевание встречается редко и рассматривается в составе генетических заболеваний.
Приобретённая нефропатия также протекает с другими заболеваниями (гемолитическая, миеломная болезнь, воспалительные изменения почек). В качестве неблагоприятного фактора, запускающего механизм нарушения обмена мочевой кислоты, может быть длительный приём «агрессивных» лекарственных препаратов (цитостатики, диуретики).
Фосфатная обменная нефропатия — последняя из дисметаболических нарушений, которая характеризуется накоплением и выведением солей (фосфатов) с мочой. Данное состояние протекает в виде вторичной патологии наряду с заболеваниями почек (пиелонефрит, инфекция мочевыводящей системы, тубулоинтерстициальный нефрит).
Обменная форма нефропатии возникает при воздействии целого комплекса факторов. К примеру, первичная форма заболевания нередко развивается по причине нарушений обменных процессов у родителей ребенка. Накопленные генетические мутации провоцируют ухудшение метаболизма, что затрудняет предстоящее лечение.
Среди общих причин, приводящих к дисметаболической нефропатии, выделяют:
- интоксикацию;
- чрезмерные физические нагрузки;
- продолжительное применение медикаментов;
- монодефицитные диеты.
Вторичная обменная нефропатия развивается по причине передозировки определенными веществами или из-за замедления их вывода из организма. В норме моча должна содержать растворенные соли. Однако при воздействии ряда причин они кристаллизуются и выпадают в осадок.
К таким факторам относят:
- жаркий и сухой климат;
- недостаток витаминов;
- жесткая вода;
- профицит протеинов, щавелевой кислоты, пуринов;
- алкоголизм;
- лечение диуретиками, цитостатиками и сульфаниламидами;
- частые походы в сауну.
Выделяют также внутренние факторы:
- врожденные нарушения почек и мочеточников;
- сбои в гормональном фоне;
- инфекции мочевыводящих путей;
- продолжительное соблюдение постельного режима;
- иммобилизация;
- наследственные нарушения метаболизма.


соли в моче
Данные факторы приводят к формированию солей и их скоплению в почечных тканях. В результате запускается воспалительный процесс. Местное отложение кристаллов провоцирует появление камней в почках.
Нередко возникновение дисметаболической нефропатии у детей, страдающих нервно-артрическим диатезом. На развитие болезни могут повлиять осложнения во время беременности матери, в том числе токсикоз на поздних сроках, гипоксия плода.
Кроме того, выделяют множество частных причин дисметаболической нефропатии, которые связаны непосредственно с видом заболевания. Оксалатная форма обуславливается нарушением метаболизма оксалатов: солей, кальция, щавелевой кислоты. Провоцирующим фактором для развития патологии становится недостаток витаминов А, Е, В6 и избыток витамином D вследствие лечения рахита, нехватка калия и магния, а также профицит оксалатов из-за определенных продуктов.
При уратной форме дисметаболической нефропатии в почках откладываются ураты – соли натрия, которые также выделяются с мочой. Первичная форма болезни поражает детей, страдающих синдромом Леша-Найхана, вторичная протекают на фоне миеломы, пиелонефрита, гемолитической анемии, эритремии. Уратная нефропатия почек может быть спровоцирована приемом цитостатических средств, тиазидовых диуретиков, сциклоспорина А, салицилатов.
Фосфатурию провоцируют хронические инфекции мочевых путей, гиперпаратиреоз, поражения центральной нервной системы. Цистинурия развивается на фоне цистиноза и характеризуется отложением кристаллов цистина в кровяных клетках, лимфатических узлах, печени, селезенке, тканях мышц и нервов, костном мозге, почках. Вторичная форма цистинурии развивается при наличии пиелонефрита и тубулярного интерстициального нефрита.
Причины дисметаболической нефропатии у ребенка:
– инфекции мочевыводящих путей
– нарушения обмена веществ (щавелевой кислоты, кальция, фосфатов, цистина, мочевой кислоты)
– эндокринные болезни
– застой мочи
– онкологические проблемы
– болезни ЖКТ (лямблиоз, глисты)
– лучевая терапия
– влияние некоторых лекарств
Причины оксалурии:
- повышенное поступление оксалатов с пищей
- наследственные дефекты некоторых ферментов
- перенесенные операции на кишечнике
- воспалительные заболевания кишечника
- язвенный колит
- болезнь Крона
- избыточное потребление аскорбиновой кислоты
- дефицит витамина В6
Причины уратурии у детей:
- повышенное потребление мясных продуктов
- наследственные причины (дефект почечных канальцев, усиленные обмен пуринов)
- длительный прием фуросемида
- лечение химиопрепаратами
Две группы предрасполагающих факторов:
– экзогенные
– эндогенные
Экзогенные факторы:
- питьевая вода высокой жесткости
- сухой и жаркий климат
- содержание микро- и макроэлементов во внешней среде (избыток кальция, недостаток магния и пр.)
- уровень солнечной радиации
- гипервитаминоз D
- дефицит витаминов А, В6, РР
- избыточное употребление продуктов с высоким содержанием пуринов, белка, щавелевой кислоты
- недостаточность питьевого режима
- недостаточное употребление продуктов с ненасыщенными жирными кислотами
- прием алкогольных напитков
- частое посещение сауны
- прием диуретиков, сульфаниламидов, цитостатиков
Эндогенные факторы:
- воспалительные процессы в почках и по ходу мочевых путей
- врожденные аномалии почек и мочевыводящих путей
- повышенные потери воды при экстраренальных потерях, физических нагрузках высокой интенсивности
- нарушение водно-солевого обмена при гиперпаратиреозе
- наследственные варианты нарушения обмена веществ
- увеличение всасывания кальция и оксалатов при повышенной проницаемости кишечной стенки
- нарушение обмена кальция у пациентов, лечение которых включает длительный постельный режим
Признаки оксалатной формы дисметаболической нефропатии могут диагностироваться сразу после рождения, но чаще всего такое заболевание протекает бессимптомно в течение продолжительного времени. По статистике у большинства больных детей есть родственники страдающие подагрой, мочекаменной и желчнокаменной болезнями, спондилезом, артропатией, сахарным диабетом.
Факт кристаллизации обычно диагностируется в возрасте 5–7 лет, причем происходит это случайно по результатам стандартного исследования мочи. Однако родители могут заметить изменения в моче ребенка самостоятельно – она становится мутной, выпадает осадок, а на стенках горшка образуется стойкий налет.
При внимательном отношении к детям дисметаболическую нефропатию можно диагностировать на ранних стадиях, что облегчит лечение в дальнейшем.Кроме того, дети, страдающие данной патологией, подвержены ряду болезней, среди которых присутствуют:
- кожные аллергические высыпания;
- диспепсия;
- головные боли;
- вегето-сосудистая дистония;
- энурез;
- ожирение;
- мышечная гипотония;
- зуд и покраснение в паховой области.
У ребенка страдающего дисметаболической нефропатией наблюдаются следующие симптомы:
- быстрая утомляемость;
- колющие боли в спине;
- вздутие живота;
- частые позывы в туалет;
- болезненность мочеиспускания;
- субфебрильная температура тела.
Если Вас интересуют еще какие-нибудь виды болезней и группы заболеваний человека или у Вас есть какие-либо другие вопросы и предложения –
напишите нам
, мы обязательно постараемся Вам помочь.
Симптоматика болезни
Дисметаболические нефропатии, вне зависимости от вида, сопровождаются нарушением очистительной функции, уролитиазом и пиелонефритом. Для заболеваний почек свойственно расстройство мочеиспускания, которое сопровождается болями, резями и жжением в мочевыделительном канале, снижением объема мочи.
При дисфункции почек нарушается работа сердечно-сосудистой системы, что проявляется повышением/снижением артериального давления, тахикардией. Со стороны пищеварительного тракта отмечается ухудшение аппетита, метеоризм, запоры.
Из-за ухудшения отхождения мочи нарастает отечность, жажда. Пациент жалуется на регулярные головные боли и чрезмерную потливость. В результате нарушенного обмена у ребенка может развиться склонность к аллергии, избыточному весу. Обострение симптомов приходится на переходный возраст, что связано с гормональными изменениями в детском организме.
Проявляется заболевание у детей следующим образом:
- повышенная потливость;
- жажда;
- сердечные боли;
- снижение аппетита;
- боли в области живота;
- запоры;
- энурез или другие расстройства мочевой системы;
- головные боли;
- сухость кожи;
- отечность век, особенно утром.
Оксалатно-кальциевая нефропатия
Этому заболеванию более всего подвержены дети. Причиной его возникновения могут являться нарушения обмена оксалатов (соли щавелевой кислоты) и обмена кальция. Оксалаты вырабатывает организм, или они могут попасть в организм с едой.
Причины, по которым могут образовываться оксалаты
- Кишечник, пораженный язвенным колитом, кишечными анастомозами, болезнью Крона.
- Повышенное синтезирование организмом.
- Чрезмерное употребление пищи с оксалатами.
Оксалатная нефропатия у детей
Заболевание может быть вызвано многими факторами. Как полагают некоторые авторы, наследственность проявляется в 70–75% случаев. Кроме того, огромную роль играют такие факторы, как: стресс, неблагоприятная экологическая обстановка, питание и т.п.
Впервые болезнь может проявиться в любом возрасте, даже у новорожденных. Но наиболее часто они проявляются в 5-7 лет. При общем анализе мочи обнаруживаются незначительное содержание белка, эритроцитов, лейкоцитов, кристаллов оксалатов. Кроме того, повышается удельная плотность мочи.
Дети, больные оксалатной нефропатией страдают от аллергии, вегетативно-сосудистой дистонии с тенденцией к гипотонии (пониженному артериальному давлению), головных болей. Но общее развитие при этом не нарушается. В период полового созревания (10-14 лет) болезнь обостряется. Скорее всего, это связано с перестройкой гормональной системы. Если оксалатная нефропатия прогрессирует, у больного может развиться мочекаменная болезнь, воспаление почек, а также бактериальная инфекция.
Фосфатная нефропатия у детей
При заболеваниях, которые сопровождаются нарушениями кальциевого и фосфорного обменов, встречается довольно часто. Но основной причиной фосфатурии является хроническое инфицирование мочевой системы. Фосфатно-кальциевая нефропатия очень часто сопутствует оксалатно-кальциевой, но выражается в гораздо меньшей степени.
Уратная нефропатия (нарушения обмена мочевой кислоты)
В сутки организм вырабатывает 570–1000 мг мочевой кислоты, треть которой секретируется в кишечник, в котором и разрушается бактериями. Оставшиеся две трети фильтруются почками. Большая часть всасывается обратно, а 6-12% профильтрованной кислоты выводятся с мочой. Первичные уратные нефропатии связаны с нарушениями обмена мочевой кислоты, вызванными наследственностью.
Вторичные уратные нефропатии являются осложнениями иных болезней, таких как хроническая гемолитическая анемия, эритремия, миеломная болезнь и др. Кроме того, могут быть вызваны применением определенных препаратов: циклоспорина А, цитостатиков, салицилатов, тиазидовых диуретиков и др. еще одной причиной могут стать нарушения физико-химических свойств мочи (при воспалении почек, например) или функции канальцев почек. Кристаллы уратов могут откладываться в почках, что становится причиной развития воспаления и снижает почечные функции.
Первые симптомы нередки уже в раннем возрасте, но чаще всего длительное время процесс протекает скрыто. В общем анализе мочи выявляют небольшое количество эритроцитов и белка, ураты. Если количество уратов большое, моча становится кирпичного цвета.
Нарушения обмена цистина у детей
Цистин – продукт обмена аминокислоты метионина. В моче цистин концентрируется по двум причинам.
1. Нарушено обратное всасывание цистина в почечных канальцах.
2. Чрезмерное накопление цистина в почках.
Накопление цистина в клетках является результатом генетической патологии фермента цистинредуктазы. Такое нарушение обмена имеет системный характер и носит название цистиноз. Внеклеточное и внутриклеточное накопление кристаллов цистина обнаруживается не только в канальцах и интерстиции почки, но и в других органах: мышечной ткани, лимфоузлах, нервной системе, печени, костном мозге, клетках периферической крови.
Обратное всасывание цистина в канальцах почек может быть нарушено в результате генетического дефекта транспортировки через стенки клеток аминокислот – орнитина, цистина, лизина, аргинина.
Клинические проявления дисметаболической нефропатии не специфичны. Поэтому на основании симптомов заболевания диагноз поставить невозможно. Патологические изменения в мочевом осадке выявляют случайно при диспансерном наблюдении в возрасте 3 — 5 лет.
Родители могут заметить жёлтый налёт на поверхности горшка, который без усилий не отмывается.
Одновременно у некоторых пациентов могут присутствовать симптомы интоксикации (головная боль, слабость, вялость, снижение аппетита). Но такие проявления слабо выражены.
Иногда можно наблюдать снижение артериального давления, а также повышение массы тела. Типичная клиническая картина, характерная для заболеваний почек, отсутствует.
Возможно уменьшение объёма выделяемой мочи за сутки, при этом никогда не наблюдается появление отёков. Вследствие того, что диурез снижается, моча приобретает более концентрированный цвет и мутный характер.
В соответствие с видом нефропатии, клинические проявления могут также различаться. Важно знать некоторые особенности, характерные для той или иной формы обменных нарушений.
При оксалатной нефропатии нередко наблюдается болевой синдром в области живота. Маленькие пациенты не могут с точностью определить локализацию боли. Появляются болезненные ощущения при мочеиспускании.
Уратные нефропатии также характеризуются появлением абдоминальных болей, которые трудно локализовать. А также могут наблюдаться болезненные ощущения в области поясницы, издалека напоминающие почечную колику. Объём мочи за сутки снижается.
При фосфатурии характерно появление болей в животе только для фосфатно-кальциевой кристаллурии.
Для диагностики используют не только данные анамнеза. Обязательной является лабораторно-инструментальная диагностика. Выявляют повышение концентрации солей, проводят биохимическое исследование мочи. В общем анализе мочи у детей ищут кристаллы соли. Проводят исследование антикристаллообразующей способности мочи, тесты на кальцифилаксию и перекиси в моче, а также ультразвуковую диагностику почек.
Если кристаллы соли обнаружены только в общем анализе мочи, дисметаболическую нефропатию у детей еще не диагностируют. Иногда такое явление проходит само по себе, не требуя лечения. Чтобы подтвердить диагноз, необходимо биохимическое исследование мочи. При УЗИ можно выявить микрокамушки или включения, но эти изменения нельзя назвать специфическими именно для рассматриваемой болезни.
На начальных этапах заболевания обменными нефропатиями может заниматься педиатр. Если у доктора появляются сомнения или болезнь имеет тяжёлое течение, наблюдается риск развития осложнений, то педиатр может направить на консультацию ребёнка к детскому урологу или нефрологу.
Наследственный анамнез, как правило, отягощён. У родственников могут наблюдаться заболевания мочевыделительной системы, желудочно-кишечного тракта, обменные нарушения, воспалительные заболевания суставов.
Диагностический поиск имеет свои особенности при различных видах нефропатий. При постановке диагноза важно обращать внимание на присутствие других заболеваний, существование которых могло спровоцировать формирование обменных нарушений.
В случае постановки диагноза оксалатной нефропатии имеют значение заболевания желудочно-кишечного, билиарного и мочеполового трактов, эндокринные и аллергические заболевания.


Диагностика метаболических нефропатий должна обязательно в себя включать: биохимическое исследование осадка мочи, при необходимости возможно дополнительное исследование (специальные пробы, определяющие функциональную способность почек). К инструментальным методам можно отнести ультразвуковое исследование почек и мочевыводящих путей.
Итак, разберём вопросы диагностики. При оксалатном обменном нарушении наблюдаются изменения в общем анализе мочи (увеличение концентрации, моча внешне имеет насыщенный цвет и мутный осадок, появляется белок и эритроциты, а также кристаллы оксалата кальция).
При выявлении оксалатов необходимо выполнить биохимический анализ мочи, позволяющий определить суточное количество. При оксалатной нефропатии выделение оксалатов у детей достигает более 20 мг/сутки. Ультразвуковое исследование почек и мочевыводящих путей может указывать на отложение солей на стенках органов (повышение эхогенности паренхимы почек, лоханок, мочеточников).
Уратная нефропатия также имеет свои особенности в диагностике. В общем анализе мочи можно наблюдать повышенную концентрацию, выпадение осадка, увеличение количества белка и эритроцитов, а также кристаллов мочевой кислоты. Биохимический анализ крови указывает на увеличение концентрации мочевой кислоты, альбуминов.
Фосфатная форма обменных нарушений характеризуется следующим изменением в общем анализе мочи — сдвигом рН в щелочную сторону, тогда как в норме среда кислая. Осадок также наблюдается, но он имеет белый оттенок. В осадке наблюдается большое количество кристаллов фосфата (более 2,5 мкг). Также в моче выявляют бактерии с уреазной активностью.
Чтобы назначить адекватное лечение дисметаболической нефропатии, врачу необходимо провести обследование, главной целью которой является обнаружение кристаллизации. Все процедуры проходят под наблюдением педиатра, детского уролога и нефролога.
Кристаллизация выявляется по результатам УЗИ почек и мочевого пузыря. Обнаруженные кристаллы свидетельствуют о присутствии песка или конкрементов. Проводится анализ мочи на биохимические показатели, определяющий увеличенное содержание солей. Дополнительно берутся функциональные пробы мочи, проводится анализ ее микрофлоры.
Оксалатная нефропатия
Оксалурия является наиболее распространенным видом нефропатий, развивающихся в результате нарушения обмена веществ. Делится на 2 подвида: оксалатно-калициевую нефропатию и оксалатурию. Первая развивается при нарушении процесса транспортировки и усвоения кальция, фосфора и щавелевой кислоты. Оксалатурия – вид нефропатии, который возникает при нарушении обмена щавелевой кислоты в организме. Данный вид нефропатии может развиться в любом возрасте, даже у новорожденных.
Причины и симптомы
Более чем в половине случаев оксалатная нефропатия является врожденной патологией и развивается при наследственном дефиците некоторых ферментов, что негативно сказывается на обмене веществ. Повышению количества оксалатов способствуют воспалительные патологии органов пищеварительного тракта, язвы, болезнь Крона.
Еще одной причиной является неправильное питание с повышенным содержанием щавелевой и аскорбиновой кислоты и недостаточным поступлением витамина В6. Также к повышению уровня щавелевой кислоты приводит недостаток жидкости в организме.
Заподозрить развитие заболевание крайне тяжело, так как оксалатурия редко оказывает отрицательное влияние на состояние здоровья. Обнаруживается случайно по результатам планового исследования мочи. При оксалатурии в урине повышается содержание оксалатов, уровень белка, лейкоцитов и эритроцитов. Также происходит рост плотности урины.
При подозрении на оксалатную нефропатию ребенку необходимо сдать суточную урину на определение концентрации солей. Важное место в постановке диагноза играет УЗИ органов мочевыделительной системы, которое помогает определить расположение, размеры и свойства оксалатов.
На основе полученных диагностических данных оксалатная дисметаболическая нефропатия у детей лечится с помощью изменения рациона и назначения лекарственных препаратов. Диета поможет снизить нагрузку на почки и сократить поступление щавелевой и аскорбиновой кислот в организм вместе с пищей. Под запрет попадают все мясные и рыбные продукты и блюда из них.
Также следует исключить зелень, кислые ягоды и фрукты, свеклу, морковь и продукты, содержащие какао. В рацион необходимо включить сухофрукты, груши, яблоки, арбузы, дыни, картофель и капусту. Важно соблюдать питьевой режим, рекомендованный врачом, – вода способствует вымыванию лишних солей из организма.


Достаточное поступление витаминов группы В способствует улучшению обмена жиров и антиоксидантов. Витамин А нормализует процесс расщепления и усвоения белка и сахара. Витамин Е улучшает связь белка и сахаров в клетках. Для снижения концентрации оксалатов рекомендуется принимать окись магния.
Терапия дисметаболической нефропатии у детей базируется на таких принципах:
- правильный питьевой режим
- нормализация образа жизни
- специфические методы терапии
- диетотерапия
Чтобы уменьшить концентрацию растворимых веществ в моче, необходим прием большого количества жидкости. Нужно увеличить большой объем мочеиспускания, для этого ребенку дают достаточно жидкости прямо перед сном. В качестве жидкости выбирают обычную или минеральную воду (лучше – без газа). Снижение солевой нагрузки на почки снижается при помощи специальной диеты.
Лечение оксалатной нефропатии у детей
Основные принципы диетотерапии:
1. Из рациона исключают такие продукты
- крепкие мясные бульоны
- холодцы
- шпинат
- щавель
- свекла
- клюква
- морковь
- какао, шоколад, продукты с содержанием какао
2. Диета должна быть картофельно-капустной, что снижает поступление оксалатов с пищей.
3. В рацион вводят минеральные воды, чернослив, курагу и груши.
Медикаментозное лечение оксалатной нефропатии
– витамин В6
– пиридоксин
– витамин А
– токоферола ацетат (витамин Е)
– мембраностабилизаторы: ксидифон и димефосфон
– цистон (эффективен при кристаллурии)
– окись магния в дозе 0,15–0,2 г/сут
Лечение уратной нефропатии у детей
Принципы построения диеты:
– включать в рацион продукты молочные и растительные
– исключают из диеты почки, печень, бульоны на мясе, фасоль и горох, все виды орехов, какао и прочие продукты с пуриновыми основаниями
– ребенок должен пить 1-2 литра воды в сутки: минеральные воды, отвар овса, отвар укропа, полевого хвоща, брусничного или березового листа, спорыша, клевера и т.д.
Ребенку дают цитратные смеси:
Средства для снижения синтеза мочевой кислоты:
- никотинамид
- аллопуринол
- цистон
- оротовая кислота
- цистенал
- этамид
- фитолизин
Лечение фосфатной нефропатии у детей
– подкисление мочи при помощи минеральных вод и приема препаратов: метионин, аскорбиновая кислота, цистенал
– в рационе ограничивают продукты с высоким содержанием фосфора: печень, сыр, курицу, икру, бобовые, шоколад и т.п.
Лечение цистиноза и цистинурии у ребенка
Лечение цистиноза и цистинурии включает диету, высокожидкостный режим и медикаментозную терапию. В рационе ограничивают рыбу, творог, мясо, яйца. Такого рациона придерживаются 4 недели, а потом расширяют, приближая к нормальному. Но всё же продолжают не давать ребенку творог, рыбу и яйца. Ребенок должен пить 2 литра жидкости в сутки, особенно перед отходом ко сну.
Медикаментозная терапия цистиноза и цистинурии:
- растворы гидрокарбоната натрия
- цитратная смесь
- блемарен
- пеницилламин или купренил в сочетании с ксидифоном и другими мембраностабилизаторами
- витамин А
При цистинозе у детей может понадобиться трансплантация почки, которая проводится до развития терминальной стадии хронической почечной недостаточности. Этот метод увеличивает продолжительность жизни пациента на 15-19 лет.
Фитотерапия дисметаболической нефропатии у детей:
– петрушка
– можжевельник
– хвощ полевой
– листья березы
– толокнянка
– листья брусники
– зверобой
– ромашка
– пол-пола
– тысячелистник
– василек
– почечный чай
– марена красильная
Прогноз при дисметаболической нефропатии у детей
Прогноз благоприятный в большинстве случаев. Показатели в моче нормализируются, если введена выше описанная диета, проведена адекватная лекарственная терапия. Если лечение неэффективно, возникают мочекаменная болезнь и воспаление почек. Частым осложнением является пиелонефрит.
Если есть признаки, что у детей развивается такое заболевание, тогда стоит обратиться за помощью к врачу. Он назначит терапию, которая будет сводиться к следующему:
- нормальный жизненный уклад, правильный распорядок дня, нормальный сон;
- соблюдение режима питья;
- специфические терапевтические методы;
- диета.
Данная патология требует уменьшения концентрации растворимого вещества в моче. Один из эффективных способов — это увеличение объема выделяемой мочи в ночное время. Это достигается благодаря принятой жидкости перед ночным отдыхом. Лечение этого заболевания требует, чтобы предпочтение отдавалось минеральной лечебной
Дисметаболическая нефропатия у детей что это такое диета


Что такое дисметаболическая нефропатия?
Это заболевание вызвано нарушением обменных процессов, в результате чего изменяется состав мочи. В ней обнаруживается повышенное содержание белка, эритроцитов, лейкоцитов и солей. Последние приводят к возникновению камней и развитию мочекаменной болезни, повреждению почечных структур, нарушению функционирования почек.
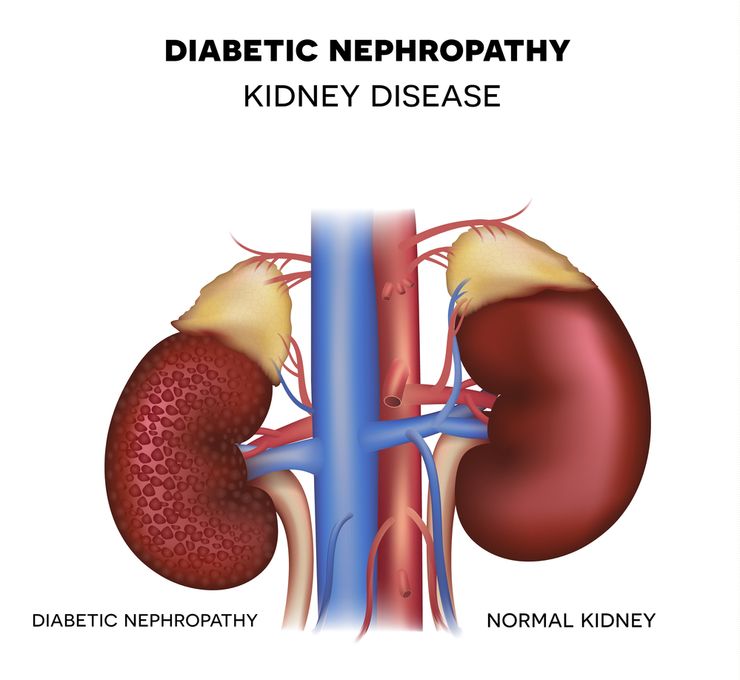

Дисметаболическая нефропатия у детей сопровождается структурными изменениями почек
К сожалению, за последние годы дисметаболическая нефропатия (ДН) помолодела. Она диагностируется даже у детей младшей возрастной группы, в возрасте 4–5 лет, что значительно ухудшает прогнозы.
Причины
Дисметаболическая нефропатия чаще развивается у детей при воздействии нескольких предрасполагающих факторов, которые могут быть внутренними или внешними. К первым принадлежат обменные нарушения, в частности нарушенный обмен оксалатов, кальция, фосфатов, уратов, цистина, триптофана.
Не последнюю роль в появлении ДН играют такие факторы:
- наследственность;
- врожденные аномалии почек и мочевых путей;
- избыток или дефицит витаминов и полезных веществ – А, В6, С, Д, Е, магния и калия;
- гемолитическая анемия;
- энтерит, колит, болезнь Крона;
- панкреатит;
- мезаденит;
- болезни желудочно-кишечного тракта;
- глистные инвазии;
- сахарный диабет;
- эндокринные нарушения, например гиперфункция паращитовидных желез;
- пиелонефрит;
- дискинезия желчевыводящих путей;
- миеломная болезнь;
- инфекция мочевыводящих путей;
- онкологические заболевания, когда есть необходимость проведения курса химиотерапии или облучения.
Вероятность появления признаков данной болезни повышается при воздействии внешних факторов. К ним принадлежат:
- интоксикация или отравление;
- прием медикаментов, в частности длительная терапия цитостатиками, диуретиками, циклоспоринами или салицилатами;
- неправильное или скудное питание, повышение доли животных белков, щавелевой кислоты в рационе ребенка;
- сухой и жаркий климат, воздействие интенсивного ультрафиолетового излучения;
- неблагоприятная экологическая обстановка;
- несоблюдение питьевого режима, употребление воды повышенной жесткости;
- тяжелые физические нагрузки.
В группе риска также находятся дети, рожденные при беременности, протекавшей с гипоксией и токсикозом.
Классификация
Согласно этиологии происхождения существует две формы:
- первичная – вызвана наследственной предрасположенностью и возникшими вследствие этого обменными нарушениями;
- вторичная – развивается на фоне болезней, воздействия неблагоприятных факторов окружающей среды.
Первичная форма чаще сопровождается возникновением осложнений.
Существует классификация в зависимости от состава солей. Есть такие разновидности ДН:
Первая разновидность встречается в 80–90% случаев, вызвана нарушенным обменом кальция.
Симптомы
Для заболевания характерно латентное течение, то есть болезнь может не давать о себе знать длительное время. Чаще выявляется случайно в ходе обследования. Именно изменение мочи – первый признак ДН. Меняется не только ее состав, но также и цвет. Она становится мутной; если долго находится в горшке, то выпадает осадок, на стенках может оставаться налет, который без бытовой химии тяжело удалить.
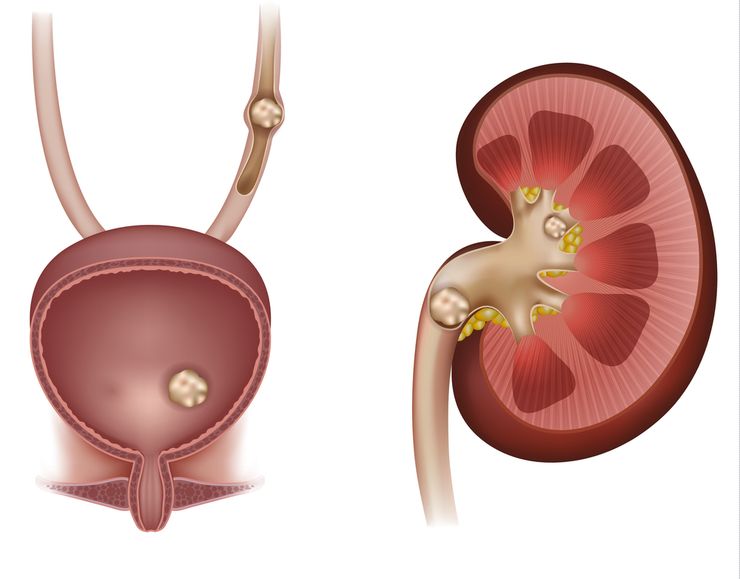

При образовании камней симптомы становятся более выраженными
Основные признаки болезни:
- головная боль;
- усталость;
- мышечная слабость;
- боль в пояснице, в области почек;
- субфебрильная температура тела;
- покраснение в области половых органов, зуд, дискомфортные ощущения;
- вздутие живота;
- аллергические высыпания на коже;
- понижение артериального давления;
- вегето-сосудистая дистония;
- лишний вес.
Накопление солей сопровождается воспалением, запускается процесс формирования камней, мочеиспускание становится болезненным, возможен энурез.
Диагностика
При появлении симптомов ДН ребенка нужно показать педиатру, а затем нефрологу и урологу. Именно эти специалисты назначат комплексное обследование:
- общий анализ мочи;
- пробы мочи по Земницкому;
- моча по Нечипоренко;
- определение кислотности.
Если в анализах заметны отклонения, назначается инструментальная диагностика, которая предполагает УЗИ органов мочевыделительной системы.
Лечение
Терапия не базируется на одних только медицинских препаратах. Основу составляет изменение рациона питания и питьевого режима. Клинические рекомендации следующие:
- увеличение объема потребляемой жидкости до 1,5–2 литров в день;
- принудительное мочеиспускание каждые 2 ч. для очищения почек;
- диета.
Без диетического питания выздоровление невозможно. Подбор диеты осуществляется врачом исходя из вида заболевания. При оксалатной ДН стоит отдать предпочтение капусте и картофелю. Именно эти овощи снижают уровень оксалатов. Полезно есть сухофрукты, пить минеральную воду. Нужно отказаться от наваристых мясных бульонов, свеклы, моркови, щавелевой кислоты, которая содержится в щавеле, а также от продуктов, содержащих какао.

Клинические рекомендации играют важную роль в лечении
При повышении содержания уратов стоит исключить мясные блюда, животные субпродукты и бобовые. Полезна молочная продукция и растительная пища. При фосфатной ДН стоит ограничить потребление фосфатных продуктов, например бобовых, шоколада. Подкисление мочи производится с помощью минеральной воды. Также оправдан прием витамина С.
При цистинозе нельзя употреблять в пищу продукты, богатые серой и метионином. Поэтому из рациона ребенка исключается рыбная и мясная пища, под запретом творог и яйца. Диетического питания стоит придерживаться не менее месяца. Возвращаться к обычному меню можно только после одобрения врача.
В лечении заболеваний мочевыводящей системы важен именно питьевой режим. Чем чаще происходит мочеиспускание, тем меньше вероятность отложения солей и формирования камней.
Одновременно с диетическим питанием проводится медикаментозное лечение, которое предполагает использование антиоксидантов, фитопрепаратов и витаминных средств. Медикаменты назначаются врачом.
При отсутствии правильного и эффективного лечения могут возникнуть последствия в виде моче- или желчнокаменной болезни, пиелонефрита, цистита, артропатии, подагры. Самым тяжелым осложнением является почечная недостаточность.
Профилактика
Профилактические мероприятия предполагают терапию существующих заболеваний и поддержание нормальных обменных процессов. Важно обеспечить ребенка всеми необходимыми питательными веществами, для этого питание должно быть сбалансированным, пищевая ценность продуктов подобрана по возрасту.
При обменных нарушениях нужно придерживаться диеты. Также необходимо укреплять иммунитет ребенка, не допускать переохлаждения и оградить малыша от сильных стрессов.
Прогноз при данном заболевании благоприятный. Главное – нормализовать состав мочи до появления осложнений. После стоит беречь ребенка, поскольку он находится в группе риска, важно следить за тем, что он ест и сколько он пьет жидкости.
Дисметаболическая нефропатия – группа почечных заболеваний. Они развиваются вследствие нарушения вещественного обмена. Если заболевание данного типа у ребенка прогрессирует, тогда это приводит к почечному воспалению, циститу или мочекаменной болезни.


Симптомы
Проявляется заболевание у детей следующим образом:
- повышенная потливость;
- жажда;
- сердечные боли;
- снижение аппетита;
- боли в области живота;
- запоры;
- энурез или другие расстройства мочевой системы;
- головные боли;
- сухость кожи;
- отечность век, особенно утром.
Лечение
Если есть признаки, что у детей развивается такое заболевание, тогда стоит обратиться за помощью к врачу. Он назначит терапию, которая будет сводиться к следующему:
- нормальный жизненный уклад, правильный распорядок дня, нормальный сон;
- соблюдение режима питья;
- специфические терапевтические методы;
- диета.
Данная патология требует уменьшения концентрации растворимого вещества в моче. Один из эффективных способов — это увеличение объема выделяемой мочи в ночное время. Это достигается благодаря принятой жидкости перед ночным отдыхом. Лечение этого заболевания требует, чтобы предпочтение отдавалось минеральной лечебной или обычной воде.
Кристаллообразование предупреждает лечение специфической терапией. Благодаря ей у детей из организма выводятся соли и нормализуются процессы обмена. Дисметаболическая нефропатия включает в себя разные заболевания, которые требуют своего подхода.
Лечение оксалатной нефропатии включает антиоксиданты и мембранотропные препараты:
- мембраностабилизирующее действие оказывают витамины А, В6, также препараты ксидифон, димефосфон и магне В6;
- антиоксидантное действие оказывает витамин Е;
- цистон назначают при кристаллургии;
- если обнаружено высокое содержание оксалатов, тогда лечение производится окисью магния.
При урартном виде заболевания лечение производится:
- цитратными смесями, такими, как магурлит и уралит-У, соломик и блемарен – это требуется для того, чтобы в организме поддерживался нужный уровень цитратных смесей;
- для уменьшения мочевой кислоты используют препараты никотинамид и аллопуринол. Следует сказать, что аллопуринол назначается строго под контролем врача, так как может вызвать разные виды осложнений.
Лечение фосфатного вида заболевания должно быть направлено на то, чтобы подкислить мочу, назначаются препараты:
Лечение изначально необходимо направить на подщелачивание мочи, для чего используются минеральные щелочные воды, гидрокрбонатриевые растворы, цитратная смесь. Также лечение производится:
- пеницилламином или купренилом для недопущения кристаллизации и цистиновой растворимости;
- мембраностабилизирующие средства – витамин А и Е;
- антибактериальная терапия;
- трансплантация почки, если есть подозрение на развитие хронического заболевания – почечной недостаточности. Но, к сожалению, это не является панацеей, так как уже через десять лет, возможно, чуть больше, цистиноз начинает развиваться и в донорской почке.
Диета


Данная патология требует и соблюдения особого режима питания.
Оксалатная нефропатия включает такие особенности диеты для детей:
- капустно-картофельное питание, при котором оксалаты поступают в меньшем количестве, что уменьшает нагрузку на почки;
- также необходимо ввести в рацион такие продукты, как чернослив и курага, груши;
- исключаются – мясные наваристые бульоны и холодцы, овощи – морковь и свекла, травы – шпинат и щавель, ягоды клюквы, сладкое – шоколад и какао;
- воду нужно пить ежедневно от трех до пяти литров.
Уратный вид заболевания у детей требует особенного режима питания:
- продукты, богатые на пуриновые основания исключаются. Это почки и печень, бульоны, сваренные на мясной основе, фасоль и горох, какао и орехи и т.п.;
- ввести в питание необходимо растительные и молочные продукты;
- Употреблять воду нужно в количестве одного-двух литров каждый день. Желательно, чтобы это была слабоминерализованная и слабощелочная вода. Также можно принимать настои трав из укропа и хвоща полевого, березового и брусничного листа, спорыша и клевера, отвар овса.
Фосфатная нефропатия ограничивает питание детей продуктами, богатых на содержание фосфора. Это бобовые и шоколад, мясо курицы и печень, икра и сыр.
Для цистиноза диета необходима, чтобы предотвратить попадание продуктов питания, которые содержат метионин и другие кислоты. Из-за этого необходимо ограничить рацион детей употреблением мясом и рыбой, яйцами и творогом и т.п.
Но так как метионин нужен организму крохи для роста, нельзя применять длительно ограниченную диету. И поэтому уже через месяц рацион питания у детей расширяется. Воду необходимо употреблять ежедневно в количестве двух литров и обязательно перед сном.
Стоит понимать, что при первичном заболевании, прогноз далеко не благоприятный, так как процесс развивается быстро и может перерасти в почечную недостаточность. Вторичные признаки заболевания характеризуются уже благоприятным течением.
Если придерживаться всех рекомендаций врача, соблюдать диетический и питьевой режим, применять медикаментозную терапию, тогда можно добиться нормализации показателей мочи. Также необходимо вовремя диагностировать инфекционные заболевания, в противном случае они могут привести к нежелательным осложнениям.
Дисметаболическая нефропатия – болезнь почек, которая характеризуется структурными и функциональными изменениями в органе. Основная причина развития патологии – нарушение обменных процессов. Заболевание протекает с множеством симптомов, устранить которые можно медикаментами, диетой, фитотерапией.
Дисметаболическая нефропатия и ее особенности
Обменная нефропатия у детей и взрослых имеет код по МКБ-10 — N16.3. Болезнь характеризуется повышением уровня содержания в моче солей (ураты, оксалаты, фосфаты), что последует за собой повреждение почечных структур.
Условия развития описываемой аномалии включают в себя целый спектр предпосылок. В педиатрии встречаются случаи, когда детская болезнь развивается на фоне следующих патологических состояний:


проникновение инфекции в мочевыводящий путь;- нарушение обменных процессов в организме в отношении таких кислот, как мочевая и щавелевая, а также фосфатных, кальциевых соединений;
- сопутствующее развитие эндокринного заболевания;
- застойные процессы в мочевыводящих путях;
- онкологическое заболевание;
- патология желудочно-кишечного тракта;
- глистные инвазии;
- лечение некоторыми лекарственными препаратами, в том числе — проведение лучевой терапии.
Дисметаболическая обменная нефропатия у детей, а именно – оксалатурия, связана с такими предпосылками:
- повышением объема оксалатов в организме, поступающих из продуктов питания;
- наследственным дефектом некоторых ферментов;
- перенесенным оперативным вмешательством на кишечнике;
- заболеванием кишечника воспалительного характера;
- язвенным колитом;
- болезнью Крона, избыточным содержанием в организме витамина С;
- недостаточным содержанием в организме витамина В6.
Обменная уратная нефропатия у ребенка часто развивается по таким причинам:
На развитие нефропатии у ребенка влияют экзогенные и эндогенные факторы. В первую группу относят:
- употребление воды, имеющей высокую жесткость;


проживание в условиях сухого и жаркого климата;- превышение в организме объема витамина Д и недостаток ретинола, В6 и РР;
- злоупотребление пищей с высоким содержанием белков, щавелевой кислоты, пуринов;
- нарушенный питьевой режим;
- злоупотребление алкогольными напитками.
К эндогенным факторам относят:
- Развитие воспалительного заболевания в парном органе или в иных мочевыводящих путях.
- Врожденное нарушение строения почек или иного мочевыводящего пути.
- Усиленную потерю жидкости организмом, что возникает, например, на фоне физической нагрузки.
- Наследственное нарушение обменных процессов.
- Повышенную проницаемость кишечных стенок, что увеличивает всасывание кальция и оксалатных соединений.
Дети с обменной нефропатией входят в группу риса по возникновению болезней, таких как пиелонефрит, интерстициальный нефрит мочекаменная патология.
Организм выполняет множество защитных функций, одной из которых выступает удержание солей нерастворенными, что обеспечивается действием определенных веществ – коллоидов. Их секреция происходит посредством канальцевых эпителиальных клеток. При недостаточном функционировании таковых формируются солевые отложения по типу кристаллов, что и характеризует патогенез болезни.
При дисметаболической нефропатии у детей отложение кристаллов наблюдается в области собирательных трубочек, канальцев и интерстиции парного органа. На начальном этапе происходит развитие неспецифического воспалительного процесса, который со временем переходит в иммунокомплексное воспаление, вовлекающее в поражение различные зоны нефронов.
С учетом уровня поражения почки дисметаболическое заболевание может протекать в нескольких формах:
- в виде тубуло-интерстициального нефрита;
- острой почечной недостаточности;
- мочекислого диатеза;
- уролитиаза;
- в бессимптомной форме.


История болезни и соответствующие наблюдения в педиатрии подтверждают большую частоту диагностирования нефропатии вторичного типа. Первичная патология встречается редко.
Чтобы подобрать правильное лечение, необходимо опираться на приведенную ниже классификацию. Учитывая, какой обмен нарушается в организме, выделяют 4 вида нефропатии:
- Оксалатная, связанная с нарушением обмена кальциевых соединений и солей щавелевой кислоты.
- Уратная, связанная с отложением в органе мочевых кислот, их кристаллов.
- Фосфатная, связанная с нарушением обмена фосфатных соединений.
- Цистиновая, связанная с отложением кристаллов метионина (аминокислота).
Терапия нефропатии разного вида как у детей, так и у взрослых будет отличаться. Обобщенный метод лечения патологий не существует.
Клинические симптомы дисметаболической патологии у грудничков возникают редко. Первые проявления заболевания развиваются лишь к 5-7 годам. До этого времени оно протекает в скрытой форме. В комплексе с обменной нефропатией часто происходит развитие подагры, спондилеза, мочекаменной болезни, сахарного диабета, артропатии.
Дети имеют склонность к аллергической реакции на эпидермисе, к таким патологиям, как гипотония, вегето-сосудистая дистония, артралгия, ожирение. Ребенок быстро утомляется, возникает колющий болевой синдром в поясничном отделе, дискомфорт при мочеиспускании, мышечная слабость, диспепсия.
Усиливаются симптомы и признаки нефропатии в своей интенсивности в пубертатный период, что вызвано гормональной перестройкой.
Если своевременно начать лечение заболевания, можно надеяться на благоприятный прогноз. При длительном развитии патологии могут возникать осложнения: 

- Воспалительный процесс в чашках и лоханках органа острого или хронического характера (пиелонефрит).
- Воспалительный процесс в почечных канальцах (нефрит).
- Формирование камнеподобных отложений в органе (мочекаменная болезнь).
Среди наиболее опасных негативных последствий – развитие хронической почечной недостаточности.
В первую очередь, необходимо посетить доктора-терапевта. В обязательном порядке требуются консультации нефролога и детского уролога. По мнению известного педиатра Комаровского, наиболее информативными методами диагностики нефропатии выступают лабораторные:
- Общий анализ мочи: диагностируется кристаллурия, протеинурия, гематурия, цилиндрурия, абактериальная лейкоцитурия.
- Биохимический анализ мочи: диагностируется повышение концентрации определенных солей.
- Функциональная проба мочи по Нечипоренко, Зимницкому, Аддису-Каковскому.
- Определение уровня рН урины.
- Бактериологическая диагностика урины на микрофлору.
УЗИ парного органа назначают как средство, позволяющее выявить кристалловые отложения, – песок или камни.
Дифференциальный анализ проводят с транзиторной кристаллурией, вызванной острой респираторной инфекцией.
Описание лечебного процесса
Лечебные рекомендации сводятся к соблюдению правильного питания и режима питья, приему лекарственных препаратов. Особенности терапии могут отличаться в зависимости от типа нефропатии (уратной, фосфатной и др.).
Медикаменты для ребенка любого года жизни должен назначать только врач. Такое лечение контролируется специалистом.


Учитывая вид нефропатии, могут использоваться следующие препараты:
Любая дисметаболическая нефропатия требует достаточной водной нагрузки, что позволяет уменьшить объем содержания в моче солей. Эффективно принудительное опорожнение пузыря по специальному режиму – каждые 2 часа.
При разных типах нефропатии у ребенка требуется отличительная диета. Например, если в организме преобладают оксалаты, исключают следующие продукты:
- мясной бульон;
- холодец;
- свеклу и морковь;
- щавель, шпинат;
- смородину и клюкву;
- какао.
Наоборот, полезными при оксалатах будут картошка, капуста, курага и чернослив, груша.
При фосфатной нефропатии нет существенных ограничений по питанию, однако стоит уменьшить употребление:
- молока и продуктов, его содержащих;
- солений и копченостей;
- сладостей, выпечки.
Полезны при фосфатурии мясо, рыба, крупы, овощи и фрукты с кислинкой.
Если диагностирован цистиноз, требуется уменьшить потребление белок-содержащих продуктов. На запущенном этапе развития диета не эффективна. В таком случае проводят трансплантацию органа.
При уратах требуется исключение из рациона такой пищи:
- мяса и мясного бульона;
- орехов и бобовых;
- сладостей, сдобы;
- какао;
- жирных, жареных, острых продуктов.
Полезной при уратах будет молочная продукция, крупы, овощи и фрукты.
Профилактика и прогноз
В большинстве случаев прогноз при дисметаболической нефропатии у детей и взрослых благоприятный. Если придерживаться правильного питания, проводить лекарственную терапию, уже за короткий период времени можно добиться нормализации состава мочи.
Не всегда назначенное лечение дает положительные результаты. В некоторых случаях, особенно при неполноценной терапии, могут развиваться осложнения – пиелонефрит, почечная недостаточность и др. Чтобы предотвратить негативные последствия и заболевание в целом, рекомендуется 

придерживаться следующих правил:
- правильно питаться;
- соблюдать питьевой режим;
- своевременно выявлять и лечить провоцирующие патологии;
- 2 раза в год проходить контрольные обследования мочевыводящих путей.
Для предупреждения рецидива заболевания врач назначает курсы антимикробной терапии уросептиками и фитоуросептиками. В любом случае ребенка ставят на диспансерный учет. Что касается армии, подросток годен к прохождению военной службы, но только при отсутствии сопутствующих осложнений.
Дисметаболическая нефропатия у ребенка или взрослого пациента – не приговор. Несмотря на благоприятный прогноз, полагаться на самолечение все же не стоит. Любое заболевание требует квалифицированной помощи.
Нефропатия почек у детей (дисметаболическая нефропатия) — это заболевание почек вследствие нарушения обмена веществ в детском организме. Различают первичную и вторичную нефропатию.
Первичная нефропатия обусловлена наследственным фактором. В данном случае отмечается прогрессирующее течение, раннее развитие мочекаменной болезни и хронической почечной недостаточности. Данная форма нефропатии встречается довольно редко.
Вторичная дисметаболическая нефропатия связана с поступлением в организм некоторых веществ, при этом нарушается их обмен вследствие дисфункции некоторых органов и их систем. Нарушение функций пищеварительной система, например, может быть связано с приемом некоторых лекарств.
В основном дисметаболические нефропатии возникают вследствие нарушения обмена кальция, избытка щавелевой кислоты, фосфатов, оксалатов или уратов. Бывают смешанные нефропатии.
Чаще всего возникает у детей. Причина — в нарушении обмена кальция и солей щавелевой кислоты. Оксалаты поступают в организм с продуктами питания или же синтезируются в самом организме.
Оксалаты образуются вследствие воздействия следующих факторов:
- Повышенное содержание оксалатов в пище.
- Болезни кишечника, в том числе наследственные (болезнь Крона), язвенные колиты и др.
- Повышенный синтез оксалатов организмом.
В данном случае кроме генетического фактора огромную роль играет влияние окружающей среды, стресс, питание, физическое перенапряжение. Заболевание может проявиться в любом возрасте, даже у младенцев. Общее состояние и развитие детей с данной формой нефропатии обычно не изменено, однако для них характерны, как правило, такие нарушения обмена веществ как ожирение, аллергия, ВСД, головные боли.
Обострение заболевания может происходить в период полового созревания и гормональной перестройки организма. Прогрессируя, оксалатная нефропатия почек у детей может привести к формированию мочекаменной болезни, присоединению инфекции и появлению воспаления почек.
Основной причиной данной формы нефропатии почек у детей является нарушение фосфорно-кальциевого обмена и хронический инфекционный процесс в почках.
Вызвано нарушением обмена уратов (мочевой кислоты). Кристаллы уратных солей откладываются и накапливаются в ткани почек, нарушая их функцию. Моча при накоплении уратов становится насыщенного кирпичного цвета.
Данная форма нефропатии почек у детей связана с генетическим дефектом. Цистин представляет собой продукт обмена аминокислот метионинов. При этом отмечается избыток накопления цистина и нарушение процессов обратного всасывания в канальцах почек.
Прогрессируя, заболевание приводит к мочекаменной болезни и воспалению почек вследствие присоединения инфекционного процесса.
Для выявления заболевания проводят:
- УЗИ почек;
- анализы мочи клинические с выявлением кристаллов солей;
- проведение тестов АКОСМ, кальцифилаксию.
Лечение должно быть комплексным и направленным на выполнение следующих правил:
- Здоровый образ жизни.
- Рациональное питание и организация питьевого режима.
- Диета.
- Специфическая терапия.
Увеличивается объем потребляемой жидкости, благодаря чему снижается концентрация в моче растворимых веществ. Кроме того, целенаправленно повышают ночной объем мочеиспусканий благодаря приему жидкости перед сном. При этом лучше всего пить минеральную или простую чистую воду. Снижается солевая нагрузка на почки в результате назначения диеты.
При оксалатной нефропатии почек у детей исключаются мясные бульоны, щавель, морковь, какао, шоколад, клюква, свекла. Рекомендуется употребление картофеля, капусты, кураги, чернослива, груш. Назначают прием минеральных вод (Славяновская, Смирновская). Назначают витамины А, Е, В6, препараты магния.
При уратной нефропатии предпочтение отдается молочной и растительной диете. Ограничивается потребление мясных продуктов, фасоли, орехов, какао. Важным моментом является достаточное потребление жидкости (до двух литров в сутки). Минеральную воду нужно пить слабощелочную. Предпочтительно пить отвары хвоща полевого, укропа, спорыша, березовых почек. Хорошо помогает отвар из овса. Под строгим наблюдением назначают аллопуринол и никотинамид, фитолизин.
При фосфатной нефропатии почек у детей назначают минеральные воды Нарзан, Дзау-Суар. Из препаратов: цистинал, витамин С, метионин. Ограничивают потребление сыра, печени, шоколада, икры.
Цистиновую нефропатию лечат с помощью диеты, включающей в себя ограничение или исключение из рациона рыбы, яиц, мяса, творога. Минеральные воды желательно потреблять щелочные. Важно потреблять не менее двух литров жидкости. Полезно пить много перед сном.
Длительно осуществляют лечение пеницилламином, а также его менее токсичным аналогом купренилом. Назначают прием витаминов А, Е. Кроме того, при цистинозе успешно применяют трансплантацию почки, которую следует проводить в молодом возрасте, желательно до 18−19 лет. Однако существует опасность поражения пересаженной почки также.
Прогноз при нефропатиях почек у детей обычно благоприятный при соблюдении всех норм лечения и профилактики обострений данного заболевания.
Профилактические мероприятия направлены обычно на поддержание и соблюдение строгой диеты, плановые осмотры и лабораторно-инструментальные методы исследования функций почек, проведение анализов мочи.
Осуществляют санаторно-курортное лечение и оздоровление детей. Желательно посещать минеральные источники курортов Моршина, Трускавца и т.д.
Нефропатия: симптомы и лечение диабетической нефропатии, дисметаболической, токсической
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Антибиотики
- Антисептики
- Биологически активные добавки
- Витамины
- Гинекологические
- Гормональные
- Дерматологические
- Диабетические
- Для глаз
- Для крови
- Для нервной системы
- Для печени
- Для повышения потенции
- Для полости рта
- Для похудения
- Для суставов
- Для ушей
- Желудочно-кишечные
- Кардиологические
- Контрацептивы
- Мочегонные
- Обезболивающие
- От аллергии
- От кашля
- От насморка
- Повышение иммунитета
- Противовирусные
- Противогрибковые
- Противомикробные
- Противоопухолевые
- Противопаразитарные
- Противопростудные
- Сердечно-сосудистые
- Урологические
- Другие лекарства
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- Ортопедия и травматология
- Питание
- Пластическая хирургия
- Процедуры и операции
- Психология
- Роды и послеродовый период
- Сексология
- Стоматология
- Травы и продукты
- Трихология
- Другие статьи
- Словарь терминов
- [А] Абазия .. Ацидоз
- [Б] Базофилы .. Богатая тромбоцитами плазма
- [В] Вазопрессин .. Выкидыш
- [Г] Галлюциногены .. Грязи лечебные
- [Д] Деацетилазы гистонов .. Дофамин
- [Ж] Железы .. Жиры
- [И] Иммунитет .. Искусственная кома
- [К] Каверна .. Кумарин
- [Л] Лапароскоп .. Лучевая терапия
- [М] Макрофаги .. Мутация
- [Н] Наркоз .. Нистагм
- [О] Онкоген .. Отек
- [П] Паллиативная помощь .. Пульс
- [Р] Реабилитация .. Родинка (невус)
- [С] Секретин .. Сыворотка крови
- [Т] Таламус .. Тучные клетки
- [У] Урсоловая кислота
- [Ф]
Симптомы, стадии, причины и лечение
Диабетическая нефропатия — это хроническое заболевание почек, которое может поражать людей с диабетом. Это происходит, когда высокий уровень глюкозы в крови нарушает работу почек.
Диабетическая нефропатия — это разновидность хронической болезни почек (ХБП). Почки помогают регулировать уровень жидкости и солей в организме, что жизненно важно для контроля артериального давления и защиты сердечно-сосудистой системы.
Когда человек страдает диабетом типа 1, типа 2 или гестационным диабетом, его организм не может использовать или производить инсулин должным образом.Гестационный диабет возникает во время беременности и может повысить риск развития диабета 2 типа в более позднем возрасте.
Диабет приводит к повышению уровня сахара в крови. Со временем этот высокий уровень глюкозы может повредить различные области тела, включая сердечно-сосудистую систему и почки. Возникающее в результате повреждение почек известно как диабетическая нефропатия.
Диабетическая нефропатия — основная причина хронической болезни почек и терминальной стадии почечной недостаточности (ESRD). При ХПН почки перестают работать достаточно хорошо, чтобы удовлетворять потребности повседневной жизни.ТПН может привести к почечной недостаточности с потенциально опасными для жизни последствиями.
В этой статье рассматривается, как диабет может повлиять на почки, доступные методы лечения и способы снижения риска.
Узнайте больше о диабете 1 и 2 типа.
Нефропатия может поражать людей с любым типом диабета, потому что она возникает в результате повреждения из-за высокого уровня глюкозы в крови.
Высокий уровень глюкозы в крови влияет на артерии в организме, и почки фильтруют кровь из этих артерий.
Авторы исследования, проведенного в 2016 году, отмечают, что у 20–40% людей с диабетом развивается какое-либо заболевание почек.
Анализы могут показать, что у человека есть одно или оба из следующих признаков:
Высокий уровень альбумина в моче : Когда почки здоровы, моча не должна содержать ни одного белка, известного как альбумин.
Низкая скорость клубочковой фильтрации (СКФ) : Ключевая функция почек — фильтровать кровь. Повреждение почек влияет на их способность делать это.В идеале почки должны функционировать на 100% или иметь СКФ 100. Если тесты показывают, что СКФ составляет 60% или выше, врач не диагностирует заболевание почек. У 15–60% наблюдается заболевание почек. Ниже 15% указывает на почечную недостаточность.
ХПН — последняя стадия заболевания почек. Диабетическая нефропатия — наиболее частая причина ТПН в США. Примерно 40–50% всех случаев ТПН связаны с диабетом. Человеку с ХПН потребуется диализ.
Контроль уровня сахара в крови может снизить риск.Независимо от того, страдает ли человек диабетом 1 или 2 типа, он может снизить риск диабетической нефропатии с помощью:
- мониторинга уровня глюкозы в крови и поддержания его в пределах целевого диапазона
- при соблюдении здоровой диеты с низким содержанием сахара и соли
- регулярные физические упражнения
- в соответствии с планом лечения, который может включать использование инсулина или других лекарств
- поддержание здорового веса
Что такое хроническая болезнь почек? Узнайте больше здесь.
Повреждение почек создает нагрузку на эти жизненно важные органы и препятствует их нормальной работе.
Когда это происходит:
- организм начинает терять белок с мочой
- почки не могут удалить продукты жизнедеятельности из крови
- почки не могут поддерживать здоровый уровень жидкости в организме
Диабетическая нефропатия развивается медленно. Согласно одному исследованию, у трети людей наблюдается высокий уровень альбумина в моче через 15 лет после установления диагноза диабет.Однако менее чем у половины этих людей разовьется полная нефропатия.
Статистика показывает, что заболевание почек редко встречается у людей, страдающих диабетом менее 10 лет. Кроме того, если у человека нет клинических признаков нефропатии через 20-25 лет после начала диабета, вероятность его развития в дальнейшем у него низкая.
Диабетическая нефропатия менее вероятна, если человек с диабетом эффективно контролирует уровень глюкозы.
Высокий уровень глюкозы в крови увеличивает риск высокого кровяного давления из-за повреждения кровеносных сосудов.Высокое кровяное давление или гипертония могут способствовать заболеванию почек.
Другие факторы риска
К другим факторам риска относятся:
Курение : повреждение почек может быть результатом связи между курением и повышенным уровнем воспаления. Хотя связь между курением и диабетом остается неясной, похоже, что среди курящих людей чаще встречается диабет, а также гипертония и заболевания почек.
Возраст : Заболевание почек, особенно низкая СКФ, чаще встречается у людей в возрасте 65 лет и старше.
Пол : Заболевание чаще встречается у мужчин, чем у женщин.
Раса, этническая принадлежность или и то, и другое : Это чаще встречается у афроамериканцев, коренных американцев и американцев азиатского происхождения.
Состояние здоровья : Ожирение, хроническое воспаление, высокое кровяное давление, инсулинорезистентность и повышенный уровень липидов (жиров) в крови могут способствовать заболеванию почек.
Некоторые из этих рисков либо являются, либо являются факторами, способствующими развитию диабета или его осложнениями.
Диабетическая нефропатия — это не то же самое, что диабетическая невропатия, поражающая нервную систему. Узнайте больше о диабетической нейропатии и периферической невопатии.
На ранних стадиях диабетической нефропатии человек может не замечать никаких симптомов. Однако изменения артериального давления и баланса жидкости в организме могут уже присутствовать. Со временем продукты жизнедеятельности могут накапливаться в крови, что приводит к появлению симптомов.
Этапы
Врач может разбить стадии заболевания почек в зависимости от СКФ, которая также представляет собой процент эффективной функции почек.
Стадия 1 : Поражение почек присутствует, но функция почек нормальная и СКФ 90% или выше.
Стадия 2 : Повреждение почек с некоторой потерей функции и СКФ 60–89%.
Стадия 3 : потеря функции от легкой до тяжелой и СКФ 30–59%.
Стадия 4 : Серьезная потеря функции и СКФ 15–29%.
Стадия 5 : Почечная недостаточность и СКФ менее 15%.
Симптомы
Поделиться на Pinterest Человек с нефропатией 4 или 5 стадии может заметить такие симптомы, как темная моча.На ранних стадиях человек может не замечать никаких симптомов. На стадии 4 или 5 они могут плохо себя чувствовать и испытывать следующие симптомы:
- опухшие лодыжки, ступни, голени или руки из-за задержки воды
- более темная моча из-за крови в моче
- одышка
- усталость из-за недостатка кислорода в крови
- тошнота или рвота
- металлический привкус во рту
Осложнения поздней стадии заболевания почек включают сердечно-сосудистые заболевания.
Следование плану лечения диабета и регулярные медицинские осмотры могут помочь человеку с диабетом контролировать уровень сахара в крови, снизить риск проблем с почками и как можно раньше определить, нужно ли ему действовать.
При скрининге человек сдает анализ мочи для проверки наличия белков в моче. Однако наличие белков в моче не обязательно указывает на заболевание почек, так как это также может быть связано с инфекцией мочевыводящих путей.
Раннее лечение может отсрочить или предотвратить развитие диабетической нефропатии.
Основная цель лечения — поддержание и контроль уровня глюкозы в крови и артериального давления. Это может включать использование лекарств.
Медикаментозное лечение
Ингибиторы ангиотензинпревращающего фермента (АПФ) или блокаторы рецепторов ангиотензина (БРА) могут помочь снизить артериальное давление, защитить функцию почек и предотвратить дальнейшее повреждение.
Врач также может прописать витамин D, поскольку у людей с заболеваниями почек часто низкий уровень витамина D, или статины для снижения уровня холестерина.
В 2018 году Американский колледж кардиологов выпустил руководящие принципы, рекомендующие использование ингибиторов натрий-глюкозного котранспортера 2 (SGLT2) или агонистов рецепторов глюкагоноподобного пептида-1 (GLP-1RA) для людей с диабетом 2 типа и ХБП. Эти препараты могут снизить риск прогрессирования CDK, сердечно-сосудистых событий или того и другого.
Диетические изменения
Если человек страдает заболеванием почек, его врач может попросить его отслеживать следующие питательные вещества:
Вода : Несмотря на необходимость, слишком много воды или жидкости может увеличить риск отека и высокого кровяного давления
Натрий : Может повышать кровяное давление, поскольку входит в состав соли.
Белок : У человека с заболеванием почек белок может вызывать накопление шлаков в крови, оказывая дополнительное давление на почки.
Фосфор : встречается во многих белковых и молочных продуктах. Слишком много фосфора может ослабить кости и оказать давление на почки.
Калий : Люди с заболеванием почек могут иметь более высокий уровень калия, чем здоровый, что может повлиять на нервные клетки.
Щелкните здесь, чтобы узнать больше о продуктах с высоким содержанием калия, которых следует избегать людям с заболеваниями почек.
Контроль уровня сахара в крови
Это очень важно для снижения риска осложнений диабета, таких как заболевания почек, сердечно-сосудистые заболевания и диабетическая невропатия, поражающая нервную систему.
Эти условия также могут привести к дальнейшим осложнениям. Контроль уровня сахара в крови также может помочь предотвратить их развитие.
Если диабетическая нефропатия прогрессирует до ТПН, человеку потребуется диализ или трансплантация почки. Обычно им требуется диализ до конца жизни или до тех пор, пока не будет доступна трансплантация почки.
Диализ
Диализ почек — это процедура, при которой обычно используется аппарат для отделения продуктов жизнедеятельности из крови и удаления их из организма. Диализ заменяет здоровую почку.
Существуют различные типы диализа:
Гемодиализ : Кровь покидает тело через иглу в предплечье и проходит через трубку в диализный аппарат. Машина фильтрует кровь за пределами тела, и кровь возвращается через другую трубку и иглу.
Человек может делать это от трех до семи раз в неделю и проводить от 2 до 10 часов в сеансе, в зависимости от выбранного им варианта.
Человек может пройти диализ в диализном центре или дома, а в некоторых местах доступны варианты на ночь. Гибкие варианты все чаще позволяют людям приспособить диализ к работе и личному графику.
Перитонеальный диализ : При этом используется внутренняя оболочка брюшной полости или брюшины для фильтрации крови внутри тела.
- При непрерывном амбулаторном перитонеальном диализе (CAPD) диализирующая жидкость попадает в брюшную полость через катетер. Жидкость остается внутри в течение нескольких часов, фильтруя отходы перед сливом. Слив длится 30–40 минут.
- При непрерывном перитонеальном диализе с помощью циклера (CCPD) или автоматическом перитонеальном диализе человек проводит 8–10 часов в течение ночи, подключенный к диализному аппарату, пока он спит. Машина контролирует слив жидкости.
Человек может проводить перитонеальный диализ дома, на работе или во время путешествия.Он предлагает гибкость и позволяет человеку контролировать свое состояние. Человеку нужно будет научиться пользоваться необходимым оборудованием и убедиться, что у него есть все необходимое, например, для путешествий.
Пересадка почки
Врач может порекомендовать трансплантацию почки, если диабетическая нефропатия достигает последней стадии и если подходящий донор может предоставить почку. Поиск донора может занять некоторое время.
Человек может выжить только с одной работающей почкой, поэтому некоторые предлагают пожертвовать почку, например, близкому человеку.
Однако человек, получивший почку, может обнаружить, что его тело отвергает новый орган. Трансплантация от члена семьи обычно дает организму наилучшие шансы принять почку.
Человеку с трансплантатом почки нужно будет принимать лекарства, чтобы снизить риск отторжения новой почки. Это может иметь некоторые побочные эффекты, например, повышать риск развития инфекции.
Финансовая помощь доступна многим. По данным Национального института диабета, болезней органов пищеварения и почек (NIDDK), Medicare и Medicaid обычно покрывают лечение почечной недостаточности.
Человек может получить Medicare от ESRD в любом возрасте, если выполняются все следующие условия:
- Его почки больше не работают.
- Им нужен регулярный диализ или им была сделана трансплантация почки.
- Они проработали необходимое время в системе социального обеспечения, в Пенсионном управлении железной дороги или в качестве государственного служащего.
- Они уже получают или имеют право на пенсионные пособия по социальному обеспечению или железнодорожному транспорту.
- Они являются супругами или детьми-иждивенцами кого-то, кто соответствует любому из вышеуказанных требований.
Человек должен поговорить со своей страховой компанией или врачом о возможных вариантах.
Лучший способ снизить риск диабетической нефропатии для людей с диабетом — это правильно контролировать уровень сахара в крови и артериальное давление.
Изменения образа жизни, которые могут помочь в этом, включают:
- соблюдение питательной диеты с высоким содержанием клетчатки и низким содержанием сахара, переработанных углеводов и соли
- регулярные упражнения
- ограничение потребления алкоголя
- отказ от табака
- проверка крови уровень глюкозы регулярно
- после любого плана лечения, который предлагает их врач
- ограничение стресса там, где это возможно
Как можно больше узнать о диабете и его осложнениях, включая заболевание почек, он может чувствовать себя более уверенно и лучше контролировать их состояние и способы его предотвращения.
Национальная образовательная программа NIDDK по заболеваниям почек предоставляет загружаемые записи с результатами тестов, которые могут помочь человеку отслеживать свои тесты почек и прогресс.
Перспективы людей с диабетической нефропатией будут зависеть от того, насколько хорошо они контролируют уровень сахара и артериального давления в крови, а также от стадии, на которой им поставят диагноз. Чем раньше начнется лечение, тем лучше прогноз.
Лечение может замедлить или предотвратить прогрессирование диабетической нефропатии.Люди с диабетом должны пройти обследование, как рекомендует их врач, и предпринять ранние шаги, чтобы предотвратить прогрессирование заболевания почек.
Узнайте больше о том, как работают почки.
Q:
Можно ли обратить вспять повреждение почек, если оно началось?
A:
В зависимости от причины можно лечить некоторые типы заболеваний почек и замедлять прогрессирование поражения. Например, лекарство от высокого кровяного давления, называемое ингибитором АПФ, может сохранить некоторую функцию почек.Определенные диетические предпочтения могут снизить нагрузку на почки. У каждого человека могут быть разные вещи, которые следует учитывать, поэтому лучше поговорить с врачом о способах предотвращения или замедления поражения почек, с которым связан диабет.
Дебора Уэтерспун, доктор философии, RN, CRNA Ответы отражают мнение наших медицинских экспертов. Весь контент носит исключительно информационный характер и не может рассматриваться как медицинский совет. .Причины, симптомы и варианты лечения
Проверено с медицинской точки зрения Drugs.com. Последнее обновление: 11 октября 2019 г.
Что такое диабетическая нефропатия?

Диабетическая нефропатия — заболевание почек, являющееся осложнением диабета. Это может произойти у людей с диабетом 2 типа, который наиболее распространен и вызван резистентностью к инсулину, или у людей с диабетом 1 типа, который чаще возникает в раннем возрасте и является следствием снижения выработки инсулина.Диабетическая нефропатия вызывается повреждением мельчайших кровеносных сосудов. Когда мелкие кровеносные сосуды начинают повреждаться, обе почки начинают выделять белки с мочой. По мере продолжения повреждения кровеносных сосудов почки постепенно теряют способность удалять продукты жизнедеятельности из крови.
До 40% людей с диабетом 1 типа в конечном итоге развивают серьезное заболевание почек, которое иногда требует диализа или трансплантации почки.Лишь от четырех до шести процентов всех пациентов с диабетом 2 типа в конечном итоге требуется диализ, хотя примерно у 20–30% людей с диабетом 2 типа разовьется по крайней мере некоторое повреждение почек. Около 40 процентов всех людей, которым необходимо начать диализ, страдают почечной недостаточностью от диабета 1 или 2 типа.
Симптомы
На ранних стадиях диабетической нефропатии симптомы обычно отсутствуют. Когда симптомы действительно начинают появляться, они могут включать отек лодыжек и легкую усталость.Поздние симптомы включают сильную усталость, тошноту, рвоту и меньшее мочеиспускание, чем обычно.
Диагностика
Первым признаком поражения почек является белок в моче, который врач может измерить в микроскопических количествах, что называется микроальбуминурией. Небольшое количество альбумина обнаруживается в моче за 5-10 лет до серьезного повреждения почек.
Если у вас диабет, ваш врач порекомендует вам регулярно проверять анализы мочи и крови, чтобы проверять здоровье ваших почек.
Иногда врача может беспокоить, что повреждение почек у диабетика связано с отдельной проблемой. В этом случае могут быть рекомендованы другие тесты, такие как УЗИ или биопсия почки. При биопсии небольшой кусочек ткани почек удаляется через иглу и исследуется в лаборатории.
Ожидаемая длительность
Заболевание почек нельзя обратить вспять после нанесения ущерба. Заболевание почек от диабета прогрессирует, то есть продолжает ухудшаться.Тем не менее, хороший контроль уровня сахара в крови и артериального давления и лечение препаратами любой из двух групп (см. Профилактику ниже) могут замедлить прогрессирование заболевания.
Профилактика
Лучший способ предотвратить диабетическую нефропатию — это контролировать уровень сахара в крови и поддерживать кровяное давление в пределах нормы. Систолическое давление, «верхнее» значение артериального давления, должно быть постоянно ниже 130 миллиметров ртутного столба (мм рт. Ст.).
Два типа лекарств от кровяного давления защищают от повреждения почек способами, которые выходят за рамки снижения кровяного давления.Любой человек, страдающий диабетом и повышенным артериальным давлением, должен регулярно принимать одно из этих лекарств. Эти лекарства происходят из группы препаратов, называемых ингибиторами ангиотензинпревращающего фермента (ингибиторы АПФ), включая лизиноприл (Зестрил, Принивил), эналаприл (Вазотек), моэксиприл (Униваск), беназеприл (Лотензин) и другие, либо из группы препаратов. так называемые блокаторы рецепторов ангиотензина (БРА), включая лозартан (Козаар), валсартан (Диован) и другие.
Избегание лекарств, которые иногда могут оказывать вредное побочное действие на почки, также может помочь предотвратить заболевание почек.Если у вас тяжелое заболевание почек, ваш врач может посоветовать вам избегать обезболивающих из группы нестероидных противовоспалительных средств (группа НПВП), таких как ибупрофен.
Низкобелковая диета (от 10% до 12% или менее от общего количества калорий) также может замедлить или остановить прогрессирование заболевания почек. Если вы курите сигареты, вам следует бросить курить.
Лечение
Если у вас диабет с повышенным артериальным давлением, микроальбуминурия или анализ крови свидетельствует о заболевании почек, вам важно принимать лекарство из группы ингибиторов АПФ или БРА.Эти лекарства замедляют прогрессирование заболевания почек у людей с диабетом, хотя заболевание почек продолжает развиваться постепенно. Эти две группы лекарств тесно связаны, поэтому лекарства обычно не сочетаются друг с другом.
Уменьшение количества белка в рационе также может помочь замедлить прогрессирование заболевания почек.
Когда нефропатия достигает поздней стадии, вам может потребоваться диализ для удаления продуктов жизнедеятельности из крови. Существует два типа диализа: гемодиализ и перитонеальный диализ.
Гемодиализ отфильтровывает отходы и лишнюю жидкость из крови. Гемодиализ обычно проводится в диализном центре в течение трех-четырехчасовых сеансов три раза в неделю. Перитонеальный диализ не фильтрует кровь напрямую. Вместо этого для этой формы диализа стерильной жидкости позволяют течь в брюшную полость через катетер, который постоянно вводится через кожу. Затем жидкость удаляется после того, как она впитала отработанные вещества.
После практики можно проводить перитонеальный диализ дома.Для некоторых это хорошая альтернатива, хотя она требует значительного времени и ухода за собой.
Альтернативный способ лечения запущенной болезни почек — пересадка почки. Трансплантация почек позволила многим людям с тяжелым заболеванием почек избежать диализа или прекратить его. Однако донор и реципиент должны совпадать генетически, иначе организм отвергнет новую почку. Срок ожидания соответствующей донорской почки составляет от двух до шести лет.
Препараты против отторжения, подавляющие иммунную систему, помогают организму принять пожертвованный орган.Реципиент органа может рассчитывать на прием таких лекарств, пока пересаженная почка продолжает функционировать. Трансплантированная почка, вероятно, будет функционировать не менее 10 лет, если ее генетика точно совпадает. Если пересаженная почка перестает функционировать, необходим диализ или новая трансплантация.
Другим возможным лечением является пересадка почки и поджелудочной железы у человека с диабетом 1 типа и почечной недостаточностью. Этот вариант доступен только для небольшого числа людей из-за нехватки доноров органов, рисков хирургического вмешательства и необходимости пожизненного приема иммунодепрессантов.В случае успеха пересаженная поджелудочная железа начинает вырабатывать инсулин и может обратить вспять диабет.
Когда звонить профессионалу
Если у вас диабет, ваше артериальное давление следует проверять каждые шесть месяцев или год или чаще, если оно выше целевого. Если у вас не диагностирована диабетическая нефропатия, следует проверять мочу на микроальбумин не реже одного раза в год, чтобы проверить наличие этой проблемы и как можно раньше диагностировать ее. Людям с заболеванием почек необходимо регулярно проходить тесты на функцию почек — один раз в год или чаще.Если у вас есть симптомы, указывающие на запущенную болезнь почек, вам следует обсудить их с врачом.
Прогноз
Хотя почечную недостаточность не всегда можно предотвратить, ее ухудшение можно замедлить с помощью лекарств и контроля факторов риска. При полной почечной недостаточности диализ и трансплантация почки — это варианты, которые позволяют людям продолжать вести активный образ жизни.
Узнайте больше о диабетической нефропатии
Сопутствующие препараты
IBM Watson Micromedex
Mayo Clinic Ссылка
Внешние ресурсы
Национальная информация по диабету
http: // www.диабет.niddk.nih.gov
Национальный институт диабета, нарушений пищеварения и почек
http://www.niddk.nih.gov/
Американская диабетическая ассоциация
http://www.diabetes.org/
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности
.Детский нефротический синдром | NIDDK
На этой странице:
Что такое детский нефротический синдром?
Детский нефротический синдром не является заболеванием сам по себе; скорее, это группа симптомов, которые
- указывают на повреждение почек — особенно повреждение клубочков, крошечных единиц в почке, через которые фильтруется кровь.
- приводит к выбросу слишком большого количества белка из организма в мочу
При повреждении почек белковый альбумин, обычно содержащийся в крови, просачивается в мочу.Белки — это большие сложные молекулы, которые выполняют в организме ряд важных функций.
Два типа детского нефротического синдрома:
- первичный — наиболее распространенный тип детского нефротического синдрома, который начинается в почках и поражает только почки.
- вторичный — синдром вызван другими заболеваниями
Медицинский работник может направить ребенка с нефротическим синдромом к нефрологу — врачу, который специализируется на лечении заболеваний почек.По возможности, ребенку следует обратиться к детскому нефрологу, который имеет специальную подготовку для лечения проблем с почками у детей. Однако во многих частях страны не хватает детских нефрологов, поэтому ребенку, возможно, придется путешествовать. Если путешествие невозможно, некоторые нефрологи, лечащие взрослых, также могут лечить детей.
Что такое почки и что они делают?
Почки — это два органа в форме бобов, каждый размером с кулак. Они расположены чуть ниже грудной клетки, по одной с каждой стороны позвоночника.Каждый день почки фильтруют от 120 до 150 литров крови, чтобы произвести от 1 до 2 литров мочи, состоящей из отходов и лишней жидкости. Дети производят меньше мочи, чем взрослые, и количество мочи зависит от их возраста. Моча течет из почек в мочевой пузырь по трубкам, называемым мочеточниками. Мочевой пузырь хранит мочу. Когда мочевой пузырь опорожняется, моча выходит из организма через трубку, называемую уретрой, расположенной в нижней части мочевого пузыря.
Моча течет из почек в мочевой пузырь по трубкам, называемым мочеточниками.Почки работают на микроскопическом уровне. Почки — это не один большой фильтр. Каждая почка состоит примерно из миллиона фильтрующих элементов, называемых нефронами. Каждый нефрон фильтрует небольшое количество крови. Нефрон состоит из фильтра, называемого клубочком, и канальца. Нефроны работают в два этапа. Клубочки пропускают через себя жидкости и продукты жизнедеятельности; однако он предотвращает прохождение клеток крови и крупных молекул, в основном белков. Отфильтрованная жидкость затем проходит через канальцы, которые отправляют необходимые минералы обратно в кровоток и удаляют отходы.
Каждая почка состоит примерно из миллиона фильтрующих элементов, называемых нефронами. Каждый нефрон фильтрует небольшое количество крови. Нефрон состоит из фильтра, называемого клубочком, и канальца.Что вызывает детский нефротический синдром?
Хотя идиопатические или неизвестные заболевания являются наиболее частой причиной первичного детского нефротического синдрома, исследователи связали определенные заболевания и некоторые специфические генетические изменения, повреждающие почки, с первичным детским нефротическим синдромом.
Причина вторичного детского нефротического синдрома — основное заболевание или инфекция. Это основное заболевание или инфекция, называемая первичным заболеванием, вызывает изменения в функции почек, которые могут привести к вторичному нефротическому синдрому у детей.
Врожденные болезни — болезни, которые присутствуют при рождении — также могут вызывать детский нефротический синдром.
Нефротический синдром первичного детского возраста
К различным типам идиопатического детского нефротического синдрома относятся следующие заболевания:
- Болезнь минимальных изменений включает повреждение клубочков, которое можно увидеть только в электронный микроскоп.Этот тип микроскопа показывает крошечные детали лучше, чем любой другой микроскоп. Ученые не знают точной причины болезни минимальных изменений.
Болезнь минимальных изменений является наиболее частой причиной идиопатического детского нефротического синдрома. 1 - Фокальный сегментарный гломерулосклероз рубцевание в отдельных участках почки:
- «Очаговая» означает, что только некоторые клубочки покрываются рубцами.
- «Сегментарный» означает, что повреждение затрагивает только часть отдельного клубочка.
- Мембранопролиферативный гломерулонефрит — это группа заболеваний, связанных с отложениями антител, которые накапливаются в клубочках, вызывая утолщение и повреждение. Антитела — это белки, вырабатываемые иммунной системой для защиты организма от чужеродных веществ, таких как бактерии или вирусы.
Нефротический синдром вторичного детского возраста
Некоторые общие заболевания, которые могут вызывать вторичный нефротический синдром у детей, включают
- диабет, состояние, которое возникает, когда организм не может использовать глюкозу — тип сахара — обычно
- IgA-васкулит, заболевание, при котором мелкие кровеносные сосуды в организме воспаляются и протекают.
- гепатит, воспаление печени, вызванное вирусом
- Вирус иммунодефицита человека (ВИЧ), вирус, изменяющий иммунную систему
- волчанка, аутоиммунное заболевание, которое возникает, когда организм атакует собственную иммунную систему
- Малярия, болезнь крови, переносимая комарами
- стрептококковая инфекция, инфекция, которая возникает, когда бактерии, вызывающие фарингит или кожную инфекцию, остаются без лечения
Другие причины вторичного детского нефротического синдрома могут включать определенные лекарства, такие как аспирин, ибупрофен или другие нестероидные противовоспалительные препараты, а также воздействие химических веществ, таких как ртуть и литий.
Врожденные болезни и детский нефротический синдром
Врожденный нефротический синдром встречается редко и поражает младенцев в первые 3 месяца жизни. 2 Этот тип нефротического синдрома, иногда называемый инфантильным нефротическим синдромом, может быть вызван
- наследственных генетических дефектов, которые передаются от родителей к ребенку через гены
- инфекций на момент рождения
Более подробная информация об основных заболеваниях или инфекциях, вызывающих изменения функции почек, представлена в разделе здоровья NIDDK «Гломерулярные заболевания».
У каких детей чаще развивается детский нефротический синдром?
В случаях первичного детского нефротического синдрома, причина которого является идиопатической, исследователи не могут точно определить, у каких детей этот синдром более высок. Однако по мере того, как исследователи продолжают изучать связь между генетикой и детским нефротическим синдромом, возможно, удастся предсказать синдром для некоторых детей.
У детей выше вероятность развития вторичного детского нефротического синдрома, если они
- страдают заболеваниями, которые могут повредить почки
- принимать лекарства
- развивают определенные виды инфекций
Каковы признаки и симптомы детского нефротического синдрома?
Признаки и симптомы детского нефротического синдрома могут включать
- отек — опухоль, чаще всего на ногах, ступнях или лодыжках, реже на руках или лице
- альбуминурия — когда в моче ребенка высокий уровень альбумина
- гипоальбуминемия — когда в крови ребенка низкий уровень альбумина
- гиперлипидемия — когда уровень холестерина и жира в крови ребенка выше нормы
Кроме того, у некоторых детей с нефротическим синдромом может быть
- кровь в моче
- Симптомы инфекции, такие как лихорадка, летаргия, раздражительность или боль в животе
- потеря аппетита
- диарея
- высокое кровяное давление
Каковы осложнения детского нефротического синдрома?
Осложнения детского нефротического синдрома могут включать
- инфекция. При повреждении почек у ребенка повышается вероятность развития инфекций, поскольку организм теряет белки, которые обычно защищают от инфекции. Поставщики медицинских услуг пропишут лекарства для лечения инфекций. Дети с детским нефротическим синдромом должны получать пневмококковую вакцину и ежегодные прививки от гриппа для предотвращения этих инфекций. Детям также следует сделать соответствующие возрасту прививки, хотя поставщик медицинских услуг может отложить введение некоторых живых вакцин, пока ребенок принимает определенные лекарства.
- тромбов. Сгустки крови могут блокировать поток крови и кислорода через кровеносный сосуд в любом месте тела. У ребенка повышается вероятность образования тромбов, когда он или она теряет белки с мочой. Врач лечит тромбы с помощью разжижающих кровь препаратов.
- высокий холестерин в крови. Когда альбумин попадает в мочу, уровень альбумина в крови падает. Печень производит больше альбумина, чтобы восполнить его низкий уровень в крови.В то же время печень производит больше холестерина. Иногда детям может потребоваться лечение препаратами для снижения уровня холестерина в крови.
Как диагностируется детский нефротический синдром?
Поставщик медицинских услуг диагностирует детский нефротический синдром с помощью
- Медицинский и семейный анамнез
- медицинский осмотр
- Анализы мочи
- анализ крови
- УЗИ почек
- Биопсия почки
Медицинский и семейный анамнез
Изучение медицинского и семейного анамнеза — одна из первых вещей, которые врач может сделать для диагностики детского нефротического синдрома.
Физический осмотр
Медицинский осмотр может помочь диагностировать детский нефротический синдром. Во время медицинского осмотра поставщик медицинских услуг чаще всего
- осматривает тело ребенка
- постукивает по определенным участкам тела ребенка
Анализы мочи
Медицинский работник может назначить следующие анализы мочи, чтобы определить, есть ли у ребенка повреждение почек в результате детского нефротического синдрома.
Тест на альбумин. Тест с помощью индикаторной полоски, выполняемый на образце мочи, может обнаружить присутствие альбумина в моче, что может означать повреждение почек. Ребенок или воспитатель собирает образец мочи в специальный контейнер. Для проведения теста медсестра или техник помещает полоску химически обработанной бумаги, называемую щупом, в образец мочи ребенка. Пятна на щупе меняют цвет, когда в моче присутствует альбумин.
Отношение альбумина к креатинину в моче. Медицинский работник использует это измерение для оценки количества альбумина, попавшего в мочу за 24-часовой период.Ребенок сдает образец мочи на приеме у врача. Креатинин — это продукт жизнедеятельности, который фильтруется в почках и выводится с мочой. Высокое соотношение альбумина к креатинину в моче указывает на то, что почки выделяют большое количество альбумина с мочой.
Анализ крови
Анализ крови включает забор крови в офисе поставщика медицинских услуг или в коммерческом учреждении и отправку образца в лабораторию для анализа. Лаборатория тестирует образец, чтобы оценить, сколько крови фильтруют почки каждую минуту, что называется оценочной скоростью клубочковой фильтрации или рСКФ.Результаты теста помогают врачу определить степень повреждения почек. Поставщики медицинских услуг могут также назначить другие анализы крови, чтобы определить основное заболевание, которое может вызывать нефротический синдром у детей.
УЗИ почек
Ультразвук использует устройство, называемое преобразователем, которое безопасно и безболезненно отражает звуковые волны от органов, чтобы создать изображение их структуры. Специально обученный техник выполняет эту процедуру в офисе поставщика медицинских услуг, амбулаторном центре или больнице.Радиолог — врач, специализирующийся на медицинской визуализации — интерпретирует изображения, чтобы увидеть, нормально ли выглядят почки; ребенку обезболивание не требуется.
Биопсия почки
Биопсия почки — это процедура, при которой берется небольшой кусочек ткани почек для исследования под микроскопом. Медицинский работник выполняет биопсию в амбулаторном центре или больнице. Лечащий врач назначит ребенку легкую седацию и местную анестезию; однако в некоторых случаях ребенку потребуется общая анестезия.Патолог — врач, специализирующийся на диагностике заболеваний — исследует ткани в лаборатории. Тест может помочь диагностировать детский нефротический синдром.
Когда поставщик медицинских услуг подозревает, что у ребенка болезнь минимальных изменений, он или она часто начинает лечение с помощью лекарств, не выполняя биопсию. Если лекарство подействует, ребенку биопсия не требуется. В большинстве случаев поставщик медицинских услуг не выполняет биопсию детям младше 12 лет, если он или она не считает, что причиной является другое заболевание.
Как лечится детский нефротический синдром?
Медицинские работники решат, как лечить детский нефротический синдром, в зависимости от типа:
- Первичный детский нефротический синдром: лекарства
- Вторичный детский нефротический синдром: лечение основного заболевания
- Врожденный нефротический синдром: лекарства, операция по удалению одной или обеих почек и трансплантация
Нефротический синдром первичного детского возраста
Медицинские работники лечат идиопатический детский нефротический синдром с помощью нескольких типов лекарств, которые контролируют иммунную систему, удаляют лишнюю жидкость и снижают кровяное давление.
- Управляйте иммунной системой. Кортикостероиды — это группа лекарств, которые снижают активность иммунной системы, уменьшают количество альбумина, теряемого с мочой, и уменьшают отек. Медицинские работники обычно используют преднизон или родственные кортикостероиды для лечения идиопатического детского нефротического синдрома. Около 90 процентов детей достигают ремиссии при ежедневном приеме кортикостероидов в течение 6 недель, а затем немного меньшей дозе через день в течение 6 недель. 2 Ремиссия — это период, когда у ребенка отсутствуют симптомы.
У многих детей наблюдается рецидив после начальной терапии, и медицинские работники лечат их более коротким курсом кортикостероидов до тех пор, пока болезнь снова не перейдет в ремиссию. У детей могут быть множественные рецидивы; однако чаще всего они выздоравливают без длительного повреждения почек.
Если у ребенка частые рецидивы или он не реагирует на лечение, врач может прописать другие лекарства, снижающие активность иммунной системы.Эти лекарства препятствуют выработке организмом антител, которые могут повредить ткани почек. Они включают
- циклофосфамид
- микофенолят (CellCept, Myfortic)
- циклоспорин
- такролимус (Гекория, Програф)
- Удалите лишнюю жидкость. Врач может прописать мочегонное средство — лекарство, которое помогает почкам удалять лишнюю жидкость из крови.Удаление лишней жидкости часто помогает снизить кровяное давление.
- Пониженное артериальное давление. У некоторых детей с детским нефротическим синдромом развивается повышенное артериальное давление, и им может потребоваться прием дополнительных лекарств для снижения артериального давления. Два типа препаратов, снижающих артериальное давление, ингибиторы ангиотензинпревращающего фермента и блокаторы рецепторов ангиотензина, имеют дополнительное преимущество в замедлении прогрессирования заболевания почек. Многим детям с нефротическим синдромом требуется два или более лекарств для контроля артериального давления.
Нефротический синдром вторичного детского возраста
Медицинские работники лечат вторичный детский нефротический синдром путем лечения основной причины первичного заболевания. Например, поставщик медицинских услуг может вылечить детей до
.- Назначение антибиотиков при инфекции
- корректирующие лекарства для лечения волчанки, ВИЧ или диабета
- Замена или прекращение приема лекарств, которые, как известно, вызывают вторичный детский нефротический синдром
При лечении основной причины врач также будет лечить ребенка для улучшения или восстановления функции почек с помощью тех же лекарств, которые используются для лечения первичного детского нефротического синдрома.
Опекуны должны следить за тем, чтобы дети принимали все прописанные лекарства и следовали плану лечения, рекомендованному их лечащим врачом.
Врожденный нефротический синдром
Исследователи обнаружили, что лекарства неэффективны при лечении врожденного нефротического синдрома, и что большинству детей потребуется пересадка почки к 2–3 годам. Трансплантация почки — это операция по помещению здоровой почки от только что умершего человека или от живого донора, чаще всего члена семьи, в тело человека, чтобы взять на себя работу поврежденной почки.Чтобы сохранить здоровье ребенка до трансплантации, врач может порекомендовать следующее:
- Инъекции альбумина для восполнения потери альбумина с мочой
- мочегонные средства для удаления лишней жидкости, вызывающей отеки
- антибиотики для лечения первых признаков инфекции
- Гормоны роста для стимуляции роста и созревания костей
- Удаление одной или обеих почек для уменьшения потери альбумина с мочой
- диализ для искусственной фильтрации шлаков из крови при отказе почек
Как можно предотвратить детский нефротический синдром?
Исследователи не нашли способа предотвратить детский нефротический синдром, если причина идиопатическая или врожденная.
Питание, диета и питание
Детям с нефротическим синдромом может потребоваться внести изменения в свой рацион, например
- ограничение количества натрия, часто из соли, которое они принимают каждый день
- сокращение количества выпиваемой жидкости каждый день
- придерживаться диеты с низким содержанием насыщенных жиров и холестерина для контроля повышенного уровня холестерина
Родители или опекуны должны поговорить с лечащим врачом ребенка, прежде чем вносить какие-либо изменения в диету ребенка.
Ресурсы
Национальный фонд почек
Дети с хроническим заболеванием почек: советы родителям
Справочник работодателя
Веб-сайт Nemours KidsHealth
Когда у вашего ребенка хроническое заболевание почек
Что делать с диализом?
Nephkids
Группа киберподдержки
Объединенная сеть обмена органами
Трансплантация органов: что нужно знать каждому ребенку (PDF, 1.67 МБ)
Министерство здравоохранения и социальных служб США, Центры услуг Medicare и Medicaid
Покрытие Medicare услуг диализа и трансплантации почки (PDF, 1080 КБ)
Управление социального обеспечения США
Пособия для детей с ограниченными возможностями (PDF, 413 КБ)
Клинические испытания
Национальный институт диабета, болезней органов пищеварения и почек (NIDDK) и другие подразделения Национальных институтов здравоохранения (NIH) проводят и поддерживают исследования многих заболеваний и состояний.
Что такое клинические испытания и какую роль в исследованиях играют дети?
Клинические испытания — это исследования с участием людей всех возрастов. Клинические испытания ищут новые способы предотвращения, обнаружения или лечения заболеваний. Исследователи также используют клинические испытания для изучения других аспектов медицинской помощи, таких как улучшение качества жизни. Исследования с участием детей помогают ученым
- определить уход, который лучше всего подходит для ребенка
- найди лучшую дозу лекарств
- найти лечение состояний, которые затрагивают только детей
- лечат состояния, которые ведут себя по-разному у детей
- понять, как лечение влияет на организм растущего ребенка
Узнайте больше о клинических испытаниях и детях.
Какие клинические испытания открыты?
Клинические испытания, которые в настоящее время открыты и набираются, можно просмотреть на сайте www.ClinicalTrials.gov.
Список литературы
[1] Нефротический синдром. Медицинская онлайн-библиотека руководств Merck. www.merckmanuals.com. Обновлено в июле 2013 г. Проверено 7 июля 2014 г.
[2] Баккалоглу С.А., Шефер Ф. Заболевания почек и мочевыводящих путей у детей. В: Taal MW, Chertow GM, Marsden PA, et al., Eds. Бреннер и Ректор Почка .9 изд. Филадельфия: Сондерс; 2011: 2622–2643.
.Мембранозная нефропатия | Центр почек UNC
Что такое мембранозная нефропатия?
Мембранозная нефропатия (МН) — это заболевание почек, которое поражает фильтры ( клубочков, ) почек и может вызывать появление белка в моче, а также снижение функции почек и отек. Иногда это также можно назвать мембранозной гломерулопатией (эти термины могут использоваться как синонимы и означают одно и то же).
Мембранозная нефропатия — одна из наиболее частых причин нефротического синдрома у взрослых.Нефротический синдром включает значительное количество белка в моче (не менее 3,5 граммов в день), низкий уровень белка в крови (альбумин) и отек (отек).
Мембранозная нефропатия может возникать сама по себе ( первичная ) или вследствие другого заболевания или основной причины ( вторичная ). Это будет обсуждено позже, но некоторые факторы, которые могут вызвать вторичный ЗН, включают волчанку, рак или определенные лекарства. Эта веб-страница будет в основном посвящена первичному MN.
Мембранозная нефропатия считается аутоиммунным заболеванием, что означает, что она вызвана собственной иммунной системой организма.ЗН вызывается накоплением иммунных комплексов внутри фильтров (клубочков) самой почки. Иммунная система обычно создает антител для распознавания и прикрепления к чему-либо (называемому антигеном). Когда антитело прикрепляется к антигену, это называется иммунным комплексом. Антигены обычно чужеродны для организма, например, вирусы или бактерии. Однако иногда организм может вырабатывать антитела, которые распознают и прикрепляются к чему-то в самом организме (не чужеродному) — эти типы антител называются аутоантителами .Иммунные комплексы обычно выводятся из крови, прежде чем вызывать какие-либо проблемы, но при определенных условиях они могут накапливаться в разных частях тела. В MN эти иммунные комплексы (антитела, вырабатываемые иммунной системой, прикрепленные к антигенам) попадают в почечные фильтры (клубочки). В большинстве случаев ЗН вырабатываются антитела к антигену, который является частью самого почечного фильтра (клубочка). Вместе эти антитела и антигены создают иммунные комплексы, которые застревают в почечном фильтре (клубочках) и вызывают заболевание.
Недавно были обнаружены и идентифицированы антитела, вызывающие большинство случаев мембранозной нефропатии. Примерно у 70-80% пациентов с первичным ЗН (это означает, что их ЗН не связан с другими заболеваниями или причинами или не связан с ними) в почках и / или кровотоке обнаруживается антитело anti-PLA2R . Антитело против PLA2R (сокращение от антитела против рецептора фосфолипазы A2) прикрепляется к рецептору фосфолипазы A2 (антигену). Рецептор фосфолипазы А2 — это белок, обнаруженный в почечном фильтре (клубочках), в частности в клетке, называемой подоцитом, которая составляет часть этого фильтра (см. Ниже).Другое антитело, названное anti-THSD7A (сокращение от 7A, содержащего домен антитромбоспондина типа 1), также было обнаружено, но обнаруживается у гораздо меньшего числа пациентов с первичным MN, всего около 2-3%. Это антитело к другому антигену, THSD7A, который также содержится в почечном фильтре (другой белок в подоцитах).
Как это выглядит?
Ниже представлена диаграмма того, как иммунные комплексы откладываются в почках. На этом снимке показан поперечный разрез части почечного фильтра (клубочка).Сюда входят различные слои, в том числе клетки, составляющие капиллярный кровеносный сосуд (эндотелиальные клетки, желтый цвет), базальная мембрана (серый цвет) и слой клеток почек (подоцит, зеленый цвет). Кровь внутри капиллярного кровеносного сосуда фильтруется через эти слои и становится мочой. Антитела (Y-образные, черные на рисунке) в кровотоке прикрепляются к антигенам (треугольники, черные на рисунке) и образуют иммунные комплексы, которые застревают и накапливаются между слоями фильтра (клубочки).Эти иммунные комплексы также активируют иммунную систему, вызывая воспаление. Наращивание этих иммунных комплексов, а также воспаление приводят к тому, что фильтр перестает работать должным образом и может привести к повреждению почек. Обычно фильтр (клубочки) позволяет воде, электролитам и некоторым отходам превращаться в мочу, а более крупные предметы, такие как клетки крови и белки, слишком велики, чтобы пройти через фильтр, поэтому они остаются в крови. Однако при этом заболевании белок и клетки крови могут просачиваться в мочу, потому что фильтр не работает должным образом.
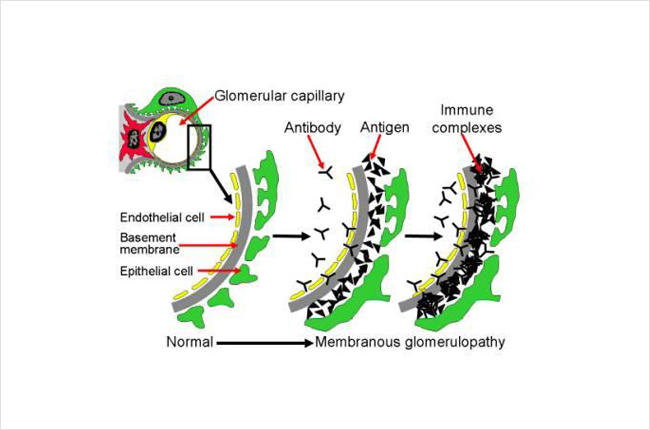
На рисунке ниже показана часть клубочка в сравнении нормального и пораженного ЗН. Справа черные точки или комочки (на одну указывает стрелка) представляют собой скопления иммунных комплексов (комплексов антиген-антитело). По мере того, как больше этих иммунных комплексов накапливается между слоями фильтров, они становятся более плотными. Клетки почек (зеленые на этом рисунке, называемые подоцитами), которые составляют часть фильтра, повреждаются из-за иммунных комплексов и воспаления, вызванного иммунной системой, и перестают работать должным образом.На картинке справа видно, что серый слой (базальная мембрана) стал толще и начал заполнять промежутки между черными пятнами / комками. Вы также можете видеть, что зеленая ячейка не выглядит так, как в нормальном здоровом фильтрующем контуре (капиллярной петле) слева.
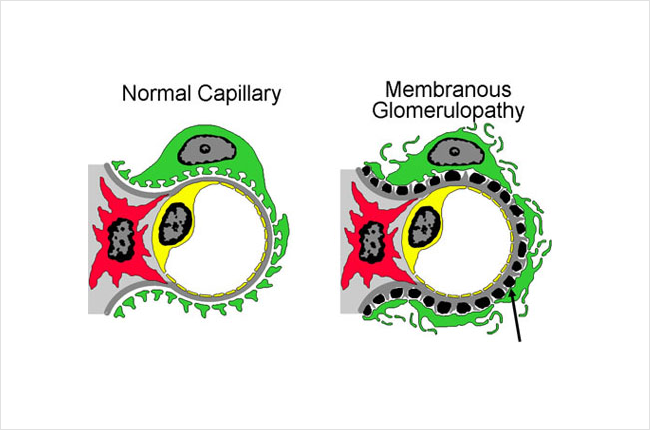
Под микроскопом фильтры (клубочки) в почках становятся утолщенными, отсюда и произошло название мембранозная нефропатия.
Пример этого показан ниже — из 2 разных образцов биопсии почек.Это поперечные сечения, поэтому петли — это сечения капиллярных кровеносных сосудов и фильтров. Слева — нормальный клубок (фильтр), а справа петли в клубочках утолщены у человека с мембранозной нефропатией. Черные стрелки на фотографиях указывают толщину капилляра (стенки небольшого кровеносного сосуда). Обратите внимание, насколько толще эта стенка у пациента с ЗН (справа).
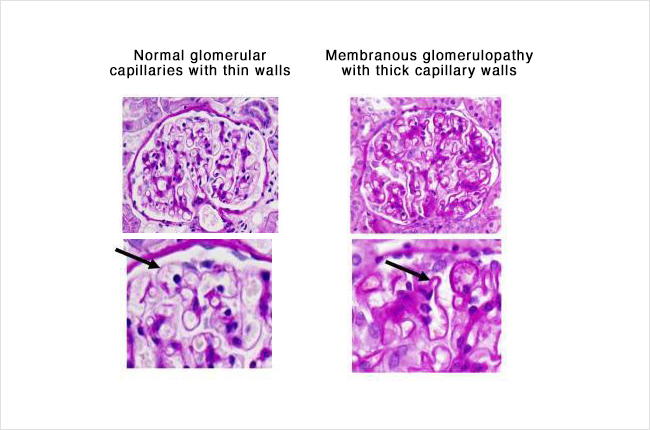
Рисунок ниже — это еще одно изображение под микроскопом образца биопсии почки человека с ЗН.Этот снимок был сделан с помощью электронного микроскопа, который увеличивает образец даже больше, чем изображения выше (примерно в миллион раз больше, чем действительный размер). Темно-серые комочки / капли — это скопления иммунных комплексов, застрявших между слоями фильтрующей петли (капиллярной петли) в клубочках. Капилляр (крошечный кровеносный сосуд) имеет овальную форму, проходящую через изображение, поскольку на этом изображении показано поперечное сечение кровеносного сосуда.
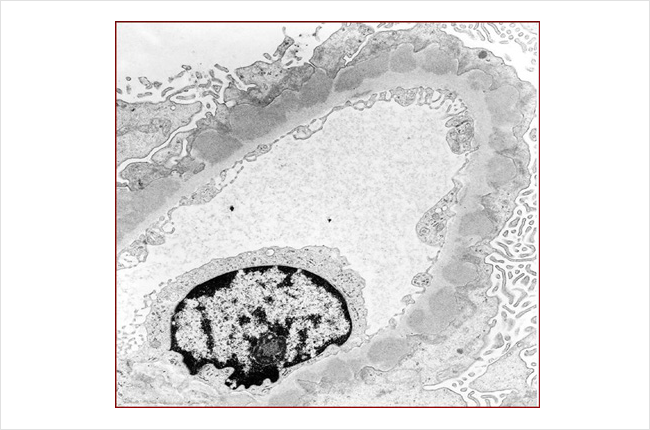
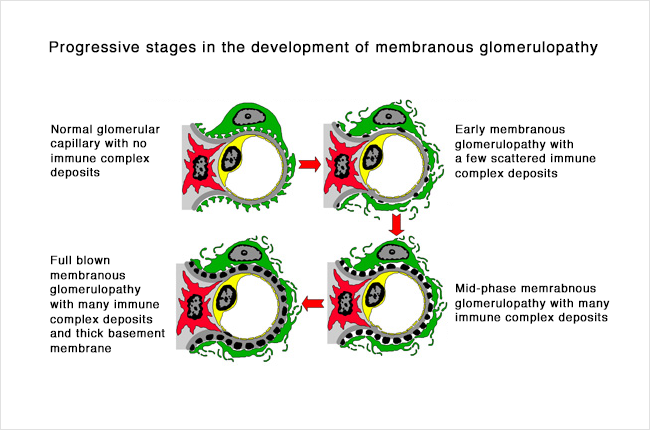
Кто болеет мембранозной нефропатией?
MN чаще всего встречается у людей старшего и среднего возраста в возрасте от 50 до 60 лет, хотя может возникнуть раньше или позже.У детей встречается редко. Мужчины страдают чаще, чем женщины, и это гораздо чаще встречается у кавказцев (по сравнению с чернокожими).
Как я его получил?
Хотя мы кое-что понимаем в том, как работает болезнь, как происходит повреждение белка в моче и почек, мы не совсем понимаем, почему это происходит с определенными людьми. То есть мы не знаем, почему у некоторых людей вырабатываются эти антитела, а у большинства нет, и почему болезнь возникает именно тогда (обычно в более позднем возрасте), а не в любое другое время.
Как и в случае с другими видами аутоиммунных заболеваний (такими как волчанка, ревматоидный артрит или болезнь Крона), мы думаем, что, вероятно, есть несколько факторов, которые способствуют развитию болезни, то есть несколько вещей, которые должны произойти для иммунной системы, чтобы нацеливаться и атаковать. / повредить тело (а не просто нацеливаться на инородные предметы, такие как инфекции). У некоторых людей может быть ген или гены, которые повышают вероятность аутоиммунного заболевания (более подвержены их развитию).Хотя некоторые люди с большей вероятностью заболеют аутоиммунными заболеваниями, если в их семье есть аутоиммунные заболевания, ЗН не является генетическим заболеванием и не передается от родителей к их ребенку. У людей, которые могут подвергаться более высокому риску аутоиммунного заболевания, определенные события или триггеры могут привести к его окончательному развитию — например, инфекция или другое воспаление в организме, которое может активировать иммунную систему. Однако это гипотезы, и на данный момент мы не понимаем, почему один человек получает MN, а другие — нет.
Как упоминалось ранее, ЗН может быть первичным (аутоиммунное заболевание, которое обычно вызывается антителом против PLA2R без других связанных причин или заболеваний) или может быть вторичным (из-за другого заболевания или причины). В s вторичный MN, такой же тип повреждения почек возникает, но связан с чем-то другим или вызван им. Некоторые из наиболее распространенных заболеваний:
- Системная красная волчанка (СКВ или волчанка)
- Гепатиты B и C
- Рак (особенно легких или толстой кишки)
Вторичный ЗН также был связан с некоторыми лекарствами.Наиболее распространены НПВП (нестероидные противовоспалительные препараты, такие как ибупрофен, напроксен или диклофенак). Поскольку гепатит и рак могут быть связаны с мембранозной нефропатией, любой, у кого обнаружен ЗН, должен пройти обследование на гепатит и убедиться, что он прошел соответствующий возрастной скрининг на наличие рака. Для проверки на гепатит можно сделать анализ крови. Соответствующий возрасту скрининг на рак может включать такие тесты, как мазок Папаниколау, маммограмма, колоноскопия или компьютерная томография легких (у курильщиков или курильщиков).Ваш врач может уточнить, какие из этих тестов вам подходят или необходимы.
Нефротический синдром
Мембранозная нефропатия часто вызывает нефротический синдром. Нефротический синдром — это группа симптомов или изменений, которые часто возникают вместе у человека, который теряет много белка с мочой. Нефротический синдром также может возникать при других заболеваниях, которые вызывают потерю большого количества белка с мочой. Хотя многие люди с ЗН имеют нефротический синдром, не все.Нефротический синдром включает следующие данные:
- Не менее 3,5 граммов белка в моче в день (протеинурия) . Это можно измерить на 24-часовом сборе мочи, но также можно оценить на одном образце мочи. Чтобы оценить количество протеинурии в одном образце мочи, используется соотношение белка в моче к креатинину — это дает оценку того, сколько граммов белка будет в 24-часовом образце мочи.
- Низкий уровень белка (альбумина) в крови
- Отек (иногда называемый отеком)
Также может включать:
- Высокий холестерин
- Повышенный риск образования тромбов
Какие симптомы?
Наиболее частым признаком ЗН является отек (иногда называемый отеком).Он может варьироваться от легкого до тяжелого. У большинства людей с этим заболеванием наблюдается припухлость, которая часто оказывается первым признаком, который замечают люди. При ЗН (в отличие от некоторых других заболеваний, вызывающих белок в моче и нефротический синдром) отек обычно возникает медленно (в течение нескольких недель или месяцев), но иногда и быстрее. Обычно он начинается в ступнях, лодыжках или ногах, но может возникать в любом месте тела, включая живот, кисти рук и лицо.
Набухание ЗН возникает из-за накопления жидкости в организме, особенно в различных тканях.Когда жидкость накапливается, она иногда может попасть в легкие и вызвать затрудненное дыхание или одышку. Это менее распространено, чем отек, но у людей, у которых оно есть, оно может быть наиболее заметно при ходьбе, физических нагрузках или лежа в горизонтальном положении.
Некоторые люди с ЗН, в частности люди с нефротическим синдромом (с большим количеством белка в моче и низким уровнем белка в крови), чувствуют сильную усталость или истощение. Мы не знаем точно, как и почему это происходит, но некоторые люди с ЗН (и другими заболеваниями, вызывающими нефротический синдром) замечают это.
Когда белок попадает через фильтр в почках в мочу, моча может стать пенистой или пузырьковой. Некоторые люди могут заметить это изменение в моче до того, как у них появятся другие симптомы.
Есть и другие симптомы, которые могут возникать при ЗН, но перечисленные выше являются одними из наиболее распространенных и тех, которые люди с ЗН часто замечают первыми.
Как диагностируется?
Мембранозная нефропатия — необычное заболевание, диагноз которого иногда можно отложить.Поскольку отек, наиболее распространенный симптом, может быть вызван множеством различных заболеваний или проблем (включая проблемы с почками, сердцем или печенью), почки нельзя сразу определить как причину. Чаще всего это диагностируется при обследовании человека на наличие белка в моче (обычно в моче не должно быть белка). Некоторые люди обращаются к врачу из-за симптомов (например, отека), а анализы мочи выявляют белок в моче. В других случаях анализ мочи может быть выполнен по другой причине (например, при обычном физическом обследовании), и в моче обнаруживается белок.Уровни протеина можно измерить (или количественно) на 24-часовом сборе мочи или оценить по одному образцу мочи. Другая оценка обычно включает измерение функции почек (анализ крови, называемый креатинином), и другие анализы крови.
Различные почечные заболевания — не только MN — могут вызывать белок в моче, и биопсия почек в конечном итоге необходима для диагностики конкретного заболевания, вызывающего белок в моче. Биопсия почки — это процедура, при которой с помощью иглы берется образец почечной ткани для исследования под микроскопом.Это позволяет увидеть отдельные клубочки (почечные фильтры) под большим увеличением. Для постановки диагноза можно провести дополнительные тесты на ткани почек из биопсии. Анализы крови и определение белка в моче могут быть полезны для понимания серьезности заболевания и исключения или поиска определенных причин, поэтому эти анализы часто проводятся в рамках обследования, но для диагностики ЗН необходима биопсия.
Поскольку у большинства людей с ЗН есть антитела к PLA2R, можно провести анализ крови для проверки на наличие этих антител.Если он положительный, очень вероятно, что у кого-то есть ЗН. Однако отрицательный результат теста не означает, что у кого-то нет ЗН, и биопсия почки важна для подтверждения диагноза, а также для получения дополнительной информации для руководства.
Что такое лечение?
Лечение ЗН обычно включает несколько этапов, которыми руководит нефролог (специалист по почкам).
- Ингибитор АПФ или ARB — — это лекарства от артериального давления, которые могут снизить количество белка в моче.Эти лекарства обычно являются первым шагом в лечении ЗН. Хотя они были разработаны как лекарства от артериального давления, при МН они используются для уменьшения количества протеина, попадающего в мочу, и могут иметь дополнительное преимущество, помогая контролировать артериальное давление, если оно повышено. Иногда эти лекарства нельзя использовать, если у кого-то артериальное давление слишком низкое (поскольку они могут снизить артериальное давление) или если у кого-то высокий уровень калия в крови (поскольку они могут повышать уровень калия). Однако большинству людей следует использовать одно из этих лекарств, если нет противопоказаний.
АПФ (ингибиторы ангиотензинпревращающего фермента) включают лизиноприл (Зестрил, Принивил), эналаприл (Вазотек), рамиприл (Альтаце), беназеприл (Лотензин) и квинаприл (Аккуприл). БРА (блокаторы рецепторов ангиотензина II) включают лозартан (Козаар), валсартан (Диован), ирбесартан (Авапро), телмисартан (Микардис), олмесартан (Беникар) и кандесартан (Атаканд).
- Жидкое лекарство ( диуретик ) — их можно использовать для лечения отека, если он возникает.Отек может быть очень неприятным или проблемным симптомом ЗН, поэтому эти лекарства могут быть важной частью лечения болезни. Однако они не лечат сам MN. Диуретики включают фуросемид (Лазикс), торсемид, буметанид (Бумекс) и иногда другие.
- Иммунодепрессанты — не всем людям с ЗН потребуются лекарства для подавления иммунной системы, но они являются важной частью лечения многих людей, страдающих этим заболеванием. Причины, по которым кому-то может потребоваться иммунодепрессивное лечение, включают: ухудшение функции почек, высокий уровень белка в моче (особенно если они не улучшаются после периода наблюдения) или осложнения нефротического синдрома (например, образование тромба).
Поскольку ЗН является аутоиммунным заболеванием, при котором иммунная система организма нацелена и повреждает собственные ткани организма (в данном случае часть клубочков), у многих людей для лечения этого заболевания необходимы лекарства для подавления или ослабления иммунной системы. Существуют различные иммуноподавляющие препараты, которые можно использовать для лечения ЗН. Поскольку все эти лекарства подавляют иммунную систему, все они увеличивают риск заражения. Однако, помимо этого, они имеют разные индивидуальные побочные эффекты, и различные возможные побочные эффекты могут быть фактором при принятии решения, какой из них использовать.
- Циклофосфамид (Цитоксан) — это лекарство, которое можно вводить в виде ежемесячной инфузии или ежедневных таблеток (внутрь). Одна из наиболее распространенных схем лечения ЗН включает чередование циклофосфамида и кортикостероидов в течение 6 месяцев (протокол Понтичелли).
- Ритуксимаб (Ритуксан) — это лекарство, которое вводится в виде инфузии, либо 4 приема в неделю, либо 2 приема с интервалом в 2 недели. Его действие длится около 6 месяцев в организме, и иногда поддерживающая (повторная) доза может быть введена через 6 месяцев.
- Ингибиторы кальциневрина (циклоспорин или такролимус) — эти лекарства принимают внутрь в виде таблеток, как правило, два раза в день.
- Кортикостероиды (преднизон) — это лекарство, которое часто используется с одним из других иммунодепрессантов, указанных выше (чаще всего с циклофосфамидом или одним из ингибиторов кальциневрина). Кортикостероиды сами по себе не эффективны для лечения ЗН, но могут использоваться как часть других схем.
- Лекарства от холестерина — поскольку уровень холестерина может быть повышен у людей с нефротическим синдромом, лечение может включать в себя лекарства от этого.Наиболее распространенный тип называется «статин», и к ним относятся аторвастатин (липитор), ловастатин, правастатин (правахол) и розувастатин (крестор).
- Контроль артериального давления — артериальное давление часто повышается у людей с заболеваниями почек, включая МН. Важно контролировать артериальное давление, чтобы предотвратить повреждение почек. В дополнение к ингибитору АПФ или БРА, которые могут помочь с белком в моче (см. Выше), есть много других лекарств, которые можно использовать для лечения высокого кровяного давления.Ограничение потребления соли может помочь контролировать артериальное давление, а также уменьшить отек.
- Разжижители крови — поскольку люди с нефротическим синдромом (белок в моче, низкий уровень белка в крови и отек) подвержены более высокому риску образования тромбов, лечение также может включать разжижитель крови для предотвращения образования тромбов. Решение о применении разбавителя крови основано на балансе риска образования сгустка и риска кровотечения из-за приема разбавителя крови. Есть веб-сайт, который вы можете использовать вместе со своим врачом, чтобы решить, будет ли вам полезен разбавитель крови.В большинстве случаев прием разбавителя крови следует прекратить, когда нефротический синдром улучшится и уровень белка в крови повысится.
Наконец, если MN считается вторичным по отношению к чему-то еще , , тогда наиболее важно вылечить основное заболевание (инфекцию, рак и т. Д.) Или прекратить действие лекарственного средства, являющегося причиной. Этого часто бывает достаточно, и лечения иммуноподавляющими препаратами можно избежать.
Каковы мои шансы поправиться?
До трети пациентов с диагнозом ЗН самопроизвольно переходят в ремиссию в течение 5 лет, даже без иммуносупрессивной терапии.После лечения болезнь у большинства пациентов перейдет в стадию ремиссии. Полная ремиссия означает стабильную (или улучшенную) функцию почек и снижение уровня белка в моче до нормального. Частичная ремиссия означает стабильную или улучшенную функцию почек, а также снижение уровня белка в моче до менее половины исходного уровня, а не до диапазона нефротического синдрома (<3,5 г / день).
Тем не менее, рецидивы являются обычным явлением при ЗН, и у пациентов, которые входят в ремиссию спонтанно или в ответ на иммунодепрессанты, болезнь может вернуться позже.В долгосрочной перспективе (в течение десятилетий) примерно у 1/3 пациентов разовьется терминальная стадия заболевания почек (почечная недостаточность, требующая диализа), примерно у 1/3 будет продолжаться содержание белка в моче без почечной недостаточности, и примерно у 1/3 будет наблюдаться нарушение функции почек. ремиссия.
К факторам, предсказывающим лучший долгосрочный исход при ЗН, относятся более низкий уровень белка в моче, принадлежность к женщине, возраст моложе (менее 60 лет) и достижение ремиссии.
Пересадка почки при мембранозной нефропатии
К сожалению, у некоторых пациентов с диагнозом ЗН в конечном итоге развивается почечная недостаточность.К счастью, пересадка почки — это вариант лечения для некоторых людей.
Прочтите общую информацию о пересадке почки здесь.
Вернется ли перепончатая нефропатия при трансплантации почки?
Вероятность того, что ЗН вернется в пересаженной почке, составляет 40%. К сожалению, не было выявлено факторов, которые позволили бы нам составить представление о пациентах, подверженных риску этой проблемы. Как правило, рецидив заболевания происходит в течение первых 2 лет после трансплантации.
Есть ли какое-либо лечение мембранозной нефропатии, которая возвращается при трансплантации?
Не было никаких испытаний для оценки различных методов лечения ЗН, который возвращается в трансплантированной почке. Однако ритуксимаб — это один из вариантов, который успешно применялся для лечения.
Эта страница была проверена и обновлена в сентябре 2018 г. специалистом по медицине Шеннон Мерфи.
.

