Ингаляции с физраствором для взрослых: инструкция по применению раствора для приема внутрь и ингаляции Лазолван®
ПРАВИЛА ПРОВЕДЕНИЯ ИНГАЛЯЦИЙ. Статьи компании «Медтехника для дома»
Выбрать ингалятор > > > >
1. Ингаляции следует принимать не ранее чем через 1-1,5 часа после еды, при этом не следует отвлекаться разговором. После ингаляций в течение 1 часа не рекомендуется разговаривать, принимать пищу, выходить на улицу (в прохладную погоду).
2. При заболеваниях верхних дыхательных путей (носа, околоносовых пазух и носоглотки) вдох и выдох необходимо делать через нос, используя маску. Дышать спокойно, без напряжения.
3. При заболеваниях средних дыхательных путей (горло, гортань) вдох и выдох следует делать через рот, используя маску. Дышать следует спокойно в обычном режиме
4. При заболеваниях трахеи, бронхов, легких рекомендуется вдыхать аэрозоль через рот, используя мундштук. Дышать глубоко и ровно.
5. Большинство растворов для ингаляций приготовляются на основе физиологического раствора 0,9% хлорида натрия (NaCl) в качестве растворителя и увлажнителя.
6. Хранить приготовленный раствор нужно в холодильнике не более суток. Перед употреблением обязательно подогреть до комнатной температуры
7. При одновременном назначении нескольких препаратов следует соблюдать очередность. Первым ингалируется бронхорасширяющее средство, спустя 15-20 минут – средство разжижающее и выводящее мокроту, затем, после отхождения мокроты, – антибиотик или противовоспалительное средство
8. Курс лечения зависит от сложности заболевания и применяемого препарата (от 5 до 10 дней)
9. Хотя небулайзерная терапия не относится к тепловым физиотерапевтическим процедурам, тем не менее, не рекомендуется проводить ингаляции при повышенной температуре тела
10. В небулайзерах запрещено использовать масляные препараты. Различные масла используются для лечения заболеваний только верхних дыхательных путей, для которых достаточно воздействие крупнодисперсных частиц, поэтому для ингаляций маслами используются паровые ингаляторы.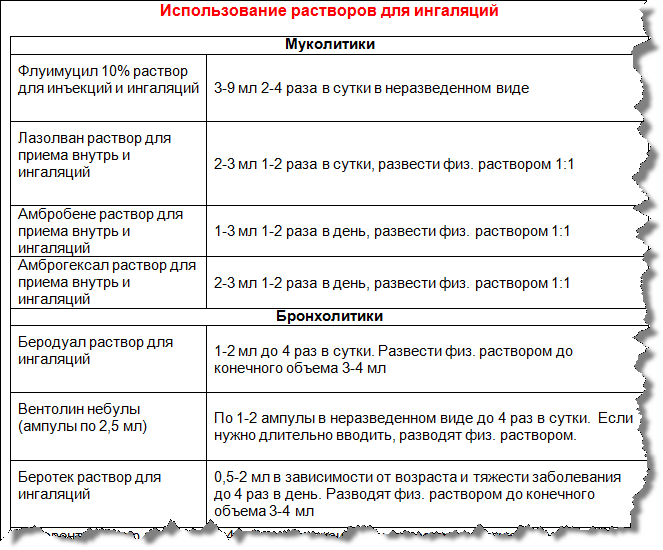 Небулайзер производит мелкодисперсные частицы. При использовании масляных растворов, происходит попадание мелкодисперсных частиц масла в легкие, а это существенно повышает риск развития так называемых масляных пневмоний. Так же применение эфирных масел в небулайзерах повышает риск возникновения аллергии по причине высокой концентрации активных веществ в легких.
Небулайзер производит мелкодисперсные частицы. При использовании масляных растворов, происходит попадание мелкодисперсных частиц масла в легкие, а это существенно повышает риск развития так называемых масляных пневмоний. Так же применение эфирных масел в небулайзерах повышает риск возникновения аллергии по причине высокой концентрации активных веществ в легких.
11. В большинстве небулайзеров не разрешено использование самостоятельно приготовленных отваров и настоев трав, поскольку они имеют взвесь, которая значительно крупнее частиц аэрозоли и небулайзер не может их пропустить, что в свою очередь может привести к поломке прибора. По той же причине в небулайзерах не используют суспензии и сиропы (за исключением специальных суспензий для ингаляций). Хотя существуют небулайзеры, которые способны работать с отварами трав.
12. Такие лекарственные препараты как Эуфиллин, Папаверин, Димедрол и им подобные средства, так же не могут быть использованы в небулайзерах, поскольку они не имеют «точек приложения» на слизистой оболочке.
13. НЕ ЗАБУДЬТЕ ПРОКОНСУЛЬТИРОВАТЬСЯ С ВРАЧОМ!
1.Препараты, расширяющие бронхи (Бронхолитики)
- Беродуал, действующее вещество: фенотерол и бромид ипратропиума (раствор для ингаляций) – Предупреждение и лечение удушья при хронических обструктивных заболеваниях дыхательных путей. Наиболее эффективный из бронхорасширяющих препаратов, обладает наименьшими побочными действиями.
- Взрослым и детям старше 12 лет – 2 мл (40 капель) препарата на 1 ингаляцию, до 4 раз в день
- Детям от 6 до 12 лет – 1 мл (20 капель) препарата на 1 ингаляцию, до 4 раз в день
- Детям до 6 лет – 0,5 мл (10 капель) препарата на 1 ингаляцию, до 3 раз в день
- Для приготовления ингаляционного раствора следует к рекомендуемой дозе препарата добавить 3 мл физраствора
- Беротек, действующее вещество: фенотерол (0,1%-ный раствор для ингаляций) –для купирования приступа бронхиальной астмы:
- Взрослым и детям старше 12 лет – 0,5 мл (0,5 мг – 10 капель), в тяжелых случаях – 1 мл (1 мг – 20 капель)
- Детям 6–12 лет (масса тела 22–36 кг) – 0,25-0,5 мл (0,25-0,5 мг – 5-10 капель), в тяжелых случаях – 1 мл (1 мг – 20 капель)
Профилактика и симптоматическое лечение бронхиальной астмы и хронической обструктивной болезни легких:
- Взрослым и детям старше 6 лет – 0,5 мл (0,5 мг – 10 капель) на 1 ингаляцию, до 4 раз в день
- Детям до 6 лет (масса тела менее 22 кг) – 0,25-1 мл (0,25-1 мг – 5-20 капель), до 3 раз в день
- Рекомендованную дозу непосредственно перед применением разводят физраствором до объема 3–4 мл.
 Интервал между ингаляциями не должен быть менее 4 часов.
Интервал между ингаляциями не должен быть менее 4 часов. - Сальгим, Вентолин Небулы, действующее вещество: сальбутамол (0,1%-ный раствор для ингаляций) – Купирование приступов удушья, профилактика и симптоматическое лечение бронхиальной астмы и хронической обструктивной болезни легких. По эффекту значительно уступает Беротеку
- Взрослым и детям – 2,5 мл (2,5 мг) на 1 ингаляцию, до 4 раз в день с интервалом между ингаляциями не менее 6 часов
- Предназначен для использования в неразведенном виде
- Атровент, действующее вещество: бромид ипратропиума (0,025%-ный раствор для ингаляций) – Купирование приступов удушья, профилактика и симптоматическое лечение бронхиальной астмы и хронической обструктивной болезни легких. По эффекту несколько уступает Беротеку и препаратам сальбутамола, но основным достоинством является безопасность применения
- Взрослым и детям старше 12 лет – 0,5 мг (40 капель) на 1 ингаляцию, 3–4 раза в день
- Детям 6–12 лет – 0,25 мг (20 капель) на 1 ингаляцию, 3–4 раза в день
- Детям до 6 лет – по 0,1–0,25 мг (8-20 капель) на 1 ингаляцию, 3–4 раза в день (под наблюдением врача).

- Рекомендованную дозу непосредственно перед применением разводят физраствором до объема 3–4 мл. Интервал между ингаляциями не менее 2 часов
2. Препараты, разжижающие мокроту (Муколитики) и выводящие мокроту (Секретолитики, отхаркивающие)
- Флуимуцил, АЦЦ Инъект, действующее вещество: ацетилцистеин
- Взрослым и детям старше 12 лет – 3 мл препарата на 1 ингаляцию, 1-2 раза в день
- Детям от 6 до 12 лет – 2 мл препарата на 1 ингаляцию, 1-2 раза в день
- Детям от 2 до 6 лет – 1-2 мл препарата на 1 ингаляцию, 1-2 раза в день
- Рекомендуемую дозу препарата следует развести с физраствором в соотношении 1:1
- Курс лечения – не более 10 дней
- Препараты ацетилцистеина не следует применять одновременно с приемом антибиотиков, т.к. они снижают всасываемость антибиотиков.

- Лазолван, Абмробене, действующее вещество: амброксол (раствор для ингаляций и приема внутрь) – Острые и хронические заболевания дыхательных путей с выделением вязкой мокроты
- Взрослым и детям старше 6 лет – 2-3 мл раствора на 1 ингаляцию, 1-2 раза в день
- Детям от 2 до 6 лет – 2 мл раствора на 1 ингаляцию 1-2 раза в день
- Детям до 2 лет – 1 мл раствора на 1 ингаляцию, 1-2 раза в день
- Для приготовления ингаляционного раствора следует рекомендуемую дозу препарата развести с физраствором в соотношении 1:1
- Курс лечения – не более 5 дней
- Препараты на основе амбоксола не следует применять одновременно с противокашлевыми препаратами (например: кодеин, либексин, фалиминт, бронхолитин, пектуссин, синекод и др.
 ). Применение препаратов амброксола способствует хорошему всасыванию антибиотиков.
). Применение препаратов амброксола способствует хорошему всасыванию антибиотиков. - Нарзан, Боржоми (слабощелочные минеральные воды)
- На 1 ингаляцию используют 3-4 мл минеральной воды, 2-4 раза в день.
- Перед ингаляцией минеральную воду следует отстоять до дегазации.
- Синупрет, гомеопатический фитопрепарат (капли на основе экстрактов растений: корень генциана (горечавки), щавель, первоцвет, бузина, вербена) – Восстанавливает защитные свойства и уменьшает отек слизистой оболочки дыхательных путей при острых и хронических синуситах. Способствует оттоку экссудата из придаточных пазух носа
- Для приготовления ингаляционного раствора препарат необходимо предварительно развести в физрастворе:
- Для взрослых и детей старше 16 лет – в соотношении 1:1 (на 1 мл препарата 1 мл физраствора)
- Для детей от 6 до 16 лет – в соотношении 1:2 (на 1 мл препарата 2 мл физраствора)
- Для детей от 2 до 6 лет – в соотношении 1:3 (на 1 мл препарата 3 мл физраствора)
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.

- Геделикс, фитопрепарат (капли на основе экстракта плюща) – Заболевания верхних дыхательных путей и бронхов с трудноотделяемой мокротой, кашель (в т.ч. сухой)
- Для приготовления ингаляционного раствора препарат необходимо предварительно развести в физрастворе:
- Для взрослых и детей старше 10 лет – в соотношении 1:1 (на 1 мл препарата 1 мл физраствора)
- Для детей до 10 лет – в соотношении 1:2 (на 1 мл препарата 2 мл физраствора)
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
- Микстура от кашля, фитопрепарат (порошок (детский и взрослый) для приготовления раствора на основе экстрактов растений: анис, корень солодки, корень алтея, термопсис) – Заболевания дыхательных путей, сопровождающиеся кашлем, особенно при затрудненном отхождении мокроты
- Для приготовления ингаляционного раствора следует содержимое 1 упаковки растворить в 15 мл физраствора до полного рстворения без осадка
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.

- Мукалтин, фитопрепарат (таблетки на основе экстракта корня алтея) – Отхаркивающее средство при заболеваниях дыхательных путей и легких
- Для приготовления ингаляционного раствора следует 1 таблетку растворить в 80 мл физраствора до полного растворения без осадка
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
- Пертуссин, фитопрепарат (раствор на основе экстракта растений: чабрец, тимьян) – Отхаркивающее средство при трахеите, бронхите, коклюше
- Для приготовления ингаляционного раствора препарат необходимо предварительно развести в физрастворе:
- Для взрослых и детей старше 12 лет – в соотношении 1:1 (на 1 мл препарата 1 мл физраствора)
- Для детей до 12 лет – в соотношении 1:2 (на 1 мл препарата 2 мл физраствора)
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
3. Противовоспалительные препараты
- Ротокан, фитопрепарат (спиртовой настой экстарактов растений: календула, ромашка, тысячелистник) – Острые воспалительные заболевания верхних и средних дыхательных путей
- Раствор для ингаляции готовят путем разведения препарата в физрастворе в отношении 1:40 (1 мл препарата на 40 мл физраствора)
- На 1 ингаляцию используют 4 мл полученного раствора, 3 раза в день.

- Прополис, фитопрепарат (настойка) – Воспалительные процессы, боль и травмы верхних и средних дыхательных путей
- Раствор для ингаляции готовят путем разведения препарата в физрастворе в отношении 1:20 (1 мл препарата на 20 мл физраствора)
- На 1 ингаляцию используют 3 мл полученного раствора, 3 раза в день.
- Противопоказания – аллергия к продуктам пчеловодства
- Эвкалипт, фитопрепарат (спиртовая настойка) – Воспалительные заболевания верхних и средних дыхательных путей
- Раствор для ингаляции готовят путем разведения 10-15 капель препарата в 200 мл физраствора
- На 1 ингаляцию используют 3 мл полученного раствора, 3-4 раза в день
- Противопоказания – бронхиальная астма, бронхоспазм (удушье)
- Малавит, биологически активная добавка (спиртовая настойка на основе минеральных веществ и экстрактов растений) – Острые воспалительные заболевания и боль верхних и средних дыхательных путей
- Раствор для ингаляции готовят путем разведения препарата в физрастворе в отношении 1:30 (1 мл препарата на 30 мл физраствора)
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.

- Тонзилгон Н, гомеопатический фитопрепарат (капли на основе экстрактов растений: корень алтея, листья грецкого ореха, хвощ, ромашка, тысячелистник, кора дуба, одуванчик) – Острые и хронические заболевания верхних отделов дыхательных путей (тонзиллит, фарингит, ларингит)
- Для приготовления ингаляционного раствора препарат необходимо предварительно развести в физрастворе:
- Для взрослых и детей старше 7 лет – в соотношении 1:1 (на 1 мл препарата 1 мл физраствора)
- Для детей от 1 до 7 лет – в соотношении 1:2 (на 1 мл препарата 2 мл физраствора)
- Для детей до 1 года – в соотношении 1:3 (на 1 мл препарата 3 мл физраствора)
- На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
- Календула, фитопрепарат (спиртовой настой экстаракта календулы) – Острые воспалительные заболевания верхних отделов дыхательных путей
- Раствор для ингаляции готовят путем разведения препарата в физрастворе в отношении 1:40 (1 мл препарата на 40 мл физраствора)
- На 1 ингаляцию используют 4 мл полученного раствора, 3 раза в день
4. Противовоспалительные гормональные препараты (Глюкокортикостероиды) и противоаллергические препараты (Антигистамины)
Противовоспалительные гормональные препараты (Глюкокортикостероиды) и противоаллергические препараты (Антигистамины)
- Пульмикорт, действующее вещество: будесонид (суспензия для ингаляций, выпускается в «детской» (0,25 мг/мл) и «взрослой» (0,5 мг/мл) дозировках) – Острые воспалительные заболевания нижних дыхательных путей (бронхиальная астма, хроническая болезнь легких), требующие лечения гормональными препаратами. Обладает противовоспалительным и противоаллергическим действием.
- Взрослые/пожилые и дети старше 12 лет – 1 мг на 1 ингаляцию, 1-3 раза в день
- Дети от 6 мес. и до 12 лет – 0,25 мг на 1 ингаляцию, 1-3 раза в день
- Данный препарат не применяют в ультразвуковых небулайзерах. Если разовая доза препарата менее 2 мл, то следует добавить физраствор для увеличения объема ингалируемого раствора до 2 мл. В остальных случаях препарат ингалируют в чистом виде (без разведения в физрастворе).
- Суточная доза препарата:
0,25 мг/мл – 1 мл по 0,25 мг/мл
0,5 мг/мл – 2 мл по 0,25 мг/мл
0,75 мг/мл – 3 мл по 0,25 мг/мл
1 мг/мл – 4 мл по 0,25 мл/мг или 2 мл по 0,5 мг/мл
1,5 мг/мл – 3 мл по 0,5 мг/мл
2 мг/мл – 4 мл по 0,5 мг/мл
- Дексаметазон, (0,4%-ный раствор для инъекций, 4 мг/мл) – Острые воспалительные заболевания дыхательных путей, требующие лечения гормональными препаратами
- На 1 ингаляцию используют 0,5 мл (2 мг) препарата, до 4 раз в день.

- Курс лечения не более 7 дней
- Для приготовления ингаляционного раствора к рекомендуемой дозе препарата следует добавить 3 мл физраствора.
- Также можно ампулы с препаратом предварительно развести в физрастворе в соотношении 1:6 (на 1 мл препарата 6 мл физраствора) и ингалировать по 3-4 мл полученного раствора на 1 ингаляцию.
- Кромогексал, действующее вещество: кромоглициевая кислота (раствор для ингаляций, 20 мг / 2 мл) – Обладает антиаллергическим, противовоспалительным, антиастматическим действием.
- Взрослым и детям старше 2 лет ингалировать по содержимому 1 флакона (без разведения с физраствором) 4 раза в день, по возможности, в равные временные интервалы.
- При необходимости рекомендованная доза может быть увеличена в 2 раза, а частота применения может быть увеличена до 6 раз.
5. Противомикробные и антибактериальные препараты (Антибиотики и Антисептики)
- Флуимуцил-антибиотик, действующее вещество: ацетилцистеин и тиамфеникол (порошок для инъекций и ингаляций в комплекте с растворителем) – Необходимость одновременного введения антибиотика и препарата разжижающего и выводящего мокроту и слизь из нижних и верхних дыхательных путей.

Выбрать ингалятор > > > >
Купить ингалятор компрессорный (небулайзер) в нашем магазине просто ― закажите его оформив заявку на сайте самостоятельно или позвоните менеджеру. Подробнее > > > >
Цены актуальны при самовывозе из офиса в Омске. Также продажа медтехники осуществляется с помощью курьерской доставки, а в другие регионы Почтой России или транспортными компаниями. Подробнее > > > >
Оставьте свой отзыв о стоимости медтехники, применении прибора и работе магазина «Медицинская техника для дома». Подробнее > > > >
инструкция по применению и какие использовать
|
Статья подготовлена Беликовой Екатериной Вячеславовной, врач, с высшим образованием. Специально для сайта medprostor.by |
При заболеваниях респираторного тракта терапевты часто назначают раствор для ингаляции. Для этого необходимо иметь специальный прибор – небулайзер. Такой способ лечения применим при патологии любого отдела респираторного тракта. Необходимо правильно подобрать раствор и его дозировку, чтобы получить лечебные действия без побочных эффектов.
Для этого необходимо иметь специальный прибор – небулайзер. Такой способ лечения применим при патологии любого отдела респираторного тракта. Необходимо правильно подобрать раствор и его дозировку, чтобы получить лечебные действия без побочных эффектов.
Классификация препаратов для ингаляций
Выделяется обширная классификация растворов, применяемых для ингаляций. Разновидность препарата зависит от диагноза.
-
Бронхолитики. Применяются для расширения бронхов при их сужении (обструктивный бронхит, бронхиальная астма). Используя Беродуал, Атровент, Беротек.
-
Муколитики. Разжижают и выводят мокроту вверх по респираторному тракту. Используются в случае, если мокрота становится слишком вязкой. Применяют Амброксол, АЦЦ, Лазолван.
-
Противовоспалительные и гормональные средства. Применяют при ларингите и других заболеваниях, сопровождающихся воспалением.
 Использовать Пульмикорт, Декасан.
Использовать Пульмикорт, Декасан.
-
Антибактериальные препараты, антисептики. Используют только при доказанной природе инфекционного заболевания, например, трахеит или бронхит с гнойной мокротой. Применяют Фурацилин, Флуимуцил-Антибиотик ИТ.
-
Антигистаминные средства. Применяют во время аллергии: Кромгексал.
-
Иммуномодуляторы. Используют в качестве дополнительной терапии, когда человек часто болеет респираторными вирусными инфекциями. Используют Интерферон, Деринат.
Категорически не рекомендуется применение средства самостоятельно. Могут возникнуть серьезные побочные эффекты. Например, если использовать антибиотики при вирусных заболеваниях, состояние пациента может обостриться грибковой инфекцией.
Какие растворы подходят для детей
Раствор для ингаляций включает инструкцию по применению, ей следует строго руководствоваться. На всех средствах указан возраст, с которого можно начинать использовать раствор.
На всех средствах указан возраст, с которого можно начинать использовать раствор.
Большинство антибактериальных препаратов для ингаляции применимы только с 2-3 летнего возраста. Гормональные средства рекомендуется применять с 4-6 летнего возраста. Для усиления выведения мокроты при продуктивном кашле используют Амбробене, Амброксол. Они применимы с 3 месяцев. Более серьезным считается Флуимуцил. Его используют с 2 лет.
Чтобы снизить концентрацию препарата, его необходимо развести. Педиатр расскажет, как разводить препарат физраствором для ингаляций, чтобы получить эффект.
Какие растворы подходят для взрослых
Для назначения лекарства учитывают состояние здоровья. Например, если человек страдает от иммунодефицита, не рекомендуется применять ингаляции с антибиотиками. Это вызовет грибковую инфекцию. Гормональные ингаляции не делают людям эндокринными нарушениями.
Если здоровье пациента удовлетворительно, он может использовать любые препараты для ингаляции, в соотношении с определяемыми симптомами болезни. У терапевта узнают, какие растворы для ингаляций применимы.
У терапевта узнают, какие растворы для ингаляций применимы.
Подбор раствора для ингаляции в зависимости от диагноза
Лекарственные средства определяются врачом терапевтом, инфекционистом, пульмонологом и другими специалистами в зависимости от поставленного диагноза. Если самостоятельно выбрать раствор, высок риск осложнений, так как нужно знать, как развести раствор для ингаляции правильно.
Многие препараты разбавляют физраствором. Некоторые пациенты не знают, каким физраствором делать ингаляцию. Для этого применяется стерильная жидкость из аптеки, которую набирают шприцем и перемещают в небулайзер.
Не рекомендуется самостоятельно делать физраствор из поваренной соли, так как он должен быть стерилен. Поэтому пациенту нет необходимости знать, как приготовить раствор для ингаляций, его только покупают.
Бронхит
Бронхит – воспалительное заболевания бронхиального дерева. При нем возможен сухой или влажный кашель.
-
Пертуссин. Разжижает и выводит мокроту. Препарат примененим для влажного и сухого кашля. Обладает сильным противокашлевым действием. Взрослые осуществляют ингаляции до еды по 15 мл 3 раза в сутки. Для детей от 3 до 6 лет используется 5 мл 2 раза в сутки. После 6 лет применяют 10 мл 3 раза в сутки.
-
Лазолван, Амброгексал. Раствор для ингаляций, разжижающий и выводящий мокроту. В основе средства лежит амброксола гидрохлорид. По инструкции к применению средство используют с 2-летнего возраста в концентрации 2 мл до 2 раз в сутки. Детям старше 6 лет: 3 мл 2 раза в день. Взрослым: 4 мл 3 раза в сутки.
-
Минеральная вода Боржоми или Нарзан. В них содержится на соль, которая способствует увлажнению слизистой оболочки. Раствор можно применять для любых возрастов. В детском возрасте используют 3-4 мл 2-3 раза в сутки. Взрослым: 5 мл 3-4 раза в сутки.

-
Хлорофиллипт. Обладает антисептическим эффектом. Подходит для бронхита с гнойной мокротой. Разведение осуществляют в концентрации 1 мл препарата на 10 мл физраствора. Детям делают ингаляции 2 в день по 3 мл раствора. Взрослым можно делать 4 ингаляции в день концентрации 5 мл раствора.
-
АЦЦ, Флуимуцил. Сильно разжижают и выводят мокроту. Детям с 2 до 6 лет применяют 2 мл средства до 2 раз в день. С 6 до 12 лет дозировка увеличивают до 2 мл 3 раза в сутки. Взрослым можно использовать 3 мм до 4 раз в сутки.
-
Пульмикорт. Относится к гормональным веществам на основе будесонида. Показан при воспалительном бронхите. Его разводят в соотношении 1 мл препарата на 2 мл физраствора. Детям от 6 месяцев и старше применяют дозировку 0,25- 0,5 мг за 1 сутки. Для взрослых дозировку увеличивают до 2 мг в сутки.
Чтобы не переразжижить мокроту, все дозировки следует соблюдать полностью.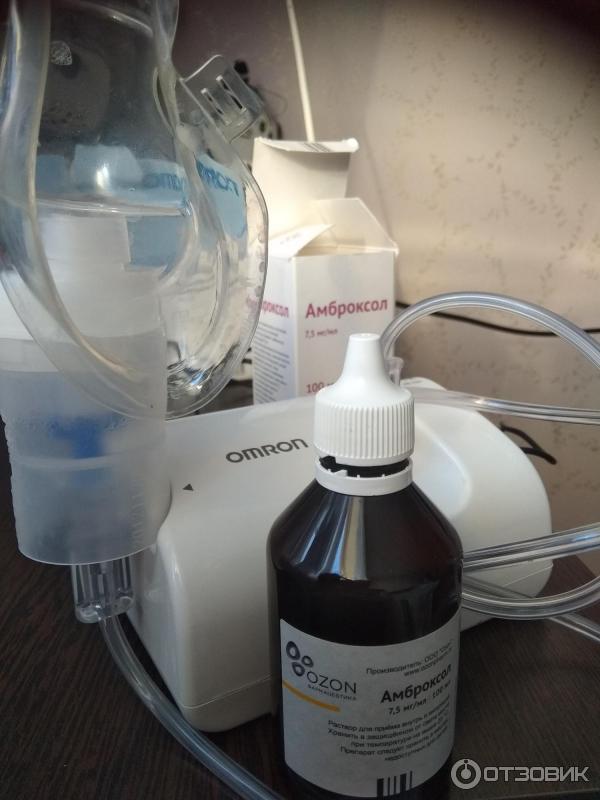
Бронхоспазм
При бронхоспазме сужается просвет бронхов, поэтому мокрота не может выйти наружу.
-
Беродуал. Расширяет просвет бронхов, степень действия зависит от количества препарата. Для детей до 6 лет средство должно применяться не более 10 капель. Детям старше 6 лет применяют до 40 капель, в зависимости от тяжести заболевания. Взрослым можно применять по 80 капель в тех же критериях.
-
Пульмовент. Раствор для ингаляций, по инструкции устраняет спазм бронхов. Детям до 6 лет назначают до 12 капель. После 6 лет используют до 24 капель. Взрослым – до 48 капель. Применяют 3-4 раза в день.
Бронхоспазм – опасное состояние, которое необходимо быстрее устранить.
Насморк
Перед проведением ингаляции рекомендуется прочистить носовые ходы, чтобы пары проходили беспрепятственно.
-
Синупрет.
 Растительное средство, снимающее воспаление, отек. Обладает небольшим антибактериальным действием. Устраняет воспаление в носовых пазухах. Используют для детей от 2 лет. Его разводят соотношении 1 мл препарата на 2 мл физраствора. Применяют 2 раза в сутки. Для детей от 6 лет разведение 1:2, применяют 2 раза в сутки. Для взрослых разведение 1:1, применяется в 3 раз в сутки.
Растительное средство, снимающее воспаление, отек. Обладает небольшим антибактериальным действием. Устраняет воспаление в носовых пазухах. Используют для детей от 2 лет. Его разводят соотношении 1 мл препарата на 2 мл физраствора. Применяют 2 раза в сутки. Для детей от 6 лет разведение 1:2, применяют 2 раза в сутки. Для взрослых разведение 1:1, применяется в 3 раз в сутки.
-
Эвкалиптовое масло. Препарат разводят в соотношении 7 капель на 100 гр. раствора. Вдхание может осуществляться только с помощью паровых приборов, но не небулайзеров. Обладает увлажняющим, антибактериальным действием. Снимает раздражение и воспаление.
-
Физраствор. Это наиболее подходящее средство, практически не имеет противопоказаний, применяется в любом возрасте. Родители должны знать, как делать ингаляции с физраствором ребенку. Используют концентрацию 2 мл для детей, 4-5 мл – для взрослых. Ингаляции делают 2-3 раза в сутки.
 Как заправить ингалятор физраствором: жидкость помещается в контейнер и плотно закручивается крышкой, подсоединяются трубочки и маска.
Как заправить ингалятор физраствором: жидкость помещается в контейнер и плотно закручивается крышкой, подсоединяются трубочки и маска.
Также можно применять ингаляции с помощью Нарзана и Боржоми в той же концентрации.
Гайморит
Гайморит – воспалительный процесс в носовых пазухах. Применяются те же препараты, что и при насморке, но обязательно должны употребляться системные антибактериальные средства.
Фарингит
Фарингит – воспаление горла и окружающей лимфоидной ткани.
-
Тонзилгон Н. Растительное, антисептическое средство. Подходит для детей с самого рождения. Для детей с 1 года применяют 1мл препарата на 2 мл физраствора. Для взрослых используется в отношении 1:1. Используют 1-2 раза в сутки.
-
Ротокан. Это средство на основе ромашки, календулы. Обладает антисептическим, успокаивающим действием.
 Для получения необходимой жидкости 10 мл препарата разводят 50 мл физраствора. Для детей используют концентрацию 2 мл 2 раза в сутки, взрослым можно использовать 4мл 4 раз в сутки.
Для получения необходимой жидкости 10 мл препарата разводят 50 мл физраствора. Для детей используют концентрацию 2 мл 2 раза в сутки, взрослым можно использовать 4мл 4 раз в сутки.
При фарингите средства используются редко, в основном применимы для полоскания.
Ларингит
Ларингит – воспаление гортани, которое сопровождает простудное заболевание.
-
Дексаметазон. Гормональное средство, показано для снятия воспаления. Как сделать раствор для ингаляции: 2 мл препарата на 2 мл физраствора. Показан к применению с трёхлетнего возраста. Рекомендуется единократное использование для устранения лающего кашля.
-
Применяют те же препараты, что и при фарингите.
Рекомендовано перед применением гормонального средства проконсультироваться с терапевтом для снижения риска побочных эффектов.
Ангина
Ангина – гнойное воспаление миндалин.
-
Хлорофиллипт в том же разведении, что и для бронхита.
-
Мирамистин. Обладает антисептическим, успокаивающим действием. Как приготовить раствор для ингаляции: 2 мл средства на 2 мл физраствора. Ингаляции 2 раза в сутки.
- Фурацилин. Антибактериальное средство. Его не разводят, оно практически не имеет противопоказаний, применимо с детского возраста. Используется 2 мл для детей, 5 мл для взрослых. Можно применять 2-3 раза в день.
Если появилось побочное действие от выбранного препарата, следует незамедлительно прекратить его употребление. После завершения лечения рекомендуется повторно пройти обследование у врача.
Краткие выводы
- Раствор для ингаляции выбирается исходя из диагноза поставленного врачом.

- Раствор для ингаляции детям должен выбираться только под руководством врача, так как дети более чувствительны на лекарства.
- Взрослый выбирает раствор для ингаляции в зависимости от состояния здоровья. Если человек страдает от иммунодефицита, не использование антибиотиков, в любом другом случае применяется любое лекарство в зависимости от поставленного диагноза
Ингаляции: показания и противопоказания — Санатории им. Воровского
Для лечения и профилактики заболеваний нижних и верхних дыхательных путей в Санатории имени Воровского проводится ингаляционная терапия – вдыхание воздуха, насыщенного лекарственными средствами. Основное назначение процедуры – разжижение мокроты и ее вывод из легких и бронхов.
Мельчайшие частицы лечебных веществ в виде пара или аэрозоля равномерно оседают на ткани дыхательных путей и через кровь быстрее разносятся по организму. В качестве лечебных составляющих используют травы, минеральную воду, эфирные масла, медицинские препараты.
Кому полезны ингаляции
Эта процедура является одной из основных в комплексной терапии хронических заболеваний дыхательной системы. В санатории имени Воровского ингаляции проводят для профилактики и лечения респираторных заболеваний, неврозов, ринитов, аллергических реакций. Кроме этого, данную процедуру назначают людям пожилого возраста для увлажнения слизистой носоглотки, работникам «пыльных» производств, профессиональным ораторам или певцам.
Лечебные эффекты процедуры
В зависимости вводимого в организм лекарства можно добиться следующих лечебных эффектов:
- противовоспалительного;
- антимикробного;
- отхаркивающего;
- бронхолитического;
- иммуноукрепляющего;
- успокаивающего.
Показания к процедуре
В большинстве случаев ингаляции показаны при следующих заболеваниях:
- бронхите, фарингите, ларингите и др.;
- бронхиальной астме;
- гайморите;
- ОРВИ и ОРЗ и др.
Также терапия полезна для укрепления иммунитета, лечения бессонницы, аллергии, в послеоперационный период.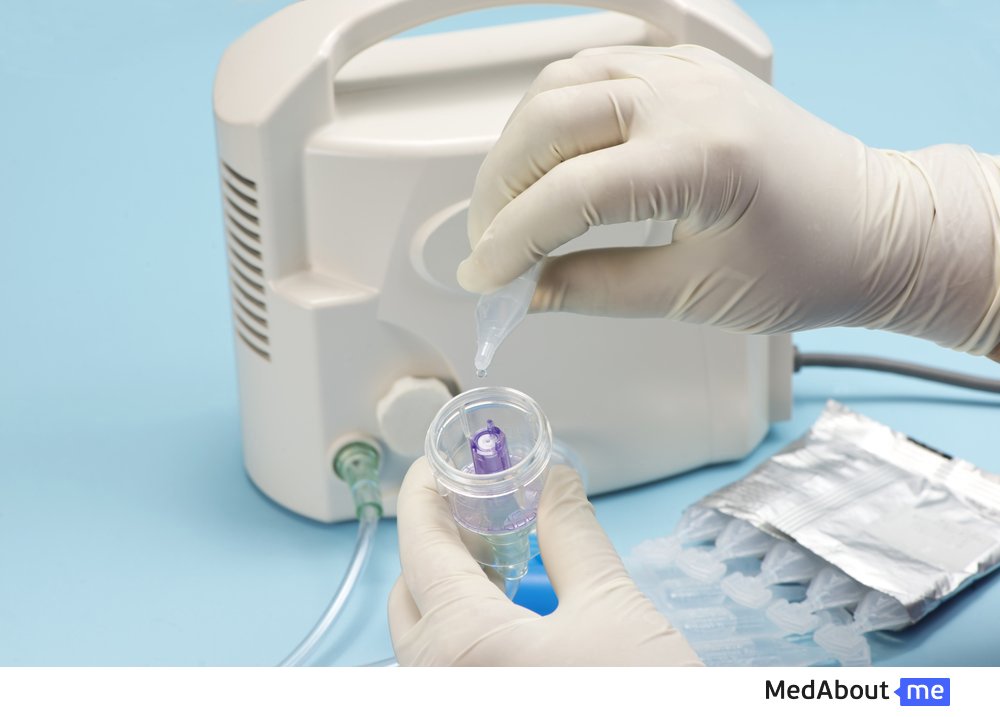
Противопоказания
К общим противопоказаниям процедуры относятся:
- повышенная температура тела;
- носовые кровотечения и предрасположенность к ним;
- эмфизема легких в тяжелой форме;
- сердечно-сосудистые заболевания, отягощенные дыхательной недостаточностью;
- индивидуальная непереносимость компонентов и др.
Санаторий имени Воровского располагает широким ассортиментом лекарственных препаратов для проведения ингаляций. Это дает возможность применять целебную терапию для пациентов с различными недугами.
Лекарства для небулайзерной терапии и ингаляций
Группы ингаляционных препаратов:
- Антисептики (Фурацилин, Диоксидин, Мирамистин)
- Антибиотики (Гентамицин, Тобрамицин)
- Анестетики (Лидокаин)
- Гормональные препараты (Кромогексал, Будесонит, Пульмикорт, Дексаметазон)
- Иммуномодуляторы (Интерферон, Деринат)
- Муколитики (Флуимуцил, Лазолван, Амброксол, Амброгексал, Пульмозим, Ацетилцистеин)
- Бронходилятаторы (Беродуал, Фенотерол, Вентолин, Беротек, Саламол)
- Фитотерапия (Ротокан, Туссамаг, Хлорофиллипт)
- Сосудосуживающие средства (Адреналин, Нафтизин)
- Щелочные и солевые растворы (0,9% физиологический раствор)
Не рекомендуются использовать для небулайзеров:
- Все растворы, содержащие масла
- Суспензии и растворы, содержащие взвешенные частицы, в том числе отвары и настои трав
- Растворы эуфиллина, папаверина, платифиллина, димедрола и им подобные средства
- Препараты, содержащие спиртовые растворы
- Рекомендации при проведении ингаляций детям:
- Нельзя заставлять ребенка дышать часто во время ингаляций
- Нельзя проводить ингаляции сразу после еды
- Нельзя самопроизвольно назначать или увеличивать лекарственные дозы, назначенные врачом
- После ингаляций дайте ребенку отдохнуть
Растворы для ингаляций при лечении детей:
-
Бронходилятаторы (препараты, которые расширяют бронхи)
Беродуал (фенотерол и бромид ипратропиума раствор для ингаляций)
Взрослым и детям старше 12 лет – 2 мл (40 капель) препарата на 1 ингаляцию, до 4 раз в день
Детям от 6 до 12 лет – 1 мл (20 капель) препарата на 1 ингаляцию, до 4 раз в день
Детям до 6 лет – 0,5 мл (10 капель) препарата на 1 ингаляцию, до 3 раз в день
Атровент (бромид ипратропиума 0,025% раствор для ингаляций)
Взрослым и детям старше 12 лет – 0,5 мг (40 капель) на 1 ингаляцию, 3–4 раза в день
Детям 6–12 лет – 0,25 мг (20 капель) на 1 ингаляцию, 3–4 раза в день
Детям до 6 лет – по 0,1–0,25 мг (8-20 капель) на 1 ингаляцию, 3–4 раза в день (под наблюдением врача).
Рекомендованную дозу перед применением разводят физиологическим раствором до объема 4 мл.
- Муколитики (препараты, разжижающие мокроту
АЦЦ (ацетилцистеин 10% раствор для инъекций)
Взрослым и детям старше 12 лет – 3 мл препарата на 1 ингаляцию, 1-2 раза в день
Детям от 6 до 12 лет – 2 мл препарата на 1 ингаляцию, 1-2 раза в день
Детям от 2 до 6 лет – 1-2 мл препарата на 1 ингаляцию, 1-2 раза в день
Рекомендуемую дозу препарата необходимо развести с физиологическим раствором в соотношении 1:1.
Лазолван (амброксол — раствор для ингаляций и приема внутрь)
Взрослым и детям старше 6 лет – 2-3 мл раствора на 1 ингаляцию, 1-2 раза в день
Детям от 2 до 6 лет – 2 мл раствора на 1 ингаляцию 1-2 раза в день
Детям до 2 лет – 1 мл раствора на 1 ингаляцию, 1-2 раза в день
Для приготовления ингаляционного раствора необходимо развести дозу препарата с физиологическим раствором в соотношении 1:1
Нарзан, Боржоми (слабощелочные минеральные воды)
На 1 ингаляцию используют 3-4 мл минеральной воды, 2-4 раза в день.
Перед ингаляцией минеральную воду следует отстоять до дегазации.
Синупрет (гомеопатический фитопрепарат — капли на основе экстрактов растений)
Для приготовления ингаляционного раствора препарат необходимо предварительно развести в физиологическом растворе:
Для взрослых и детей старше 16 лет – в соотношении 1:1 (на 1 мл препарата 1 мл физраствора)
Для детей от 6 до 16 лет – в соотношении 1:2 (на 1 мл препарата 2 мл физраствора)
Для детей от 2 до 6 лет – в соотношении 1:3 (на 1 мл препарата 3 мл физраствора)
На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
Мукалтин (таблетки на основе экстракта корня алтея)
Для приготовления ингаляционного раствора необходимо 1 таблетку растворить в 80 мл физиологического раствора до полного растворения таблетки без оставления осадка
На 1 ингаляцию используют 3-4 мл полученного раствора, 3 раза в день.
- Гормональные и антигистаминные препараты
Пульмикорт (будесонид — суспензия для ингаляций. «детская» (0,25 мг/мл) и «взрослая» (0,5 мг/мл) дозировка
Взрослые/пожилые и дети старше 12 лет – 1 мг на 1 ингаляцию, 1-3 раза в день
Дети от 6 мес. и до 12 лет – 0,25 мг на 1 ингаляцию, 1-3 раза в день
Этот препарат не используют в ультразвуковых небулайзерах. Если разовая доза препарата меньше 2 мл, то необходимо добавить физиологический раствор для увеличения объема раствора до 2 мл.
Суточная доза препарата:
0,25 мг/мл – 1 мл по 0,25 мг/мл
0,5 мг/мл – 2 мл по 0,25 мг/мл
0,75 мг/мл – 3 мл по 0,25 мг/мл
1 мг/мл – 4 мл по 0,25 мл/мг или 2 мл по 0,5 мг/мл
1,5 мг/мл – 3 мл по 0,5 мг/мл
2 мг/мл – 4 мл по 0,5 мг/мл\
Дексаметазон (0,4% раствор для инъекций, 4 мг/мл)
На 1 ингаляцию используют 0,5 мл (2 мг) препарата, до 4 раз в день.
Для приготовления ингаляционного раствора добавляют к рекомендуемой дозе 3 мл физиологического раствора.
- Антибиотики и антисептики
Фурацилин (нитрофурал 0,024% водный раствор, 1:5000)
Для ингаляции используют готовый раствор фурацилина по 4 мл на 1 ингаляцию 2 раза в день. Раствор приготавливается и покупается в аптеке, также можно приготовить раствор самостоятельно, растворив 1 таблетку фурацилина в 100 мл физиологического раствора до полного растворения таблетки без осадка.
Гентамицин (4% раствор сульфата гентамицина для инъекций, 40 мг/мл)
Взрослым и детям старше 12 лет – 0,5 мл (20 мг) препарата на 1 ингаляцию, 1-2 раза в день
Детям от 2 до 12 лет – 0,25 мл (10 мг) препарата на 1 ингаляцию, 1-2 раза в день
Для приготовления ингаляционного раствора к дозе препарата следует добавить 3 мл физиологического раствора.
Мирамистин (0,01% раствор)
Взрослым и детям старше 12 лет для ингаляции используют готовый 0,01%-ный раствор мирамистина по 4 мл на 1 ингаляцию 3 раза в день.
Детям до 12 лет для приготовления раствора для ингаляций препарат следует развести физиологическим раствором в соотношении 1:2.
Как выбрать небулайзер и ингалятор для детей и взрослых – лечение болезней
Ингалятор — это прибор для вдыхания лекарств для профилактики и лечения заболеваний дыхательных путей. В этой статье мы расскажем, как выбрать ингалятор, чем отличаются такие приборы, какие их виды существуют и кому они подходят.
Отличия ингалятора и небулайзера
Существует четыре вида ингаляторов. Самые простые — паровые. Они превращают лекарство во вдыхаемый пар. Остальные три — более сложные системы, которые называются «небулайзеры». Они превращают лекарства не в пар, а в мелкодисперсный аэрозоль. В зависимости от технологии, бывают компрессорные, ультразвуковые и меш-небулайзеры. Несмотря на эту разницу, слова «ингалятор» и «небулайзер» часто употребляют как синонимы.
Паровой ингалятор
Паровой ингалятор нагревает и испаряет лекарство. Получившийся пар состоит из крупных частиц. Они не могут проникнуть в нижние дыхательные пути, поэтому паровые ингаляторы подходят только для лечения верхних органов дыхания — полости носа, носовой и ротовой частей глотки.
Получившийся пар состоит из крупных частиц. Они не могут проникнуть в нижние дыхательные пути, поэтому паровые ингаляторы подходят только для лечения верхних органов дыхания — полости носа, носовой и ротовой частей глотки.
Паровые ингаляторы дешевле и имеют свои недостатки.
- Концентрация распыляемого вещества часто оказывается ниже минимально необходимой для терапевтического действия.
- С паровым ингалятором можно использовать не так много лекарств: большинство медикаментов разрушается при нагреве. Поэтому для ингалятора подходят эфирные масла, физрастворы или минеральная вода.
- Паровые ингаляции противопоказаны при высокой температуре тела.
- Ингаляции на паровых приборах дают результат только в начале болезни или применяются для профилактики.
Виды небулайзеров
- Компрессорный небулайзер
Компрессорный небулайзер образует аэрозоль за счёт воздуха, который под давлением поступает в камеру с лекарством. Лучше всего такой ингалятор помогает при кашле и насморке. Однако ингаляции можно делать только дома — такие приборы работают от сети и занимают много места. С компрессорным небулайзером можно использовать любые лекарства.
Лучше всего такой ингалятор помогает при кашле и насморке. Однако ингаляции можно делать только дома — такие приборы работают от сети и занимают много места. С компрессорным небулайзером можно использовать любые лекарства.
Ультразвуковые небулайзеры
Ультразвуковые небулайзеры создают аэрозоль вибрацией пьезоэлемента на поверхности раствора. Они компактны и бесшумны, поэтому их удобно брать с собой. Бесшумность позволяет проводить ингаляции маленьким детям, даже когда они спят. Недостаток такой технологии — в приборе нельзя использовать антибиотики, гормоны, муколитики и другие вещества, которые разрушаются при нагревании. Можно делать ингаляции физраствора, минеральной воды, лекарств на основе растительных экстрактов.
Меш-ингаляторы
Меш-ингаляторы образуют аэрозоль, просеивая лекарство через мелкосетчатую мембрану (mesh по-английски — «сетка»). Такие небулайзеры хорошо подходят аллергикам и астматикам. С ними можно использовать любые лекарства и проводить ингаляции где угодно — они компактны и работают от батареек. Наклон не влияет на работу меш-ингалятора, поэтому с его помощью можно проводить процедуры лёжа. Обычно приборы этого типа дороже прочих.
Такие небулайзеры хорошо подходят аллергикам и астматикам. С ними можно использовать любые лекарства и проводить ингаляции где угодно — они компактны и работают от батареек. Наклон не влияет на работу меш-ингалятора, поэтому с его помощью можно проводить процедуры лёжа. Обычно приборы этого типа дороже прочих.Из чего состоит небулайзер
Основная часть небулайзера — небольшой блок из безопасного пластика. Его главная задача — преобразовывать жидкость с лекарством в мелкодисперсный пар. К нему подсоединяется гибкий силиконовый шланг, на который, в свою очередь, крепятся разные насадки для носа и горла. В некоторых ингаляторах есть клапан, прекращающий подачу лекарства во время выдоха. Это позволяет экономить лекарство.О чём говорит размер частиц аэрозоля
От среднего размера частиц аэрозоля зависит эффективность небулайзера в лечении того или иного заболевания. Размер частиц принято измерять в микрометрах (мкм).Небулайзеры образуют аэрозоль с частицами различного размера.
- Частицы диаметром 5–10 мкм — оседают в гортани и носоглотке.
- 2–5 мкм — в трахее и бронхах.
- 0,5–2 мкм — проникают в альвеолы.
У многих моделей можно переключать размер частиц для целенаправленной терапии того или иного участка дыхательной системы.
При каких заболеваниях используют ингалятор и небулайзер
Ингаляторы призваны бороться с различными заболеваниями дыхательной системы, но их можно использовать и для профилактики. Как правило, процедуры назначают для смягчения сухого кашля при простуде. Небулайзер позволяет снять отек и увлажнить дыхательные пути. Кашель с мокротой также лечится ингалятором, который позволяет вывести мокроту из лёгких.
Как правило, процедуры назначают для смягчения сухого кашля при простуде. Небулайзер позволяет снять отек и увлажнить дыхательные пути. Кашель с мокротой также лечится ингалятором, который позволяет вывести мокроту из лёгких.
Также небулайзер используют для укрепления иммунитета и при следующих острых и хронических заболеваниях.
- Насморк.
- Острый или хронический ринит.
- Лёгкие формы бронхита.
- Неострая форма пневмонии.
- Грибковые и вирусные поражения.
- Воспаление слизистых оболочек.
Ещё ингалятор используют при сложных заболеваниях с острыми приступами — астме и аллергических реакциях — для быстрого облегчения самочувствия. Лекарства в таких случаях подбирает врач.
Советы по выбору ингалятора
Если вы принимаете препараты со строгой дозировкой (например, гормоны), выбирайте небулайзер, синхронизирующийся с дыханием. Такие модели подают аэрозоль только на вдохе, что позволяет экономить лекарство и точно соблюдать дозировку.
Такие модели подают аэрозоль только на вдохе, что позволяет экономить лекарство и точно соблюдать дозировку. Вот подходящие модели.
Компрессорные ингаляторы подойдут тем, кто ищет средство от кашля, а также пациентам с хроническими заболеваниями, которым нужны частые ингаляции. Для этих целей хороши мощные небулайзеры с высокой скоростью ингаляции.
Тяжелобольным, которым нужны длительные процедуры, подойдут модели с большим объёмом камеры и мощным компрессором, работающие непрерывно. Например, B.Well PRO-110, A&D CN-233, OMRON CompAir NE-C28 Plus, A&D CN-231.
Маленькие дети могут испугаться громкого прибора, поэтому, если ингалятор для ребёнка, — обращайте внимание на уровень шума. Как говорилось выше, самые тихие небулайзеры — ультразвуковые. Меш-ингаляторы тоже работают тихо. Многие компрессорные ингаляторы для детей выпускаются в виде игрушек или с различными весёлыми рисунками, чтобы заинтересовать малыша.
Если нужно, чтобы ингалятор всегда был под рукой, выбирайте небулайзер с меш-технологией. Ультразвуковые ингаляторы тоже портативны, но помните, что с ними можно использовать не все лекарства. Например, вам подойдут Little Doctor LD-207U, A&D UN-233.
Ультразвуковые ингаляторы тоже портативны, но помните, что с ними можно использовать не все лекарства. Например, вам подойдут Little Doctor LD-207U, A&D UN-233.
Выбирая ингалятор, обращайте внимание на показатель остаточного объёма лекарства в камере. Чем он меньше, тем экономнее будет расходоваться средство. Это важно, если речь идёт о дорогих медикаментах.
Для лечения заболеваний верхних дыхательных путей подойдёт паровой ингалятор или любой небулайзер, распыляющий аэрозоль крупными частицами, размером в 5–10 мкм. В качестве универсального прибора можно выбрать небулайзер с возможностью регулировать размер частиц.
С какого возраста можно использовать ингалятор
Перед тем, как применять аппарат, следует знать, с какого возраста можно использовать ингалятор.Небулайзер можно использовать детям с самого раннего возраста. Педиатры советуют применять такие приборы даже при лечении грудничков. Для маленьких детей приобретают ингалятор с удобными насадками (мундштук, наконечник для носа, маленькая маска для лица). У некоторых брендов детская маска продаётся отдельно.
У некоторых брендов детская маска продаётся отдельно.
Как выбрать ингалятор для детей
- Чтобы выбрать ингалятор для ребёнка, перед покупкой внимательно ознакомьтесь с инструкцией. Главный параметр — безопасная эксплуатация. Поэтому детям до года нельзя использовать паровые приборы: малышам сложно откашливать мокроту.
- Для маленького ребёнка лучше выбрать ультразвуковой или меш-ингалятор, так как эти приборы бесшумны и имеют регулировку температуры.
- Также важен элемент развлечения, отвлекающий от процедуры. Поэтому многие производители предлагают небулайзеры в виде игрушек с ярким и красочным дизайном.
- Лечение детей должно проходить под строгим надзором взрослых. При этом процедура не должна длиться дольше 5 минут.
Что важно запомнить
- Если вам нужен прибор только для взрослых на случай лечения простуды без температуры — возьмите простой паровой ингалятор.

- Если нужен ингалятор для детей, который поможет при кашле и насморке, или нужна универсальная семейная модель, выбирайте компрессорный прибор. Он будет работать со всеми видами лекарств.
- Страдающим от астмы, аллергикам или тем, кому лучше всегда иметь под рукой ингалятор, стоит выбирать меш-небулайзеры. Они компактны и работают с любыми лекарствами.
- Для ингаляций детям и младенцам лучше выбирать между меш-ингаляторами и ультразвуковыми. Они работают тише компрессорных и подают аэрозоль в любом положении: можно делать ингаляции даже во время сна ребёнка. Однако помните, что ультразвуковые устройства могут распылять не все виды лекарств.
Ответы врачей на вопросы об ингаляторах / bwell-swiss.ru
Ответы врачей на часто задаваемые вопросы пациентов
Небулайзерная терапия1. Чем отличается «небулайзер» от «ингалятора»?
Небулайзер – это вид ингалятора, который производит аэрозоль с размером частиц менее 5 микрон для лечения всех отделов дыхательной системы. «Ингалятор» более широкое понятие. К ингаляторам относятся и паровые приборы, и небулайзеры. Сомневаетесь, что выбрать? Проверьте инструкцию и технические характеристики прибора.
«Ингалятор» более широкое понятие. К ингаляторам относятся и паровые приборы, и небулайзеры. Сомневаетесь, что выбрать? Проверьте инструкцию и технические характеристики прибора.
2. Насколько эффективна ингаляционная терапия, чем она отличается от остальных методов лечения?
При ингаляционной терапии лекарство напрямую попадает в дыхательные пути, действует быстро и эффективно, происходит лучшая всасываемость препарата, отсутствуют или минимальны побочные действия. Ингаляции — самый современный и эффективный способ лечения кашля и других заболеваний нижних отделов дыхательной системы у детей и взрослых.
2. При каких болезнях рекомендована небулайзерная терапия?
Небулайзерная терапия применяется при лечении сухого кашля, ОРВИ, заложенности носа, обструктивном бронхите, бронхиальной астме, пневмонии и ложном крупе и других бронхо-легочных заболеваниях.
3. Какой эффект оказывает небулайзерная терапия?
Все зависит от того, какой препарат используется. Это может быть бронхорасширяющее, противоотечное, муколитическое, антисептическое действие — все зависит от назначения врача и решаемой проблемы.
Это может быть бронхорасширяющее, противоотечное, муколитическое, антисептическое действие — все зависит от назначения врача и решаемой проблемы.
4. Можно ли применять небулайзерную терапию для профилактики? Например, бронхита нет, есть сухой кашель.
Если есть кашель, то состояние болезни уже присутствует и нужен небулайзер. Если же признаки заболевания отсутствуют, то и ребенок совершенно здоров, и лишнее лечение ни к чему. Приобретите увлажнитель воздуха для создания благотворного климата в детской, это важно.
6. Подойдет ли небулайзерная терапия для лечения боли в горле, насморке?
Насморк относится к заболеваниям верхних дыхательных путей, если используется небулайзер с физраствором и для ингаляции применяется маска, то разжижается мокрота в носоглотке, поэтому, да, помогает.
7. Почему именно детям показана небулайзерная терапия?
Дети часто отказываются пить лекарство, потому что оно невкусное. Кроме того, нередки аллергические реакции на прием суспензий и сиропов. Небулайзерная терапия широко применяется педиатрами для облегчения симптомов заболевания, так как этот метод позволяет доставить лекарство напрямую в больной орган, избежать побочного воздействия.
Кроме того, нередки аллергические реакции на прием суспензий и сиропов. Небулайзерная терапия широко применяется педиатрами для облегчения симптомов заболевания, так как этот метод позволяет доставить лекарство напрямую в больной орган, избежать побочного воздействия.
8. С какого возраста можно использовать небулайзер?
Небулайзерная терапия подходит для детей с рождения по назначению врача.
9.Ребенок боится ингалятора, что делать?
Приобретите модель, созданную специально для детей! Это может быть небулайзер-игрушка от швейцарского производителя B.Well PRO-115 — в виде паровозика или модель компрессорного небулайзера MED-125 с пониженным уровнем шума. В комплектацию обоих приборов входят детская и младенческая маска, а также наклейки с забавными зверушками, которые развлекут ребенка, позволяет «подружиться» с прибором.
10.Есть ли противопоказания? Какие?
Небулайзерную терапию не рекомендуется проводить при повышенной температуре. Помните, небулайзерная терапия должна назначаться врачом.
Помните, небулайзерная терапия должна назначаться врачом.
11.Как быстро следует ожидать эффект от ингаляции, через какое время должно наступить выздоровление?
Эффект от ингаляции зависит от заболевания и назначенного препарата. Например, при использовании гормонального препарата эффект заметен сразу – симптомы заболевания «снимаются» как только ребенок начинает дышать в небулайзер.
Выздоровление при использовании небулайзера наступает в среднем 1.5-2 раза быстрее, чем без его использования.
12.Какие лекарства можно использовать для ингаляций с небулайзером?
Все лекарственные препараты, предназначенные для небулайзерной терапии. Масла и отвары трав использовать в небулайзере нельзя! Помните, лекарство должен назначать врач.
13.Врач назначил ингаляции 3 раза в день по 10 минут, но ингалятор распыляет лекарство быстрее/медленнее, что делать?
Обратите внимание, что первичным при назначении является объем лекарственного препарата. Врач также может рекомендовать оптимальное время ингаляции – например, 5 или 10 минут. Но фактическая продолжительность ингаляции зависит от технических характеристик небулайзера (скорости распыления, остаточного объема лекарства) и вязкости лекарства. Это значит, что разные небулайзеры будут распылять один и тот же раствор за разное время. Учитывайте это при подготовке препарата: можно добавить большее количество физраствора, чтобы объем лекарства соответствовал оптимальному времени процедуры. В ассортименте B.Well есть небулайзеры MED-121 и MED-125, которые имеют регулируемую скорость распыления и позволяют выбрать оптимальный темп ингаляции.
Врач также может рекомендовать оптимальное время ингаляции – например, 5 или 10 минут. Но фактическая продолжительность ингаляции зависит от технических характеристик небулайзера (скорости распыления, остаточного объема лекарства) и вязкости лекарства. Это значит, что разные небулайзеры будут распылять один и тот же раствор за разное время. Учитывайте это при подготовке препарата: можно добавить большее количество физраствора, чтобы объем лекарства соответствовал оптимальному времени процедуры. В ассортименте B.Well есть небулайзеры MED-121 и MED-125, которые имеют регулируемую скорость распыления и позволяют выбрать оптимальный темп ингаляции.
При использовании небулайзера выздоровление наступает в 1,5-2 раза быстрее!
Помните, что отвары трав, масла и сиропы в ингалятор заливать нельзя! Для небулайзерной терапии подходят только специальные стерильные препараты, которые назначает врач.
Поделитесь статьёй с друзьями
Что надо знать о COVID-19 пневмонии
Чем опасна пневмония при COVID-19? Какие симптомы нельзя оставлять без внимания? Как восстановить здоровье легких после коронавирусной пневмонии? Можно ли делать ингаляции, если заболел COVID-19? Эти и другие вопросы журналист информационного портала «Здоровые люди» задала главному внештатному пульмонологу Минздрава, заведующей отделом пульмонологии и хирургических методов лечения болезней органов дыхания РНПЦ пульмонологии и фтизиатрии, к. м.н. Елене Давидовской.
м.н. Елене Давидовской.
Чем пневмония, вызванная коронавирусом, отличается от обычной?
Пневмония, ассоциированная с коронавирусной инфекцией (COVID-19 пневмония), – особый вид поражения легких, который более точно отражает термин «пневмонит». Это подразумевает вовлечение в патологический процесс интерстициальной ткани легких, альвеолярных стенок и сосудов. То есть воспаление развивается во всех структурах легких, участвующих в газообмене, что препятствует нормальному насыщению крови кислородом.
Возможно ли при ковиде бессимптомное воспаление легочной ткани, когда несмотря на изменения в легких у пациентов нет ни кашля, ни одышки, ни лихорадки?
Бессимптомное или малосимптомное течение больше характерно для форм заболевания без поражения легких. Действительно, при проведении компьютерной томографии (КТ) органов грудной клетки у пациентов с легким течением COVID-19 могут обнаруживаться КТ-признаки вирусной пневмонии нетяжелого течения. При этом газообменная функция легких не страдает, количество кислорода, доставляемого в кровь, остается нормальным, и не требуется изменения терапевтической тактики.
При этом газообменная функция легких не страдает, количество кислорода, доставляемого в кровь, остается нормальным, и не требуется изменения терапевтической тактики.
Когда, как правило, появляются такие симптомы при коронавирусе, как дыхательный дискомфорт, одышка?
Инкубационный период инфекции, вызываемой вирусом SARS-CoV-2, составляет в среднем 5-7 суток (от 2 до 14), а значит, и симптомы могут появляться в эти сроки. Течение болезни может быть разным – от нетяжелых проявлений обычной ОРВИ (повышение температуры тела, кашель, слабость, головная боль) до тяжелой пневмонии с дыхательной недостаточностью. Всегда стоит внимательно относиться к таким проявлениям болезни, как одышка (нарастание частоты дыхания), чувство нехватки воздуха, боли или чувство стеснения в груди в любой период болезни.
Изменения в легких появляются у большинства пациентов, перенесших COVID-19?
В большинстве случаев – до 80% – коронавирусная инфекция протекает нетяжело, без вовлечения легких. COVID-19 пневмонии развиваются примерно в 20% случаев заболевания, из них от 2 до 10% могут протекать тяжело. Длительность течения и последствия болезни зависят от многих факторов: объема поражения легких, сопутствующих заболеваний, своевременности обращения за медицинской помощью, соблюдения рекомендаций по лечению, возможности развития осложнений и др.
COVID-19 пневмонии развиваются примерно в 20% случаев заболевания, из них от 2 до 10% могут протекать тяжело. Длительность течения и последствия болезни зависят от многих факторов: объема поражения легких, сопутствующих заболеваний, своевременности обращения за медицинской помощью, соблюдения рекомендаций по лечению, возможности развития осложнений и др.
Когда следует выполнять КТ при тяжелой ковидной пневмонии? Есть ли необходимость в повторном исследовании?
Действительно, в силу высокой чувствительности метод КТ является основным для выявления характерных для COVID-19 изменений в легких. В комплексной оценке вместе с историей развития болезни, эпидемиологическими данными и клинической картиной КТ позволяет с высокой степенью вероятности подтвердить случай коронавирусной инфекции. Однако стоит отметить несколько важных моментов:
— применение КТ для скрининга (т.е. выявления патологии при отсутствии симптомов) как пневмоний в целом, так и при COVID-19 (в том числе при положительных лабораторных тестах) нецелесообразно;
— применительно к коронавирусной инфекции, выявленные на КТ изменения у пациентов с бессимптомной или легкой формами заболевания без факторов риска не влияют на тактику лечения;
— при легком течении COVID-19 КТ-диагностика проводится по клиническим показаниям при наличии факторов риска или с целью дифференциальной диагностики с другими патологическими состояниями;
— проведение КТ исследования целесообразно выполнять в сроки не ранее 3-5 дней с момента появления симптомов;
— оценка динамики течения и исхода выявленной ранее COVID-19 пневмонии проводится по клиническим показаниям, сроки определяются индивидуально.
Отличается ли снимок компьютерной томографии у пациента с коронавирусной пневмонией и обычной пневмонией?
Лучевые методы диагностики, к которым в том числе относится КТ, не заменяют комплексную клиническую диагностику. Наличие характерных КТ-признаков позволяет определить вероятность (с градацией «высокая-средняя-низкая-нехарактерные признаки») COVID-19 пневмонии и установить объем поражения.
Какие существуют методы лечения коронавирусной пневмонии?
Подходы к лечению COVID-19 формировались и менялись по мере появления информации о течении инфекции, понимания механизмов ее развития и возможных последствий на основании анализа большого количества международных публикаций и результатов исследований, накапливающегося клинического опыта. Спустя год от начала пандемии в арсенале применяемых лекарственных средств этиотропной терапии с доказанной эффективностью по-прежнему нет.
При COVID-19 пневмонии важное место занимают немедикаментозные методы – прон-позиция (положение лежа на животе) как самостоятельная лечебная мера, кислородотерапия, варианты аппаратной респираторной поддержки. Во всех случаях коронавирусной инфекции необходимо следить за объемом потребляемой жидкости.
Во всех случаях коронавирусной инфекции необходимо следить за объемом потребляемой жидкости.
Учитывая механизмы развития заболевания, в алгоритм фармакотерапии COVID-19 пневмоний включены противовирусные препараты, лекарственные средства для профилактики тромбообразования, гормональная противовоспалительная терапия, при наличии признаков присоединения бактериальной инфекции — антибиотики.
Несмотря на алгоритмизацию терапевтических подходов, что, несомненно, важно в эпидемических условиях, объем фармакотерапии и выбор конкретных препаратов из каждой группы определяет врач, и только исходя из конкретной клинической ситуации и индивидуальных особенностей пациента.
Всегда ли нужно пациентов с пневмониями, вызванными коронавирусной инфекцией, лечить в больнице?
В домашних условиях возможно лечение нетяжелой пневмонии у человека без факторов риска, при наличии условий, обеспечивающих изоляцию и соблюдение рекомендаций по лечению, а также врачебный (в том числе дистанционный) контроль.
Можно ли при коронавирусной пневмонии делать ингаляции?
При коронавирусной инфекции от ингаляций (паровые ингаляции, небулайзерная терапия), как аэрозольобразующих процедур, стоит отказаться. Исключения составляют дозирующие ингаляционные устройства – аэрозольные и порошковые, использующиеся для постоянной базисной терапии и неотложной помощи при хронических заболеваниях – бронхиальной астме и хронической обструктивной болезни легких.
Небулайзерная терапия должна применяться лишь по жизненным показаниям с соблюдением мер предосторожности распространения инфекции через аэрозоль (изоляция пациента во время ингаляции, проветривание после ингаляции, обработка поверхностей антисептиками).
Как восстановить легкие после коронавирусной пневмонии? Например, дыхательная гимнастика. Когда можно начинать? Сразу после выздоровления или стоит подождать?
Период восстановления после COVID-19 пневмонии, как и «набор» восстановительных процедур, зависит от тяжести перенесенной пневмонии и тех изменений, которые остались в легких после заболевания.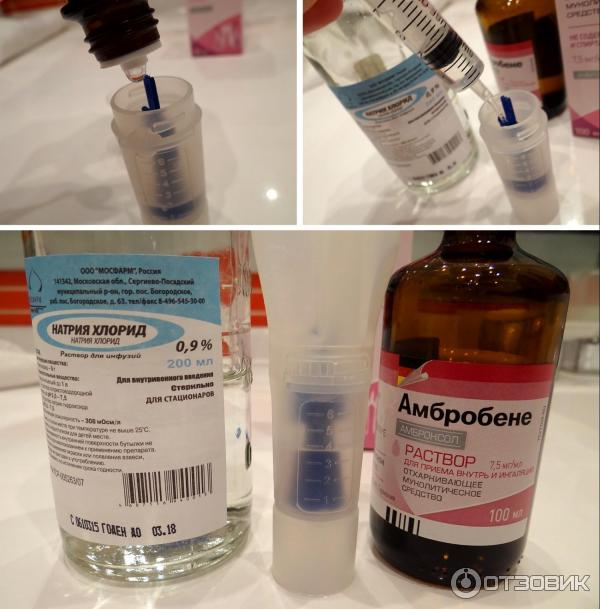 Кроме того, для определения программы восстановления имеют значение сопутствующие заболевания, вес, уровень физической тренированности до болезни и др.
Кроме того, для определения программы восстановления имеют значение сопутствующие заболевания, вес, уровень физической тренированности до болезни и др.
Реабилитация после COVID-19
Начинать реабилитационные мероприятия можно после купирования острого воспалительного процесса – нормализации температуры тела, улучшения или нормализации лабораторных показателей (требуется оценка врача!) и при отсутствии признаков декомпенсации сопутствующих заболеваний.
Реабилитационные программы включают дыхательную гимнастику, лечебную физкультуру, лечебный массаж, сбалансированное питание, питьевой режим, физиотерапевтические процедуры.
В случаях, когда после перенесенной тяжелой пневмонии в легких сохраняются обширные участки поствоспалительных изменеий, одышка, уровень насыщения крови кислородом (сатурация — SpO2) по данным пульсоксиметрии ниже 95% и потребность в кислородной поддержке, на реабилитацию может потребоваться несколько месяцев.
Информация подготовлена по материалам сайта 24health.by
Механизмы и способы применения гипертонического раствора
J R Soc Med. 2011 июл; 104 (Дополнение 1): S2 – S5.
Отделение респираторной медицины, Больница Королевского принца Альфреда, Миссенден-роуд, Кампердаун 2050, Австралия
Авторские права © 2011 Королевское медицинское общество Эта статья цитируется другими статьями в PMC.Введение
Гипертонический физиологический раствор — это сильный стерильный раствор соленой воды, который можно вдыхать в виде небулайзерного лекарства для людей с муковисцидозом (CF).Чтобы изучить, как его следует применять в клинической практике, стоит рассмотреть механизмы, с помощью которых он влияет на процесс заболевания, а также на какие признаки, симптомы и другие клинические исходы он влияет. Наконец, стоит подумать о том, как на эффект влияет полученная доза, и должно ли это влиять на то, как она применяется в клинической практике. В этой статье мы рассмотрим эту информацию и свяжем ее с клиническим применением гипертонического раствора.
Механизмы действия
Таксономия мукоактивных агентов 1 состоит из нескольких классов лекарств, определяемых по способу действия: муколитики, отхаркивающие средства, мукокинетики, модификаторы ионного транспорта и другие мукорегуляторные соединения.Гипертонический раствор трудно отнести к этой таксономии, потому что он имеет несколько механизмов действия.
Муколитики нарушают структуру геля слизи, тем самым снижая ее вязкость и эластичность. Таким образом, цель муколитической терапии состоит в том, чтобы улучшить вязкоэластичность секрета дыхательных путей, чтобы облегчить их удаление из дыхательных путей. Было высказано предположение, что гипертонический раствор не является муколитиком, потому что муколиз не является его основным механизмом действия. 2 Однако гипертонический солевой раствор способен разрушать ионные связи в слизистом геле, что может уменьшить сшивание и сцепление. 3 Этот муколитический эффект может быть причиной того, что мокрота заметно снижает свою вязкость при добавлении к ней гипертонического раствора. 4 Нитевидная способность мокроты CF также значительно снижается при добавлении гипертонического раствора. 5 Эти опосредованные физиологическим раствором изменения реологических свойств мокроты при МВ связаны с улучшенной транспортабельностью в модели трахеи крупного рогатого скота. 6 , 7 Похожий механизм — который не влияет напрямую на сам слизистый гель — заключается в том, что гипертонический раствор диссоциирует ДНК от мукопротеина, что позволяет естественным протеолитическим ферментам затем переваривать мукопротеин. 8 Следовательно, гипертонический раствор, по-видимому, обладает несколькими муколитическими механизмами, которые действительно улучшают переносимость слизи in vitro .
Другой мукоактивный класс лекарств — это отхаркивающие средства, которые добавляют воду к поверхности дыхательных путей. Это особенно актуально для дыхательных путей при МВ, поскольку аномальный или отсутствующий белок трансмембранного регулятора проводимости при муковисцидозе (CFTR) не инициирует секрецию хлорид-иона в просвет дыхательных путей и не ингибирует абсорбцию ионов натрия из просвета дыхательных путей через эпителиальный натрий. канал. 9 Поскольку абсорбция ионов натрия увеличивается, а секреция ионов хлора снижается, в дыхательных путях остается недостаточно соли для поддержания обычной гидратации эпителиальной поверхности. Это также приводит к обезвоживанию секрета дыхательных путей и нарушению мукоцилиарного механизма. Это позволяет задерживать слизь, которая становится очагом инфекции. 10 Измерения жидкости поверхности дыхательных путей на эпителиальной поверхности in vitro показывают, что гипертонический раствор заметно увеличивает глубину этого жидкого слоя — не только за счет осаждения на поверхность, но и за счет осмотического втягивания дополнительной воды на поверхность. поверхность дыхательных путей. 11 В зависимости от дозы гипертонического раствора, достигнутой локально, степень восстановления жидкости на поверхности дыхательных путей варьируется, но обычно она временно достигает высокого пика и возвращается к уровню, близкому к уровню до обработки в течение примерно 10 минут, хотя она может иметь более длительный более мягкий эффект, если доза адекватна. 11 , 12 Если избыток воды втягивается в дыхательные пути, слой слизи может принять ее и при необходимости отдать жидкость обратно на поверхность дыхательных путей. 13 Таким образом, избыточная вода, поступающая в дыхательные пути осмотически, накапливается в слое слизи, делая ее реологические свойства более благоприятными для очистки. 4 , 5
Другой класс мукоактивных веществ — это мукокинетики, которые улучшают очищение от кашля за счет увеличения потока воздуха или уменьшения прилипания мокроты. Нам неизвестны какие-либо доказательства того, что гипертонический раствор имеет одно из этих немедленных преимуществ, но он действительно вызывает кашель 14 , а кашель еще больше увеличивает количество слизи, выводимой из легких.Увеличение мукоцилиарного клиренса при применении гипертонического раствора и дополнительный клиренс при кашле были объективно продемонстрированы in vivo при муковисцидозе с использованием радиоаэрозольных исследований. 15 , 16
Гипертонический раствор может также иметь некоторые другие механизмы, которые не являются строго мукоактивными. Недавнее исследование in vitro и показало, что гипертонический раствор снижает образование биопленок под действием Pseudomonas aeruginosa и производство связанных факторов вирулентности. 17 Наконец, гипертонический раствор, по-видимому, увеличивает уровни двух тиолов, которые защищают от окислительного повреждения — глутатиона и тиоцианата — в жидкости на поверхности дыхательных путей. 18
Клинические преимущества
Непосредственным преимуществом увеличения клиренса слизи является возможность поставить микробиологический диагноз тем пациентам, которые не могут спонтанно откашливать образец мокроты. Разовая доза увеличивает шанс получить образец в этой популяции. 19 — 22 Из 40 пациентов, протестированных в этих исследованиях, 39 (97%) смогли получить образец после вдыхания солевого раствора различной концентрации до 6%. Девятнадцать из этих образцов были протестированы на наличие альвеолярных макрофагов, а в 16 (84%) они присутствовали. 19 Для пациентов, которые могут спонтанно откашливаться, гипертонический раствор значительно увеличивает размер образца, независимо от того, измеряется ли он по весу 21 , 22 или по объему. 23 Количество колоний и процент неплоскоклеточных клеток также были выше. 20 , 22 Однако, несмотря на эти образцы лучшего качества, выявление патогенов не улучшилось, что позволяет предположить, что гипертонический раствор не требуется при получении образцов мокроты для микробиологического тестирования от пациентов с МВ, которые могут откашливать образец спонтанно.
Ридлер и его коллеги 23 провели перекрестное исследование с участием 10 подростков с обострением заболевания легких, вызванного МВ.Перед сеансом физиотерапии субъекты были рандомизированы для вдыхания либо 6% гипертонического солевого раствора, либо контрольного физиологического раствора. На следующий день перед идентичным сеансом физиотерапии вдыхали альтернативный раствор. Мокроту собирали между началом ингаляции и 60 мин после окончания режима физиотерапии. После приема гипертонического раствора было отхаркировано значительно больше мокроты, чем в контрольной группе (p = 0,006). Субъекты также оценили, насколько яснее стала их грудь после физиотерапии, со значительно лучшими оценками при использовании гипертонического раствора (p = 0.04) — эффект также отмечен у взрослых и детей. Eng и соавторы 24 рандомизировали 52 ребенка и взрослых с МВ на ингаляции 6% гипертонического раствора или контрольного физиологического раствора два раза в день. В течение двух недель среднее улучшение ОФВ1 среди тех, кто принимал гипертонический раствор, составило 15% (стандартное отклонение 16), тогда как в контрольной группе улучшилось только на 3% (стандартное отклонение 13) (p = 0,004). Через две недели после прекращения ингаляций существенной разницы в функции легких не было.
Улучшение функции легких сохраняется при длительном применении.В рандомизированном исследовании, в котором участвовали 164 взрослых и детей с МВ, группа, принимавшая гипертонический раствор, поддерживала значительно более высокую функцию легких в течение 48-недельного периода наблюдения. 25 Другими клиническими преимуществами были уменьшение частоты и продолжительности обострений и меньшее количество дней, пропущенных из-за болезни. Эти преимущества сопровождались улучшением качества жизни в нескольких сферах. На протяжении всего испытания также проводился тщательный мониторинг образцов мокроты для выявления любых побочных эффектов на приобретение организмов, плотность организма и воспаление.В целом, эти результаты не показали отрицательного эффекта от длительного использования режима ингаляций с гипертоническим раствором два раза в день. Преимущество, которое часто упускают из виду, заключалось в том, что пациенты в активной группе исследования оценивали легкость отхождения мокроты как значительно большую в конце исследования. Вероятно, это имеет важные социальные последствия. Если пациенты могут более эффективно очищать свои секреты во время очистки дыхательных путей, это позволяет им заниматься своей работой, учебой и общественными мероприятиями, не беспокоясь о продуктивном кашле во время взаимодействия с другими людьми.
Ни одно исследование не выявило подгруппу пациентов с МВ, которые особенно хорошо реагируют на терапию гипертоническим раствором. Например, в долгосрочном исследовании влияние гипертонического раствора на обострения не различается значительно между пользователями и лицами, не принимающими физиотерапию, между субъектами с легким или тяжелым нарушением функции легких, а также между пользователями и не пользователями рекомбинантного человеческого препарата. дезоксирибонуклеаза (рчДНаза). Поэтому мы рекомендуем эту терапию большинству людей с МВ, которые считают ее переносимой. 26 Соответствующие испытания на переносимость описаны ниже.
Текущее исследование
Интересной особенностью большинства исследований, обсужденных выше, является наличие зависимости «доза-реакция» для гипертонического раствора. Влияние на вязкость и способность к образованию нитей усиливается по мере увеличения концентрации физиологического раствора. 4 , 5 Воздействие на жидкость поверхности дыхательных путей также намного больше, когда на эпителиальную поверхность наносится больший объем гипертонического раствора. 11 , 12 Ускорение мукоцилиарного клиренса также значительно увеличивается при использовании больших концентраций физиологического раствора. 15 , 16 Однако побочные эффекты, такие как кашель, также усиливаются с увеличением концентрации. Поэтому некоторые врачи задаются вопросом, получат ли пациенты, которые не переносят стандартную дозу, более низкую (но более переносимую) концентрацию гипертонического раствора. Мы начали рандомизированное клиническое исследование (ACTRN12610000754044), в котором будет сравниваться стандартная концентрация физиологического раствора с более низкой концентрацией гипертонического раствора, а также с физиологическим раствором в качестве контрольного состояния.
Другой подход к проблеме переносимости — это изменение гипертонического солевого раствора. Buonpensiero и его коллеги 27 исследовали гипертонический раствор, смешанный с 0,1% гиалуроновой кислотой — природным полисахаридом. Гиалуроновая кислота, по-видимому, имеет несколько других механизмов, которые могут быть полезны в дыхательных путях при МВ, но Буонпансьеро и его коллеги изучили ее влияние на переносимость и воспринимаемую соленость комбинированного раствора по сравнению с одним гипертоническим раствором.Они отметили улучшение переносимости гипертонического раствора и уменьшение ощущаемого соленого вкуса при добавлении в раствор гиалуроновой кислоты. Эти изменения были статистически и клинически значимыми.
В первоначальное долгосрочное контролируемое испытание гипертонического раствора принимали участие только участники в возрасте 6 лет. Младенческое исследование ингаляционного физиологического раствора при муковисцидозе (ISIS) рассмотрит этот вопрос путем изучения использования гипертонического физиологического раствора у младенцев и детей от 4 до 59 месяцев ({«type»: «клиническое испытание», «attrs»: {«text «:» NCT00709280 «,» term_id «:» NCT00709280 «}} NCT00709280).Первичным результатом этого исследования будет частота обострений легких, определенных протоколом, требующих лечения антибиотиками, по сравнению с частотой в контрольной группе, которая будет вдыхать физиологический раствор.
В ожидании результатов этих испытаний мы продолжаем рекомендовать применение гипертонического раствора для большинства взрослых и детей старшего возраста с МВ. Если у пациента начинается терапия гипертоническим раствором, первая доза должна контролироваться с помощью спирометрии и пульсоксиметрии до и после приема дозы, чтобы гарантировать отсутствие клинически значимого сужения дыхательных путей (т.е. падение FEV 1 более чем на 15% или заметная десатурация после приема дозы). Всем дозам, включая начальную тестовую дозу, следует вводить бронходилататор. Переносимость часто улучшается после первых 10 доз, поэтому пациентов, которым трудно переносить первые дозы, следует поощрять к упорству, при условии, что у них нет признаков заметного сужения дыхательных путей. Пациенты, не прошедшие первоначальный тест на переносимость, могут быть повторно обследованы позже; часто вторая тестовая доза переносится гораздо легче.
Гипертонический раствор также исследуется как средство лечения бронхоэктазов, не связанных с МВ, и хронической обструктивной болезни легких (ХОБЛ). Хотя гидратация поверхности дыхательных путей может быть менее важной, чем при МВ, все другие механизмы действия гипертонического раствора могут работать при бронхоэктазах. Обоснование использования при ХОБЛ менее ясно, хотя устранение задержанных секретов считается допустимой целью лечения там, где они возникают. Некоторые исследования показали значительное совпадение патологии между ХОБЛ и бронхоэктазами. 28 , 29 Поскольку гипертонический раствор может вызывать сужение дыхательных путей, это следует очень тщательно контролировать при испытаниях гипертонического раствора при обструктивных заболеваниях легких, таких как ХОБЛ. В будущих исследованиях будет также оцениваться эффект гипертонического раствора в сочетании с другими классами лекарств, такими как антибиотики или противовоспалительные средства.
ЗАЯВЛЕНИЯ
Конкурирующие интересы
Не заявлены
Этическое одобрение
Неприменимо
Участие
Оба автора внесли равный вклад
Ссылки
1.Рубин БК Таксономия мукоактивных препаратов. В: Рубин Б.К., Ван дер Сханс С.П., ред. Терапия нарушений очистки слизи. Том 188, Биология легких в здоровье и болезнях. Нью-Йорк, Нью-Йорк: Марсель Деккер, 2004: 129–45 [Google Scholar] 2. Хенке М, Ратьен Ф Муколитики при муковисцидозе. Пэд Респир Рев 2007; 8: 24–9 [PubMed] [Google Scholar] 3. Цимент I Респираторная фармакология и терапия. Филадельфия, Пенсильвания: WB Saunders, 1978: 60–104 [Google Scholar] 4. Шеффнер А.Л., Медлер Е.М., Якобс Л.В., Саретт Х.П. Снижение in vitro вязкости трахеобронхиального секрета человека за счет ацетилцистеина.Am Rev Respir Dis 1964; 90: 721–9 [PubMed] [Google Scholar] 5. King M, Dasgupta B, Tomkiewicz RP, Brown NE Реология мокроты при муковисцидозе после лечения in vitro только гипертоническим солевым раствором и в сочетании с рекомбинантной дезоксирибонуклеазой человека I. Am J Respir Crit Care Med 1997; 156: 173–7 [PubMed] [Google Scholar] 6. Уиллс П.Дж., Коул П.Дж. Хлорид натрия улучшает цилиарную транспортабельность мокроты. Am J Respir Crit Care Med 1995; 151: A720 [PubMed] [Google Scholar] 7. Уиллс П.Дж., Холл Р.Л., Чан В.М., Коул П.Дж. Хлорид натрия увеличивает цилиарную переносимость мокроты при муковисцидозе и бронхоэктазиях на обедненную слизью трахею крупного рогатого скота.J Clin Invest 1997; 99: 9–13 [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Либерман Дж., Курник Н. Б. Влияние содержания дезоксирибонуклеиновой кислоты на протеолиз мокроты и гноя. Природа 1962; 196: 988–90 [PubMed] [Google Scholar] 9. Штуттс MJ, Canessa CM, Olsen JC, et al. CFTR как цАМФ-зависимый регулятор натриевых каналов. Наука 1995; 269: 847–50 [PubMed] [Google Scholar] 10. Тарран Р., Грабб Б.Р., Парсонс Д. и др. Противоречие CF соли: наблюдения in vivo и терапевтические подходы. Mol Cell 2001; 8: 149–58 [PubMed] [Google Scholar] 11.Дональдсон С.Х., Беннетт В.Д., Земан К.Л., Ноулз М.Р., Тарран Р., Бушер Р. Очистка слизи и функция легких при муковисцидозе с гипертоническим раствором. New Engl J Med 2006; 354: 241–50 [PubMed] [Google Scholar] 12. Горальски Дж., Кнопка B Изучение in vitro кинетики гипертонического раствора на высоте над уровнем моря. Пед Пульмонол 2010; 45: A205 [Google Scholar] 13. Тарран Р., Грабб Б.Р., Гатзи Д.Т., Дэвис С.В., Буше Р.К. Относительные роли пассивных поверхностных сил и активного переноса ионов в модуляции объема и состава жидкости на поверхности дыхательных путей.J Gen Physiol 2001; 118: 223–36 [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Элкинс MR, Пока, PTP Ингаляционный гипертонический раствор для лечения муковисцидоза. Curr Opin Pulm Med 2006; 12: 445–52 [PubMed] [Google Scholar] 15. Робинсон М., Регнис Дж. А., Бейли Д. Л., Кинг М., Баутович Г. Дж., Пока П. Т. Влияние гипертонического раствора, амилорида и кашля на мукоцилиарный клиренс у пациентов с муковисцидозом. Am J Respir Crit Care Med 1996; 153: 1503–9 [PubMed] [Google Scholar] 16. Робинсон М., Хемминг А.Л., Регнис Дж. А. и др.Влияние увеличения доз гипертонического раствора на мукоцилиарный клиренс у пациентов с муковисцидозом. Грудная клетка 1997; 52: 900–3 [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Мюррей Т.С. Влияние гипертонического раствора на колонизацию Pseudomonas aeruginosa in vitro. Пед Пульмонол 2010; 45: A367 [Google Scholar] 18. Гулд Н.С., Готье С., Кария К.Т., Мин Э, Хуанг Дж., Дэй Б.Дж. Гипертонический раствор увеличивает содержание жидкости в эпителиальной выстилке легких, глутатиона и тиоцианата: двух тиолов, защищающих CFTR от окислительного повреждения.Respir Res 2010; 11; 119. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. де Бок К., Алифер, Вандепутте С. Индукция мокроты у молодых пациентов с муковисцидозом. Eur Respir J 2000; 16: 91–4 [PubMed] [Google Scholar] 20. Хениг Н.Р., Тонелли М.Р., Пьер М.В., Бернс Д.Л., Эйткен М.Л. Индукция мокроты как инструмент исследования для отбора проб дыхательных путей у пациентов с муковисцидозом. Грудная клетка 2001; 56: 306–11 [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Кастелик Я.А., Азиз Я., Морис А.Х. Индукция мокроты у молодых пациентов с муковисцидозом.Eur Respir J 2001; 17: 1 [PubMed] [Google Scholar] 22. Сагель С.Д., Капснер Р., Осберг I, Зонтаг М.К., Accurso FJ Воспаление дыхательных путей у детей с муковисцидозом и здоровых детей, оцениваемое по индукции мокроты. Am J Respir Crit Care Med 2001; 164: 1425–31 [PubMed] [Google Scholar] 23. Ридлер Дж., Рид Т, Баттон Б, Робертсон К.Ф. Вдыхаемый гипертонический раствор увеличивает отхождение мокроты при муковисцидозе. J Paediatr Детское здоровье 1996; 32: 48–50 [PubMed] [Google Scholar] 24. Англия, Дж. Мортон, Дуглас Дж., Ридлер Дж., Уилсон Дж., Робертсон К.Ф. Краткосрочная эффективность распыляемого ультразвуком гипертонического раствора при муковисцидозе.Пед Пульмонол 1996; 21: 77–83 [PubMed] [Google Scholar] 25. Элкинс М.Р., Робинсон М., Роуз Б.Р. и др. Контролируемое испытание длительного применения ингаляционного гипертонического раствора у пациентов с муковисцидозом. New Engl J Med 2006; 354: 229–40 [PubMed] [Google Scholar] 26. Пока, PTP, Элкинс MR Другие мукоактивные агенты при муковисцидозе. Пэд Респир Рев 2007; 8: 30–9 [PubMed] [Google Scholar] 27. Буонпансьеро П., Де Грегорио Ф, Сепе А. и др. Вдыхаемая гиалуроновая кислота улучшает комфорт и переносимость распыленного гипертонического раствора у пациентов с муковисцидозом.Adv Ther 2010; 27: 870–8 [PubMed] [Google Scholar] 29. Патель И.С., Влахос И., Уилкинсон Т.МА. и др. Бронхоэктазы, показатели обострения и воспаления при хронической обструктивной болезни легких. Am J Respir Crit Care Med 2004; 170: 400–7 [PubMed] [Google Scholar]Механизмы и применение гипертонического раствора
J R Soc Med. 2011 июл; 104 (Дополнение 1): S2 – S5.
Отделение респираторной медицины, Больница Королевского принца Альфреда, Миссенден-роуд, Кампердаун 2050, Австралия
Авторские права © 2011 Королевское медицинское общество Эта статья цитируется другими статьями в PMC.Введение
Гипертонический физиологический раствор — это сильный стерильный раствор соленой воды, который можно вдыхать в виде небулайзерного лекарства для людей с муковисцидозом (CF). Чтобы изучить, как его следует применять в клинической практике, стоит рассмотреть механизмы, с помощью которых он влияет на процесс заболевания, а также на какие признаки, симптомы и другие клинические исходы он влияет. Наконец, стоит подумать о том, как на эффект влияет полученная доза, и должно ли это влиять на то, как она применяется в клинической практике.В этой статье мы рассмотрим эту информацию и свяжем ее с клиническим применением гипертонического раствора.
Механизмы действия
Таксономия мукоактивных агентов 1 состоит из нескольких классов лекарств, определяемых по способу действия: муколитики, отхаркивающие средства, мукокинетики, модификаторы ионного транспорта и другие мукорегуляторные соединения. Гипертонический раствор трудно отнести к этой таксономии, потому что он имеет несколько механизмов действия.
Муколитики нарушают структуру геля слизи, тем самым снижая ее вязкость и эластичность. Таким образом, цель муколитической терапии состоит в том, чтобы улучшить вязкоэластичность секрета дыхательных путей, чтобы облегчить их удаление из дыхательных путей. Было высказано предположение, что гипертонический раствор не является муколитиком, потому что муколиз не является его основным механизмом действия. 2 Однако гипертонический солевой раствор способен разрушать ионные связи в слизистом геле, что может уменьшить сшивание и сцепление. 3 Этот муколитический эффект может быть причиной того, что мокрота заметно снижает свою вязкость при добавлении к ней гипертонического раствора. 4 Нитевидная способность мокроты CF также значительно снижается при добавлении гипертонического раствора. 5 Эти опосредованные физиологическим раствором изменения реологических свойств мокроты при МВ связаны с улучшенной транспортабельностью в модели трахеи крупного рогатого скота. 6 , 7 Похожий механизм — который не влияет напрямую на сам слизистый гель — заключается в том, что гипертонический раствор диссоциирует ДНК от мукопротеина, что позволяет естественным протеолитическим ферментам затем переваривать мукопротеин. 8 Следовательно, гипертонический раствор, по-видимому, обладает несколькими муколитическими механизмами, которые действительно улучшают переносимость слизи in vitro .
Другой мукоактивный класс лекарств — это отхаркивающие средства, которые добавляют воду к поверхности дыхательных путей. Это особенно актуально для дыхательных путей при МВ, поскольку аномальный или отсутствующий белок трансмембранного регулятора проводимости при муковисцидозе (CFTR) не инициирует секрецию хлорид-иона в просвет дыхательных путей и не ингибирует абсорбцию ионов натрия из просвета дыхательных путей через эпителиальный натрий. канал. 9 Поскольку абсорбция ионов натрия увеличивается, а секреция ионов хлора снижается, в дыхательных путях остается недостаточно соли для поддержания обычной гидратации эпителиальной поверхности. Это также приводит к обезвоживанию секрета дыхательных путей и нарушению мукоцилиарного механизма. Это позволяет задерживать слизь, которая становится очагом инфекции. 10 Измерения жидкости поверхности дыхательных путей на эпителиальной поверхности in vitro показывают, что гипертонический раствор заметно увеличивает глубину этого жидкого слоя — не только за счет осаждения на поверхность, но и за счет осмотического втягивания дополнительной воды на поверхность. поверхность дыхательных путей. 11 В зависимости от дозы гипертонического раствора, достигнутой локально, степень восстановления жидкости на поверхности дыхательных путей варьируется, но обычно она временно достигает высокого пика и возвращается к уровню, близкому к уровню до обработки в течение примерно 10 минут, хотя она может иметь более длительный более мягкий эффект, если доза адекватна. 11 , 12 Если избыток воды втягивается в дыхательные пути, слой слизи может принять ее и при необходимости отдать жидкость обратно на поверхность дыхательных путей. 13 Таким образом, избыточная вода, поступающая в дыхательные пути осмотически, накапливается в слое слизи, делая ее реологические свойства более благоприятными для очистки. 4 , 5
Другой класс мукоактивных веществ — это мукокинетики, которые улучшают очищение от кашля за счет увеличения потока воздуха или уменьшения прилипания мокроты. Нам неизвестны какие-либо доказательства того, что гипертонический раствор имеет одно из этих немедленных преимуществ, но он действительно вызывает кашель 14 , а кашель еще больше увеличивает количество слизи, выводимой из легких.Увеличение мукоцилиарного клиренса при применении гипертонического раствора и дополнительный клиренс при кашле были объективно продемонстрированы in vivo при муковисцидозе с использованием радиоаэрозольных исследований. 15 , 16
Гипертонический раствор может также иметь некоторые другие механизмы, которые не являются строго мукоактивными. Недавнее исследование in vitro и показало, что гипертонический раствор снижает образование биопленок под действием Pseudomonas aeruginosa и производство связанных факторов вирулентности. 17 Наконец, гипертонический раствор, по-видимому, увеличивает уровни двух тиолов, которые защищают от окислительного повреждения — глутатиона и тиоцианата — в жидкости на поверхности дыхательных путей. 18
Клинические преимущества
Непосредственным преимуществом увеличения клиренса слизи является возможность поставить микробиологический диагноз тем пациентам, которые не могут спонтанно откашливать образец мокроты. Разовая доза увеличивает шанс получить образец в этой популяции. 19 — 22 Из 40 пациентов, протестированных в этих исследованиях, 39 (97%) смогли получить образец после вдыхания солевого раствора различной концентрации до 6%. Девятнадцать из этих образцов были протестированы на наличие альвеолярных макрофагов, а в 16 (84%) они присутствовали. 19 Для пациентов, которые могут спонтанно откашливаться, гипертонический раствор значительно увеличивает размер образца, независимо от того, измеряется ли он по весу 21 , 22 или по объему. 23 Количество колоний и процент неплоскоклеточных клеток также были выше. 20 , 22 Однако, несмотря на эти образцы лучшего качества, выявление патогенов не улучшилось, что позволяет предположить, что гипертонический раствор не требуется при получении образцов мокроты для микробиологического тестирования от пациентов с МВ, которые могут откашливать образец спонтанно.
Ридлер и его коллеги 23 провели перекрестное исследование с участием 10 подростков с обострением заболевания легких, вызванного МВ.Перед сеансом физиотерапии субъекты были рандомизированы для вдыхания либо 6% гипертонического солевого раствора, либо контрольного физиологического раствора. На следующий день перед идентичным сеансом физиотерапии вдыхали альтернативный раствор. Мокроту собирали между началом ингаляции и 60 мин после окончания режима физиотерапии. После приема гипертонического раствора было отхаркировано значительно больше мокроты, чем в контрольной группе (p = 0,006). Субъекты также оценили, насколько яснее стала их грудь после физиотерапии, со значительно лучшими оценками при использовании гипертонического раствора (p = 0.04) — эффект также отмечен у взрослых и детей. Eng и соавторы 24 рандомизировали 52 ребенка и взрослых с МВ на ингаляции 6% гипертонического раствора или контрольного физиологического раствора два раза в день. В течение двух недель среднее улучшение ОФВ1 среди тех, кто принимал гипертонический раствор, составило 15% (стандартное отклонение 16), тогда как в контрольной группе улучшилось только на 3% (стандартное отклонение 13) (p = 0,004). Через две недели после прекращения ингаляций существенной разницы в функции легких не было.
Улучшение функции легких сохраняется при длительном применении.В рандомизированном исследовании, в котором участвовали 164 взрослых и детей с МВ, группа, принимавшая гипертонический раствор, поддерживала значительно более высокую функцию легких в течение 48-недельного периода наблюдения. 25 Другими клиническими преимуществами были уменьшение частоты и продолжительности обострений и меньшее количество дней, пропущенных из-за болезни. Эти преимущества сопровождались улучшением качества жизни в нескольких сферах. На протяжении всего испытания также проводился тщательный мониторинг образцов мокроты для выявления любых побочных эффектов на приобретение организмов, плотность организма и воспаление.В целом, эти результаты не показали отрицательного эффекта от длительного использования режима ингаляций с гипертоническим раствором два раза в день. Преимущество, которое часто упускают из виду, заключалось в том, что пациенты в активной группе исследования оценивали легкость отхождения мокроты как значительно большую в конце исследования. Вероятно, это имеет важные социальные последствия. Если пациенты могут более эффективно очищать свои секреты во время очистки дыхательных путей, это позволяет им заниматься своей работой, учебой и общественными мероприятиями, не беспокоясь о продуктивном кашле во время взаимодействия с другими людьми.
Ни одно исследование не выявило подгруппу пациентов с МВ, которые особенно хорошо реагируют на терапию гипертоническим раствором. Например, в долгосрочном исследовании влияние гипертонического раствора на обострения не различается значительно между пользователями и лицами, не принимающими физиотерапию, между субъектами с легким или тяжелым нарушением функции легких, а также между пользователями и не пользователями рекомбинантного человеческого препарата. дезоксирибонуклеаза (рчДНаза). Поэтому мы рекомендуем эту терапию большинству людей с МВ, которые считают ее переносимой. 26 Соответствующие испытания на переносимость описаны ниже.
Текущее исследование
Интересной особенностью большинства исследований, обсужденных выше, является наличие зависимости «доза-реакция» для гипертонического раствора. Влияние на вязкость и способность к образованию нитей усиливается по мере увеличения концентрации физиологического раствора. 4 , 5 Воздействие на жидкость поверхности дыхательных путей также намного больше, когда на эпителиальную поверхность наносится больший объем гипертонического раствора. 11 , 12 Ускорение мукоцилиарного клиренса также значительно увеличивается при использовании больших концентраций физиологического раствора. 15 , 16 Однако побочные эффекты, такие как кашель, также усиливаются с увеличением концентрации. Поэтому некоторые врачи задаются вопросом, получат ли пациенты, которые не переносят стандартную дозу, более низкую (но более переносимую) концентрацию гипертонического раствора. Мы начали рандомизированное клиническое исследование (ACTRN12610000754044), в котором будет сравниваться стандартная концентрация физиологического раствора с более низкой концентрацией гипертонического раствора, а также с физиологическим раствором в качестве контрольного состояния.
Другой подход к проблеме переносимости — это изменение гипертонического солевого раствора. Buonpensiero и его коллеги 27 исследовали гипертонический раствор, смешанный с 0,1% гиалуроновой кислотой — природным полисахаридом. Гиалуроновая кислота, по-видимому, имеет несколько других механизмов, которые могут быть полезны в дыхательных путях при МВ, но Буонпансьеро и его коллеги изучили ее влияние на переносимость и воспринимаемую соленость комбинированного раствора по сравнению с одним гипертоническим раствором.Они отметили улучшение переносимости гипертонического раствора и уменьшение ощущаемого соленого вкуса при добавлении в раствор гиалуроновой кислоты. Эти изменения были статистически и клинически значимыми.
В первоначальное долгосрочное контролируемое испытание гипертонического раствора принимали участие только участники в возрасте 6 лет. Младенческое исследование ингаляционного физиологического раствора при муковисцидозе (ISIS) рассмотрит этот вопрос путем изучения использования гипертонического физиологического раствора у младенцев и детей от 4 до 59 месяцев ({«type»: «клиническое испытание», «attrs»: {«text «:» NCT00709280 «,» term_id «:» NCT00709280 «}} NCT00709280).Первичным результатом этого исследования будет частота обострений легких, определенных протоколом, требующих лечения антибиотиками, по сравнению с частотой в контрольной группе, которая будет вдыхать физиологический раствор.
В ожидании результатов этих испытаний мы продолжаем рекомендовать применение гипертонического раствора для большинства взрослых и детей старшего возраста с МВ. Если у пациента начинается терапия гипертоническим раствором, первая доза должна контролироваться с помощью спирометрии и пульсоксиметрии до и после приема дозы, чтобы гарантировать отсутствие клинически значимого сужения дыхательных путей (т.е. падение FEV 1 более чем на 15% или заметная десатурация после приема дозы). Всем дозам, включая начальную тестовую дозу, следует вводить бронходилататор. Переносимость часто улучшается после первых 10 доз, поэтому пациентов, которым трудно переносить первые дозы, следует поощрять к упорству, при условии, что у них нет признаков заметного сужения дыхательных путей. Пациенты, не прошедшие первоначальный тест на переносимость, могут быть повторно обследованы позже; часто вторая тестовая доза переносится гораздо легче.
Гипертонический раствор также исследуется как средство лечения бронхоэктазов, не связанных с МВ, и хронической обструктивной болезни легких (ХОБЛ). Хотя гидратация поверхности дыхательных путей может быть менее важной, чем при МВ, все другие механизмы действия гипертонического раствора могут работать при бронхоэктазах. Обоснование использования при ХОБЛ менее ясно, хотя устранение задержанных секретов считается допустимой целью лечения там, где они возникают. Некоторые исследования показали значительное совпадение патологии между ХОБЛ и бронхоэктазами. 28 , 29 Поскольку гипертонический раствор может вызывать сужение дыхательных путей, это следует очень тщательно контролировать при испытаниях гипертонического раствора при обструктивных заболеваниях легких, таких как ХОБЛ. В будущих исследованиях будет также оцениваться эффект гипертонического раствора в сочетании с другими классами лекарств, такими как антибиотики или противовоспалительные средства.
ЗАЯВЛЕНИЯ
Конкурирующие интересы
Не заявлены
Этическое одобрение
Неприменимо
Участие
Оба автора внесли равный вклад
Ссылки
1.Рубин БК Таксономия мукоактивных препаратов. В: Рубин Б.К., Ван дер Сханс С.П., ред. Терапия нарушений очистки слизи. Том 188, Биология легких в здоровье и болезнях. Нью-Йорк, Нью-Йорк: Марсель Деккер, 2004: 129–45 [Google Scholar] 2. Хенке М, Ратьен Ф Муколитики при муковисцидозе. Пэд Респир Рев 2007; 8: 24–9 [PubMed] [Google Scholar] 3. Цимент I Респираторная фармакология и терапия. Филадельфия, Пенсильвания: WB Saunders, 1978: 60–104 [Google Scholar] 4. Шеффнер А.Л., Медлер Е.М., Якобс Л.В., Саретт Х.П. Снижение in vitro вязкости трахеобронхиального секрета человека за счет ацетилцистеина.Am Rev Respir Dis 1964; 90: 721–9 [PubMed] [Google Scholar] 5. King M, Dasgupta B, Tomkiewicz RP, Brown NE Реология мокроты при муковисцидозе после лечения in vitro только гипертоническим солевым раствором и в сочетании с рекомбинантной дезоксирибонуклеазой человека I. Am J Respir Crit Care Med 1997; 156: 173–7 [PubMed] [Google Scholar] 6. Уиллс П.Дж., Коул П.Дж. Хлорид натрия улучшает цилиарную транспортабельность мокроты. Am J Respir Crit Care Med 1995; 151: A720 [PubMed] [Google Scholar] 7. Уиллс П.Дж., Холл Р.Л., Чан В.М., Коул П.Дж. Хлорид натрия увеличивает цилиарную переносимость мокроты при муковисцидозе и бронхоэктазиях на обедненную слизью трахею крупного рогатого скота.J Clin Invest 1997; 99: 9–13 [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Либерман Дж., Курник Н. Б. Влияние содержания дезоксирибонуклеиновой кислоты на протеолиз мокроты и гноя. Природа 1962; 196: 988–90 [PubMed] [Google Scholar] 9. Штуттс MJ, Canessa CM, Olsen JC, et al. CFTR как цАМФ-зависимый регулятор натриевых каналов. Наука 1995; 269: 847–50 [PubMed] [Google Scholar] 10. Тарран Р., Грабб Б.Р., Парсонс Д. и др. Противоречие CF соли: наблюдения in vivo и терапевтические подходы. Mol Cell 2001; 8: 149–58 [PubMed] [Google Scholar] 11.Дональдсон С.Х., Беннетт В.Д., Земан К.Л., Ноулз М.Р., Тарран Р., Бушер Р. Очистка слизи и функция легких при муковисцидозе с гипертоническим раствором. New Engl J Med 2006; 354: 241–50 [PubMed] [Google Scholar] 12. Горальски Дж., Кнопка B Изучение in vitro кинетики гипертонического раствора на высоте над уровнем моря. Пед Пульмонол 2010; 45: A205 [Google Scholar] 13. Тарран Р., Грабб Б.Р., Гатзи Д.Т., Дэвис С.В., Буше Р.К. Относительные роли пассивных поверхностных сил и активного переноса ионов в модуляции объема и состава жидкости на поверхности дыхательных путей.J Gen Physiol 2001; 118: 223–36 [Бесплатная статья PMC] [PubMed] [Google Scholar] 14. Элкинс MR, Пока, PTP Ингаляционный гипертонический раствор для лечения муковисцидоза. Curr Opin Pulm Med 2006; 12: 445–52 [PubMed] [Google Scholar] 15. Робинсон М., Регнис Дж. А., Бейли Д. Л., Кинг М., Баутович Г. Дж., Пока П. Т. Влияние гипертонического раствора, амилорида и кашля на мукоцилиарный клиренс у пациентов с муковисцидозом. Am J Respir Crit Care Med 1996; 153: 1503–9 [PubMed] [Google Scholar] 16. Робинсон М., Хемминг А.Л., Регнис Дж. А. и др.Влияние увеличения доз гипертонического раствора на мукоцилиарный клиренс у пациентов с муковисцидозом. Грудная клетка 1997; 52: 900–3 [Бесплатная статья PMC] [PubMed] [Google Scholar] 17. Мюррей Т.С. Влияние гипертонического раствора на колонизацию Pseudomonas aeruginosa in vitro. Пед Пульмонол 2010; 45: A367 [Google Scholar] 18. Гулд Н.С., Готье С., Кария К.Т., Мин Э, Хуанг Дж., Дэй Б.Дж. Гипертонический раствор увеличивает содержание жидкости в эпителиальной выстилке легких, глутатиона и тиоцианата: двух тиолов, защищающих CFTR от окислительного повреждения.Respir Res 2010; 11; 119. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. де Бок К., Алифер, Вандепутте С. Индукция мокроты у молодых пациентов с муковисцидозом. Eur Respir J 2000; 16: 91–4 [PubMed] [Google Scholar] 20. Хениг Н.Р., Тонелли М.Р., Пьер М.В., Бернс Д.Л., Эйткен М.Л. Индукция мокроты как инструмент исследования для отбора проб дыхательных путей у пациентов с муковисцидозом. Грудная клетка 2001; 56: 306–11 [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Кастелик Я.А., Азиз Я., Морис А.Х. Индукция мокроты у молодых пациентов с муковисцидозом.Eur Respir J 2001; 17: 1 [PubMed] [Google Scholar] 22. Сагель С.Д., Капснер Р., Осберг I, Зонтаг М.К., Accurso FJ Воспаление дыхательных путей у детей с муковисцидозом и здоровых детей, оцениваемое по индукции мокроты. Am J Respir Crit Care Med 2001; 164: 1425–31 [PubMed] [Google Scholar] 23. Ридлер Дж., Рид Т, Баттон Б, Робертсон К.Ф. Вдыхаемый гипертонический раствор увеличивает отхождение мокроты при муковисцидозе. J Paediatr Детское здоровье 1996; 32: 48–50 [PubMed] [Google Scholar] 24. Англия, Дж. Мортон, Дуглас Дж., Ридлер Дж., Уилсон Дж., Робертсон К.Ф. Краткосрочная эффективность распыляемого ультразвуком гипертонического раствора при муковисцидозе.Пед Пульмонол 1996; 21: 77–83 [PubMed] [Google Scholar] 25. Элкинс М.Р., Робинсон М., Роуз Б.Р. и др. Контролируемое испытание длительного применения ингаляционного гипертонического раствора у пациентов с муковисцидозом. New Engl J Med 2006; 354: 229–40 [PubMed] [Google Scholar] 26. Пока, PTP, Элкинс MR Другие мукоактивные агенты при муковисцидозе. Пэд Респир Рев 2007; 8: 30–9 [PubMed] [Google Scholar] 27. Буонпансьеро П., Де Грегорио Ф, Сепе А. и др. Вдыхаемая гиалуроновая кислота улучшает комфорт и переносимость распыленного гипертонического раствора у пациентов с муковисцидозом.Adv Ther 2010; 27: 870–8 [PubMed] [Google Scholar] 29. Патель И.С., Влахос И., Уилкинсон Т.МА. и др. Бронхоэктазы, показатели обострения и воспаления при хронической обструктивной болезни легких. Am J Respir Crit Care Med 2004; 170: 400–7 [PubMed] [Google Scholar]Использование хлорида натрия при вдыхании, побочные эффекты и предупреждения
Общее название: хлорид натрия (ингаляция) (SOE dee um KLOR ide)
Фирменное наименование: Hyper-Sal, NebuSal, хлорид натрия, ингаляция
Лекарственные формы: раствор для ингаляций (0.45%; 0,9%; 10%; 3,5%; 3%; 6%; 7%)
Класс лекарств: Минералы и электролиты, Прочие респираторные агенты
Проверено с медицинской точки зрения Drugs.com 23 ноября 2020 г. Автор Cerner Multum.
Что такое ингаляция хлорида натрия?
Хлорид натрия — это химическое название соли. Хлорид натрия может уменьшить количество некоторых видов бактерий в определенных выделениях организма, например, в слюне.
Ингаляция хлорида натрия используется для получения мокроты (слизи или мокроты) изо рта с целью улучшения функции легких у людей с муковисцидозом или для сбора мокроты для медицинских исследований.Это лекарство также можно использовать для разбавления других лекарств, вдыхаемых через небулайзер.
Вдыхание хлорида натрия также может использоваться для других целей, не указанных в данном руководстве.
Предупреждения
Перед применением хлорида натрия сообщите врачу обо всех своих заболеваниях и аллергиях. Также убедитесь, что ваш врач знает, беременны вы или кормите грудью. В некоторых случаях вы не сможете использовать хлорид натрия, или вам может потребоваться скорректировать дозу или принять особые меры предосторожности.
Сообщите своему врачу обо всех других лекарствах, которые вы принимаете, особенно о добавках калия, диуретиках, стероидах, лекарствах от кровяного давления или лекарствах, содержащих натрий (например, Alka-Seltzer или Zegrid).
Немедленно сообщите своему опекуну, если у вас есть боль в груди, затрудненное дыхание, отек рук или ног, усталость, мышечные подергивания, спутанность сознания, неравномерное сердцебиение, сильная жажда, учащенное или уменьшенное мочеиспускание, дискомфорт в ногах, мышечная слабость или ощущение хромоты, или если вы чувствуете, что можете потерять сознание.
Перед приемом этого лекарства
Вы не должны использовать это лекарство, если у вас когда-либо была аллергическая реакция на хлорид натрия.
Чтобы убедиться, что хлорид натрия безопасен для вас, сообщите своему врачу, если у вас есть:
FDA категория беременности C. Неизвестно, вредно ли вдыхание хлорида натрия для будущего ребенка. Сообщите своему врачу, если вы беременны или планируете забеременеть во время лечения.
Неизвестно, проникает ли хлорид натрия в грудное молоко или может нанести вред кормящемуся ребенку.Сообщите своему врачу, если вы кормите ребенка грудью.
Как вводится ингаляция хлорида натрия?
Следуйте всем указаниям на этикетке с рецептом. Не используйте это лекарство в больших или меньших количествах или дольше, чем рекомендуется.
При вдыхании хлорида натрия используется небулайзер. Вы будете вдыхать лекарство через маску для лица, мундштук или другое устройство, подключенное к небулайзеру.
Ваш врач, медсестра или другой поставщик медицинских услуг может показать вам, как правильно пользоваться небулайзером.
Хлорид натрия — это жидкость, которую помещают в камеру для лекарств небулайзера. Затем к камере для лекарства прикрепляют мундштук или лицевую маску вместе с воздушным компрессором.
Чтобы подготовиться к вдыханию хлорида натрия через небулайзер, вам могут дать другое ингаляционное лекарство для предотвращения бронхоспазма (сокращения мышц в дыхательных путях легких). Врач также может попросить вас высморкаться, прополоскать рот водой или протереть внутреннюю часть рта салфеткой.Для достижения наилучших результатов внимательно следуйте инструкциям врача.
В большинстве случаев вы будете принимать это лекарство, сидя прямо в удобном положении. Дышите медленно и равномерно, используя маску, загубник или другое дыхательное устройство. Вам также могут дать зажим для носа, который закроет носовые проходы, и вы будете вдыхать только через рот.
Если вы принимаете это лекарство в рамках анализа мокроты, вам нужно будет плевать каждые 5 минут или в соответствии с указаниями вашего лечащего врача.Глубоко кашляйте грудью, чтобы получить оптимальный образец для анализа.
Продолжайте дышать через небулайзер так долго, как предписано врачом. После того, как вы завершите ингаляцию в течение предписанного времени, выбросьте всю жидкость, которая осталась в камере для лекарств. Не сохраняйте его для дальнейшего использования.
Если вы храните хлорид натрия дома, храните его при комнатной температуре вдали от влаги и тепла.
Что произойдет, если я пропущу дозу?
Поскольку ингаляции хлорида натрия иногда используются только по мере необходимости, вы можете не соблюдать график дозирования.Если вы принимаете лекарство регулярно, примите пропущенную дозу, как только вспомните. Пропустите пропущенную дозу, если пришло время для следующей запланированной дозы. Не используйте дополнительное лекарство, чтобы восполнить пропущенную дозу.
Что произойдет, если я передозирую?
Обратитесь за неотложной медицинской помощью или позвоните в справочную службу Poison по телефону 1-800-222-1222.
Чего следует избегать при использовании ингаляций хлорида натрия?
Следуйте инструкциям врача о любых ограничениях в еде, напитках или занятиях.
Побочные эффекты при вдыхании хлорида натрия
Получите неотложную медицинскую помощь, если у вас есть какие-либо из этих признаков аллергической реакции : крапивница; затрудненное дыхание; отек лица, губ, языка или горла.
Немедленно сообщите опекуну, если у вас есть:
боль в груди, затрудненное дыхание;
ощущение головокружения, будто вы можете потерять сознание;
опухоль в руках или ногах;
усталость, подергивание мышц;
спутанность сознания, неравномерное сердцебиение, сильная жажда, учащенное или уменьшенное мочеиспускание, дискомфорт в ногах, мышечная слабость или ощущение хромоты.
Другие частые побочные эффекты могут включать соленый привкус, легкое жжение или раздражение во рту.
Это не полный список побочных эффектов, которые могут возникнуть. Спросите у своего доктора о побочных эффектах. Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-FDA-1088.
Какие другие препараты повлияют на вдыхание хлорида натрия?
Расскажите своему врачу обо всех лекарствах, которые вы используете, и о тех, которые вы начинаете или прекращаете использовать во время лечения хлоридом натрия, особенно:
Этот список не полный.Другие препараты могут взаимодействовать с хлоридом натрия, включая лекарства, отпускаемые по рецепту и без рецепта, витамины и растительные продукты. В этом руководстве по лекарствам перечислены не все возможные взаимодействия.
Дополнительная информация
Помните, храните это и все другие лекарства в недоступном для детей месте, никогда не передавайте свои лекарства другим и используйте это лекарство только по назначению.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности за медицинское обслуживание
Copyright 1996-2021 Cerner Multum, Inc. Версия: 2.02.
Продукты, которые можно использовать для ингаляций
Какой продукт мне следует использовать для ингаляций? Это зависит от содержания соли.
Различные солевые растворы от PARI имеют разное содержание соли. Хотите защититься от простуды или уже простудились? Затем следует выбрать ингаляционный раствор PARI NaCl 0,9% с содержанием соли 0,9% для ингаляций с помощью небулайзера.Этот изотонический физиологический раствор увлажняет дыхательные пути и помогает слизистым оболочкам избавиться от вирусов и бактерий. Изотонический или физиологический означает, что раствор имеет такое же содержание соли, что и жидкости нашего организма, и поэтому хорошо переносится, а не вызывает дополнительное раздражение пораженных дыхательных путей.
Более высокое содержание соли для более сильного эффекта
Гипертонические солевые растворы, такие как MucoClear 3% и 6% от PARI, определяются как растворы с содержанием соли 1% или более.Эти ингаляционные растворы, содержащие больше соли, чем физиологические жидкости, разжижают слизь в носовых пазухах или легких. Это облегчает вывод слизи из дыхательных путей и снимает неприятные симптомы, особенно при тяжелых респираторных заболеваниях.
Что нельзя использовать в ингаляционном аппарате
Что нельзя использовать для ингаляционной терапии? С другой стороны, сиропы от кашля, растворы для полоскания, препараты линимента или капли, используемые для растирания или «паровой бани» с горячей водой, совершенно непригодны для использования в ингаляционных устройствах.Также следует быть осторожным с маслами лекарственных растений, побочные эффекты которых могут представлять опасность для вашего здоровья. Эти продукты также часто бывают толстыми и липкими и блокируют сопла небулайзера, который является частью вашего ингаляционного устройства.
Эфирные масла могут вызывать респираторный дистресс у людей с гиперчувствительной бронхиальной системой, особенно при слишком сильном сужении бронхов. К вдыханию воды или дистиллированной воды следует относиться критически.
Почему ромашка не подходит для ингаляционной терапии
Или просто вдыхать ромашкой над кастрюлей? Ромашка встречается почти в каждом доме в виде пакетиков чая, концентрата ромашки или даже в виде сушеных цветов.Ромашка обладает противовоспалительными и дезинфицирующими свойствами. Проверенное и проверенное домашнее средство часто рекомендуется при рините, простуде, синусите или даже головной боли, и его можно вдыхать над кастрюлей или головой над горячей миской с горячей водой. Однако при использовании кастрюли есть риск обжечься. Это может вызвать раздражение глаз, особенно у детей. Кроме того, якобы успокаивающий пар не достигает носовых пазух. Вы также никогда не должны вводить водную смесь, приготовленную из ромашки, в устройство для ингаляции.
Разбавители слизи | CF Foundation
Гипертонический физиологический раствор — это стерильный физиологический раствор различной концентрации: 3 процента, 3,5 процента и 7 процентов. Он работает за счет увеличения количества натрия (соли) в дыхательных путях.
Соль притягивает воду в дыхательные пути, которая разжижает слизь, что облегчает откашливание.Исследования показали, что вдыхание гипертонического раствора два раза в день помогает людям с муковисцидозом меньше болеть легочными инфекциями.
Кто должен это принимать?
Люди в возрасте 6 лет и старше или с объемом форсированного выдоха (FEV 1 ), превышающим или равным 40 процентам от прогнозируемого, могут принимать гипертонический раствор, но это было изучено на детях младшего возраста. Прежде чем его назначат, ваша бригада по уходу за CF может провести несколько тестов, чтобы определить, подходит ли вам гипертонический раствор.
Как мне это взять?
Хотя гипертонический раствор можно прописать в медицинском центре, чтобы вызвать кашель, чаще всего вы вдыхаете гипертонический раствор в виде тумана два раза в день через небулайзер. Однако все люди разные, поэтому ваша бригада по лечению CF назначит вам, сколько и как часто вам следует принимать гипертонический раствор, в зависимости от ваших конкретных потребностей в отношении здоровья. Чтобы убедиться, что гипертонический раствор не вызывает проблем, ваша медицинская бригада может попросить вас принять первую дозу, пока вы находитесь в медицинском центре.Спросить вашей медицинской бригаде, можете ли вы использовать небулайзер и компрессор или вам нужно другое оборудование.
Для получения полных инструкций о том, как принимать гипертонический раствор, посетите DailyMed, службу Национальной медицинской библиотеки, которая предоставляет информацию о лекарствах, в том числе дозировки и возможные побочные эффекты.
Для приема гипертонического раствора:
- Вымойте и высушите руки.
- Вылейте одноразовый флакон с гипертоническим раствором в чистую чашку небулайзера.
- Сядьте прямо на стул.
- Поместите мундштук небулайзера между зубами и на верхнюю часть языка.
- Нормально вдыхайте и выдыхайте через рот, стараясь не дышать через нос.
- Не забывайте делать пару глубоких вдохов каждую минуту или две, чтобы солевой раствор достиг ваших меньших дыхательных путей.
- Когда вы слышите звук, похожий на плевок, это означает, что гипертонический раствор почти израсходован.Постучите по небулайзеру. Продолжайте вдыхать лекарство, пока оно не будет использовано полностью.
- Не забудьте использовать полную дозу. Если по какой-то причине вам нужно откашляться или прекратить лечение, выключите компрессор. Когда вы будете готовы возобновить лечение, снова включите компрессор и продолжите лечение.
Не принимайте одновременно гипертонический раствор и другие лекарства.
Гипертонический раствор может повредить электрическое оборудование, например компьютеры, если поднести его слишком близко к электронике.Убедитесь, что вы берете гипертонический раствор в хорошо проветриваемом помещении, вдали от электроники.
Чего ожидать после приема?
В отличие от лекарств, таких как антибиотики, гипертонический раствор не остается в организме, поэтому преимущества разжиженной слизи временные. Поэтому важно выполнять методы очистки дыхательных путей сразу после приема гипертонического раствора или дорназы альфа, если вы принимаете его, пока ваша слизь все еще жидкая и ее легче выводить из дыхательных путей.
У вас могут возникнуть побочные эффекты при приеме любых лекарств, включая гипертонический раствор. Общие побочные эффекты гипертонического раствора включают:
- Усиленный кашель
- Боль в горле
- Плотность груди
При обсуждении любых новых лекарств или изменений в дозировках лекарств, которые вы уже принимаете, не забудьте спросить у вашей команды по уходу:
- Любые возможные побочные эффекты
- Какие побочные эффекты могут быть более серьезными, чем другие
- Как долго они могут просуществовать
- Когда поговорить с вашей медицинской бригадой, если побочные эффекты не проходят или влияют на качество вашей жизни
Сообщите вашей медицинской бригаде, если вы почувствуете какие-либо побочные эффекты, из-за которых вам будет трудно продолжать прием этого лекарства в соответствии с предписаниями.Ваша медицинская группа может работать с вами, чтобы помочь вам справиться с побочными эффектами или скорректировать план лечения.
Дорназа альфа (Pulmozyme ® ) — это ингаляционный препарат, разжижающий слизь. Дорназа альфа, которую иногда называют муколитиком или ДНКазой, действует как ножницы, разрезая длинные цепи ДНК, содержащиеся в белых кровяных тельцах.Разрезая эти пряди на более короткие кусочки, дорназа альфа помогает разрушить густую липкую слизь, которая часто приводит к легочным инфекциям.
Кто должен это принимать?
В рекомендациях Фонда муковисцидоза «Хронические лекарства для поддержания здоровья легких» рекомендуется использовать дорназу альфа людям с муковисцидозом в возрасте от 6 лет и старше для улучшения функции легких и уменьшения обострений или легочных инфекций.Он одобрен для людей в возрасте от 5 лет и старше, но был изучен на детях младшего возраста.
Вы не должны принимать дорназу альфа, если у вас аллергия на любой из следующих ингредиентов:
- Дорназа альфа
- Хлорид кальция
- Натрия хлорид (соль)
Как мне это взять?
Храните дорназу альфа в холодильнике, пока не будете готовы к ее использованию. Дорназа альфа принимается через небулайзер один или два раза в день в соответствии с предписаниями врача.
Чтобы получить полные инструкции о том, как принимать дорназу альфа, посетите DailyMed, службу Национальной медицинской библиотеки США, которая предоставляет информацию на этикетках FDA о продаваемых лекарствах.
Дорназа альфа выпускается в ампулах или флаконах для однократного приема.
Для приема дорназа альфа:
- Вымойте и высушите руки.
- Вылейте содержимое ампулы в чашку небулайзера.
- Сядьте прямо на стул. Поместите мундштук небулайзера между зубами и на верхнюю часть языка.
- Нормально вдыхайте и выдыхайте через рот, стараясь не дышать через нос.
- Не забывайте делать пару глубоких вдохов каждую минуту или две, чтобы лекарство достигло ваших меньших дыхательных путей.
- Когда вы слышите звук, похожий на плевок, это означает, что лекарство почти израсходовано. Постучите по небулайзеру. Продолжайте вдыхать лекарство, пока оно не будет использовано полностью.
- Не забудьте использовать полную дозу. Если по какой-то причине вам нужно откашляться или прекратить лечение, выключите компрессор.Когда вы будете готовы возобновить лечение, снова включите компрессор и продолжите лечение.
Чего ожидать после приема?
В отличие от таких лекарств, как антибиотики, дорназа альфа не остается в организме, поэтому разжижение слизи носит временный характер. Поэтому важно выполнять методы очистки дыхательных путей сразу после приема дорназы альфа, пока ваша слизь все еще жидкая и ее легче выводить из дыхательных путей.
При приеме лекарств могут возникнуть побочные эффекты.Общие побочные эффекты дорназы альфа включают:
- Изменение или потерю голоса
- Дискомфорт в горле
- Красные, слезящиеся глаза
- Сыпь
- Головокружение
- Лихорадка
- Насморк
При обсуждении любых новых лекарств или изменений в дозировках лекарств, которые вы уже принимаете, обязательно спросите свою команду по уходу о:
- Любых возможных побочных эффектах
- Какие побочные эффекты могут быть более серьезными, чем другие
- Как долго они могут просуществовать
- Когда поговорить с вашей медицинской бригадой, если побочные эффекты не проходят или влияют на качество вашей жизни
Сообщите вашей медицинской бригаде, если вы почувствуете какие-либо побочные эффекты, из-за которых вам будет трудно продолжать прием этого лекарства в соответствии с предписаниями.Ваша медицинская группа может работать с вами, чтобы помочь вам справиться с побочными эффектами или скорректировать план лечения.
Гипертонический раствор доступен как в розничных, так и в специализированных аптеках. Dornase alfa чаще всего можно приобрести в специализированных аптеках, заключивших договор с вашим страховым планом.В специализированной аптеке выписываются рецепты на лекарства, которых нет в местных розничных аптеках. Лекарства из специализированных аптек часто требуют специального обращения и хранения, а также быстрой доставки к вам домой, в офис или школу.
Если вы в настоящее время не пользуетесь услугами специализированной аптеки, попросите команду медицинского центра составить список рекомендуемых специализированных аптек, которые работают с вашим планом страхования.
Не все планы страхования покрывают гипертонический раствор или дорназу альфа. Фонд Cystic Fibrosis Foundation Compass — это бесплатная индивидуальная услуга, которая может помочь вам со страхованием, финансовыми, юридическими и другими вопросами. Специализированные менеджеры по делам Compass могут помочь в координации льгот или предоставить информацию о льготах, предлагаемых в рамках ваших планов. Свяжитесь с Compass по телефону:
844-КОМПАС (844-266-7277)
Понедельник — пятница, 9 а.м. — 19:00 ET
[email protected]
***
Ссылка на какой-либо конкретный продукт, процесс или услугу не обязательно означает или подразумевает его одобрение, рекомендацию или поддержку Фондом кистозного фиброза. Появление внешних гиперссылок не означает одобрения Фондом кистозного фиброза связанных веб-сайтов или информации, продуктов или услуг, содержащихся на них.
Информация, содержащаяся на этом сайте, не охватывает все возможные способы использования, действия, меры предосторожности, побочные эффекты или взаимодействия.Этот сайт не предназначен для замены рекомендаций по лечению от медицинского работника. Проконсультируйтесь с врачом, прежде чем вносить какие-либо изменения в свое лечение.
Информация о лекарствах, одобренных FDA, доступна на сайте dailymed.nlm.nih.gov/dailymed.
Исследователи работают над тем, чтобы больше узнать о слизи и разработать новые методы лечения, которые предотвращают, разжижают и разрушают слизь в дыхательных путях.
Ингаляционный гипертонический раствор у взрослых, госпитализированных по поводу обострения муковисцидоза: ретроспективное исследование
Краткое содержание статьи
Фокус статьи
Долгосрочное использование ингаляционных HTS улучшает легочную функцию и снижает частоту обострений у пациентов с CF.
Несмотря на отсутствие доступных данных относительно эффективности и безопасности, ингаляционные HTS часто используются во время госпитализации для обострения болезни легких при МВ.
Ключевые сообщения
Это ретроспективное нерандомизированное исследование предполагает, что ингаляционные HTS хорошо переносятся во время госпитализации по поводу обострения CF болезни легких.
Кратковременное (14 дней) использование ингаляционных HTS не дало дополнительных улучшений по сравнению со стандартным лечением (внутривенное введение антибиотиков и физиотерапия грудной клетки) в отношении легочной функции, увеличения веса или времени до следующей госпитализации.
Сильные стороны и ограничения этого исследования
Это исследование позволило внутри пациента сравнить стандартное лечение с ингаляционными HTS или без них у относительно однородной взрослой популяции в условиях стационара.
Основным ограничением этого исследования является ретроспективный и нерандомизированный дизайн и отсутствие подробных данных о соблюдении и побочных эффектах. Размер выборки соответствовал целям исследования.
Предпосылки
Заболевания легких — основная причина заболеваемости и смертности пациентов с муковисцидозом (МВ). Он характеризуется хронической бактериальной колонизацией и рецидивирующими инфекциями дыхательных путей, которые были очевидными проявлениями заболевания с момента появления термина «муковисцидоз».1 2 Мутации в гене регулятора трансмембранной проводимости при МВ приводят к дефекту эпителиального транспорта хлоридов в эпителии дыхательных путей человека, но последующие последствия этого дефекта и то, как они приводят к заболеванию легких при МВ, еще предстоит выяснить. Для МВ характерны периоды «стабильного» заболевания, перемежающиеся периодическими обострениями, во время которых такие симптомы, как выделение мокроты и кашель, имеют тенденцию к резкому усилению интенсивности и связаны с увеличением бактериальной плотности в легких и гипоксемией.5–8
Во время обострения острого заболевания легких при МВ обычное лечение включает внутривенные антибиотики, усиленные пищевые добавки и методы очистки дыхательных путей (например, частая физиотерапия грудной клетки, ингаляционный альбутерол, аэробные упражнения) .7 9 Ингаляционная рчДНаза может улучшить легочную функцию при длительном применении. термин, хотя и по относительно высокой цене. 10–12 Гипертонический раствор для вдыхания (HTS) является привлекательным дополнением, поскольку он недорог, достаточно хорошо переносится и резко увеличивает клиренс слизи из всего легкого.Было показано, что длительное лечение ингаляционными HTS улучшает легочную функцию и снижает частоту обострений.13–18 Однако использование HTS во время обострения может быть потенциально более вредным, вызывая усиление бронхоспазма или кровохарканья. Насколько нам известно, ни в одном исследовании не изучались профиль безопасности и эффективность ингаляционного лечения HTS, проводимого во время обострения легочного МВ.
В этом пилотном ретроспективном исследовании мы изучаем влияние использования УТВ в когорте взрослых пациентов, госпитализированных с обострением легочного МВ, по сравнению с той же группой пациентов во время предыдущего обострения, когда УТВ не использовались.Мы предположили, что использование ингаляционных HTS в дополнение к стандартному уходу во время госпитализации по поводу обострения CF приведет к большему улучшению общих конечных точек, таких как функция легких, масса тела и время до следующего обострения по сравнению со стандартным лечением.
Методы
Исследование было одобрено Экспертным советом Университета Айовы (200710793). Это ретроспективный обзор всех госпитализаций взрослых по поводу обострения заболевания легких при МВ в больницах и клиниках Университета Айовы в течение 2006 и 2007 годов, когда пациентам впервые предложили вдыхать HTS.Стандартное лечение состоит из внутривенных антибиотиков, выбранных на основе последнего посева мокроты и тестирования на чувствительность, пищевых добавок, легочной реабилитации и методов интенсивного очищения от слизи, таких как физиотерапия грудной клетки, четыре раза в день. Испытуемым был поставлен диагноз МВ на основании теста на содержание хлорида пота или напряжения в носу, а также генотипирования гена CFTR . Для сравнительного исследования данные были извлечены из госпитализации, во время которой HTS («второе посещение») было впервые использовано, и сравнивались с более ранней госпитализацией в предыдущем году (2005), в которой HTS не использовались («первое посещение»).
Изученные переменные включают возраст и пол, индекс массы тела при поступлении и выписке, продолжительность госпитализации, внутривенное введение антибиотиков, мутацию CF, использование физиотерапии грудной клетки, результаты посева мокроты, время до следующего обострения и использование HTS во время последующих госпитализаций. Исходные значения легочной функции были получены в результате тестирования, проведенного в день госпитализации или в предыдущие 7 дней. При поступлении два раза в неделю проводилось исследование функции легких. Один субъект был выписан через 2 дня с периферически введенным центральным катетером для завершения приема антибиотиков в домашних условиях.Субъекты получали ингаляционный агонист β 2 для минимизации риска бронхоспазма с последующей дозой 4 мл 7% раствора HTS два раза в день через небулайзер Pari LC (PARI Respiratory Equipment, Midlothian, VA, USA). Данные о соответствии представлены как общее количество дней использования HTS на общее количество дней госпитализации в исследуемой популяции. В сравнительное исследование были включены только субъекты, которые использовали HTS не менее 7 дней. Основной переменной результата сравнения было изменение процента прогнозируемого объема форсированного выдоха за одну секунду (ОФВ 1 ) от исходного уровня до выписки.Субъекты, которым не удалось достичь 90% наилучшего процента прогнозируемого ОФВ -1 за 6 месяцев до госпитализации, были определены как не отвечающие на терапию.19 Другие проанализированные исходы включают продолжительность пребывания, комплаентность, время до следующей госпитализации и увеличение веса.
Анализ мощности
Анализ мощности предложил парную выборку из 18 пациентов, чтобы выявить изменение ОФВ 1 (первичный результат) на 10,9% (первичный результат) или веса с консервативным стандартным отклонением между группами 16%, с 80% мощностью при двусторонний α = 0.05. Анализ наблюдаемой мощности для первичных и вторичных исходов подробно описан в разделе «Обсуждение».
Анализ результатов
Данные анализировали с помощью Prism 5 для Mac OS (программное обеспечение Graphpad) и SAS V.9.2 (институт SAS). Анализ мощности выполняли с использованием Statmate (программное обеспечение Graphpad). Одномерные данные представлены как средние, стандартное отклонение и пропорции. Парный t-критерий использовался для сравнений с 5% уровнем значимости. Смешанные модели для повторных измерений были использованы для сравнения изменения ОФВ 1 по сравнению с исходным уровнем в сравнительном исследовании.Точный критерий Фишера использовался для вычисления значения p анализа непредвиденных обстоятельств «не ответивших» и «респондентов» в обоих посещениях и для анализа категориальных данных в таблице 1.
Таблица 1Характеристики пациента во время госпитализации *
Результаты
Участники исследования
В период с января 2006 г. по декабрь 2007 г. 45 пациентов были госпитализированы в стационарное отделение больниц и клиник Университета Айовы. Средний возраст госпитализации для данной популяции составлял 32 года.5 ± 10,1 года, а средняя продолжительность госпитализации составила 11,1 ± 4,1 дня (p> 0,05, непарный t-критерий). 46% этих испытуемых составляли мужчины. Из 45 субъектов 25 поступили в предыдущий год. Всем 25 пациентам было проведено исследование функции легких перед поступлением и при выписке. Из этих 25 субъектов у 18 не было в анамнезе астмы или недавнего кровохарканья, поэтому им предлагалось вдыхать HTS. Таким образом, эти 18 субъектов были включены в сравнительное исследование, как описано в разделе «Методы».Исходные характеристики при поступлении для субъектов, которые соответствовали критериям включения в сравнительное исследование, показаны в таблице 1. В течение всего периода исследования использование HTS дома перед госпитализацией было редкостью (0% субъектов во время первого посещения и 5% во время второй визит). Доля пациентов, принимавших ингаляционный тобрамицин или рчДНазу, была сходной до поступления в оба госпиталя (p> 0,05), а распространенность колонизации Pseudomonas aeruginosa или Staphylococcus aureus также была одинаковой в обоих случаях госпитализации (p> 0.05).
HTS хорошо переносится большинством пациентов, госпитализированных по поводу острого обострения CF
В течение периода исследования ингаляционные HTS предлагались 34 из 45 субъектов, из которых 33 использовали его не менее 1 дня. Остальным 11 пациентам не предлагались ингаляционные HTS из-за астмы или недавнего кровохарканья в анамнезе. Среди 33 субъектов было совместное использование HTS в общей сложности 336 дней из 364 дней госпитализации. Из 28 дней полного прекращения лечения 24 были объяснены побочными эффектами (хрипы и легкое кровохарканье) у двух субъектов.Двадцать семь субъектов использовали HTS более 7 дней. Эти данные свидетельствуют о том, что вдыхаемые HTS хорошо переносятся пациентами, госпитализированными по поводу обострения заболевания легких при МВ.
HTS не улучшает легочную функцию во время госпитализации по поводу обострения CF
Среди 18 субъектов, включенных в сравнительное исследование, среднее изменение прогнозируемого процентного значения FEV 1 от исходного уровня до выписки (в процентных пунктах) составило 12,2% (95 % ДИ от 7,7% до 16,5%), когда HTS не использовался, и 8.9% (95% ДИ от 4,9% до 12,9%) при использовании HTS (рисунок 1A), предполагая, что вдыхание HTS привело к снижению ОФВ 1 при выписке (p = 0,02, 95% ДИ от 0,5% до 5,9%) . Однако средний процент прогнозируемого ОФВ 1 при поступлении был выше, когда использовался HTS (p = 0,04) (рис. 1B), в то время как средние значения ОФВ при выделении 1 значимо не отличались (p = 0,46) между двумя посещениями (рисунок 1С). Данные предполагают, что снижение ОФВ 1 , улучшение при использовании ингаляционных HTS, вероятно, связано с более высоким ОФВ при поступлении 1 во время этой госпитализации.Корректировка смешанной модели для различий в ОФВ 1 на исходном уровне не показала никаких изменений в улучшении ОФВ 1 при использовании вдыхаемого HTS (p = 0,10). Затем мы проанализировали количество субъектов, которым не удалось достичь по крайней мере 90% своего наилучшего процента FEV 1 за 6 месяцев до госпитализации в конце госпитализации. Эта стратегия пытается минимизировать смешанные эффекты недельной вариабельности ОФВ 1 ,19. Четыре субъекта не отвечали на лечение, когда HTS не использовались, и двое, когда использовались HTS (p = 0.65). В целом, эти данные предполагают, что использование ингаляционных HTS во время госпитализации по поводу обострения заболевания легких при МВ не приводит к улучшению или ухудшению ОФВ 1 по сравнению со стандартом лечения в этой небольшой популяции.
Рисунок 1Объем форсированного выдоха за одну секунду (FEV 1 ). Прием (2005 год), в котором не использовался гипертонический раствор (-), сравнивался с госпитализацией (год 2006 или 2007), в которой использовался гипертонический раствор (+). (A) Переход от приема к выписке FEV 1 .Единицы — это изменение общего процента от прогнозируемого. Показано среднее значение ± 95% ДИ. Процент прогнозируемого ОФВ 1 при поступлении (B) или выписке (C). Единицы — процент от прогнозируемого. Строки объединяют данные обоих посещений по одной и той же теме. п = 18. * p≤0,05; NS, p> 0,05.
HTS не увеличивает прибавку в весе во время госпитализации по поводу обострения CF
По нашему опыту, пациенты, госпитализированные по поводу обострения CF болезни легких, набирают вес во время визита, вероятно, в результате повышенного потребления калорий и / или контроля воспалительного процесса. состояние в легких в результате инфекции.На рисунке 2 показано, что добавление вдыхаемых HTS не было связано с улучшением или ухудшением набора веса во время госпитализации. Среднее увеличение веса составило 3,4% (95% ДИ от 0,44% до 6,3%), когда HTS не использовалось, и 1,5% (95% ДИ от -1,3% до 4,3%), когда использовалось HTS (p = 0,24, 95% ДИ от -1,4 до 5.0).
Рис. 2Изменение веса по сравнению с исходным. Прием (2005 год), в котором не использовался гипертонический раствор (-), сравнивался с госпитализацией (год 2006 или 2007), в которой использовался гипертонический раствор (+). Единицы — это процентное изменение веса от поступления до выписки.п = 18. Данные = среднее значение ± 95% ДИ. NS, p> 0,05.
HTS не увеличивает время до следующей госпитализации после острого обострения CF
Поскольку ингаляционные HTS использовались во время госпитализации, но не в амбулаторных условиях в нашей клинической практике в течение этого периода исследования и в 2008 году, мы смогли изучить эффект своевременного поступления в стационар по поводу легочного обострения. Среднее время до следующей госпитализации составило 247 дней, когда HTS не применяли (95% ДИ от 154 до 340 дней), и 176 дней, когда использовался HTS (95% ДИ от 98 до 253 дней).На рис. 3 показано, что HTS было связано с уменьшением времени до следующего госпитализации, но это снижение не является статистически значимым (p = 0,08, 95% ДИ от –9,8 до 152,7). Невозможность увеличения времени до следующей госпитализации, вероятно, связана с краткосрочным использованием HTS в этом исследовании.
Рисунок 3Время до следующего приема. Прием (2005 год), в котором не использовался гипертонический раствор (-), сравнивался с госпитализацией (год 2006 или 2007), в которой использовался гипертонический раствор (+). Единицы измерения — количество дней между выпиской и следующей госпитализацией с диагнозом обострения муковисцидоза легких.п = 18. Данные = среднее значение ± 95% ДИ. NS, p> 0,05.
Выводы
В этом ретроспективном пилотном исследовании субъектов, госпитализированных по поводу обострения заболевания легких с МВ, использование ингаляционных HTS не было связано с дополнительным преимуществом по сравнению со стандартным лечением, которое включает внутривенное введение антибиотиков, улучшенные пищевые добавки и терапию очистки дыхательных путей. Два недавно опубликованных исследования показали, что вдыхание HTS улучшает результаты у пациентов с МВ, предположительно, за счет гидратации жидкости с поверхности дыхательных путей и улучшения выведения секрета из дыхательных путей.HTS может улучшить функцию легких и клиренс слизи у пациентов со стабильным заболеванием легких, вызывающим МВ, даже при использовании в течение короткого времени (2 недели) .13 20 В большом многоцентровом рандомизированном контролируемом исследовании стабильных субъектов с МВ дважды в день вдыхали 7% HTS Было показано, что более 48 недель снижает частоту обострений по сравнению с изотоническим физиологическим раствором.15 Снижение частоты обострений также наблюдается на более поздних стадиях заболевания.21 Единственное исследование использования HTS в стационаре, насколько нам известно, — это исследование госпитализированных младенцев с вирусный бронхиолит, при котором небулайзерная 3% HTS хорошо переносилась и значительно сокращала продолжительность пребывания в стационаре.22 В другом недавнем исследовании было обнаружено, что 7% HTS безопасны и хорошо переносятся младенцами с CF.17
Пациентам, поступившим с обострением заболевания легких, были предложены ингаляционные HTS в качестве дополнения к традиционной терапии в нашем учреждении (и других -словесное общение). Решение об использовании ингаляционных HTS основано на предположении, что польза от них перевешивает риск нежелательных явлений (которые были минимальными в большинстве исследований), а также на низкой стоимости и простоте введения этого агента.10–12 14 15 23–26 Однако вдыхаемый HTS может вызвать кашель20–12 14 20 23 24 26 у людей и использовался для провоцирования сужения бронхов.25 27 В предыдущих исследованиях ингаляционных HTS для CF, кашель и одышка были причинами для прекращения использования и исключения из исследования. 14 20 23 24 Усиление воспаления дыхательных путей может сделать госпитализированных пациентов особенно восприимчивыми к HTS-индуцированному бронхоспазму. Одной из основных целей этого исследования было изучение переносимости HTS в этой группе высокого риска. Мы не наблюдали увеличения частоты бронхоспазма или ухудшения физиологии обструкции при использовании HTS.
Недавний анализ факторов риска, связанных с невозможностью восстановления спирометрического исходного уровня (не менее 90% наилучшего ОФВ 1 за 6 месяцев до обострения) после внутривенного лечения антибиотиками, показал, что примерно 25% субъектов не выздороветь по крайней мере через 3 месяца после эпизода.19 В нашем исследовании четыре из 18 субъектов не смогли восстановиться до спирометрического исходного уровня при выписке, когда HTS не использовались, тогда как двое из 16 не смогли этого сделать, когда использовались HTS. Этот анализ также не может продемонстрировать значительную пользу использования HTS во время обострения CF, хотя данные обоих исследований нельзя напрямую сравнивать, поскольку анализируются популяции пациентов с различными характеристиками.
Почему мы не смогли обнаружить каких-либо улучшений в тестах функции легких или прибавки в весе у этой группы стационарных пациентов с МВ? В отличие от предыдущих исследований, 13-15 эта группа субъектов не имеет стабильного заболевания легких.У пациента с обострением, который уже получает максимальное лечение, включая внутривенное введение антибиотиков, физиотерапию грудной клетки и рчДНазу, дополнительная польза от HTS может быть тривиальной из-за эффекта потолка. Тот факт, что ОФВ 1 при поступлении во время визита, во время которого использовалась ВТШ, в целом был выше, в то время как ОФВ при выписке 1 был аналогичным в обоих посещениях, также подтверждает возможный эффект потолка, при котором возможно только определенное улучшение, даже с максимальной терапией.
Ограничения этого исследования включают ретроспективный характер сбора данных из одного учреждения и недоступность подробных профилей соответствия и побочных эффектов. Из-за присущего ему ретроспективного характера это исследование не является рандомизированным и не использует анализ намерения лечить. Хотя мы исследовали несколько переменных, таких как ОФВ -1 , микробиология мокроты и сопутствующие вмешательства, между двумя периодами госпитализации могут быть другие неизмеряемые отклонения, которые могли ослабить или замаскировать эффект лечения.Анализ наблюдаемой мощности показывает, что размер нашей выборки и распределение данных позволяют нам обнаружить разницу не менее 3,6% ОФВ 1 (первичный результат) между ОФВ при поступлении и выписке 1 с мощностью 80% (18 пар, стандартное отклонение между группами 5.44). Эти данные будут полезны для адекватного анализа мощности до будущих исследований. Размер выборки слишком мал для проведения анализа подгрупп на основе таких факторов, как исходный ОФВ 1 и возраст. Для вторичного результата увеличения веса (14 пар, стандартное отклонение между группами по 5.65), размер нашей выборки позволяет выявить разницу в прибавке в весе между госпитализированными на 4,23 кг. В случае времени до следующей госпитализации (18 пар, стандартное отклонение между группами 163,44), что было более вариабельным исходом, размер нашей выборки позволяет обнаружить изменение на 107 дней или более. Отсутствие увеличения веса от использования HTS во время госпитализации может быть результатом недостаточного времени последующего наблюдения, хотя долгосрочное исследование также не продемонстрировало положительных результатов15.
Это исследование также подчеркивает важную клиническую дилемму в лечении пациентов с МВ. .За последнее десятилетие, по крайней мере, пять новых агентов показали преимущества по сравнению с плацебо.28 Эти ценные плацебо-контролируемые рандомизированные контрольные испытания новых методов лечения, однако, не анализируют синергизм или взаимодействие с другими методами лечения. В реальных приложениях клиницист должен применять «новую» терапию в сочетании со стандартными методами лечения (например, методами очистки дыхательных путей) и другими относительно новыми методами лечения (например, рчДНаза). Такие вопросы, как «Как клиницисту следует расставить приоритеты для этих методов лечения?» И «Есть ли важные взаимодействия между этими методами лечения?» Были подняты теми, кто пишет согласованные документы для практики МВ.29 Результаты настоящего исследования демонстрируют важность решения этих вопросов в хорошо спланированных клинических испытаниях, поскольку результаты «неконтролируемых» комбинаций в клинической практике непредсказуемы. Недавно зарегистрированное проспективное рандомизированное контролируемое исследование (ANZCTR # ACTRN12605000780651) может дать более четкие ответы относительно роли вдыхаемых HTS во время госпитализации при обострениях заболевания легких при МВ.
В заключение, в этом исследовании использование ингаляционных HTS во время госпитализации по поводу обострения МВ не было связано с улучшением ОФВ 1 , дополнительным увеличением веса или увеличением времени до следующего госпитализации по сравнению со стандартным лечением в этом ретроспективном исследовании.Вопрос о том, следует ли клиницистам предлагать или отказываться от этого лечения пациентам, госпитализированным по поводу обострения МВ, потребует хорошо контролируемых исследований комбинированного терапевтического типа, демонстрирующих дополнительную эффективность без дополнительной нагрузки. По мере того, как ожидаются новые методы лечения, исследовательское сообщество CF все чаще сталкивается с дилеммой о том, как сочетать / определять приоритеты нескольких эффективных методов лечения.
Благодарности
Авторы благодарят докторов Джозефа Забнера и Майкла Уэлша за содержательное обсуждение, доктора Бриджит Циммерман за руководство нашим статистическим анализом и Дженис Лаунспак и Ребекку Бик за отличную помощь.
Эффект 3% и 6% физиологического раствора при вирусном бронхиолите: рандомизированное контролируемое исследование
Реферат
Бронхиолит — распространенное заболевание у маленьких детей, которое часто требует госпитализации. За исключением возможного эффекта распыленного гипертонического раствора (хлорида натрия), нет доказательной терапии. В этом исследовании изучалась эффективность распыленного 3% и 6% гипертонического раствора по сравнению с 0,9% гипертоническим раствором у детей, госпитализированных с вирусным бронхиолитом.
В этом многоцентровом двойном слепом рандомизированном контролируемом исследовании дети, госпитализированные с острым вирусным бронхиолитом, были рандомизированы для получения 3%, 6% гипертонического раствора или 0,9% физиологического раствора в виде небулайзера в течение всего пребывания в больнице. Сальбутамол был добавлен для предотвращения возможного сужения бронхов. Первичной конечной точкой была продолжительность пребывания в больнице. Вторичными исходами были потребность в дополнительном кислороде и зондовом питании.
Из 292 детей, включенных в исследование (средний возраст 3.4 месяца), 247 завершили исследование. Средняя продолжительность пребывания в стационаре не различалась между группами: 69 часов (межквартильный размах 57), 70 часов (IQR 69) и 53 часа (IQR 52) для 3% (n = 84) и 6% (n = 83). ) гипертонический раствор и 0,9% (n = 80) физиологический раствор соответственно (p = 0,29). Потребность в дополнительном кислороде или питании через зонд существенно не различалась. Побочные эффекты были одинаковыми в трех группах.
Распыление гипертоническим раствором (3% или 6% хлорида натрия), хотя и безопасно, не уменьшало продолжительность пребывания в больнице, продолжительность дополнительного кислорода или зондового питания у детей, госпитализированных с вирусным бронхиолитом средней и тяжелой степени тяжести.
Аннотация
Распыление гипертоническим солевым раствором не уменьшило продолжительность госпитализации детей с вирусным бронхиолитом http://ow.ly/xRVVx
Введение
Острый вирусный бронхиолит — вирусная инфекция нижних дыхательных путей у младенцев [1, 2]. Обычные вирусы, вызывающие бронхиолит, включают респираторно-синцитиальный вирус (РСВ), метапневмовирус человека, аденовирус, вирус (пара) гриппа, риновирус и коронавирус [3]. Бронхиолит является основной причиной госпитализации младенцев в течение первого года жизни и поражает миллионы младенцев во всем мире [4].Ежегодные затраты на госпитализацию по поводу бронхиолита только в США составляют более 500 миллионов долларов [5]. До сих пор было показано, что потенциально терапевтические вмешательства, такие как распыленные кортикостероиды, адреналин, бета-агонисты, антибиотики и рекомбинантная дезоксирибонуклеаза человека, неэффективны [6–10]. Таким образом, лечение бронхиолита остается поддерживающим с добавлением кислорода, поддержанием баланса жидкости и механической вентиляции, если это необходимо [11].
Отек дыхательных путей и закупорка слизью являются преобладающими патологическими признаками у младенцев с острым вирусным бронхиолитом [12].Распыленный гипертонический раствор (HS) с использованием хлорида натрия может иметь положительный эффект при бронхиолите, так как он может уменьшать отек подслизистой оболочки, уменьшать медиаторы воспаления и вязкость слизи, а также улучшать клиренс слизистых оболочек [13–16]. In vitro , HS улучшает реологические свойства слизи (эластичность и вязкость) и ускоряет скорость транспорта слизи [17]. Исследования последнего десятилетия показали, что легкая небулайзерная терапия HS сокращает продолжительность пребывания в больнице младенцев с легким и умеренно тяжелым бронхиолитом [4, 18–25].Все эти исследования, кроме одного, включали небольшое количество пациентов из отдельных центров и использовали плохо определенные результаты; исследовательские группы были неоднородными, а некоторые не были четко определены [4, 26–28]. Исследования на пациентах с муковисцидозом показали, что распыленный HS в концентрации 5–7% более эффективен, чем изотонический раствор, и этот эффект оказался дозозависимым [29–34]. У младенцев в возрасте 4 месяцев и старше с муковисцидозом было доказано, что HS безопасен [35]. Поэтому мы провели рандомизированное контролируемое исследование различных концентраций распыленного HS у младенцев, госпитализированных по поводу вирусного бронхиолита.Мы предположили, что распыление HS в зависимости от дозы сократит продолжительность пребывания в больнице и продолжительность поддерживающей терапии.
Методы и материалы
Настройка
Это двойное слепое рандомизированное контролируемое исследование проводилось в 11 больницах общего профиля и одном медицинском центре третичного уровня в Нидерландах. Исследование было одобрено центральным комитетом по медицинской этике Нидерландов (Голландский регистр испытаний, номер: NTR 1494) и местными комитетами по этике всех участвующих больниц.Перед началом исследования от имени каждого ребенка по крайней мере один законный опекун подписал форму информированного согласия.
Пациенты
Дети в возрасте 0–24 месяцев соответствовали критериям участия в исследовании, если они были госпитализированы в одну из участвующих больниц из-за легкого или тяжелого вирусного бронхиолита и имели балл Ванга ≥3 на момент обращения. Шкала клинической тяжести Wang состоит из четырех пунктов: частота дыхания, хрипы, втягивания и общее состояние (таблица 1) [36]. Диагноз «бронхиолит» ставился клинически по симптомам инфекции верхних дыхательных путей с хрипом, тахипноэ и одышкой [11].Чтобы снизить вероятность включения детей с атопическим хрипом, все дети получали однократную ингаляцию 2,5 мг сальбутамола перед включением в исследование. Дети были исключены, если оценка Ванга улучшилась как минимум на 2 балла после ингаляции. Другими критериями исключения были гемодинамически важные врожденные пороки сердца, хронические предсуществующие заболевания легких, Т-клеточный иммунодефицит, лечение кортикостероидами и предшествующие хрипы, (пищевая) аллергия или экзема.
Таблица 1- Система оценки клинической тяжести инфекций нижних дыхательных путей у младенцев по шкале ВангаИсследуемое лекарство
Исследуемый препарат для всех центров был подготовлен международно сертифицированным фармацевтом-исследователем (Sterop Pharmacobel, Брюссель, Бельгия).Для предотвращения возможной бронхиальной обструкции к каждой дозе добавляли 2,5 мг сальбутамола. Концентрации физиологического раствора рассчитывались таким образом, чтобы концентрация окончательного раствора с сальбутамолом составляла 0,9%, 3% или 6% хлорида натрия, а общий объем составлял 4 мл на ингаляцию.
Все участники, лица, осуществляющие уход, и медицинский персонал не знали о составе исследуемых растворов, которые были идентичны по упаковке флаконов, цвету, запаху и другим физическим характеристикам. Флаконы использовались до 24 часов после открытия.Срок годности всех флаконов — 31 декабря 2011 года. Код был сдан на хранение фармацевту.
Дизайн исследования
Пациенты были набраны в период с ноября 2009 г. по май 2011 г., во время сезона бронхиолитов. При поступлении регистрировался клинический анамнез пациента, который включал продолжительность симптомов до госпитализации, прием лекарств, а также анамнез пациента и его семейную историю атопии. Мазок из носоглотки был взят для анализа на вирус. Если ребенок соответствовал критериям включения и было получено согласие родителей, распыление исследуемого препарата начиналось в течение 12 часов после поступления.
Все отобранные пациенты были случайным образом распределены в одну из двух групп вмешательства или в контрольную группу. Рандомизация проводилась по центрам и группировалась в блоки по шесть пациентов. Каждый пациент получил последовательно рандомизированное количество, которое соответствовало идентичным пузырькам на 20 мл, которые содержали разные растворы хлорида натрия. Группы вмешательства получали ингаляции с 3% или 6% HS, а контрольная группа получала ингаляции с 0,9% хлоридом натрия (физиологический раствор (NS)).
Растворы распыляли каждые 8 ч при постоянном потоке кислорода 6–8 л · мин. –1 из настенной розетки в сочетании с небулайзером HOT Top Plus (Intersurgical, Уден, Нидерланды), масс-медианный аэродинамический диаметр ( MMAD) 4 мкм, от до , плотно прилегающую лицевую маску, и вводили до опорожнения. Распыление продолжали до выписки.
Всех детей обследовали дважды в день, основываясь на физикальном осмотре, шкале Ванга, частоте сердечных сокращений, сатурации, частоте дыхания, потребности в дополнительном кислороде и питании через зонд.Обследование проводил дежурный педиатр. Перед началом исследования весь медицинский персонал, участвовавший в исследовании, был обучен тому, как оценивать пациентов и классифицировать систему оценки клинической тяжести Ванга, чтобы улучшить согласие между наблюдателями.
Согласно заранее определенным критериям, дополнительное кислородное питание начиналось у младенцев с насыщением воздуха в помещении 93% или ниже в течение> 10 минут или острым раскислением <85%. Это было остановлено, когда насыщение постоянно составляло> 93%.Показанием для начала и прекращения кормления через зонд было минимальное потребление, рассчитанное как 75% от нормального. Потеря жидкости из-за обезвоживания или диареи компенсировалась добавлением потерянной жидкости к минимальному потреблению. Дополнительные лекарства и другая поддерживающая терапия были предоставлены в соответствии с рекомендациями больницы.
Все дополнительные лекарства, время и количество дополнительного кислорода и зондового питания регистрировались в карточке случая, как и частота сердечных сокращений, сатурация кислорода, температура и побочные эффекты.Побочные реакции определялись как любые наблюдаемые нежелательные эффекты, независимо от того, были ли они связаны с исследуемым лекарством или нет. Возможные известные побочные эффекты ингаляции с HS включали ринорею, беспокойство, кашель и бронхиальную обструкцию [4, 34, 37].
Первичным результатом была продолжительность пребывания в больнице, которую рассчитывали как количество часов между первой дозой исследуемого лекарства и клиническим решением о выписке. Таким образом, на первичную конечную точку не повлияло дополнительное пребывание в больнице из-за социальных или административных факторов.По словам ответственного педиатра, критерии выписки, определенные протоколом, включали отсутствие необходимости в дополнительном кислороде, питании через зонд или внутривенном введении жидкости. Вторичными исходами были переводы в педиатрическое отделение интенсивной терапии (PICU) из-за дыхательной недостаточности, необходимости и продолжительности дополнительного кислорода или зондового питания. Безопасность лечения оценивалась путем регистрации нежелательных явлений.
Статистические методы
Предыдущие исследования показали уменьшение продолжительности пребывания в больнице с 4 до 3 дней после вдыхания 3% HS [18].Основываясь на этом сокращении пребывания в больнице на 25%, для текущего исследования потребовался размер выборки из 65 пациентов в каждой экспериментальной группе, чтобы достичь мощности 90% при значении p <0,05. Все данные были анонимно записаны, введены в электронную таблицу Excel (Microsoft Corp, Редмонд, Вашингтон) и импортированы в программное обеспечение SPSS версии 19.0 (SPSS Inc, Чикаго, Иллинойс) для анализа. Анализы проводились в соответствии с принципами назначения лечения и протокола. Различия между включенными и исключенными пациентами в отношении характеристик пациентов оценивались с помощью независимого t-критерия (возраст) и критерия хи-квадрат (пол и вмешательство).Все непрерывные переменные (продолжительность пребывания в больнице, часы дополнительного кислорода и зондового питания) были проверены на нормальность. В случае нормального распределения различия между тремя группами были проверены с помощью ANOVA, а в случае ненормального распределения использовался тест Крускала-Уоллиса. Для категориальных переменных различия в распределении между группами вмешательства были проверены с помощью критерия хи-квадрат. Одномерные различия во времени до выписки из больницы между группами вмешательства были проверены с помощью лог-рангового теста.
Результаты
В период с ноября 2009 г. по май 2011 г. в исследование были включены и рандомизированы 292 ранее здоровых ребенка с вирусным бронхиолитом средней и тяжелой степени тяжести (рис. 1). До включения в исследование большинство пациентов получали назальные деконгестанты: 21 — сальбутамол (спейсер), 10 — парацетамол, 4 — амоксициллин, 3 — омепразол, 3 — нистатин и 1 — вальпроевая кислота.
Фигура 1-Включение пациентов в исследование и процедуры последующего наблюдения и анализа.
Два пациента были выписаны из-за быстрого улучшения клинического состояния и поэтому были исключены из исследования до того, как была введена первая доза исследуемого лекарства. В общей сложности 290 младенцев (средний возраст 3,4 месяца, диапазон от 10 дней до 23 месяцев) были включены в исследование и проанализированы в анализе намерения лечиться. 43 (15%) пациента были исключены для анализа по протоколу, а 18 (6,2%) пациентов не завершили лечение из-за побочных эффектов. Из них девять пациентов ушли из-за кашля или возбуждения во время и после распыления, а девять других из-за клинического ухудшения, такого как повышенная потребность в кислороде, усилие дыхания или прогрессирующая обструкция дыхательных путей.Отзыв информированного согласия привел к исключению еще девяти (3,1%) пациентов. Тринадцать младенцев были исключены из исследования из-за отклонения от протокола. Трем пациентам (1,2%) потребовалась искусственная вентиляция легких в отделении интенсивной терапии интенсивной терапии в течение болезни: у одного пациента ухудшилось состояние через 5 часов после первой ингаляции с 6% HS; клиническое состояние одного пациента, рандомизированного в группу 6%, ухудшилось после 6 дней лечения и потребовалось госпитализации в реанимацию; и один пациент, получавший NS, имел дыхательную недостаточность при поступлении, и это клиническое состояние не изменилось после приема одной дозы исследуемого лекарства в ожидании перевода в PICU (рис.1). Количество отказов (по причинам) существенно не различалось между группами вмешательства (p = 0,47).
Всего 247 младенцев завершили исследование и были проанализированы в соответствии с протоколом анализа; 84 получили 3% HS, 83 получили 6% HS и 80 получили NS (рис. 1). Исходные характеристики пациентов существенно не различались между тремя группами (таблица 2). Результаты анализа намерения лечиться и анализа по протоколу не различались по исходным характеристикам или по каким-либо первичным или вторичным исходам (данные не показаны).Помимо исследуемого препарата, пациенты получали: назальные деконгестанты n = 161, парацетамол n = 30, антибиотики n = 11, сальбутамол n = 6, ибупрофен n = 1, нистатин n = 1 и ранитидин n = 1. Применение назальных деконгестантов (ксилометазолина и хлорида натрия) было равномерно распределено среди исследуемых групп (данные не показаны).
Таблица 2- Исходные характеристики зарегистрированных младенцевСредняя продолжительность пребывания в больнице составила 69 часов в группе 3% HS, 70 часов в группе 6% HS и 53 часа в группе NS (p = 0.29) (таблица 3). Различия во времени до выписки между тремя группами не были статистически значимыми (p = 0,26) (рис. 2).
Фигура 2-Процент младенцев, оставшихся в больнице, отображается в зависимости от времени до выписки в соответствии с вмешательством.
Таблица 3– Первичные и вторичные исходы для трех групп вмешательстваДополнительный кислород потребовался 50 (59,5%) младенцам в группе 3% HS, 53 (63,9%) младенцам в группе 6% HS и 51 (63,8%) младенцам в группе 0.9% группа NS (p = 0,70) со средней продолжительностью 54, 54 и 40 часов соответственно (p = 0,14).
Дополнительное зондовое питание потребовалось 29 (34,5%) младенцам в группе 3% HS, 31 (37,3%) младенцам в группе 6% HS и 22 (27,5%) младенцам в группе 0,9% NS (p = 0,39) , со средней продолжительностью 62, 52 и 54 часа соответственно (p = 0,87) (таблица 3).
Средний балл по Вангу при выписке составлял 2,0 в группе NS и в группе 3% HS и 1,0 в группе 6% HS (p = 0,53). Оценка Ванга при выписке улучшилась независимо от схемы лечения (таблицы 3 и 4) без существенных различий между группами (p = 0.80).
Таблица 4– Средний балл по Вангу через 24, 48 и 72 часа для трех групп вмешательстваЗначительное количество побочных эффектов было отмечено во всех группах лечения (таблица 5). За исключением кашля, который достоверно чаще возникал в группах HS (p = 0,03), различий между группами не обнаружено. Исключения из-за побочных эффектов не различались между группами (p = 0,59). Большинство нежелательных явлений, вероятно, были связаны с основным вирусным бронхиолитом.
Таблица 5– Нежелательные явления, зарегистрированные у зарегистрированных младенцевОбсуждение
В этом двойном слепом рандомизированном многоцентровом исследовании мы сравнили 3% и 6% HS с NS у детей, госпитализированных с вирусным бронхиолитом.Ни 3% HS, ни 6% HS не уменьшили продолжительность пребывания в больнице, оценку тяжести клинической картины Ванга при выписке, продолжительность дополнительного кислорода или зондового питания по сравнению с NS. Эти результаты контрастируют с результатами, опубликованными в литературе [18–22]. Объединенные результаты трех небольших исследований [18–20] продемонстрировали сокращение продолжительности госпитализации на 0,9 дня в пользу группы 3% HS по сравнению с группой NS, тогда как Луо и его коллеги [21, 22] обнаружили сокращение на 0,9 дня. 1.4 и 1,6 дня, соответственно, в своих исследованиях при бронхиолите от легкой до умеренной и от умеренного до тяжелого. Однако Аль-Ансари et al. [24] сравнил распыление 3% HS и 5% HS с NS при относительно легком бронхиолите у младенцев, находящихся в отделении для краткосрочного пребывания, и не показал влияния на продолжительность пребывания в больнице, которую он описал как подверженную медицинским и медицинским воздействиям. социальные факторы.
Хотя критерии диагностики вирусного бронхиолита были менее четко определены в большинстве этих исследований, за исключением исследования Kuzik et al .[20], различия в исследуемых популяциях между нашим исследованием и предыдущими исследованиями вряд ли могут объяснить различия между различными результатами. Наша исследуемая популяция была сопоставима по возрасту, клинической тяжести, продолжительности заболевания до госпитализации и с преобладанием RSV-положительных младенцев. В дополнение к критерию исключения предшествующих хрипов, атопических проявлений, таких как экзема или пищевая аллергия, мы старались избегать включения младенцев, которым может помочь сальбутамол. Действительно, недавнее исследование показало, что у детей с бронхиолитом оценка Ванга значительно улучшилась у детей с атопией, чем у детей без атопии, когда к лекарству был добавлен сальбутамол [23], что поддерживает наш подход.Принимая во внимание возможные случаи быстрого ответа на однократную дозу сальбутамола [12], можно утверждать, что наш протокол исследования привел к исключению лиц, ответивших на быстрый ответ, что, возможно, повлияло на результаты. В целом 14% всех детей, прошедших скрининг на включение, пришлось исключить из-за положительной реакции на сальбутамол. Однако, даже если бы этих младенцев включили и случайным образом распределили в исследуемые группы, их количество было бы слишком мало, чтобы существенно повлиять на результаты.
Метаанализ показал обратную зависимость между тяжестью заболевания и эффектом распыленного HS [4].Следовательно, различия в степени тяжести бронхиолита между исследуемыми популяциями могут объяснить разные результаты. Однако, похоже, что это не так, поскольку на начальном этапе оценка Ванга в нашем исследовании составляла 6,2 по сравнению с 5,8 в исследовании, на которое приходится половина веса метаанализа [21], в то время как другие исследования метаанализа в анализ были включены пациенты с более высокими оценками Ванга [18–20]. Наше исследование не было разработано для изучения подгрупп с разной степенью тяжести заболевания, и дальнейшие исследования должны выяснить, может ли HS быть особенно полезным в подгруппах младенцев с более тяжелым заболеванием.
Мы не можем исключить, что различия в типах небулайзеров и частоте небулайзеров сыграли свою роль. Мы использовали один и тот же небулайзер с MMAD 4 мкм для всех исследуемых пациентов, что привело к отложению в основном в нижних дыхательных путях [38]. Потенциально может влиять небулайзер с меньшим MMAD и другим отложением в легких [39]. Тип небулайзера и MMAD не были описаны в других исследованиях, поэтому дальнейшее сравнение невозможно. Только в двух предыдущих исследованиях участвовали участники, которым применяли небулайзер чаще, чем в нашем исследовании [20, 22].Однако не было никаких кинетических данных о периоде полураспада эффекта HS, и частое распыление не рекомендуется [20]. Следовательно, маловероятно, что различия в типах и частоте распыления могут объяснить наши выводы.
Большинство ранее опубликованных исследований были одноцентровыми исследованиями. Возможно, на результаты повлияли такие различия, как местные привычки в диагностике и лечении. Настоящее исследование представляет собой многоцентровое исследование, которое, возможно, могло бы уменьшить эти факторы.Для каждого центра была проведена рандомизация, что позволило провести анализ для каждого центра; но мы не обнаружили существенных различий между центрами.
Сильные стороны нашего исследования заключаются в использовании строгих критериев включения и выписки. Мы использовали строгое, клинически значимое определение времени выписки, на которое не влияли социальные или административные факторы [24]. Следовательно, мы ограничили продолжительность пребывания в больнице временем пребывания в больнице по медицинским показаниям. Это может объяснить нашу относительно короткую продолжительность пребывания в больнице (53, 69 и 70 часов для NS, 3% HS и 6% HS соответственно) по сравнению с 2.6–6,0 дней для 3% HS и 3,0–7,4 дня для NS в предыдущих исследованиях [18–22]. Ни в одном из этих исследований не учитывались потенциально влияющие социальные и административные факторы; в большинстве исследований использовались только клинические решения врачей.
Возможное объяснение того, почему это исследование не обнаружило разницы между группами вмешательства и контрольной группой, может заключаться в том, что NS не может быть истинным плацебо. Однако дизайн нашего исследования не может исключить положительный эффект ингаляции NS у младенцев с вирусным бронхиолитом.На этот вопрос можно было бы ответить с помощью исследования не меньшей эффективности, сравнивающего NS и HS. Физиологически адекватное количество жидкости, выстилающей дыхательные пути, имеет решающее значение для нормального функционирования мукоцилиарного клиренса дыхательных путей. Известно, что бронхиолит приводит к истощению содержания воды в жидкости слизистой оболочки дыхательных путей, вызывая уменьшение мукоцилиарного клиренса [12]. In vivo , изменение жидкости на поверхности дыхательных путей и улучшение клиренса слизи после ингаляции NS или HS, вероятно, является прямым эффектом общей массы хлорида натрия, добавленного к поверхности дыхательных путей [13].У пациентов с амбулаторным бронхиолитом распыление с большим объемом NS было так же эффективно, как и с более низким объемом 3% HS [40]. Пока это не показано для более тяжелых заболеваний. Более ранние исследования, которые показали положительный эффект 3% HS, также проводили распыление три раза в день, что дало такую же общую дозу [18, 19, 21]. Следовательно, хотя более высокая доза общего хлорида натрия может иметь влияние, это вряд ли объяснит разные результаты исследования. Наши результаты были подтверждены недавним исследованием, в котором сравнивали NS с 7% HS и использовали частоту ингаляций четыре раза в день, которое не показало положительного эффекта HS даже при более высокой общей дозе хлорида натрия [41].Ipek et al. [23] сравнивали действие распыленных NS и HS с сальбутамолом и без него у амбулаторных пациентов с легким бронхиолитом. Все исследуемые группы показали значительное снижение клинической степени тяжести без различий между группами, что позволяет предположить, что NS может иметь некоторый терапевтический эффект также у пациентов, не страдающих атопией. Это подтверждает наши выводы о том, что не было обнаружено значительных различий между использованием HS и NS у пациентов с бронхиолитом.
Хотя в текущем исследовании серьезных побочных эффектов не наблюдалось, у значительного числа детей наблюдались побочные эффекты (таблица 5), которые в значительной степени могли быть связаны с самим бронхиолитом.У 6,2% всех включенных пациентов причиной отмены были побочные эффекты. Более того, кашель был более распространенным в обеих группах HS. Это требует дальнейшего внимания, поскольку предыдущие исследования не включали точного описания побочных эффектов.
В заключение, мы показали, что распыление 3% HS или 6% HS не уменьшало продолжительность пребывания в больнице, оценку тяжести клинической картины Ванга при выписке, потребность в дополнительном кислороде или потребность в питании через зонд у детей в возрасте до 2 лет. госпитализированных с вирусным бронхиолитом, по сравнению с применением НС.Наши результаты не подтверждают рутинное использование HS у младенцев с бронхиолитом.
Благодарности
Авторы хотели бы поблагодарить следующих участников исследования: Нико Ольденхоф (Медицинский центр VieCuri, Венло, Нидерланды) за процедуру рандомизации; Грета Велдхейс (Медицинский центр Виекури, Венло, Нидерланды) за координацию работы сотрудников аптеки; Барт Роттьер (Университетский медицинский центр, Гронинген, Нидерланды) за промежуточный анализ; Тван Малдер (Университетский медицинский центр, Маастрихт, Нидерланды) и Бриджит ван дер Брюгген-Богартс (Медицинский центр VieCuri, Венло, Нидерланды), которые были независимыми врачами для пациентов с вопросами; Йохану де Йонгсте (Университетский медицинский центр, Роттердам, Нидерланды) за критический обзор рукописи; и Loes Janssen (Центр VieCuri, Венло, Нидерланды) для контроля статистических расчетов.
Участвовавшие центры: Медицинский центр VieCuri, Венло; Медицинский центр Маастрихтского университета, Маастрихт; Медицинский центр Орбис, Ситтард; Больница Катарины, Эйндховен; Медицинский центр Максима, Велдховен; Больница Лаврентия, Рурмонд; Больница Элькерлик, Хелмонд; Госпиталь Рейнстейт, Арнем; Больница Маасстад, Роттердам; Больница Амфия, Бреда; Госпиталь Тви Стеден, Тилбург; и больница Святой Елизаветы, Тилбург, Нидерланды.
Сноски
Редакционные комментарии см. На стр. 827.
Клиническое испытание: Испытание зарегистрировано в Голландском реестре испытаний, номер NTR1494, и в Реестре клинических испытаний ЕС, EudraCT, номер 2008-003886-17.
Заявление о поддержке: Финансовая поддержка исследования была предоставлена за счет образовательных грантов от Schering Plough BV (Маарссен, Нидерланды), Nutricia (Зутермейер, Нидерланды) и Фонда Кристины Бадер из детской больницы Ирэн (Арнем, Нидерланды) .
Конфликт интересов: раскрытие информации можно найти вместе с онлайн-версией этой статьи на сайте www.

 Интервал между ингаляциями не должен быть менее 4 часов.
Интервал между ингаляциями не должен быть менее 4 часов.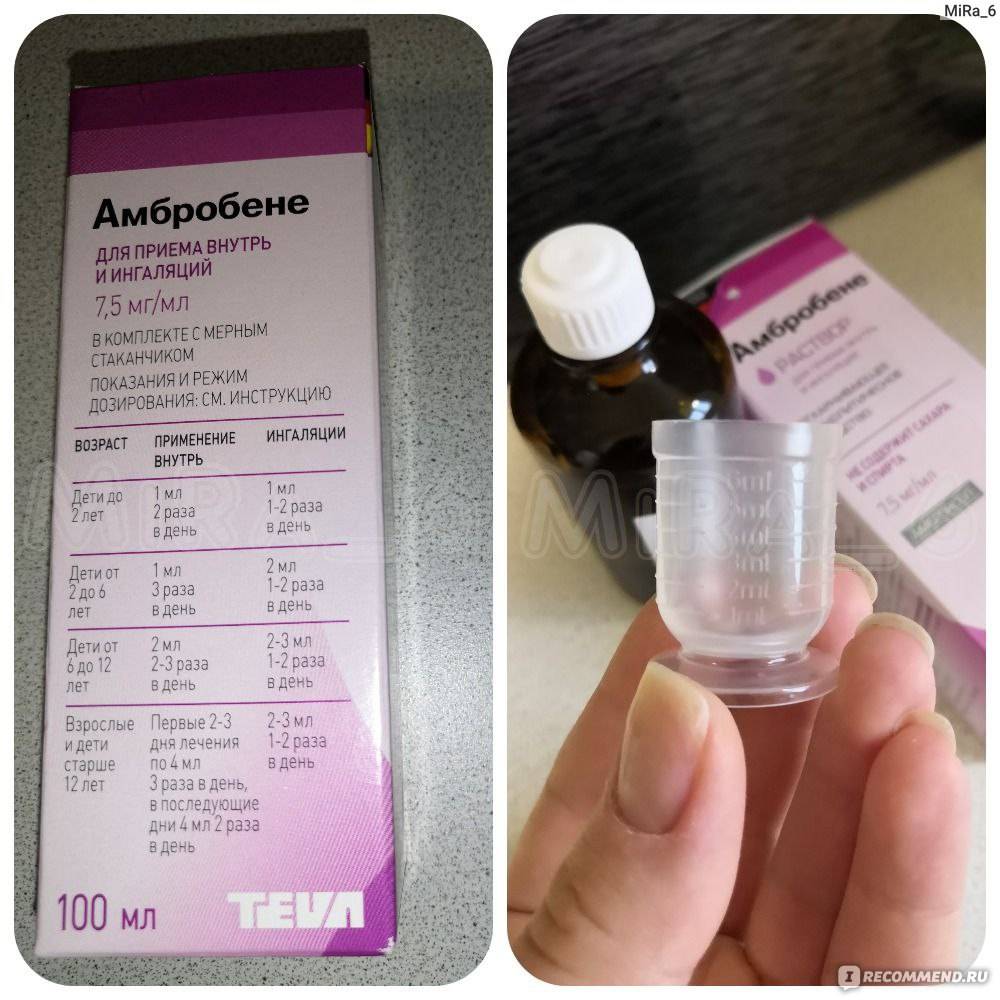

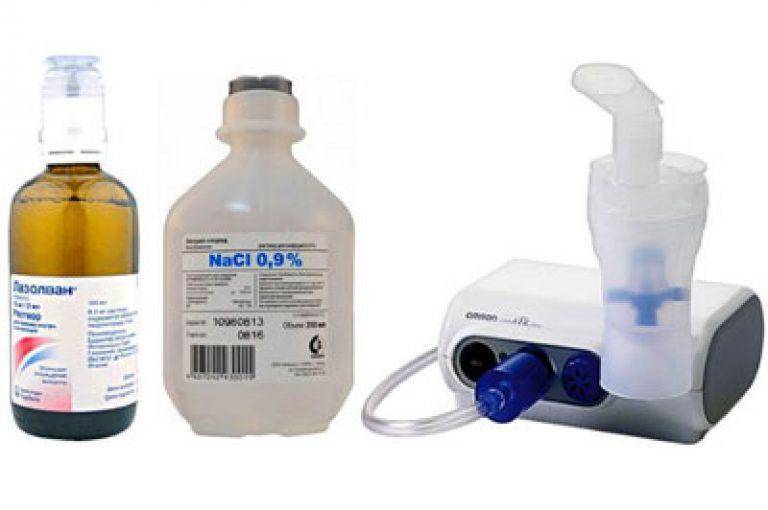 ). Применение препаратов амброксола способствует хорошему всасыванию антибиотиков.
). Применение препаратов амброксола способствует хорошему всасыванию антибиотиков.





 Использовать Пульмикорт, Декасан.
Использовать Пульмикорт, Декасан.

 Растительное средство, снимающее воспаление, отек. Обладает небольшим антибактериальным действием. Устраняет воспаление в носовых пазухах. Используют для детей от 2 лет. Его разводят соотношении 1 мл препарата на 2 мл физраствора. Применяют 2 раза в сутки. Для детей от 6 лет разведение 1:2, применяют 2 раза в сутки. Для взрослых разведение 1:1, применяется в 3 раз в сутки.
Растительное средство, снимающее воспаление, отек. Обладает небольшим антибактериальным действием. Устраняет воспаление в носовых пазухах. Используют для детей от 2 лет. Его разводят соотношении 1 мл препарата на 2 мл физраствора. Применяют 2 раза в сутки. Для детей от 6 лет разведение 1:2, применяют 2 раза в сутки. Для взрослых разведение 1:1, применяется в 3 раз в сутки.
 Как заправить ингалятор физраствором: жидкость помещается в контейнер и плотно закручивается крышкой, подсоединяются трубочки и маска.
Как заправить ингалятор физраствором: жидкость помещается в контейнер и плотно закручивается крышкой, подсоединяются трубочки и маска.
 Для получения необходимой жидкости 10 мл препарата разводят 50 мл физраствора. Для детей используют концентрацию 2 мл 2 раза в сутки, взрослым можно использовать 4мл 4 раз в сутки.
Для получения необходимой жидкости 10 мл препарата разводят 50 мл физраствора. Для детей используют концентрацию 2 мл 2 раза в сутки, взрослым можно использовать 4мл 4 раз в сутки.