Гемофильность – / . / (, ) / —
Гемофильность. Новые соединения [Цифровые космополиты в коммуникативную эпоху]
Гемофильность
В начале 1950-х годов социолог Роберт Мертон начал всестороннее исследование дружбы в двух жилых микрорайонах – в Нью-Джерси и западной Пенсильвании. Мертон и его коллеги просили жителей этих районов назвать трех ближайших друзей, а на основе полученных данных делали обобщенные выводы об общественных силах, влияющих на формирование дружеских отношений. Обнаружив, что близкая дружба чаще всего возникает между однополыми людьми одной этнической группы, Мертон предложил термин, обозначающий тенденцию, обнаруженную тысячелетиями ранее Аристотелем, который в «Никомаховой этике» пишет: «Одни полагают дружбу каким-то сходством и похожих людей – друзьями, отсюда и поговорки: “Рыбак рыбака…” и “Ворон к ворону…” и тому подобные».[117]
Чтобы описать это явление, Мертон ввел новый термин «гемофильность» – любовь к похожим на тебя. Редкость дружбы между чернокожими и белыми жителями не стала для Мертона сюрпризом, хотя для своего исследования он специально выбрал районы с расово разнообразным населением. А вот обнаружение признаков гемофильности, когда речь заходила об убеждениях и ценностях, произвело больший эффект: люди схожих взглядов относительно совместного проживания представителей разных рас в одном районе чаще становились друзьями, нежели люди, чьи представления на этот счет расходились.
С тех пор как Мертон ввел этот термин в обиход, социологи наблюдают признаки гемофильности при изучении социальных связей от таких тесных, как брак, до куда более свободных, как обмен профессиональными сведениями между коллегами или совместное посещение публичных пространств. Исследователи фиксируют гемофильность по этническим, половым, возрастным, религиозным, образовательным, профессиональным и социальным признакам. Это явление настолько распространено в нашей жизни, что авторы исследования,[118] обобщающего десятки работ по социологии, характеризуют гемофильность как «базовый организующий принцип» человеческих сообществ и групп.
Выясняется, что мы причисляем себя к определенной категории – как правило, бессознательно – по самым поверхностным признакам. В недавно опубликованной работе канадского исследователя Шина Маккиннона показывается, что студенты чаще садятся на лекциях или в компьютерном классе рядом с людьми, похожими на них по параметрам роста, цвета кожи и наличия/отсутствия очков. Когда Маккиннон спрашивал их о причинах такого поведения, студенты объясняли свой выбор сугубо субъективным восприятием: они полагали, что скорее найдут понимание у похожих на них студентов и у них будет больше шансов подружиться.[119]
Размышления о влиянии гемофильности на наше поведение способны вызвать чувство неловкости. Психолог в сфере образования и президент Университета Беверли Тэйтум назвал свою книгу о развитии расовой идентичности «Почему все чернокожие ребята сидят в столовой вместе?» В заголовке обозначилось это чувство неловкости при виде самоизоляции. (В своей книге Тэйтум утверждает, что такого рода самоизоляция нужна студентам, чтобы обрести уверенность в рамках своей расовой идентификации, что в конечном счете ведет к созданию тесных межрасовых связей.) Обычная реакция человека, ознакомившегося с социологическим исследованием в области гемофильности, – провести проверку друзей и найти среди них примеры, которые доказывают обратное и подтверждают, что мы менее зависимы от влияния гемофильности, чем среднестатистические представители человеческого рода. Мы, как правило, видим себя людьми открытыми и непредвзятыми и испытываем беспокойство, сталкиваясь с доказательствами обратного.
Было бы ошибкой экстраполировать результаты исследований гемофильности и делать вывод, что «все мы чуточку расисты», как поется в одном из номеров замечательного современного мюзикла «Avenue Q» Роберта Лопеса и Джеффа Маркса. Если вы растете в расово однородном районе, то и расовое разнообразие ваших возможных друзей будет ограниченно. Социологи называют это «базовая гемофильность». Люди заводят друзей, взаимодействуя в рамках общих занятий. Если вы играете в хоккей, вы, скорее всего, познакомитесь со многими белыми парнями с севера. Займитесь крикетом, и ваш круг общения заметно изменится. Исследуя сетевую активность, мы видим схожие результаты.
Для исследования расовой гемофильности в сети и в реальном мире социологи Андреас Виммер и Кевин Льюис использовали крупный массив данных Facebook – все посты студентов одного потока ведущего университета за целый год. Акцент делался на фотографиях, которыми делились студенты. Люди, отмеченные на совместных фотографиях, чаще оказывались «реальными» друзьями, чем те, кто просто «зафрендился» на Facebook, что является настолько рутинной практикой в большинстве университетов, что даже не предполагает реальных отношений. Виммер и Льюис разглядели значительные признаки гемофильности и смогли изучить это явление на куда более тонком уровне, нежели предшествующие исследователи. Они пришли к выводу, что определенные типы гемофильности – к примеру, склонность азиатов заводить дружбу друг с другом – являются обобщениями, выведенными на основе более специфических типов гемофильности – склонности индийских или китайских студентов заводить дружбу между собой. Кроме того, они обнаружили отчетливые признаки не этнической гемофильности, включая сильную предрасположенность к установлению дружеских отношений между студентами из штата Иллинойс, студентами-математиками и бывшими однокашниками из частных школ.[120]
Этот вывод предполагает, что структурные факторы: с кем вы учились в старших классах, с кем ходили в компьютерную лабораторию, – являются не менее важным источником гемофильности, нежели личный выбор. Наиболее важное явление, обнаруженное Виммером и Льюисом – это эффект «замыкания», описанный еще социологом Георгом Зиммелем в первой половине прошлого века.[121] Если Джим дружит с Бобом и Сью, велика вероятность, что Боб и Сью тоже подружатся, замкнув таким образом дружеский круг. Если Джим африканец, вероятность, что Боб и Сью тоже африканцы, выше. И друзей африканцев он завел не столько потому, что ему с ними комфортно, сколько в результате этого явления – социального замыкания. Замыкание приводит и к усилению прочих эффектов гемофильности, а исследование Виммера и Льюиса показывает, что весьма скорым и вероятным результатом становится как раз то, что все черные ребята сидят за одним столом. (Авторы уточняют, что если присмотреться внимательнее, то, скорее всего, мы увидим, что нигерийцы сидят с нигерийцами, а афроамериканцы из Атланты с другими ребятами из южных штатов.[122])
Иными словами, если вы обнаружили, что ваш круг общения весьма однороден – в этническом, гендерном и территориальном планах, это вовсе не обязательно означает, что вы расист, сексист или националист. Скорее всего, ваш дружеский круг сформировался под влиянием того, где вы жили, в какую ходили школу и какие у вас интересы. И хотя это, возможно, не станет новостью для тех, чей Facebook больше похож на семейное сборище, чем на заседание Организации Объединенных Наций, для университетов, чья образовательная роль, в частности, состоит в подготовке студентов к мультикультурному миру, это ситуация, требующая разрешения.
Наличие глубоких структурных факторов, объясняющих существование гемофильности, не означает, что сама гемофильность вообще неизбежна. Среди важнейших факторов, повышающих вероятность дружеских отношений, Виммер и Льюис отмечают соседство по комнате в общежитии. Университет, в котором они проводили исследования, по-видимому, внедряет политику, призванную повысить расовую интеграцию: белых студентов там редко селят с другими белыми. Виммер и Льюис приходят к безоговорочному выводу: если эта политика направлена на повышение количества дружеских связей поверх расовых барьеров, то успех ее очевиден.
Гемофильность – это напоминание, что наш взгляд на мир имеет локальный, неполный и неизбежно тенденциозный характер. Наши представления о далеких странах и наш интерес к происходящим там историям зависят от людей, которых мы знаем и любим, а таких людей, конечно, больше среди наших соотечественников, чем среди жителей других континентов.
Так же как уверенность, что Европа неумолимо скатывается к жизни по законам шариата, затрудняет продуктивный разговор о миграционной реформе, представление о том, что мы обладаем более широкой картиной мира, нежели в действительности, приводит к бесполезным искажениям и заблуждениям. Нам может казаться, что мы вполне готовы к деловым отношениям с нашими новыми японскими клиентами, но, вероятнее всего, наш космополитизм имеет воображаемый характер. Нужно отдавать себе отчет в том, читаем ли мы Times of India, или воображаем, что читаем, потому лишь, что обладаем такой возможностью. Нам нужно обращать меньше внимания на возможности интернета – и больше на реализацию этих возможностей.
Проведенное Виммером и Льюисом исследование гемофильности в конечном счете дает определенную надежду. Когда университетские администрации поняли, что студенты только выиграют от дружеских отношений поверх расовых барьеров, они нашли структурное и действенное решение: селить вместе студентов разных рас. Если мы хотим изменить корпус сведений, которые мы получаем о мире, и от воображаемого космополитизма перейти к цифровому – нам тоже нужны структурные изменения. Но сперва нам нужно подробнее рассмотреть то, как мы воспринимаем мир через СМИ.
Поделитесь на страничкеpublic.wikireading.ru
Haemophilus influenzae (гемофилюс инфлюэнца): что это, патогенность, лечение
Haemophilus influenzae (гемофилюс инфлюэнца, гемофильная палочка) является возбудителем острого воспалительного процесса в организме человека, при котором в тканях нервной и дыхательной систем образуются гнойные очаги – абсцессы. Клиническая картина патологии во многом схожа с признаками банальной простуды, а микроб имеет большое количество разновидностей. Эти особенности затрудняют диагностику инфекции и делают ее опасной в эпидемическом отношении. Медицине известны лишь самые тяжелые случаи заболевания.
Haemophilus influenzae обитает в верхних дыхательных путях здоровых людей. В обычном состоянии она не причиняет вреда здоровью. При ослаблении иммунитета эти безобидные микроорганизмы активизируются и становятся причиной целого ряда неприятностей.
Гемофильная палочка имеет несколько равнозначных наименований: палочка Пфайффера, палочка Афанасьева—Пфайффера. Haemophilus influenzae, палочка инфлюэнцы. Первым гемофильные бактерии обнаружил Кох. Свое наименование микроб получил благодаря открытию двух ученых — Афанасьева и Пфайффер. Они независимо друг от друга выделили Haemophilus influenzae из легочной ткани человека, умершего во время пандемии гриппа. В настоящее время ученые-медики продолжают изучать свойства и особенности бактерии, поскольку она является частой причиной гнойного менингита у маленьких детей.
Патология поражает преимущественно малышей от 6 месяцев до 5 лет. У них повышается температура тела, появляется насморк, боль и першение в горле, кашель, сильная головная боль. Болезнь развивается обычно в осенне-зимнее время и ранней весной, когда иммунная система организма ослаблена и не может в полном объеме выполнять свои защитные функции. Диагностика заключается в проведении физикального осмотра и лабораторных испытаний. Лечение гемофильной инфекции консервативное, этиотропное, противомикробное.
Заболевания, обусловленные Haemophilus influenzae, обычно имеют благоприятный прогноз и не угрожают жизни больных. При своевременном и правильном лечении неврологические осложнения развиваются лишь в 30% случаев. Процент летальности также невысок – 5%. Благодаря активной иммунизации населения заболеваемость составляет 25 случаев на 100.000 человек. В настоящее лечение инфекции приобретает характер общемедицинской проблемы, что связано с возрастанием устойчивости гемофильной палочки к большинству антибиотиков.
Этиология
Haemophilus influenzae — небольшая полиморфная коккобацилла, которая может существовать в 2 формах: бескапсульной и капсульной. В первом случае клетка состоит из желеобразной цитоплазмы, окруженной мягкой липидной мембраной. Такие микробы не являются болезнетворными и входят в состав нормальной микрофлоры носоглотки здоровых людей. Капсула, покрывающая бактерию поверх мягкой липидной мембраны, состоит из углеводов и белков, является прочной и защищает микроб от воздействия иммунокомпетентных клеток.
Капсула – один из факторов патогенности Haemophilus influenzae, обеспечивающий ее проникновение в эпителиоциты слизистой оболочки, лимфу и кровь. Она подавляет фагоцитарную активность лейкоцитов. Пили обеспечивают фиксацию возбудителя на клетках реснитчатого эпителия. К дополнительным факторам патогенности относятся IgA-протеазы, расщепляющие секреторные иммуноглобулины. Ферменты, продуцируемые микроорганизмом, разрушают защитные антитела слизистой оболочки, что также способствует адгезии, инвазии и развитию инфекционного процесса. При разрушении бактериальной капсулы в кровь выделяется мощный токсин — причина шока и смерти больных.
Эти аспорогенная палочковидные бактерии неподвижны. Они окрашиваются по Грамму в красный цвет и в мазке располагаются одиночно, парами или скоплениями.
В настоящее время микробиологи выделяют более пятнадцати разновидностей Haemophilus influenzae. Подразделяют их на семь биотипов по культуральных свойствам и шесть капсульных типов по антигенным свойствам.
Haemophilus influenzae – факультативный анаэроб. Она растет на питательных средах, в состав которых входит свежая кровь. Для роста и размножения бациллы требуются факторы, содержащиеся в эритроцитах: термолабильный Y и термостабильный X. Имеет бактерия К и О антигены.
Палочка инфлюэнцы неустойчива во внешней среде, чувствительна к большинству антибиотиков основных групп и к самым распространенным дезинфектантам. Она погибает при кипячении, под воздействием солнечных лучей, радиации и при высыхании.
Эпидемиология
Гемофильная инфекция — антропоноз. Она обитает только в организме человека, преимущественно на слизистой оболочке респираторного тракта. В 90% микробы выделяются из носоглотки здоровых людей. В норме у детей и взрослых количество Haemophilus influenzae не должно превышать 104 степени колониеобразующих единиц. Эти бактерии наряду со стафилококками являются частью нормальной микрофлоры человека.
Здоровое носительство обычно длится несколько месяцев и часто сохраняется даже при применении высоких доз антибиотиков. Симптоматика патологии полностью отсутствует. Бактерионоситель чувствует себя абсолютно здоровым, но при этом является опасным в эпидемическом отношении.
Распространение инфекции осуществляется аэрозольным механизмом, который реализуется воздушно-капельным путем. Возбудитель попадает во внешнюю среду во время сильного кашля, чихания, разговора вместе с отделяемым респираторного тракта. Риск заражения максимален у лиц, находящихся в радиусе трех и менее метров от больного человека. Дети заражаются от взрослых носителей в первые годы жизни. Передача возбудителя контактно-бытовым путем случается крайне редко из-за его низкой устойчивости в окружающей среде. Возможно заражение через полотенце, игрушки, посуду и иные предметы быта, обсемененные бактериями.
Группу риска по гемофильной инфекции составляют:
- Больные агаммаглобулинемией,
- Лица, перенесшие спленэктомию,
- Пациенты, принимающие цитостатики,
- Дети первых лет жизни,
- Малыши на искусственном вскармливании,
- Недоношенные дети,
- Работники дошкольных учреждений,
- Пожилые люди,
- Онкологические больные,
- Дети, проживающие в детских домах,
- Лица с врожденным или приобретенным иммунодефицитом,
- Дети, посещающие ясли и детские сады,
- Представители неевропейских рас.
Этому контингенту опасно контактировать с больными гемофильной инфекцией. Наиболее уязвимы дети от 6 до 12 месяцев. В это время перестает иммунная система поддерживаться антителами матери и начинает самостоятельно функционировать. Гемофильная инфекция у младенцев ввиду их несовершенного иммунитета нередко оканчивается генерализацией процесса с последующей комой и смертью.
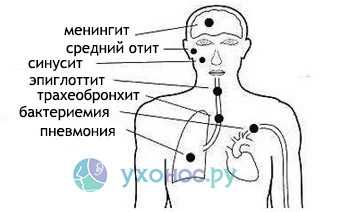
заболевания, которые может вызвать H. Influenzae
Бактерия H. Influenzae — причина различных инфекционных форм. Она поражает оболочки головного мозга, легочную ткань, носоглотку, кровь, подкожно-жировую клетчатку, кости. У детей гемофильная инфекция обычно протекает в форме менингита, эпиглоттита, целлюлита. У взрослых и пожилых людей чаще встречается пневмония. Кроме того, выделяют следующие заболевания, гемофильной этиологии: гнойный артрит, септицемию, отит, остеомиелит, синусит, перикардит, плеврит, сепсис. Нередко Haemophilus influenzae становится причиной внутрибольничной инфекции у людей, находящихся на стационарном лечении.
После перенесенной инфекции формируется стойкий иммунитет, который предотвращает повторные случаи инфицирования во взрослом состоянии.
Патогенез
Входные ворота инфекции – слизистая оболочка носоглотки. Для патологии характерна длительная персистенция возбудителя в области ворот инфекции. Это латентная стадия заболевания. При снижении общей резистентности организма она переходит в манифестную. Увеличение общей микробной массы и присоединение вирусной инфекции — условия, ускоряющие этот процесс. С такой локализацией возбудителя связаны эпиглоттит, отит, синусит.
Инфекция распространяется лимфогенным или гематогенным путем по окружающим тканям, обусловливая развитие бактериемии, септицемии и воспалительных процессов в бронхах, легких, жировой ткани. В тяжелых случаях происходит гематогенная диссеминация микробов с поражением суставов, костей и внутренних органов.
Haemophilus influenzae проникает в кровь и бессимптомно персистирует до тех пор, пока количество микробных клеток не достигнет своего максимума. Затем бацилла проникает через гематоэнцефалический барьер в ЦНС и вызывает развитие гнойного менингита.Факторы, способствующие развитию гемофильной инфекции:
- Курение,
- Алкоголизм и наркомания,
- Длительная антибиотикотерапия,
- Нервное перенапряжение и эмоциональные всплески,
- Гипо- или гипертермия,
- Плохие бытовые условия,
- Неблагополучная экологическая обстановка.
Симптоматика
Длительность инкубационного периода точно не определена. Считается, что она составляет 2-4 дня. Все это время больной является опасным для окружающих. На начальном этапе симптомы гемофильной инфекции схожи с простудными. Заболевание в большинстве случаев протекает как банальная ОРВИ. Но случается так, что инфекция становится причиной более серьезных заболеваний с конкретными проявлениями.

Клинические признаки патологии определяются локализацией патологического процесса. Интоксикационный и катаральный синдромы характерны для любой клинической формы инфекции. У больных повышается температура до 40 градусов, возникает озноб, цефалгия, ринит, дискомфорт в горле, влажный кашель, разбитость, вялость, урчание и боль в животе, нарушение стула, метеоризм, боль в мышцах и суставах.
- Если первичных очаг инфекции располагается в ухе, развивается отит. Пациенты жалуются на пульсирующую и стреляющую боль в ухе, снижение слуха, появление слизисто-гнойного отделяемого.
- При синусите появляется дискомфорт в носу, распирающая боль в проекции пораженной пазухи, гнойные выделения из носа, нарушение носового дыхания, снижение обоняния.
- Воспаление клетчатки проявляется отечностью лица, преимущественно щек, гиперемией или синюшностью кожи, болью и лихорадкой.
- Эпиглоттит — самая тяжелая форма гемофильной инфекции, характеризующаяся сильным ознобом, цианозом, одышкой, тахикардией, гиперсаливацией, стридором, втяжением податливых участков грудной клетки. Больные занимают вынужденное положение. Из-за боли нарушается глотание даже жидкой пищи. Быстро прогрессирующий круп может привести к гибели больного от асфиксии.
- Конъюнктивит у новорожденных проявляется покраснением глаз, отечностью век, обильным слезотечением, появлением гнойного секрета в уголках глза.
- При артрите поражаются крупные суставы верхних и нижних конечностей. Заболевание сопровождается покраснением кожи, отеком и местной гипертермией.
- Больные с воспалением легких жалуются на боль в груди, кашель с гнойной мокроты, лихорадку.
- Менингит проявляется обильной рвотой фонтаном без предшествующей тошноты, жаром, ознобом, потерей сознания, судорогами, менингеальными знаками, очаговыми неврологическими симптомами, заторможенностью, адинамией, быстрым истощением больных. Реже развивается сопор, в отдельных случаях — кома.
- При остеомиелите возникает сильная боль в конечности, отек тканей над пораженной костью и покраснение кожи.
- При септицемии — спленомегалия, гипотония, тахикардия, кровоизлияния на коже, отсутствие аппетита, нарушение стула. Больные много и беспокойно спят. Заболевание отличается бурным и даже молниеносным течением. Нередко оно заканчивается инфекционным шоком и смертью больного.
Haemophilus influenzae может вызывать одновременное поражение сразу нескольких органов: менингит у больных нередко сочетается с артритом, целлюлитом, эпиглоттитом.
Гемофильная инфекия – серьезная медицинская проблема, обусловленная многообразием клинических форм, частой генерализацией процесса, развитием тяжелых осложнений и высоким риском смертельного исхода.
Диагностика
Диагностикой и лечением гемофильной инфекции занимаются врачи-инфекционисты и педиатры. Они осматривают пациенты, выслушивают жалобы и изучают результаты лабораторно-инструментальных обследований. После сбора анамнеза и оценки состояния кожи врачи измеряют АД, температуру и пульс. Нередко требуется дополнительно консультация ЛОР-врача, гинеколога, хирурга, невролога, офтальмолога, пульмонолога.

Лабораторные исследования:
- Общий анализ крови и мочи – для определения признаков воспаления,
- ПЦР – для выявления ДНК возбудителя,
- Бакпосев мокроты, ликвора или отделяемого зева — для выделения возбудителя,
- Серологические пробы — для определения антител в крови,
- Иммунодиагностика – обнаружение капсульного антигена гемофильной палочки с помощью ИФА.
Инструментальные мероприятия проводятся с целью подтверждения предполагаемого диагноза и выявления имеющихся осложнений. Наиболее распространенными и информативными являются: УЗИ, рентгенография, КТ и МРТ.
Микробиологическое исследование клинического материала — основной диагностический метод, позволяющий выделить палочку от больного. В баклабораторию для анализа доставляют отделяемое верхних дыхательных путей, гной из уха, мокроту, спинномозговую жидкость, суставную жидкость, кровь. Биоматериал изучают под микроскопом и засевают на питательные среды. Для посева используют шоколадный агар с факторами роста. После выделения чистой культуры и идентификации возбудителя ставят тест на антибиотикорезистентность.
Лечение
Больных с тяжелыми и среднетяжелыми формами инфекции госпитализируют в стационар на весь лихорадочный период. Специалисты рекомендуют соблюдать постельный режим, отказаться от соленой пищи, пить не менее 2 литров воды в день.
Медикаментозное лечение гемофильной инфекции:
- Этиотропная терапия – антибиотики широкого спектра действия из группы цефалоспоринов «Цефтриаксон», «Цефтазидим», макролидов «Эритромицин», «Азитромицин», пенициллинов «Амоксиклав», «Аугментин», фторхинолонов «Ципрофлоксацин», «Офлоксацин».
- Дезинтоксикационная и дегидратационная терапия — диуретики «Фуросемид», «Гипотиазид», противовоспалительные препараты «Дексаметазон», «Преднизолон», солевые растворы.
- Симптоматическая терапия – антипиретики «Нурофен», «Парацетамол»; отхаркивающие препараты «Амброксол», «АЦЦ»; иммуномодуляторы «Ликопид», «Имунорикс»; десенсибилизирующие средства «Зодак», «Зиртек»; витаминно-минеральные комплексы.
Курс лечения составляет в среднем десять дней, но может варьироваться в зависимости от формы болезни и устойчивости возбудителя.
Прогноз при гемофильной инфекции неоднозначный. Своевременное выявление возбудителя и адекватная терапия позволяют добиться быстрого и полного выздоровления. При развитии тяжелых осложнений прогноз становится серьезным, часто неблагоприятным.
Осложнения заболеваний, вызванных haemophilus influenzae:
- Стойкая тугоухость,
- Гидроцефально-гипертензивный синдром,
- Септический шок,
- Слепота,
- Удушье,
- Отек головного мозга,
- Психические нарушения,
- Эмпиема,
- Пороки новорожденного,
- Самопроизвольный выкидыш у беременных,
- Смерть.
Профилактика
В настоящее время разработана и внедрена в практику клиницистов специфическая профилактика гемофильной инфекции. Своевременная вакцинация – это оптимальное средство защиты от инфекций, вызванных данным возбудителем. Вакцина состоит из фрагментов бактериальной капсулы и не содержит живого возбудителя. Благодаря этому ее вводят детям и людям со сниженным иммунитетом.
 Существует несколько вакцин зарубежных и отечественных:
Существует несколько вакцин зарубежных и отечественных:
- «Акт-Хиб»,
- «Хиберикс»,
- «Пентаксим»,
- «Инфанрикс Гекса»,
- «Вакцина гемофильная типа b конъюгированная сухая».
Перечисленные выше вакцины прошли лицензирование. Против каждого типа Haemophilus influenzae используется конкретное наименование лекарства. Прививку ставят детям, не достигшим 5-летнего возраста, а также лицам из группы риска.
Неспецифическая профилактика заключается в укреплении иммунной системы. Экстренная профилактика проводится после контакта с больным человеком. Для этого врачи рекомендуют пропить курс антибиотиков.
Видео: правила вакцинации от гемофильной инфекции, доктор Комаровский
Мнения, советы и обсуждение:
uhonos.ru
причины, симптомы, диагностика и лечение
Гемофилия – наследственная патология системы гемостаза, в основе которой лежит снижение или нарушение синтеза VIII, IX или XI факторов свертывания крови. Специфическим проявлением гемофилии служит склонность больного к различным кровотечениям: гемартрозам, внутримышечным и забрюшинным гематомам, гематурии, желудочно-кишечным кровотечениям, длительным кровотечениям при операциях и травмах и др. В диагностике гемофилии первостепенное значение имеет генетическое консультирование, определение уровня активности факторов свертываемости, ДНК-исследование, анализ коагулограммы. Лечение гемофилии предполагает проведение заместительной терапии: трансфузии гемоконцентратов с факторами свертывания VIII или IX, свежезамороженной плазмы, антигемофильного глобулина и др.
Общие сведения
Гемофилия – заболевание из группы наследственных коагулопатий, обусловленное дефицитом факторов свертывания плазмы крови и характеризующееся повышенной склонностью к геморрагиям. Распространенность гемофилии А и В составляет 1 случай на 10000-50000 представителей мужского пола. Чаще всего дебют заболевания приходится на ранний детский возраст, поэтому гемофилия у ребенка является актуальной проблемой педиатрии и детской гематологии. Кроме гемофилии, у детей встречаются и другие наследственные геморрагические диатезы: геморрагическая телеангиэктазия, тромбоцитопатия, болезнь Гланцмана т. п.
Гемофилия
Причины гемофилии
Гены, обусловливающие развитие гемофилии, сцеплены с половой Х-хромосомой, поэтому заболевание наследуется по рецессивному признаку по женской линии. Наследственной гемофилией болеют практически исключительно лица мужского пола. Женщины являются проводниками (кондукторами, носителями) гена гемофилии, передающими заболевание части своих сыновей.
У здорового мужчины и женщины-кондуктора с одинаковой вероятностью могут родиться как больные, так и здоровые сыновья. От брака мужчины, больного гемофилией со здоровой женщиной рождаются здоровые сыновья или дочери-кондукторы. Описаны единичные случаи гемофилии у девочек, рожденных от матери-носителя и больного гемофилией отца.
Врожденная гемофилия встречается почти у 70 % пациентов. В этом случае наследуется форма и тяжесть гемофилии. Около 30% наблюдений приходится на спорадические формы гемофилии, связанные с мутацией в локусе, кодирующем синтез плазменных факторов свертывания крови на Х-хромосоме. В дальнейшем такая спонтанная форма гемофилии становится наследственной.
Свертываемость крови, или гемостаз, служит важнейшей защитной реакцией организма. Активизация системы гемостаза происходит в случае повреждения сосудов и начала кровотечения. Свертываемость крови обеспечивается тромбоцитами и особыми веществами – плазменными факторами. При дефиците того или иного фактора свертывания своевременный и адекватный гемостаз становится невозможным. При гемофилии в связи с дефицитом VIII, IX или других факторов нарушается первая фаза свертывания крови — образование тромбопластина. При этом увеличивается время свертывания крови; иногда кровотечение не останавливается в течение нескольких часов.
Классификация гемофилии
В зависимости от дефицита того или иного фактора свертываемости крови, различают гемофилию А (классическую), В (болезнь Кристмаса), С и др.
- Классическая гемофилия составляет подавляющее большинство (около 85%) случаев синдрома и связана с дефицитом VIII фактора свертывания (антигемофильного глобулина), приводящим к нарушению образование активной тромбокиназы.
- При гемофилии В, составляющей 13% случаев заболевания, имеет место недостаток IX фактора (плазменного компонента тромбопластина, фактора Кристмаса), также участвующего в образовании активной тромбокиназы в I фазе свертывания крови.
- Гемофилия С встречается с частотой 1-2% и обусловлена недостаточностью XI фактора свертывания крови (предшественника тромбопластина). На остальные разновидности гемофилии приходится менее 0,5% случаев; при этом может отмечаться дефицит различных плазменных факторов: V (парагемофилия), VII (гипопроконвертинемия), Х (болезнь Стюарта – Прауэр) и др.
Тяжесть клинического течения гемофилии зависит от степени недостаточности коагуляционной активности плазменных факторов свертывания крови.
- При гемофилии тяжелой степени уровень недостающего фактора составляет до 1%, что сопровождается развитием тяжелого геморрагического синдрома уже в раннем детском возрасте. У ребенка с тяжелой гемофилией возникают частые спонтанные и посттравматические кровоизлияния в мышцы, суставы, внутренние органы. Сразу после рождения ребенка могут обнаруживаться кефалогематомы, длительные кровотечения из пуповинного отростка, мелена; позднее — продолжительные кровотечения, связанные с прорезыванием и сменой молочных зубов.
- При среднетяжелой степени гемофилии у ребенка уровень плазменного фактора составляет 1-5%. Заболевание развивается в дошкольном возрасте; геморрагический синдром выражен умеренно, отмечаются кровоизлияния в мышцы и суставы, гематурия. Обострения случаются 2-3 раза в год.
- Легкая форма гемофилии характеризуется уровнем фактора выше 5%. Дебют заболевания возникает в школьном возрасте, часто в связи с травмами или операциями. Кровотечения более редкие и менее интенсивные.
Симптомы гемофилии
У новорожденных детей признаками гемофилии могут служить длительное кровотечение из культи пуповины, подкожные гематомы, кефалогематомы. Кровотечения у детей первого года жизни могут быть связаны с прорезыванием зубов, оперативными вмешательствами (инцизией уздечки языка, циркумцизио). Острые края молочных зубов могут стать причиной прикусывания языка, губ, щек и кровотечений из слизистых оболочек полости рта. Однако в грудном возрасте гемофилия дебютирует редко в связи с тем, что материнском молоке содержится достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений значительно возрастает, когда ребенок с гемофилией начинает вставать и ходить. Для детей после года характерны носовые кровотечения, подкожные и межмышечные гематомы, кровоизлияния в крупные суставы. Обострения геморрагического диатеза случаются после перенесенных инфекций (ОРВИ, ветрянки, краснухи, кори, гриппа и др.) вследствие нарушения проницаемости сосудов. В этом случае нередко возникают самопроизвольные диапедезные геморрагии. Ввиду постоянных и длительных кровотечений у детей с гемофилией имеется анемия различной степени выраженности.
По степени убывания частоты кровоизлияния при гемофилии распределяются следующим образом: гемартрозы (70—80%), гематомы (10-20%), гематурия (14-20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
Гемартрозы являются наиболее частым и специфическим проявлением гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией случаются в возрасте 1-8 лет после ушибов, травм или спонтанно. При гемартрозе выражен болевой синдром, отмечается увеличение сустава в объеме, гиперемия и гипертермия кожи над ним. Рецидивирующие гемартрозы приводят к развитию хронического синовита, деформирующего остеоартроза и контрактур. Деформирующий остеоартроз приводит к нарушению динамики опорно-двигательного аппарата в целом (искривлению позвоночника и таза, гипотрофии мышц, остеопорозу, вальгусной деформации стопы и др.) и к наступлению инвалидности уже в детском возрасте.
При гемофилии часто возникают кровоизлияния в мягкие ткани – подкожную клетчатку и мышцы. У детей обнаруживаются непроходящие синяки на туловище и конечностях, часто возникают глубокие межмышечные гематомы. Такие гематомы склонны к распространению, поскольку излившаяся кровь не сворачивается и, проникая вдоль фасций, инфильтрирует ткани. Обширные и напряженные гематомы могут сдавливать крупные артерии и периферические нервные стволы, вызывая интенсивные боли, паралич, атрофию мышц или гангрену.
Довольно часто при гемофилии возникают кровотечения из десен, носа, почек, органов ЖКТ. Кровотечение может быть инициировано любыми медицинскими манипуляциями (внутримышечной инъекцией, экстракцией зуба, тонзиллэктомией и др.). Крайне опасными для ребенка с гемофилией являются кровотечения из зева и носоглотки, поскольку могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг приводят к тяжелым поражениям ЦНС или летальному исходу.
Гематурия при гемофилии может возникать самопроизвольно или вследствие травм поясничной области. При этом отмечаются дизурические явления, при образовании кровяных сгустков в мочевыводящих путях — приступы почечной колики. У больных с гемофилией нередко обнаруживаются пиелоэктазия, гидронефроз, пиелонефрит.
Желудочно-кишечные кровотечения у пациентов с гемофилией могут быть связаны с приемом НПВС и др. лекарств, с обострением латентного течения язвенной болезни желудка и двенадцатиперстной кишки, эрозивным гастритом, геморроем. При кровоизлияниях в брыжейку и сальник развивается картина острого живота, требующая дифференциальной диагностики с острым аппендицитом, кишечной непроходимостью и др.
Характерным признаком гемофилии является отсроченный характер кровотечения, которое обычно развивается не сразу после травмы, а через некоторое время, иногда спустя 6-12 и более часов.
Диагностика гемофилии
Диагностика гемофилии проводится при участии ряда специалистов: неонатолога, педиатра, генетика, гематолога. При наличии у ребенка сопутствующей патологии или осложнений основного заболевания проводятся консультации детского гастроэнтеролога, детского травматолога-ортопеда, детского отоларинголога, детского невролога и др.
Супружеские пары, находящиеся в группе риска по рождению ребенка с гемофилией, должны пройти медико-генетическое консультирование еще на этапе планирования беременности. Выявить носительство дефектного гена позволяет анализ генеалогических данных и молекулярно-генетическое исследование. Возможно проведение пренатальной диагностики гемофилии с помощью биопсии хориона или амниоцентеза и исследования ДНК клеточного материала.
После рождения ребенка диагноз гемофилии подтверждается с помощью лабораторных исследований гемостаза. Основные изменения показателей коагулограммы при гемофилии представлены увеличением времени свертывания крови, АЧТВ, тромбинового времени, МНО, времени рекальцификации; уменьшением ПТИ и др. Решающее значение при диагностике формы гемофилии принадлежит определению снижения прокоагулянтной активности одного из факторов свертывания ниже 50%.
При гемартрозах ребенку с гемофилией проводится рентгенография суставов; при внутренних кровотечениях и забрюшинных гематомах – УЗИ брюшной полости и забрюшинного пространства; при гематурии – общий анализ мочи и УЗИ почек и т. д.
Лечение гемофилии
При гемофилии полное избавление от заболевания невозможно, поэтому основу лечения составляет заместительная гемостатическая терапия концентратами VIII и IX факторов свертывания крови. Необходимая доза концентрата определяется степенью выраженности гемофилии, тяжестью и видом кровотечения.
В лечении гемофилии выделяют два направления – профилактические и «по требованию», в период проявлений геморрагического синдрома. Профилактическое введение концентратов факторов свертывания крови показано пациентам с тяжелой формой гемофилии и проводится 2-3 раза в неделю для предупреждения развития гемофилической артропатии и прочих кровотечений. При развитии геморрагического синдрома требуются повторные трансфузии препарата. Дополнительно используются свежезамороженная плазма, эритромасса, гемостатики. Все инвазивные вмешательства у больных с гемофилией (наложение швов, удаление зубов, любые операции) проводятся под прикрытием гемостатической терапии.
При незначительных наружных кровотечениях (порезах, кровотечениях из полости носа и рта) может использоваться гемостатическая губка, наложение давящей повязки, обработка раны тромбином. При неосложненном кровоизлиянии ребенку необходим полный покой, холод, иммобилизация больного сустава гипсовой лонгетой, в дальнейшем – УВЧ, электрофорез, ЛФК, легкий массаж. Больным с гемофилией рекомендуется диета, обогащенная витаминами А, В, С, D, солями кальция и фосфора.
Прогноз и профилактика гемофилии
Длительная заместительная терапия приводит к изоиммунизации, образованию антител, блокирующих прокоагулянтную активность вводимых факторов, и неэффективности гемостатической терапии в обычных дозах. В таких случаях больному с гемофилией проводится плазмаферез, назначаются иммунодепрессанты. Поскольку больным с гемофилией проводится частое переливание компонентов крови, не исключается риск инфицирования ВИЧ-инфекцией, гепатитами В, С и D, герпесом, цитомегалией.
Легкая степень гемофилии не влияет на продолжительность жизни; при тяжелой гемофилии прогноз ухудшается при массивных кровотечениях, обусловленных операциями, травмами.
Профилактика предполагает проведение медико-генетического консультирования супружеских пар, имеющих отягощенный семейный анамнез по гемофилии. Дети, больные гемофилией, всегда должны иметь при себе специальный паспорт, где указан тип заболевания, группа крови и Rh-принадлежность. Им показан охранительный режим, профилактика травм; диспансерное наблюдение педиатра, гематолога, детского стоматолога и др. специалистов; наблюдение в условиях специализированного гемофильного центра.
www.krasotaimedicina.ru
1.3.2. Гемофильные бактерии
Впервые гемофильные бактерии были выделены Р. Кохом в начале 80-х годов XIX века из конъюнктивального экссудата. Позднее М.И. Афанасьев (1891 г.) и Р. Пфейффер (1892 г.) похожего возбудителя выделили из трупа больного, погибшего от гриппа; отсюда его длительное время считали причиной гриппа, что получило отражение в видовом названии.
Классификация
Гемофильные бактерии относятся к семейству Pasteurellaceae, роду Haemophilus. Кроме него в семейство входят роды Pasteurella и Aggregatibacter. Род Haemophilus включает около 20 видов, среди них есть сапрофиты и патогенные микроорганизмы.
Наибольшую роль в патологии играет H. influenzae, вызывающий воспалительные процессы в респираторном тракте, а также менингиты, бактериемию и другие инвазивные инфекции.
По свойствам с ним сходны H. parainfluenzae, H. haemolyticus and H. parahaemolyticus (последние 2 вида проявляют гемолитическую активность).
H. ducreyi является возбудителем мягкого шанкра – заболевания, передаваемого половым путем.
Родственные микроорганизмы вида Аggregatibacter aprophilus могут вызывать подострый эндокардит.
Морфология
Являются мелкими коккобактериями с выраженным полиморфизмом. Образуют капсулу, не имеют спор и жгутиков, по Граму окрашиваются отрицательно.
Культуральные свойства
Весьма прихотливы к питательным средам. Нуждаются в наличии факторов роста в среде.
Этими факторами являются факторы Х или V, которые содержатся в эритроцитах: Фактор V – термолабильный кофермент (НАД или НАДФ), содержится в дрожжах, в тканях растений и животных, участвует в энергетическом метаболизме; фактор Х – гемин, термостабилен, входит в состав железосодержащих пигментов. Гемофильные бактерии не способны к его синтезу.
Отсюда лучшими средами для культивирования являются кроличий или лошадиный кровяной агар и шоколадный агар. На этих средах чаще вырастают S- или М- (слизистые) формы колоний. Непатогенные, бескапсульные штаммы образуют R-формы колоний.
Оптимальная температура роста 370С. Длительность роста – 36-48 часов. На кровяном агаре с добавлением сердечно-мозгового экстракта через 24 часа появляется рост мелких колоний с радужными переливами, гемолиз отсутствует. У беcкапсульных вариантов радужная расцветка не выявляется. На жидких средах с кровью рост чаще диффузный, реже – придонный.
Биохимические свойства
Факультативные анаэробы. Метаболизм смешанный.
H. influenzae разлагает глюкозу, обладает каталазой, оксидазой, нуждается в X-, V-факторах.
Часть штаммов образует индол и разлагает мочевину, по этим признакам проводится биотипирование H. influenzae.
H.ducreyi не обладает сахаролитической активностью, нуждается в X-факторе, имеет каталазу и оксидазу.
Дифференциация гемофильных бактерий по биохимическим свойствам представлена в таблице.
Антигенная структура
О – соматический (ЛПС) и К – капсульный полисахаридный антиген; по К-антигену выделяют в реакции агглютинации или преципитации с монорецепторными сыворотками 6 серовариантов (a, b, c, d, e, f). Бескапсульные штаммы обозначаются как нетипируемые.
Белковый антиген М имеется у непатогенных штаммов.
Факторы патогенности
Основным фактором вирулентности является капсула.
Большинство инвазивных инфекций вызывается капсульными штаммами Н. influenzae типа b (Hib).
Капсула Hib состоит из полирибозилрибитолфосфата (ПРРФ), то есть содержит в качестве мономера пентозу (рибозу) в отличие от других типов, содержащих гексозу, что и определяет более высокую вирулентность. ПРРФ является Т-независимым АГ.
Бактерии имеют многочисленные адгезины в составе пилей.
Обладают IgА-протеазами, разрушающими секреторный IgА, что подавляет местный иммунитет слизистых.
ЛПС клеточной стенки является эндотоксином.
Возбудитель может продуцировать β-лактамазы, что обусловливает устойчивость к антибиотикам данной группы.
Резистентность
Патогенез и характеристика заболевания
Наибольшую роль в патологии человека играет H. influenzae, а также H. ducreyi – возбудитель мягкого шанкра. A. aphrophilus иногда способен вызывать подострый эндокардит.
Н. influenzae является патогеном исключительно человека (антропонозная инфекция). Гемофильные палочки, преимущественно нетипируемые их штаммы, часто входят в состав нормальной микрофлоры слизистых оболочек верхних дыхательных путей у здоровых взрослых и детей.
Однако на фоне сопутствующих заболеваний и при снижении местного иммунитета H. influenzae размножается на слизистых оболочках внутри- и внеклеточно, попадает в кровь. При этом через гематоэнцефалический барьер возбудитель может проникать в мозговые оболочки, что приводит к менингиту.
H. influenzae вызывают большое количество различных инфекций. В целом все инфекции, обусловленные гемофильной палочкой, можно подразделить на 2 типа: неинвазивные и инвазивные.
Неинвазивные инфекции связаны с распространением и колонизацией бактериями слизистой оболочки верхних дыхательных путей. При этом страдает мукоцилиарный клиренс.
Гемофилы могут вызывать острый синусит, острый средний отит и обострение хронического бронхита. Обычно эти заболевания являются осложнениями вирусных и других респираторных инфекций.
Инвазивные инфекции вызываются главным образом штаммами варианта Hib и связаны с гематогенным распространением возбудителей.
К ним относятся тяжелые заболевания – менингит, эпиглоттит (острое воспаление надгортанника), пневмония, бактериемия и сепсис.
Основные виды инфекций H. influenzae представлены в таблице
Источники инфекции – больной человек и носители, в носоглотке которых локализуется возбудитель.
Пути передачи – воздушно-капельный, в меньшей степени контактный.
В первую очередь инфекции, вызванные H. influenzae, поражают детей младшего возраста до 4-5 лет. Для них эти возбудители представляют наибольшую опасность.
Низкая частота развития инвазивных инфекций у детей первых двух месяцев жизни обусловлена наличием материнских антител. После этого срока уровень антигемофильных АТ падает, и ребенок становится восприимчивым к инфекции.
Защитный уровень АТ постепенно приобретается к 5-6 годам, что обусловливает снижение частоты и тяжести заболеваний.
Основным факторов вирулентности является полисахаридная капсула типа b, состоящая из полирибозилрибитолфосфата. Она защищает микроорганизм от фагоцитоза, опсонизации и комплемент-опосредованного лизиса. С ростом популяции людей, обладающих антителами к полирибозилрибитолфосфату, уменьшается и частота инвазивных инфекций.
Наиболее тяжелым заболеванием, вызванным H. influenzae, является гнойный менингит. Возбудитель проникает в клетки эпителия носоглотки, далее инвазирует субэпителиальные слои и попадает в кровь. При низком уровне АТ капсула обеспечивает выживание бактерий в крови, и они проникают в сосудистые сплетения головного мозга. Возбудитель активирует острое пиогенное воспаление в ЦНС. Эндотоксин стимулирует воспалительный процесс и поражает сосуды микроциркуляции с развитием тромбофлебитов. Это приводит к некрозу мозговой ткани.
Заболевание стремительно прогрессирует, и без лечения летальность может превысить 90%. После болезни у 10% детей остаются неврологические осложнения (глухота, гидроцефалия, ментальные расстройства).
Вариантом местной пиогенной инвазии является гемофильный эпиглоттит. Он представляет собой острое гнойное воспаление надгортанника с некрозом, что в тяжелых случаях приводит к смерти от асфиксии.
У рожениц и новорожденных может развиваться гемофильный сепсис. Наиболее частой причиной его являются нетипируемые штаммы возбудителя.
У взрослых гемофильная инфекция чаще всего возникает вторично как осложнение после вирусных или бактериальных респираторных инфекций. В составе микробных ассоциаций возбудитель вызывает пневмонию или обострение бронхита
Иммунитет
Иммунитет после заболевания стойкий, в основном гуморальный; естественный пассивный иммунитет от матери сохраняется до 2-3 месяцев.
Лабораторная диагностика
В связи с тем, что гемофильная палочка вызывает широкий спектр инфекций, для микробиологической диагностики может направляться различный клинический материал.
Наибольшую диагностическую значимость представляет исследование в норме стерильных биологических жидкостей: крови, плевральной, перикардиальной, синовиальной и спинномозговой жидкости (СМЖ).
Бактериоскопический метод носит ориентировочный характер, при окраске по Грамму выявляют грамотрицательные полиморфные бактерии, чаще с капсулой.
В качестве экспресс-методов выявляют антигены возбудителя в исследуемом материале.
Для быстрой диагностики инфекций, вызванных Н. influenzae типа b, используются серологические методы обнаружения капсульного антигена в СМЖ, крови, плевральной жидкости и моче: латекс-агглютинация, реакция коагглютинации со стафилококковым протеином А и иммуноферментный анализ.
Более простыми методами являются реакции латекс- и коагглютинации с образцами СМЖ. В настоящее время наиболее широко применяется иммуноферментный анализ.
Бактериологический метод.
При исследовании образца спинномозговой жидкости необходимо немедленно начать исследование или хранить материал в термостате при температуре 35-37°С (при невозможности – при комнатной температуре не более 30 мин). Образцы СМЖ не должны помещаться в холодильник. Длительной хранение образцов может привести к гибели бактерий и ложноотрицательным результатам (за исключением теста на определение антигенов).
Для обогащения материала проводят центрифугирование СМЖ. Проводят окрашивание осадка по Граму. Далее определяют антиген Hib в надосадочной жидкости.
Затем проводят бактериологическое исследование осадка. Выполняют посев нескольких капель осадка СМЖ на поверхность чашек с шоколадным и кровяным агаром. Чашки инкубируют при температуре 35-37°С в атмосфере с 5-10% СО2.
Другие биологические жидкости (синовиальная, перикардиальная, плевральная) также должны окрашиваться по Граму и исследоваться культурально.
Делают посев на среды с кровью, шоколадный агар. Идентификацию проводят по культуральным, биохимическим и антигенным свойствам с использованием специфических монорецепторных сывороток.
Параллельно проверяют потребность в X и V-факторах. Исследуемую культуру сеют сплошным газоном на плотную питательную среду. На посев накладывают два бумажных диска, смоченных, соответственно X и V-факторами. Если рост выявляется вокруг дисков, то подтверждают зависимость культуры от этих факторов.
Можно использовать тест сателлитных культур. На чашку с посевом культуры на кровяном агаре наносят в нескольких местах культуру S. aureus. При этом за счет выделяемого ими гемолизина вокруг колоний стафилококка наблюдается обильный рост исследуемой культуры. Аналогичные результаты можно получить при использовании диска с сапонином, который также лизирует эритроциты кровяного агара, высвобождая факторы X и V.
Лечение
Гемофильный менингит требует немедленного назначения антибиотикотерапии. С учетом вероятной устойчивости возбудителя к ампициллину препаратами выбора являются цефалоспорины III поколения. Также назначают хлорамфеникол, фторхинолоны.
При лечении эпиглоттита применяют цефалоспорины III поколения, возможно назначение ингибитор-защищенных β-лактамов (амоксициллин-клавулановая кислота). Данные антибиотики используют также при отитах и синуситах.
Специфическая профилактика
Для предотвращения тяжелых, угрожающих жизни инфекций, вызываемых штаммами варианта Hib, разработаны химические комбинированные вакцины, отличающиеся высокой эффективностью и безопасностью, в том числе у детей младше 18 мес.
Они представляют собой очищенный капсульный полисахарид Hib, конъюгированный с другими АГ (например, столбнячным анатоксином или вакциной АКДС), что обеспечивает необходимую иммуногенность.
В настоящее время конъюгированная Hib вакцина внесена в расширенный календарь прививок в Республике Беларусь. Детей прививают четырехкратно в 3, 4, 5 и 18 месяцев.
Неспецифическая профилактика – изоляция и лечение больных, дезинфекция в очагах.
Таблица
Дифференциально-диагностические свойства видов рода Haemophilus
Вид | Потребность | Каталаза | Оксидаза | β-галакто- зидаза | Гемолиз* | Глюкоза | Сахароза | Лактоза | Манноза | |
X и V факторах | СО2 | |||||||||
H.influenzae | X,V | + | + | + | — | — | + | — | — | — |
H. haemophilus | X,V | — | + | + | + | + | + | — | — | — |
H.parainfluenzae | V | — | + | + | + | — | + | + | — | + |
H.ducreyi | X | — | — | — | — | — | — | — | — | — |
А. aphrophilus | H | + | — | — | + | — | + | + | + | + |
13.3. Гарднереллы
Раньше их относили к роду Haemophilus, открыл их Гарднер и Дьюкс в 1955 г. Эти возбудители не нуждаются для своего роста и развития в факторах X и V как обычные гемофилы. Имеют свои отличительные признаки и другой путь передачи. В связи с этим их выделили в самостоятельный род.
Классификация
Род Gardnerella, вид Gardnerella vaginalis.
Морфология
Коккобактерии малых размеров (0,3-2 мкм). В мазках могут располагаться одиночно, попарно, параллельно друг другу и в виде «V». По Граму окрашиваются неодинаково. Есть и грамположительные и грамотрицательные варианты. Могут иметь суданофильные включения. При окраске по Нейссеру выявляют метахроматические гранулы. Не имеют спор, капсул, жгутиков. Являются кислотонеустойчивыми. По химической структуре имеют принципиальное отличие и от грамположительных, и от грамотрицательных бактерий (отсутствуют тейхоевая и диаминопимелиновая кислоты, нет гидроксилированных жирных кислот, характерных для грамположительных бактерий).
Культуральные свойства
Хемоорганотрофы. Прихотливы к питательным средам. Нуждаются для своего роста в наличии биотина, фолиевой кислоты, ниацина, тиамина, рибофлавина. Лучшей средой является агар с кровью человека или пептон-крахмал-глюкозный агар. На кровяном агаре есть зоны гемолиза вокруг колоний, а на пептон-крахмал-глюкозном агаре в результате гидролиза крахмала образуются зоны просветления. В жидких средах дают помутнение и осадок. По типу дыхания – факультативные анаэробы. Оптимальная температура роста 35-370С, но могут расти и при температуре от 250С до 420С, рН среды 4,0, желателен доступ СО2. Длительность роста 24-48 часов.
Биохимические свойства
Гарднереллы разлагают до кислоты глюкозу, мальтозу, рибозу, крахмал, инулин, непостоянно – лактозу, сахарозу. Не разлагают маннит, белки, не выделяют индол и сероводород. Восстанавливают нитраты, не образуют каталазу. Агглютинируют на холоду эритроциты человека и лошади.
Антигенная структура
Имеют групповые антигены, общие с Candida albicans, которые определяют в реакции агглютинации или ИФА, и типовые антигены, с учетом которых в реакции преципитации выделено 7 серогрупп.
Факторы патогенности
Бактериоцины, действующие на нормальную микрофлору; фермент сиалидаза, который разрушает гликопротеины слизистой оболочки влагалища и способствует проникновению возбудителя в ткани; выражен тропизм к эпителию за счет адгезинов.
Резистентность
Характеристика заболевания
Гарднереллы вызывают поражение урогенитального тракта в виде бактериального вагиноза, при котором резко уменьшается количество лактобактерий, т.е. изменяется экосистема влагалища, повышается рН среды, что способствует накоплению патогенных микроорганизмов.
Клинические проявления зависят от изменений экосистемы влагалища. Доминирующая флора рода Lactobacillus заменяется другой флорой – Gardnerella vaginalis. Развитию этого заболевания способствуют 2 группы факторов:
– эндогенные: изменение гормонального статуса, снижение иммунологической реактивности, нарушение микробного биоценоза кишечника;
– экзогенные: предшествующая длительная антибактериальная терапия, перенесенные ранее воспалительные заболевания мочеполовой системы, применение иммунодепрессантов и гормональных препаратов.
Источник инфекции – больной человек; путь передачи – половой.
Входные ворота – слизистые оболочки влагалища.
Патогенез
Вышеуказанные факторы вирулентности приводят к уменьшению или полному исчезновению физиологических лактобактерий, уменьшается количество молочной кислоты, повышается рН влагалищной среды, что благоприятствует накоплению другой флоры, в частности Gardnerella vaginalis, которая и вызывает различные клинические формы бактериального вагиноза – гарднереллеза, при котором появляется зуд, жжение, выделения с рыбным запахом за счет образования аномальных аминов. Это заболевание часто сопутствует кандидозному и трихомонадному вагиниту.
При гарднереллезе верхних половых путей возбудитель проникает в матку, трубы, яичники. Развиваются воспалительные поражения, которые могут распространяться даже на брюшину.
Может быть гарднереллез мочевых путей. При этом возникает геморрагический цистит, пиелонефрит.
Чаще гарднереллезом болеют женщины, если болеют мужчины, у них также поражается мочеполовая система.
Клиническая картина
Лабораторная диагностика
Бактериоскопический метод. Исследуют отделяемое или соскоб из пораженного участка. Окрашивают мазок по Граму и выявляют «ключевые» клетки. Это плоские эпителиальные клетки, к краям которых прикрепляются грамотрицательные и грамположительные бактерии. В мазках обнаруживается мало лейкоцитов. Проводят выявление аномальных аминов – продуктов симбиоза гарднерелл и влагалищных анаэробов. К капле выделений добавляют каплю 5-10% КОН – соли аномальных аминов превращаются в летучие основания со специфическим запахом рыбы (аминовый тест). Для выявления антигенов в исследуемом материале используют РИФ, ИФА или РИА, ПЦР для генодиагностики
Лечение
Пенициллин, линкомицин, метронидазол, клиндамицин, иммуностимуляторы, витамины, препараты для восстановления биоценоза влагалища: лактобактерин, бифидобактерин (их применяют местно).
Профилактика только неспецифическая.
studfile.net
16.2.3. Гемофильные бактерии (род Haemophilus)
Таксономическое положение. Бактерии рода Haemophilus относятся к семейству Pasteurellaceae.
В названии рода Haemophilus (от греч. haima — кровь, philos — любить) отражена зависимость этих бактерий от крови или ее производных при росте на искусственных питательных средах. Среди представителей рода описано около 20 видов бактерий. Гемофильные бактерии — это мелкие грамотрицательные палочки,
которые культивируют на обогащенных питательных средах, содержащих кровь или ее компоненты в качестве факторов роста (см. ниже). Многие микроорганизмы этого рода в норме обитают на слизистых оболочках дыхательных путей человека. Наиболее важная роль в патологии человека принадлежит бактериям вида Haemophilus influenzae, преимущественно типа b. Они вызывают инфекции с респираторным механизмом заражения (менингиты, синуситы, бронхиты и др.), преимущественно у детей. Кроме того, патогенным для человека является возбудитель мягкого шанкра H. ducreyi.
Haemophilus influenzae
Гемофильные палочки были впервые выделены русским бактериологом М.И. Афанасьевым в 1891 г. и позднее, в 1892 г., немецким бактериологом Р. Пфейффером от больных, умерших от гриппа. Бактерии H. influenzae долгое время считали возбудителем гриппа и называли палочкой инфлюэнцы (от англ. influenzae — грипп). Традиционно также и другое название — «палочка Пфейффера».
Морфология и тинкториальные свойства. Гемофильные бактерии — мелкие грамотрицательные сферические, овоидные или палочковидные бактерии, которые располагаются парами в виде коротких цепочек или нитей. Они неподвижны, спор не образуют, имеют пили. Наличие капсулы является непостоянным признаком, и ее обнаружение может служить маркером вирулентности штамма (см. далее).
Культуральные свойства. Факультативные анаэробы, но лучше растут в аэробных условиях. Гемофилы не способны синтезировать гем, входящий в состав ферментов дыхательной цепи, и/или НАД (НАДФ), являющийся кофактором окислительно- восстановительных ферментов, поэтому они нуждаются в факторах роста, присутствующих в крови: Х-факторе (протопорфирин IX в составе гематина или гемина), а также V-факторе (НАД или
НАДФ).
Для культивирования гемофильной палочки применяют шоколадный агар — питательную среду коричневого цвета, которую получают путем прогревания кровяного агара при 80 ?С в течение 15 мин. Оптимальная температура роста бактерий 35-37 ?С. Колонии появляются через 36-48 ч. Для H. influenzae характерна R-, S-диссоциация, т.е. способность к образованию R- и S-форм
колоний. Слизистые, более крупные (диаметр 3-4 мм) радужные S-формы колоний характерны для капсульных вирулентных штам- мов. Слабовирулентные бескапсульные варианты гемофильной палочки образуют R-колонии — более мелкие (около 1 мм), мелкозернистые, с неровными краями.
Характерной особенностью гемофильных бактерий является «феномен кормушки» или «феномен сателлита»: они могут расти на кровяном агаре вокруг колоний стафилококков или других бактерий, вызывающих гемолиз или продуцирующих НАД. Гемофильные бактерии гемолитической активностью не обладают.
Биохимическая активность. Идентификация гемофильных палочек основана на их потребности в факторах роста и некоторых биохимических тестах.
Гемофильные бактерии ферментируют глюкозу до кислоты, восстанавливают нитрат до нитрита. H. influenzae подразделяют на 8 биоваров (I-VIII) в зависимости от их способности продуцировать индол, уреазу, орнитиндекарбоксилазу. Кроме того, вид H. influenzae включает биовар aegyptius (см. табл. 16.4 и 16.5). Каталазная и оксидазная активность различны у разных видов гемофильных бактерий.
Антигенные свойства. H. influenzae обладают соматическим О-антигеном и капсульным полисахаридным К-антигеном, в за- висимости от особенностей строения которого H. influenzae делят на 6 серотипов (а, b, c, d, e, f). Капсульный антиген наиболее важного в патологии человека серотипа b гемофильной палочки представляет собой полимер рибозы и рибитола — полирибозорибитолфосфат (PRP).
Капсульные варианты гемофильных бактерий могут быть идентифицированы с помощью теста набухания капсулы или РИФ со специфическими сыворотками. Большинство вариантов H. influenzae, представителей нормальной микрофлоры верхних отделов респираторного тракта, являются бескапсульными формами, которые принято называть нетипируемыми.
Факторы вирулентности. Ведущим фактором вирулентности H. influenzae является капсула, которая защищает бактерии от фагоцитоза. Штаммы, имеющие капсулу (преимущественно серотипа b), вызывают наиболее тяжело протекающие инфекции.
Гемофильные палочки могут также продуцировать IgA-протеазу, инактивирующую секреторные антитела. IgA-протеаза и пили (фим- брии) возбудителя играют ведущую роль в прикреплении микроорганизмов к эпителию респираторного тракта и его колонизации.
ЛПС наружной мембраны H. influenzae играет роль эндотоксина, участвуя также в процессах адгезии и инвазии гемофильной палочки. Эндотоксин может также вызывать паралич ресничек мер- цательного эпителия респираторного тракта человека, способствуя тем самым микробной колонизации верхних дыхательных путей.
Резистентность. Бактерии малоустойчивы в окружающей среде. Гемофильные бактерии довольно чувствительны к нагреванию и обычным дезинфицирующим средствам. H. influenzae может продуцировать β-лактамазу, придающую ей устойчивость к некоторым β-лактамным антибиотикам.
Эпидемиология. H. influenzae патогенны только для человека.
Источник инфекции — больной человек или бактерионоситель. Ведущий механизм заражения гемофильной инфекцией — респи- раторный, путь передачи воздушно-капельный (при распылении капель секрета верхних дыхательных путей при кашле, разговоре, чиханье).
Гемофильные палочки вызывают пневмонии, средние отиты (поражение среднего уха), синуситы (воспаление придаточных пазух носа), ларинготрахеиты, бронхиты и другие инфекции дыхательных путей. Наиболее опасны менингиты и септицемии гемофильной этиологии, которым чаще подвержены дети в возрасте от 2 мес до 6 лет. Встречается гемофильная инфекция и у пациентов старшего возраста, в особенности у больных с хрони- ческой легочной патологией, сниженным иммунитетом, а также у курильщиков.
Патогенез и клиническая картина. Проникая через верхние дыхательные пути, H. influenzae прикрепляется к мерцательному эпителию и колонизирует его. Затем бактерии проникают в подслизистый слой и с помощью эндотоксина вызывают местные гнойно-воспалительные процессы.
H. influenzae, преимущественно типа b, может распространяться в организме гематогенно, вызывая септицемию, септический артрит, эндокардит. После проникновения через гематоэнцефалический барьер капсульные варианты гемофильной палочки вызывают тяжелые гнойные менингиты. Воспалительный экссудат накапливается в спинно-мозговом канале и желудочках мозга и служит хорошей питательной средой для гемофильной палочки, способствуя ее размножению. Нарушение оттока жидкости из субарахноидального пространства приводит к повышению внутричерепного давления, субдуральному отеку, а васкулит и тромбофлебит мягкой мозговой оболочки — к некротическим изменениям мозговой ткани. Гнойный менингит, вызванный H. influenzae типа b, заканчивается летально в 5% случаев даже при проведении адекватной терапии. Гнойные поражения твердой и мягкой мозговых оболочек могут приводить к тяжелым осложнениям: потере зрения, глухоте, гидроцефалии, слабоумию. H. influenzae типа b является также возбудителем острого бактериального эпиглоттита (воспаление надгортанника) у детей 2-5 лет, который приводит к нарушению проходимости дыхательных путей и асфиксии.
Иммунитет. В течение первых 3-6 мес жизни дети защищены от инфекции материнскими антителами класса IgG, полученными через плаценту. Поэтому в этом возрасте заболевания редки. PRP капсульного антигена типа b является Т-независимым антигеном, антитела к которому образуются без участия Т-хелперов. У младенцев способность синтезировать антитела к таким антигенам снижена, поэтому они не способны синтезировать необходимое количество антител к этому антигену и пик заболеваемости гемофильной инфекцией (в особенности типа b) приходится на возраст от 6 мес до 2 лет, когда концентрация материнских антител заметно снижается.
Иммунитет после перенесенной гемофильной инфекции мало изучен. Однако известно, что к 5-6 годам в сыворотке крови мно- гих детей (даже невакцинированных и непереболевших) имеются естественно приобретенные протективные антитела к капсульному антигену H. influenzae типа b (анти-PRP-антитела). Тем не менее пневмония и артрит, вызванные H. influenzae, могут развиваться у взрослых даже при наличии таких антител.
Диагностика. Симптомы гемофильных инфекций обычно определяются локализацией воспалительного процесса, а не этиологическим агентом, поэтому их диагностика базируется главным образом на выделении и идентификации возбудителя.
Материалом для исследования служат мазок из носоглотки, кровь, мокрота или ликвор, гнойное отделяемое (при отитах и синуситах), суставная жидкость (при септических артритах). Бактериоскопиче- ский метод применяют при гнойном менингите (изучение мазков из цереброспинальной жидкости, окрашенных по Граму). Для ускоренной диагностики и дифференциации гемофильной палочки от других возбудителей менингита используют тесты для обнаружения b-капсульного антигена H. influenzae: встречный иммуноэлектрофорез, прямую РИФ или реакцию латекс-агглютинации с анти-b- антителами. При высокой концентрации возбудителя в исследуемом материале возможна также постановка теста набухания капсулы.
Бактериологический метод исследования применяют для выделения и идентификации возбудителя из исследуемого материа- ла. Для дифференциации H. influenzae от других родственных им грамотрицательных палочек определяют их потребность в Х- и V-факторах роста, отсутствие гемолиза на кровяном агаре и пр. (см. табл. 16.4 и 16.5).
Лечение проводят с помощью антибиотиков. При отсутствии адекватного лечения летальность от гемофильного менингита и септицемии составляет около 90%, причем смерть может наступить в первые 24 ч от начала заболевания. Поэтому лечение назначают эмпирически до получения результатов антибиотикограммы. Препаратами выбора являются цефалоспорины III поколения (например, цефтриаксон, цефотаксим).
При синуситах, отитах и других инфекциях дыхательных путей гемофильной этиологии назначают β-лактамные антибиотики с ингибиторами β-лактамазы (например, амоксициллин с клавулановой кислотой) или бисептол.
Профилактика. Для профилактики гемофильной инфекции типа b разработана субкорпускулярная вакцина, содержащая очищенный капсульный антиген (RPR). Вакцинацию проводят по эпидемиологическим показаниям детям старше 1,5 лет из-за ее низкой иммуногенности. В России плановая вакцинация против гемофильной инфекции не проводится.
Для повышения эффективности вакцинации против H. influenza типа b предложено использовать конъюгированные вакцины, содержащие RPR-антиген на белке-носителе, например в составе комбинированной вакцины для профилактики менингококкового и гемофильного менингитов. Применение вакцины не защищает от носительства гемофильных палочек.
studfile.net
Гемофилы и инфекции, вызванные гемофильной бактериями
Гемофилы инфлюэнцы
В 1889 г. М.И. Афанасьев и в 1892 г. Р. Пфейффер и С. Китасато при изучении этиологии гриппа из мокроты больных выделили мелкие палочковидные грамотрицательные микроорганизмы. Выделенные бактерии, которые впоследствии были включены в род Haemophilus, долгие годы считались возбудителем гриппа. При дальнейшем их изучении было установлено, что они не являются возбудителями гриппа, а способны вызывать различные воспалительные процессы.Морфология и физиология
Haemophilus influenzae имеет вид мелких палочек. Встречаются нитевидные формы. Свежевыделенные бактерии имеют капсулу. Спор не образуют. Палочки инфлюэнцы требовательны к условиям культивирования, они нуждаются в присутствии гемина и НАД (никотинамиддинуклеотида). Гемин освобождается из эритроцитов при нагревании. Для культивирования используют агар с гретой кровью. В настоящее время разработаны Синтетические питательные среды с добавлением факторов роста. Выросшие колонии небольшие, прозрачные, плоские. Обладают небольшой ферментативной активностью. Расщепляют глюкозу и сахарозу с образованием кислоты, менее постоянно расщепляют галактозу, фруктозу, мальтозу и ксилозу.Антигены
Видовая антигенная специфичность обусловливается капсульным полисахаридом. Капсульные штаммы на основании различия в капсульном полисахариде разделяются на несколько сероваров: а, b, с и т.д. Некапсульные штаммы имеют только термостабильный соматический антиген. Наиболее часто из организма выделяются штаммы серовара b.Патогенность и патогенез
Вирулентные свойства Н.influenzae связаны с капсульным полисахаридом, который защищает бактерии от фагоцитоза. Токсичность связана с ЛПС и продукцией мембранотоксина (гемолизина). Гемофилы инфлюэнцы выделяют фермент протеазу, разрушающую секреторные иммуноглобулины (SIgA). В организме человека Haemophilus influenzae локализуется на слизистой оболочке верхних дыхательных путей и вызывает у человека заболевания с различными клиническими проявлениями: менингит, эндокардит, поражения дыхательного тракта, отит, конъюнктивит, гнойные воспалительные поражения суставов и др. Некапсульные варианты возбудителя часто выделяются от больных хроническими бронхитами, бронхиальной астмой. Наиболее часто болеют дети до 5 лет.Экология и эпидемиология
У здоровых людей средой обитания Н. influenzae является слизистая оболочка верхних дыхательных путей. Источник инфекции — человек. Передача происходит воздушно-капельным путем. Во многих случаях является причиной вторичных инфекций, которые возникают как осложнения после перенесения основного заболевания в связи с развитием иммунодефицита.Инфекции, вызванные гемофильной бактериями
Часто возбудителем менингита, септицемии, пневмонии, бронхита, отита, эндокардита, острых респираторных и вторичных инфекций может быть Haemophilus influenzae. Наиболее чувствительными к гемофильная бактерий дети от 3-х месяцев до 6 лет. По структуре капсульных антигенов HAnfluenzae разделяют на 6 сероваров (a, b, с, d, е, f). Тяжелые формы заболеваний, особенно менингита, как правило, вызывает серовар Ь. Вторым патогенным представителем рода гемофил является Н. ducrey — возбудитель мягкого шанкра. Остальные 14 видов для человека не патогенны.Материалы для исследования
Материалом для исследования при менингите служит ликвор, септицемии — кровь, при пневмонии — мокроты, при других процессах — навоз и слизь из носоглотки, которые забирают от больных с помощью ватных тампонов.Микроскопические исследования
Изготовлены и зафиксированы мазки окрашивают по Граму или водным фуксином в течение 5 мин. При микроскопии видны мелкие палочковидные грамотрицательные бактерии, которые не образуют спор, но имеют капсулы, располагаются поодиночке, реже в виде цепочек. При большом количестве возбудителя в исследуемом материале (спинномозговая жидкость, гной, слизь, мокрота) его легко и быстро можно обнаружить с помощью феномена набухание капсул или реакции иммунофлуоресценции, если использовать соответствующие диагностические сыворотки.Бактериологические исследования
Чистые культуры гемофильная бактерий выделяют путем немедленного посева исследуемого материала на специальные питательные среды (кровяной, шоколадный или сердечно-мозговой агар, среда Левинталя или Файлдса). Для подавления кокковой флоры к сред добавляют 15-25 ЕД / мл пенициллина. На простых средах гемофильные бактерии не растут.Спинномозговую жидкость и серозные обшлага сначала центрифугируют и осадок сеют петлей на одном из плотных сред. При септицемии сеют 10 мл крови в 100 мл жидкой среды Файддса. Через 24 часа делают высев на агар, где через сутки вырастают маленькие выпуклые прозрачные колонии. На шоколадном агаре колонии появляются через 36-48 ч, они немного больше по размерам и полупрозрачные. На кровяном агаре с добавлением сердечно-мозгового экстракта через сутки вырастают мелкие выпуклые колонии с радужными переливами. Колонии безкапсульних вариантов гемофил не имеют такого радужного расцвета. Из типичных колоний готовят мазки и окрашивают по Граму. При обнаружении маленьких грамотрицательных палочек сообщают врачу предварительные результаты. Н. influenzae первых генерациях может быть в капсульные и безкапсульний форме.Для окончательной идентификации выделенных культур проводят реакцию набухание капсул, исследуют потребности для роста X-и Y-факторов, Каталазную, оксидазно, уреазный, в-галактозидазной и гемолитическую активность, ферментацию углеводов, выделение индола и сероводорода.H.influenzaeпродукуе каталазу, уреазу, в-галакгозидазу, нитратредуктазы, выделяет индол, постоянно ферментирует глюкозу и сахарозу. Другие из перечисленных биохимических тестов отрицательные. Основное значение для идентификации имеют феномен набухания капсул и исследование потребности для роста X-и Y-факторов. Для выявления такой необходимости исследуемый материал засевают на среду, на поверхность которого затем кладут стандартные полоски бумаги, пропитанные X-и Y-факторами. Интенсивный рост бактерий вокруг полосок (а не в других участках агара) подтверждает наличие Н. influenzae.Серологическую идентификацию культур, еще на этапе получения изолированных колоний, можно провести с помощью реакции агглютинации на стекле с капсульный антиген (a, b, с, d, е, f) с соответствующими поли-и монорецепторными диагностическими сыворотками. Выделенные культуры необходимо дифференцировать от возбудителей коклюша и паракоклюш.Для диагностики менингита, вызванный гемофильной бактериями, используют также метод встречного имуноелекгрофорезу. Образование линий преципитации обнаруживает полисахаридные антигены гемофил, что доказывает этиологическую роль H.influenzae в возникновении заболевания.vse-zabolevaniya.ru
Гемофильная инфекция. Гемофильная палочка. Симптомы заболевания. Много Фото
Гемофильная инфекция. Гемофильная палочка. Симптомы заболевания. Много ФотоГемофильная инфекция представляет собой группу инфекционных заболеваний, причиной которых является гемофильная палочка (палочка инфлюэнцы, палочка Пфейффера). Механизм заражения — аэрогенный. Инфекция широко распространена среди детей, так как наибольшее количество бактерионосителей отмечается именно в этом возрасте.
Первичное заболевание часто протекает под маской ОРЗ. При попадании бактерий в кровяное русло возникает бактериемия. Далее микробы оседают во внутренних органах и вызывают гнойное воспаление мозговых оболочек, суставов, легких, подкожной клетчатки. Поражается надгортанник, перикард, придаточные пазухи носа, развивается отит и септицемия. Заболевание часто протекает поразительно долго, иногда с тяжелыми осложнениями и нередко заканчивается летальным исходом. Смертность от гемофильной инфекции особенно распространена среди детей младшего возраста.
Прививка от гемофильной инфекции позволяет значительно снизить заболеваемость среди детей. Так в Великобритании при введении плановой вакцинации регистрируется 1-2 случая в год. В РФ бесплатная прививка от гемофильной инфекции проводится только для некоторых категории детей (дети, проживающие в домах ребенка, больные онкологическими заболеваниями и носители ВИЧ-инфекции).
Рис. 1. На фото гемофильные палочки (вид в электронном микроскопе).
Гемофильная палочка
Гемофильная палочка является грамотрицательной коккобацилой. Впервые микроорганизм был выделен немецким ученым Р. Пфейффером в 1892 г. Бактерия принадлежит к роду гемофилюсов, куда входит 16 видов бактерий. Для своего роста вне организма они требуют добавления крови в питательную среду, в эритроцитах которой содержатся так необходимые для бактерий термолабильный фактор V и термостабильный фактор X.
Рис. 2. На фото гемофильные палочки (микроскопия, окраска по Граму). Они имеют вид мелких коккобацилл (фото слева). При росте в неблагоприятных условиях бактерии приобретают вид длинных нитей (фото справа).
Рис. 3. На фото рост колоний гемофильной палочки на средах с разрушенными эритроцитами (слева). Для идентификации возбудителей инфекции в некоторых случаях производят одномоментный посев золотистых стафилококков, вокруг колоний которых отмечается рост палочек инфлюэнцы (фото справа). Подобный феномен (феномен сателлизма) обуславливается выделением стафилококками факторов роста, необходимых для роста гемофильным палочкам.
- Существуют формы гемофильных палочек с капсулой и без нее. При росте на твердых питательных средах они имеют разный вид. Капсульные формы выглядят зернистыми, бескапсульные формы имеют слизистый или блестящий вид.
Наружная капсула позволяет бактериям длительно уклоняться от иммунной системы человека, поэтому защитные антитела либо не вырабатываются организмом вовсе, либо вырабатываются в небольшом количестве.
Наружная капсула (мембрана) гемофильных палочек содержит эндотоксин. Изучено 6 капсульных типов антигенов от a до f. Определение капсульного антигена имеет эпидемиологическое значение. Самым опасным подтипом являются гемофильные палочки тип b. Палочки этого подтипа вызывают развитие тяжелой инфекции. Они обладают большой инвазивной (проникающей) способностью благодаря наличию ворсинок (фимбрий). Палочки этого типа легко проникают в кровь больного и вызывают развитие множественных гнойно-септических очагов во внутренних органах.
- В последнее время отмечается рост развития у гемофильных палочек устойчивости к антибактериальным препаратам. Ампициллин, эритромицин, левомицетин и тетрациклин — главные из них. Все чаще регистрируется развитие множественной лекарственной устойчивости штаммов Н. influenzae типа b к тетрациклину, левомицетину и/или ампициллину.
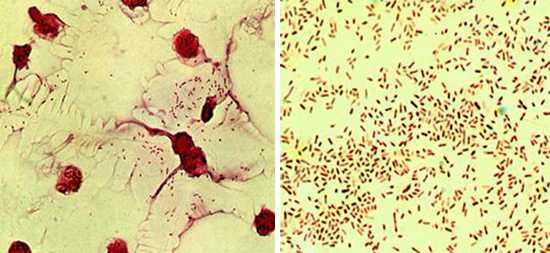
Рис. 4. На фото Haemophilus influenzae. Мазок сделан из спинномозговой жидкости (фото слева) и из чистой культуры (фото справа). Бактерии имеют вид мелких грамотрицательных палочек. Увеличение х 900.
к содержанию ↑Эпидемиология гемофильной инфекции
- Заболевания, которые вызываются гемофильными палочками, распространены повсеместно. В средних широтах заболевание наиболее часто встречается в конце зимы и весной.
- Источником инфекции являются здоровые носители и больные локальными и распространенными формами заболеваний.
- Гемофильная инфекция распространяется по воздуху при разговоре, чихании и кашле с мельчайшими капельками слизи из дыхательных путей. Бактерии проникают в организм человека (верхние дыхательные пути) воздушно-капельным путем, воздушно-капельным путем и контактным путем у маленьких детей.
- Гемофильная палочка, являясь условно-патогенным микроорганизмом, часто (до 90% случаев), присутствует в нормальной микрофлоре слизистых оболочек дыхательных путей (здоровое носительство). Наибольшее количество бактерионосителей отмечается в детском возрасте. Бактерии типа b составляют около 5%. Носители инфекции представляют собой внешне совершенно здоровых людей, поэтому именно они являются наиболее опасными с эпидемиологической точки зрения. Бактерионосители выделяют во внешнюю среду наименее опасные типы бактерий.
- Чаще всего болеют маленькие дети от 6 месяцев до 2-х лет. Алкоголизм и наркомания, плохие материально-бытовые условия являются факторами повышенного риска. В группу риска входят пожилые люди, малыши, находящиеся на искусственном вскармливании, больные с иммунодефицитами (онкология, болезни крови, ВИЧ-инфекция и др.), лица с удаленной селезенкой, дети из домов ребенка и детских домов.
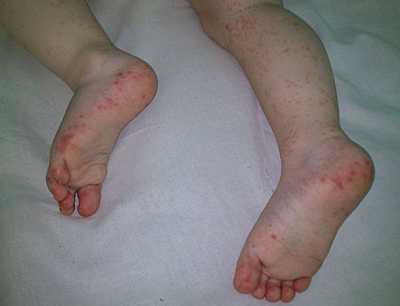
Рис. 5. На фото проявления сепсиса при гемофильной инфекции у ребенка.
к содержанию ↑Как развивается гемофильная инфекция (патогенез заболеваний)
Бактерии проникают в организм человека (верхние дыхательные пути) воздушно-капельным путем, у маленьких детей — воздушно-капельным путем и контактным путями. Хороший местный иммунитет не позволяет инфекции распространяться и возбудители могут длительное время пребывать в дыхательных путях (латентная бессимптомная инфекция).
Большое количество внедрившихся бактерий и сопутствующая вирусная инфекция способствует тому, что гемофильная инфекция приобретает манифестную форму. Капсульные вещества возбудителей подавляют фагоцитоз и возбудители, разрывая межклеточные соединения, быстро проникают в кровь. Развивается бактериемия. В крови гемофильные палочки пребывают несколько суток, пока их общая микробная масса не достигнет критического уровня. Далее микробы оседают во внутренних органах и вызывают гнойное воспаление мозговых оболочек, суставов, легких, подкожной клетчатки. Поражается надгортанник, перикард, придаточные пазухи носа, развивается отит и септицемия.
Бескапсульные штаммы гемофильной палочки инфицируют в основном слизистые оболочки дыхательных путей. Причиной системных заболеваний являются капсульные штаммы бактерий, наиболее опасными из которых являются бактерии типа b.
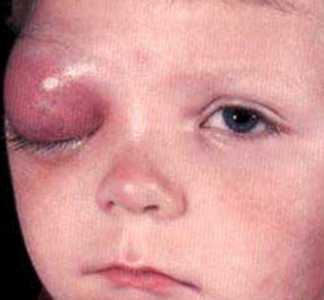
Рис. 6. На фото орбитальный целлюлит гемофильной природы.
к содержанию ↑Признаки и симптомы гемофильной инфекции
Гемофильная палочка поражает как верхние дыхательные пути, так и вызывает инвазивные системные заболевания. Наиболее часто проникают в кровь бактерии типа b. Заболевания почти всегда протекают остро и часто имеют затяжной характер. Воспалительный процесс носит гнойный характер.
У детей 6 — 9-месячного возраста чаще регистрируется менингит, у детей 1-го года жизни — целлюлит, у детей 2-х лет и старше — эпиглотит, у взрослых — пневмония. При заболевании так же поражаются суставы, перикард, придаточные пазухи носа, развивается отит и септицемия.
Инкубационный период при заболевании установить трудно. У здоровых бактерионосителей гемофильная инфекция длительное время себя ничем не проявляет. Размножение бактерий начинается при снижении иммунных механизмов.
Первичное проявление инфекции напоминает ОРЗ. Как только бактерии попадают в кровь и разносятся по всему организму, возникают локальные формы заболевания.
Признаки и симптомы гемофильной инфекции при гнойном менингите
Гнойный менингит развивается чаще всего у детей с 6 -и месяцев до 4-х лет. Заболевание начинается с симптомов ОРЗ. Бактериальный менингит нередко сочетается с такими проявлениями гемофильной инфекции, как эпиглотит, целлюлит, гнойный артрит, перикардит, воспаление легких и гнойный плеврит.
Болезнь протекает тяжело и часто принимает затяжное течение. Летальность составляет 10%. При благоприятном течении заболевание заканчивается выздоровлением на 2 — 3 неделе.
Применение бактериологических методов диагностики и обнаружение капсульного антигена гемофильной палочки в спинномозговой жидкости позволяют быстро установить диагноз.
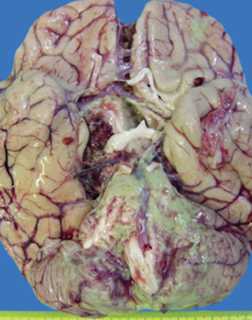
Рис. 7. На фото гнойный менингит. Мягкие мозговые оболочки утолщены, тусклые, пропитаны гноем зеленоватого цвета. Кровеносные сосуды переполнены кровью.
При стойкой высокой температуре тела, головной боли, постоянном плаче ребенка, мышечных подергиваниях, рвоте или срыгивании следует незамедлительно обратиться за медицинской помощью.
Признаки и симптомы гемофильной инфекции при целлюлите
Заболевание регистрируется у детей от 6-и месяцев до 2-х лет. Воспаление подкожной клетчатки чаще всего локализуется в области щек и вокруг глазницы. На стороне поражения в ряде случаев регистрируется воспаление среднего уха. Целлюлит развивается очень быстро. Буквально за несколько часов появляется припухлость, болезненная на ощупь, характерной окраски. У детей старшего возраста целлюлит может появляться на конечностях.
Рис. 8. На фото целлюлит области правой щеки у ребенка (слева) и целлюлит в области нижней конечности (справа).
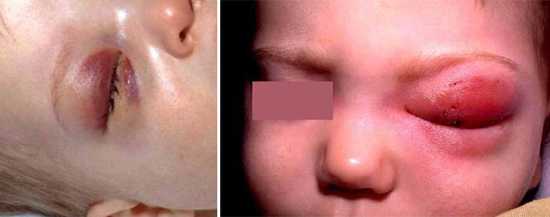
Рис. 9. На фото гемофильный целлюлит орбиты правого глаза у ребенка. Верхнее веко отечно, имеет цианотический оттенок.
Признаки и симптомы гемофильной инфекции при пневмонии
Пневмонии при гемофильной инфекции бывают очаговыми и долевыми. У 75% детей пневмонии протекают с гнойными плевритами. В ряде случаев (до 5%) вместе с пневмонией регистрируется гнойный перикардит.
Гемофильные пневмонии часто имеют затяжное течение, что вызывает у врачей подозрение на туберкулезную инфекцию. Воспаление легких и плевры чаще регистрируется у пожилых людей. В группе риска находятся лица с хронической патологией дыхательных путей.
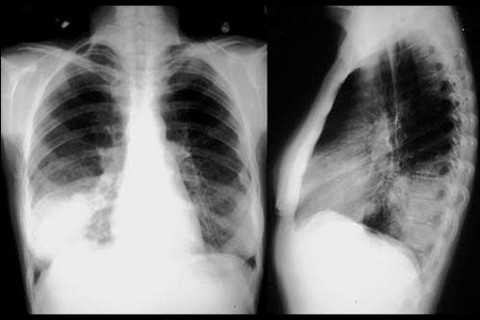
Рис. 10. На фото на рентгенограмме легких гемофильная пневмония.
Признаки и симптомы гемофильной инфекции при воспалении надгортанника
Эпиглотит — тяжелая форма гемофильной инфекции. Из всех эпиглотитов 95% случаев заболевания приходится на гемофильный эпиглотит.
Болезнь всегда начинается остро. Температура тела повышается до высоких цифр. Нарастает слабость и интоксикация. Развивается отек и воспаление надгортанника. В процесс вовлекаются другие отделы глотки, которые расположены выше надгортанника. Поступление воздуха в легкие затрудняется. Заболевание требует быстрого диагностического решения, так как полная непроходимость дыхательных путей приводит к асфиксии и смерти ребенка. Спасут больного эндотрахеальная интубация или трахеостомия.
Сильная боль в горле, запрокидывание головы, одышка и невозможность сделать глоток воды или произнести слово, высокая температура тела являются поводом срочно обратиться за медицинской помощью.
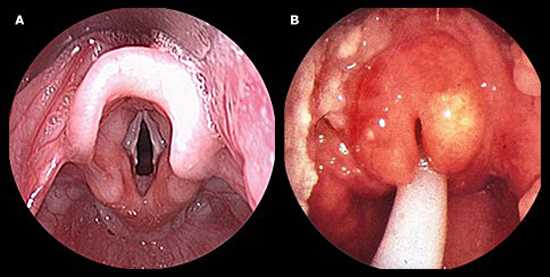
Рис. 11. На фото эпиглотит (воспаление надгортанника).
Признаки и симптомы гемофильной инфекции при сепсисе
Сепсис при гемофильной инфекции чаще развивается у детей от 6-и месяцев до 1-го года. Заболевание протекает бурно и молниеносно без признаков поражения внутренних органов. При этом у ребенка повышается температура тела до 39°С и выше, он становится беспокойным и вялым, отмечается увеличение селезенки, быстро падает артериальное давление, появляется тахикардия, на коже конечностей, туловища и лица появляются кровоизлияния, в периферической крови повышается количество нейтрофилов.
Болезнь часто заканчивается септическим шоком и смертью больного.
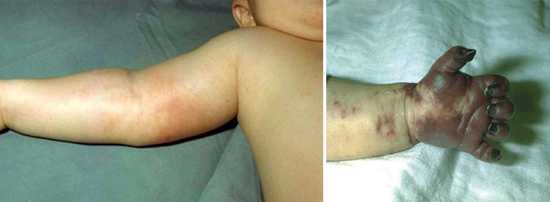
Рис. 12. На фото кровоизлияния при гемофильном сепсисе у детей.
Очень высокая температура тела, вялость, сонливость, отказ от еды, посинение губ, тахикардия, появление на коже ребенка пятен темного цвета разной величины являются поводом срочно обратиться за медицинской помощью.
Признаки и симптомы гемофильной инфекции при гнойном артрите
Гнойный артрит развивается при поражении суставов палочкой Пфейффера типа b. Заболевание чаще всего регистрируется у детей до 2-летнего возраста. Обычно поражается один, реже несколько суставов, несущих нагрузку (крупные суставы). У 5-й части больных гнойные артриты сопровождаются остеомиелитом.
Другие проявления гемофильной инфекции
Перикардит и пневмония при гемофильной инфекции у ребенка часто встречаются вместе. Заболевание имеет затяжное течение. Отличительной особенностью синуситов является зловонное дыхание и носоглоточные выделения. Описаны случаи воспаления глаза (эндофтальмит), почек (пиелонефрит) и внутренних оболочек сердца (эндокардит).
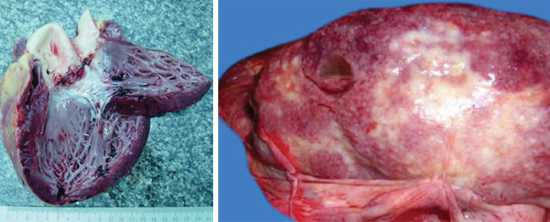
Рис. 13. На фото гнойный эндокардит (слева) и гнойный нефрит (справа).
к содержанию ↑Осложнения гемофильной инфекции
- Развитие гемофильного менингита может привести к отеку и абсцессу мозга.
- Острая гемофильная пневмония осложняется острой дыхательной недостаточностью.
- Вследствие эпиглотита развивается асфиксия.
- Септицемия осложняется септическим шоком.
Иммунитет при гемофильной инфекции
На внедрение бактерий или после введения вакцины организм больно вырабатывает антитела — IgA. Капсульные виды гемофильных палочек выделяют протеазы, которые инактивируют антитела.
Исследователями было установлено, что у лиц, переболевших системной гемофильной инфекцией, и у лиц после иммунизации иммунный ответ имел разную степень выраженности в разных возрастных категориях. Дети младшего возраста иммунитет либо не приобретали вовсе, либо иммунитет был выражен слабо. Умеренная степень выраженности имел иммунитет у детей среднего возраста. У лиц подросткового возраста и взрослых иммунитет был выражен и ревакцинация (повторная вакцинация) не требовалась.
к содержанию ↑Перенесенная гемофильная инфекция оставляет после себя стойкий иммунитет. Повторные заболевания возможны у лиц с иммунодефицитами.
Диагностика гемофильной инфекции
- На гемофильную инфекцию указывают характерные проявления заболевания.
- Бактериологическая диагностика предполагает обнаружение гемофильных палочек в мазках биологического материала (микроскопия) и рос колоний возбудителей на питательных средах.
- Обнаружение в 95% случаев капсульного антигена в цереброспинальной жидкости больных менингитом.
- Пункционная биопсия легких и краевых участков целлюлита с последующим исследованием биологического материала используется у больных с осложненным течением заболевания.
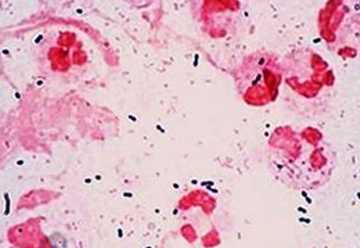
Рис. 14. На фото гемофильные палочки (микроскопия).

Рис. 15. На фото рост колоний возбудителей. Для культурального исследования используются питательные среды с добавлением крови.
ССЫЛКИ ПО ТЕМЕСтатьи раздела «Гемофильная инфекция»Самое популярноеПОНРАВИЛАСЬ СТАТЬЯ?
Подпишитесь на нашу рассылку!
Статьи раздела «Гемофильная инфекция» Новые статьи Популярные статьи Похожие статьи О микробах и болезнях © 2019 Наверхmicrobak.ru
