Прививка акдс от чего делается детям: Как АКДС влияет на здоровье детей?
АКДС: возможные реакции и противопоказания. Справка
Как и любая вакцина, АКДС может вызвать у детей различные, в том числе острые реакции.
Возможные реакции на введение вакцины АКДС
У части привитых в первые двое суток могут развиваться кратковременные общие (повышение температуры, недомогание) и местные (болезненность, гиперемия, отечность) реакции. В редких случаях могут развиваться осложнения: судороги (обычно связанные с повышением температуры), аллергические реакции (крапивница, полиморфная сыпь, отек Квинке).
Учитывая возможность развития аллергических реакций немедленного типа у особо чувствительных детей, за привитыми необходимо обеспечить медицинское наблюдение в течение по меньшей мере 30 минут.
Противопоказания к АКДС
Противопоказаниями к вакцинации являются прогрессирующие заболевания нервной системы, афебрильные судороги в анамнезе, развитие на предшествующее введение АКДС-вакцины сильной общей реакции (повышение температуры в первые двое суток до 40 градусов С и выше) или осложнения.
Дети с противопоказаниями к применению АКДС-вакцины могут быть привиты вакциной АДС (против дифтерии, столбняка) в соответствии с инструкцией по его применению.
Детей, перенесших острые заболевания, прививают не ранее, чем через 4 недели после выздоровления; при легких формах респираторных заболеваний (ринит, легкая гиперемия зева и т.д.) прививка допускается через 2 недели после выздоровления. Больных хроническими заболеваниями прививают по достижении стойкой ремиссии (не менее 4 недель).
Стабильные проявления аллергического заболевания (локализованные кожные проявления, скрытый бронхоспазм и т.п.) не являются противопоказанием к вакцинации, которая может быть проведена на фоне соответствующей терапии.
Детей, родившихся с весом менее 2 кг, прививают при нормальном физическом и психомоторном развитии; отставание в весе не является основанием к отсрочке вакцинации.
С целью выявления противопоказаний врач-педиатр или иммунолог в день прививки проводит опрос родителей и осмотр ребенка с обязательной термометрией. Дети, временно освобожденные от прививки, должны быть взяты под наблюдение и учет и своевременно привиты.
Дети, временно освобожденные от прививки, должны быть взяты под наблюдение и учет и своевременно привиты.
Следует соблюдать условия хранения и транспортировки вакцины. Вакцину хранят и транспортируют в в сухом защищенном от света месте при температуре от 4 до 8 градусов С.
Противники вакцинации детей утверждают, что вне зависимости от условий хранения АКДС неэффективна и небезопасна для здоровья.
Материал подготовлен на основе информации открытых источников
Стоит ли делать прививки в разгар пандемии — Российская газета
Как должна проводиться вакцинация в период пандемии коронавируса, можно ли прививками перегрузить иммунную систему, что будет, если отказаться от них вовсе, рассказала «РГ» заведующая отделением вакцинопрофилактики детей с отклонениями в состоянии здоровья и семейной вакцинации «НМИЦ здоровья детей» Минздрава России Наталья Ткаченко.
Нужно делать плановые прививки ребенку в разгар эпидемии коронавируса?
Наталья Ткаченко: Категорического запрета на плановую вакцинацию детей пока не было.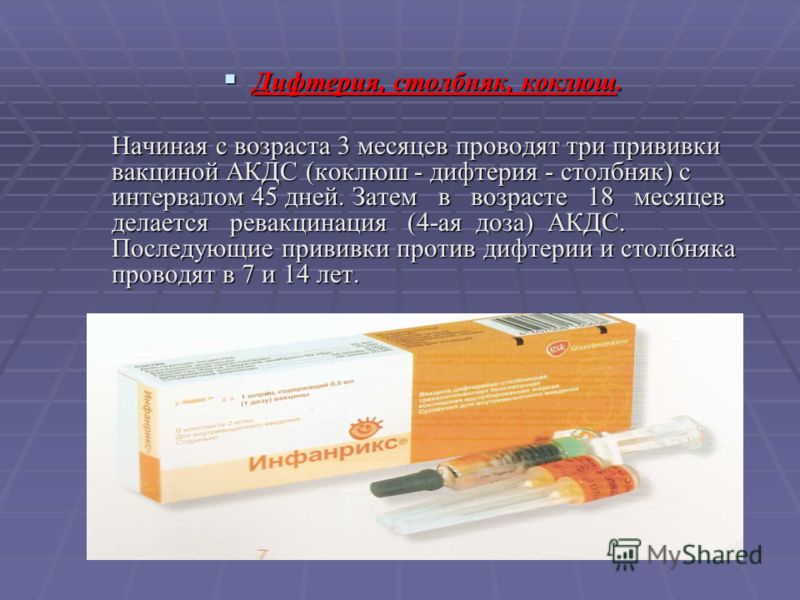 По совершенно понятной причине: если отказаться от прививок, то через 3-6 месяцев мы получим вспышки других заболеваний, в числе которых — коклюш, пневмококковая инфекция, корь, краснуха, паротит, ветрянка и другие. Даже в условиях эпидемии коронавируса вакцинация должна проводиться, но с соблюдением всех мер предосторожности.
По совершенно понятной причине: если отказаться от прививок, то через 3-6 месяцев мы получим вспышки других заболеваний, в числе которых — коклюш, пневмококковая инфекция, корь, краснуха, паротит, ветрянка и другие. Даже в условиях эпидемии коронавируса вакцинация должна проводиться, но с соблюдением всех мер предосторожности.
Стоит опасаться, что из-за прививки ослабнет иммунитет ребенка?
Наталья Ткаченко: Нет… Прививка стимулирует иммунитет, она заставляет его вырабатывать антитела против инфекции. Суть вакцинации — это обучение иммунной системы.
Активный иммунитет, который мы приобретаем к инфекционным болезням, можно получить только двумя способами: переболеть или сделать прививку. Первый способ опасен тем, что сложно предсказать, как человек будет болеть: легко или очень тяжело.
Можно прививками перегрузить иммунную систему?
Наталья Ткаченко: Многие боятся прививаться, а уж использовать комбинированные многокомпонентные вакцины тем более! Например, есть шестивалентная вакцина против коклюша, дифтерии, столбняка, полиомиелита, вирусного гепатита B и гемофильной инфекции. Приходят родители и просят все сделать по отдельности, чтобы уменьшить «нагрузку» на иммунную систему ребенка. То есть предлагают сначала три раза сделать прививку от полиомиелита, потом отдельно три раза от коклюша, дифтерии, столбняка и гепатита B. О чем они беспокоятся? Вакцина полиомиелитная инактивированная содержит 3 антигена, противококлюшная — столько же, против дифтерии и столбняка — по одному антигену. Для сравнения — нагрузка цельноклеточной вакцины АКДС, которая начала применяться во второй половине ХХ века в Советском Союзе и до сих пор широко используется, равна трем тысячам антигенов. Почувствуйте разницу: три тысячи или всего десять антигенов! От чего вы хотите освободить ребенка? Современные вакцины высокоэффективны, хорошо переносятся, не угнетают иммунную систему, а, скорее наоборот, стимулируют ее.
Приходят родители и просят все сделать по отдельности, чтобы уменьшить «нагрузку» на иммунную систему ребенка. То есть предлагают сначала три раза сделать прививку от полиомиелита, потом отдельно три раза от коклюша, дифтерии, столбняка и гепатита B. О чем они беспокоятся? Вакцина полиомиелитная инактивированная содержит 3 антигена, противококлюшная — столько же, против дифтерии и столбняка — по одному антигену. Для сравнения — нагрузка цельноклеточной вакцины АКДС, которая начала применяться во второй половине ХХ века в Советском Союзе и до сих пор широко используется, равна трем тысячам антигенов. Почувствуйте разницу: три тысячи или всего десять антигенов! От чего вы хотите освободить ребенка? Современные вакцины высокоэффективны, хорошо переносятся, не угнетают иммунную систему, а, скорее наоборот, стимулируют ее.
Осторожность в прививках необходима при врожденном или приобретенном иммунодефиците, например, в том случае, когда ребенок получает иммуносупрессивную терапию, которая снижает иммунный ответ организма. В частности, абсолютно противопоказана вакцинация живыми вакцинами после трансплантации почки, печени, сердца, легких, а также детям с онкологическими заболеваниями, которым назначена химиотерапия. Живые вакцины противопоказаны также при беременности, поэтому позаботиться о своем здоровье и здоровье будущего ребенка женщина, планирующая беременность, должна заранее!
В частности, абсолютно противопоказана вакцинация живыми вакцинами после трансплантации почки, печени, сердца, легких, а также детям с онкологическими заболеваниями, которым назначена химиотерапия. Живые вакцины противопоказаны также при беременности, поэтому позаботиться о своем здоровье и здоровье будущего ребенка женщина, планирующая беременность, должна заранее!
Какие бывают противопоказания для того, чтобы на время отложить вакцинацию?
Наталья Ткаченко: Если ребенок заболел, к примеру, у него температура или понос, рвота, тогда на некоторое время вакцинация откладывается. Но нужно смотреть на общее состояние пациента. Если болезнь протекала легко и это была обычная сезонная респираторная инфекция без высокой температуры, то на самом деле через 2-3 дня после нормализации температуры прививку можно делать. Если болезнь сопровождается лихорадкой, ребенок лечится антибиотиками, лучше подождать, иногда необходимо отложить вакцинацию до месяца. Зависит от того, как будет улучшаться состояние.
Зависит от того, как будет улучшаться состояние.
Живые вирусы содержатся в вакцинах против кори, краснухи, ветряной оспы, паротита, полиомиелита. Фото: istock / Bet_Noire
Насколько оправданы прививки в грудном возрасте? Можно от них отказаться?
Наталья Ткаченко: Когда 1,5 года назад мы проводили анкетирование родителей по вакцинации детей против пневмококковой инфекции, которая начинается в 2 месяца, то были удивлены. Это одна из самых ранних вакцин в Национальном календаре профилактических прививок России. В тех случаях, когда эта вакцинация не проводилась, мы ожидали на первом месте увидеть отказы родителей от нее. Но были страшно удивлены, когда на первое место вышли рекомендации врача. Причем зачастую это были не письменные медотводы, а устные советы об отказе или переносе сроков иммунизации! Это был шок, потому что наиболее тяжело пневмококковая инфекция протекает именно у ребенка самого раннего возраста. Если это отит — то гнойный, с частыми осложнениями, если пневмония, то она зачастую приобретает деструктивный характер. Кроме того, именно у маленьких детей отмечается самый высокий уровень заболеваемости пневмококковыми менингитами!
Кроме того, именно у маленьких детей отмечается самый высокий уровень заболеваемости пневмококковыми менингитами!
Новорожденный ребенок рождается «стерильным». Сразу после рождения его иммунная система сталкивается с огромным количеством антигенов. Это всевозможные бактерии, которые находятся вокруг, вирусы, пищевые антигены, например, те, что он получает с молоком матери, антигены пылевые и пыльцевые. Но его иммунная система с этим благополучно справляется. Другое дело, что она еще не обучена и не готова сопротивляться инфекционным болезням. Вакцинация восполняет собой эту слабость, позволяя заблаговременно выработать антитела к разным инфекциям.
Бывает, что организм не может справиться с вирусом или микробом, который содержит вакцина?
Наталья Ткаченко: На самом деле большинство вакцин — неживые. Это значит, что инфекционный агент в них предварительно умерщвлен. Более того, часто они содержат лишь часть бактериальной клетки или вируса. Это касается прививок от вирусных гепатитов А и B, вируса папилломы человека, полиовируса, коклюша, дифтерии, столбняка. Любая инактивированная вакцина не содержит патогена, который вызывает болезнь. Живые вирусы содержатся в вакцинах против кори, краснухи, ветряной оспы, паротита, полиомиелита, но культуры в них настолько ослаблены, что не способны размножаться в организме. Они не вирулентны, то есть не могут причинить вреда организму, в отличие от инфекции.
Это касается прививок от вирусных гепатитов А и B, вируса папилломы человека, полиовируса, коклюша, дифтерии, столбняка. Любая инактивированная вакцина не содержит патогена, который вызывает болезнь. Живые вирусы содержатся в вакцинах против кори, краснухи, ветряной оспы, паротита, полиомиелита, но культуры в них настолько ослаблены, что не способны размножаться в организме. Они не вирулентны, то есть не могут причинить вреда организму, в отличие от инфекции.
Что будет, если вовсе отказаться от прививок?
Наталья Ткаченко: Как только падает процент охвата вакцинацией населения в каком-либо регионе, там возникает вспышка инфекции. Так было в 90-е годы в России. Советский Союз распался в 1991 году, и уже в 1993-1994 годах было зарегистрировано порядка 40 тысяч случаев дифтерии в Российской Федерации. В 2011 году Европа получила мощнейшую вспышку кори, когда резко упала привитость населения против этого заболевания. Тогда и в Российской Федерации был отмечен резкий подъем заболеваемости корью, и мы тоже были вынуждены последние несколько лет активно проводить догоняющую вакцинацию взрослых против кори. Не будет вакцинации от гриппа — будут вспышки гриппа, колоссальные вспышки.
Не будет вакцинации от гриппа — будут вспышки гриппа, колоссальные вспышки.
Насколько эффективна прививка от гриппа, учитывая, что вирус постоянно мутирует?
Наталья Ткаченко: Истинная мутация — это то, что произошло с коронавирусом: где, когда и как он мутировал, на этот вопрос не ответит никто. Доподлинно неизвестно, когда конкретно появится эффективная вакцина. А когда мы говорим о вакцинации против гриппа, это рутинная вакцинация, это обыденное дело для человечества. Истинных мутаций встречается не так уж и много. На самом деле это просто чередование видов гриппа А и гриппа B. Все штаммы хорошо известны, пути распространения гриппа тоже понятны и изучены. Как правило, шествие гриппа начинается с Юго-Восточной Азии, где сезонная вспышка начинается весной. Штаммы отбираются, исследуются, и уже летом производится вакцина для других территорий. Выбранную вакцину запускают в производство, чтобы в дальнейшем опередить волну гриппа, которая неизбежно придет.
От себя добавлю, что в предстоящем эпидсезоне 2020-2021 гг. особое внимание надо уделить именно вакцинации против пневмотропных инфекций, таких как грипп, пневмококковая инфекция и коклюш.
Прививки детям | Детская городская больница
Во время прививок в организм вводится особый медицинский препарат – вакцина. В ответ на введение вакцины организм вырабатывает особые клетки – специфические антитела, которые и защищают человека от соответствующей болезни.
В чем суть профилактических прививок
Во время прививок в организм вводится особый медицинский препарат – вакцина. В ответ на введение вакцины организм вырабатывает особые клетки – специфические антитела, которые и защищают человека от соответствующей болезни.
Каждая вакцина имеет свои сроки, свою схему и свои пути введения (через рот, внутримышечно, подкожно, внутрикожно).
На каждую вакцину организм реагирует по-разному. В некоторых случаях одной прививки воле достаточно для выработки длительного иммунитета, в других — требуется многократная ревакцинация ( повторное введение вакцины).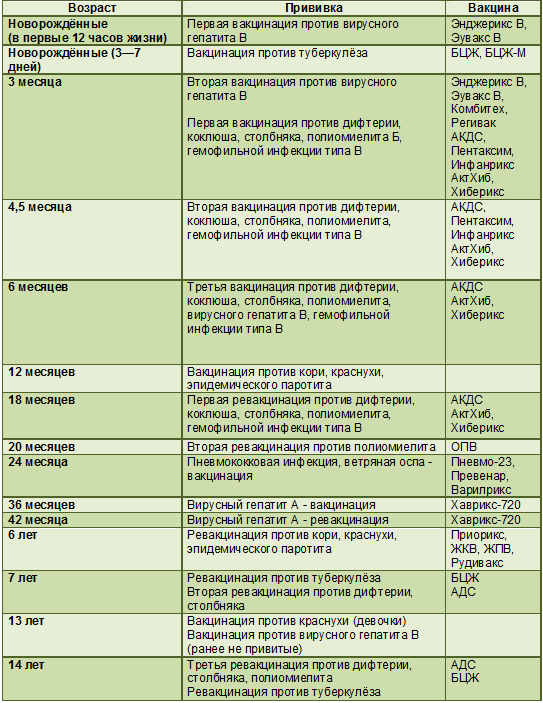
Суть вакцинации — добиться выработки специфических антител в количестве, достаточном для профилактики конкретной болезни. Но этот стартовый защитный уровень снижается, необходимо повторное введение вакцины для поддержания достаточного количества антител (ревакцинация).
Какие прививки мы делаем своим детям?
Самая первая прививка – это прививка от туберкулеза. Она, как правило, делается непосредственно в роддоме на 4-7 день, однократно. В дальнейшем ревакцинация осуществляется в 7, 12 и 16-17 лет. Вопрос о том, делать или не делать ревакцинацию против туберкулеза во многом зависит от пробы Манту. Пробу или реакцию Манту детям делают довольно часто.
Практически каждый человека рано или поздно инфицируется бактерией туберкулеза, т.е. микроб попал, а организм благодаря прививке имеет защитное количество антител, и болезнь не развивается, хотя туберкулезная бактерия присутствует.
Реакция Манту – это не прививка, это проба на инфицирование туберкулеза. И если в организме туберкулезных бактерий нет, то проба отрицательная, а после инфицирования она становится положительной. Ревакцинация проводится туберкулиноотрицательным детям, т.е. не инфицированным микобактериями туберкулеза.
И если в организме туберкулезных бактерий нет, то проба отрицательная, а после инфицирования она становится положительной. Ревакцинация проводится туберкулиноотрицательным детям, т.е. не инфицированным микобактериями туберкулеза.
В возрасте 3 месяцев вакцинация начинается непосредственно в детском медицинском учреждении. За три введения с интервалом в 1-1,5 месяца осуществляют вакцинацию сразу от четырех болезней – полиомиелита (вакцина жидкая, её капают ребенку в рот), а также коклюша, дифтерии и столбняка. Эта прививка называется АКДС, она делается с помощью укола. На втором году жизни проводится ревакцинация от всех этих болезней.
В возрасте одного года ребенка прививают от кори, краснухи и паротита.
График вакцинации в нашей стране определяется национальным календарем прививок.
Конечно прививка – это нагрузка на детский организм, поэтому родители должны знать о возможных реакциях на прививку.
Когда можно и когда нельзя делать прививки?
В этом вопросе главный советчик детский врач, который наблюдает ребенка и осматривает его перед прививкой.
Прежде всего, необходимо помнить, что любая прививка делается ребенку, у которого в этот момент нет никакой острой инфекционной болезни – ни насморка, ни поноса, ни сыпи, ни повышения температуры тела. Почему именно отсутствие инфекционной болезни?
Потому, что любая инфекция это нагрузка на иммунитет. Для того, чтобы отреагировать на прививку правильно и выработать достаточное количество антител, организм и должен быть более менее свободен от других дел, в свою очередь связанных с выработкой иммунитета. Другими словами, если у ребенка нога в гипсе, то это не противопоказание к прививке.
Но некоторые инфекционные болезни специфически поражают именно те клетки человеческого организма, которые ответственны за выработку иммунитета. Это, к примеру, ветряная оспа и инфекционный мононуклеоз. Даже в том случае, если у ребенка ветрянка, но нормальная температура и общее состояние, это не является поводом к тому. чтобы делать прививку
чтобы делать прививку
Кроме того, некоторые перенесенные ребенком инфекционные заболевания вызывают длительное ослабление защитных сил организма и это, в свою очередь, является противопоказанием к проведению прививок на определенный срок (до 6 месяцев после выздоровления). К таким болезням относится менингит, гепатит, инфекционный мононуклеоз.
Для каждой болезни – аллергической, врожденной, неврологической и т.д. разработаны соответствующие правила : как, когда и чем прививать. Все это учитывает врач, дающий разрешение на прививку. Детские врачи, направляя ребенка на прививку, учитывают все многообразие факторов, которые могут повлиять на решение о проведении вакцинации.
В некоторых случаях по показаниям вопрос о прививке решается совместно с другими специалистами: аллергологом, неврологом, кардиологом и другими.
Как подготовиться к прививке?
Специально ничего делать не нужно. Ну, разве что, избегать экспериментов в отношении еды, стараться не давать никаких новых продуктов.
Поскольку место укола 1-2 дня не желательно мочить, желательно перед вакцинацией хорошо помыться.
Что нужно делать после прививки?
- Стараться немного недокармливать ( при хорошем аппетите) или кормить только по аппетиту (если аппетит отсутствует или снижен).
- Побольше пить – минеральная вода, компот из сухофруктов, зеленый, фруктовый, ягодный чай.
- Поддерживать в помещении прохладный влажный воздух.
- Если температура тела ниже 37,5 вполне можно гулять на свежем воздухе.
- Максимально ограничить контакты ребенка.
Что должны знать родители о реакции на прививку
После любой прививки может иметь место детского реакция организма – повышение температуры, отказ от еды. Это нормально — организм вырабатывает иммунитет (защиту) к конкретной болезни. Одни вакцины переносятся очень легко и почти не дают серьезных реакций. Типичный пример вакцина против полиомиелита. Введение других препаратов может сопровождаться выраженным повышением температуры и нарушением состояния ребенка.
Типичный пример вакцина против полиомиелита. Введение других препаратов может сопровождаться выраженным повышением температуры и нарушением состояния ребенка.
Например, коклюшный компонент вакцины АКДС. Но эти реакции обычно кратковременны и не вызывают серьезных нарушений в организме. Такие реакции возникают в первые сутки после прививки и исчезают на 3-и сутки.
Для родителей очень важно осознавать принципиальную разницу между реакцией на вакцину и осложнением после прививки.
Реакции на прививку, в той или иной степени выраженности, просто обязаны быть и это, как мы уже отметили, абсолютно нормально. Именно для того, чтобы вакцинация прошла безболезненно для ребенка, перед прививкой предусмотрен осмотр ребенка педиатром и по показаниям проведение необходимых обследований.
Прививки детям в Москве — цены, платная вакцинация детей и новорожденных в клинике «СМ-Доктор»
Вакцинация детей — введение антигенного материала с целью вызвать иммунитет к болезни, который предотвратит заражение, или ослабит его последствия.
Виды профилактических прививок
В нашей клинике проводится вакцинация детей против гепатита В, дифтерии, столбняка, коклюша, полиомиелита, кори, краснухи и паротита, инфекций, входящих в Национальный календарь профилактических прививок. Более того в клинике «СМ-Доктор» вы можете провести вакцинацию ребенка от:
Вышеперечисленные инфекции включены в Региональный календарь профилактических прививок действующий в Москве с января 2009 года.
В арсенале нашей клиники имеются на ваш выбор вакцины против дифтерии, как российского, так и импортного производства.
В клинике «СМ-Доктор» вакцинация детей проводится только после консультации врача-педиатра, специалиста по вакцинопрофилактике.
Врач во время медицинского осмотра ребенка оценит состояние его здоровья, ознакомится с графиком уже проведенных прививок и с историей перенесенных заболеваний. Особого внимания требуют дети, подверженные аллергическим заболеваниями, часто болеющие дети — им необходим индивидуальный график вакцинации, составленный с учетом общего и текущего состояния здоровья ребенка.
После вакцинации вашему ребенку необходимо будет оставаться в клинике под наблюдением медицинского персонала в течение 30 минут. В связи с этим, просим Вас рассчитывать время визита в клинику.
Вакцинация: 4 легких шага для детей и родителей
1. Планируйте визит заранееЕсли вы знаете, что вам предстоит поход в поликлинику на прививку, постарайтесь заранее собраться и спланировать время так, чтобы ребенок к моменту посещения поликлиники был отдохнувшим от прогулки или другой активности, поел и был одет по погоде.
2. Оставайтесь спокойнымиТак как дети чувствуют, когда вы расстроены или нервничаете, постарайтесь оставаться расслабленными и спокойными во время визита к врачу. Если вы все же чувствуете легкое волнение, несколько раз медленно глубоко вздохните.
3. Развлекайте вашего малыша
Хорошо захватить с собой в кабинет к врачу детскую книжку. Пока врач или медсестра делают вашему ребенку прививку, читайте вслух вашему ребенку мягким ровным и спокойным голосом. Если у вас нет с собой книжки, расскажите малышу историю, отвлекайте и развлекайте его, делайте все, чтобы малыш улыбался!
Если у вас нет с собой книжки, расскажите малышу историю, отвлекайте и развлекайте его, делайте все, чтобы малыш улыбался!
Если ребенок расстроен и плачет после прививки, дайте ему время успокоиться, снова почувствовать себя в безопасности в кабинете врача. В таком случае в следующий раз малыш бесстрашно пойдет к доктору снова.
Записаться на приём или задать вопросы можно круглосуточно по телефону +7 (495) 292-59-86
Вакцинация против гриппа – тема для бесконечных споров и обсуждений. Прививка не является обязательной и выполняется по желанию родителей, а также при наличии медицинских показаний. Статистика утверждает, что своевременно введенная вакцина против гриппа значительно снижает заболеваемость и детей, и взрослых.
 В клинике «СМ-Доктор» доступны современные препараты импортного и отечественного производства.
В клинике «СМ-Доктор» доступны современные препараты импортного и отечественного производства.Клещевой энцефалит – острое инфекционное заболевание, которое преимущественно поражает центральную нервную систему. Источником вируса являются иксодовые клещи, при укусе инфицированного клеща вирус передается человеку. Энцефалит особенно опасен для детей, поскольку последствия заражения чрезвычайно серьезны – от приводящих к инвалидности нарушений здоровья до коматозных состояний и смерти. Эффективного лечения клещевого энцефалита не существует, но заражение можно предупредить благодаря введению вакцины.
Прививка от гепатита А не входит в обязательный график вакцинации детей.
 Она проводится по желанию родителей и создает стойкий иммунитет, сохраняющийся на протяжении 7-20 лет. В клинике «СМ-Доктор» всегда доступны современные и безопасные для детей вакцины против гепатита А, которые можно использовать уже с 12 месяцев.
Она проводится по желанию родителей и создает стойкий иммунитет, сохраняющийся на протяжении 7-20 лет. В клинике «СМ-Доктор» всегда доступны современные и безопасные для детей вакцины против гепатита А, которые можно использовать уже с 12 месяцев.Прививка от гепатита В делается всем детям при отсутствии противопоказаний, поскольку входит в список обязательных. Она обеспечивает надежную защиту от вируса и крайне редко вызывает осложнения и побочные реакции. Врачи клиники «СМ-Доктор» приглашают детей на вакцинацию от гепатита В в соответствии с графиком.
Прививка против полиомиелита – это единственный способ защитить детей и взрослых от тяжелого заболевания, способного вызвать смертельный паралич.
 Комплекс из нескольких введений препарата входит в обязательный календарь вакцинации по всему миру. В клинике «СМ-Доктор» имеются безопасные и эффективные вакцины, которые помогут сформировать стойкий иммунитет к заболеванию.
Комплекс из нескольких введений препарата входит в обязательный календарь вакцинации по всему миру. В клинике «СМ-Доктор» имеются безопасные и эффективные вакцины, которые помогут сформировать стойкий иммунитет к заболеванию.Прививка от ветрянки (ветряной оспы) не входит в стандартный график вакцинации детей в России. Ее делают по желанию родителей, которые хотят защитить ребенка от малоприятной инфекции. За рубежом иммунизацию проводят в обязательном порядке. В клинике «СМ-Доктор» в Москве Вы можете сделать прививку от ветрянки по доступной цене с использованием вакцин, безопасных для детей и взрослых.
Вакцинация против кори входит в календарь обязательных для детей прививок и проводится, согласно графику.
 Только благодаря этому удается держать заболевание под контролем и избегать масштабных эпидемий. Клиника «СМ-Доктор» приглашает всех детей сделать прививку от кори качественной вакциной, помните, цена пренебрежения может быть очень высокой.
Только благодаря этому удается держать заболевание под контролем и избегать масштабных эпидемий. Клиника «СМ-Доктор» приглашает всех детей сделать прививку от кори качественной вакциной, помните, цена пренебрежения может быть очень высокой.Прививка от пневмококковой инфекции (пневмококка) вошла в график обязательной вакцинации детей сравнительно недавно – в 2014 году. С тех пор количество простудных заболеваний и их осложнений в детских садах и школах существенно сократилось. В клинике «СМ-Доктор» всегда в наличии качественные и безопасные вакцины от пневмококка, которые подходят для детей первого года жизни и формируют стойкий иммунитет.
Прививка от менингококковой инфекции не входит в обязательный график вакцинации детей, однако цена пренебрежения ей может быть очень высока.
 Заражение вполне может привести к тяжелейшим последствиям вплоть до летального исхода в течение нескольких часов. В клинике «СМ-Доктор» всегда есть в наличии качественные и безопасные вакцины, которые надежно защитят малыша от опасности.
Заражение вполне может привести к тяжелейшим последствиям вплоть до летального исхода в течение нескольких часов. В клинике «СМ-Доктор» всегда есть в наличии качественные и безопасные вакцины, которые надежно защитят малыша от опасности.Прививка от столбняка входит в стандартный график вакцинации детей. Она дает возможность обезопасить малыша от опасного заболевания, которым можно заразиться даже через небольшую царапину. В клинике «СМ-Доктор» Вы всегда можете пройти плановую или экстренную вакцинацию в соответствии с показаниями.
Прививка против дифтерии назначается каждому ребенку в соответствии с календарем вакцинации.
 Она позволяет предотвратить заражение опасной инфекцией и ее дальнейшую передачу.
Она позволяет предотвратить заражение опасной инфекцией и ее дальнейшую передачу.Прививка от коклюша входит в календарь иммунизации детей. Она вводится несколько раз в составе комплексной вакцины и формирует стойкий иммунитет. В клинике «СМ-Доктор» доступны препараты для вакцинации от коклюша, дифтерии и столбняка, а также других опасных инфекций.
Прививка от краснухи входит в стандартный календарь вакцинации детей. Большинство малышей переносят ее очень легко и в результате получают стойкий иммунитет к заболеванию, особенно опасному для беременных женщин.
Прививка от ротавируса (ротавирусной инфекции) предназначена для детей первых месяцев жизни.
 Ее введение не является обязательным, но многочисленные исследования доказали, что своевременная вакцинация надежно защищает малыша от тяжелого гастроэнтерита, вызванного вирусом.
Ее введение не является обязательным, но многочисленные исследования доказали, что своевременная вакцинация надежно защищает малыша от тяжелого гастроэнтерита, вызванного вирусом.
Прививка АКДС в Одинцово и Звенигороде, сделать прививку АКДС детям и взрослым
Чем опасны болезни?
Столбняк поражает нервную систему, вызывает напряжение в мышцах и судороги. Это острое инфекционное заболевание передается через раны, порезы, повреждения тканей и является смертельно опасным для человека.
Коклюшем можно заразиться воздушно-капельным путем. Основным симптомом является спазматический мучительный кашель, а также катаральные симптомы. Коклюшем болеют и взрослые, и дети, но у детей он протекает значительно тяжелее (в раннем возрасте приступ кашля может сопровождаться остановкой дыхания).
Дифтерия – инфекционное заболевание, которое наносит удар по дыхательным путям, поражая слизистую, провоцируя образование плотных фиброзных пленок, способных вызвать удушье и смерть. Высока опасность паралича и асфиксии гортани, почечной недостаточности, поражения сердечной мышцы. Заболеть могут как дети, так и взрослые.
Высока опасность паралича и асфиксии гортани, почечной недостаточности, поражения сердечной мышцы. Заболеть могут как дети, так и взрослые.
Схема вакцинации АКДС
Первая прививка АКДС детям рекомендована по достижении трех месяцев, две последующие делают через каждые полтора месяца (в 4,5 месяцев и 6 месяцев). В полтора года вакцинация ребенка завершается ещё одной прививкой (если нарушены сроки прививок, то через 12-13 месяцев после последней вакцинации АКДС вакциной). Если интервалы между прививками нужно увеличить (по медицинским показаниям или иным причинам), то очередную прививку следует проводить в ближайший срок, определяемый состоянием здоровья ребёнка.
Прививка АКДС в «ВЕРАМЕД»
Если вам нужно сделать прививку АКДС, вы можете обратиться в наши медицинские центры в Одинцово или Звенигороде, где компетентные специалисты помогут вам спланировать график прививок и подберут нужную вакцину.
В МЦ «ВЕРАМЕД» представлены препараты «Пентаксим», «Инфанрикс», «Инфанрикс Гекса», признанные высококачественными импортными разновидностями отечественной вакцины АКДС. Чтобы понять, какая вакцина предпочтительнее для вашего ребенка, нужно проконсультироваться с врачом.
Чтобы понять, какая вакцина предпочтительнее для вашего ребенка, нужно проконсультироваться с врачом.
Сертифицированные препараты помогут достичь необходимой напряженности иммунитета к возбудителям опасных заболеваний. И что немаловажно – для этого не нужно ждать в очередях и опасаться, что цена вакцины ударит по семейному бюджету. Постоянно повышая качество медицинских услуг, мы сохраняем приемлемые цены и предоставляем скидки социально незащищенной категории граждан.
Прививки первого года жизни | Сургутская городская клиническая поликлиника № 4
Возраст ребенка | Тип вакцины |
Новорожденные дети (первые 12 часов после рождения) | Делается первая прививка от вирусного гепатита В. |
Новорожденные дети (первые 3-7 дней после рождения) | Прививка против туберкулеза — БЦЖ (сокращение от Бацилла Кальметта — Герена).
|
1 месяц | 2ая прививка против вирусного гепатита B. |
2 месяца | 1ая вакцина против пневмококковой инфекции у детей. 3я прививка против вирусного гепатита В. |
3 месяца | Первая прививка против дифтерии, коклюша, столбняка — прививка АКДС + прививка от полиомиелита. Первая вакцинация против гемофильной инфекции у детей. |
4,5 месяца | 2ая прививка против дифтерии, коклюша, столбняка — АКДС + прививка полиомиелита. 2ая вакцина против гемофильной инфекции. 2я прививка против пневмококковой инфекции. |
6 месяцев | 3я прививка против дифтерии, коклюша, столбняка — АКДС + прививка от полиомиелита. 3я вакцинация против вирусного гепатита B. 3я вакцинация против гемофильной инфекции. |
12 месяцев | Прививка против кори, краснухи и паротита. |
Какие могут быть противопоказания при проведении прививок?
Факторы, которые могут стать причиной отмены или переноса прививки, делятся на абсолютные и относительные. Абсолютными считаются факторы, при которых проведение прививки является опасным для жизни и здоровья. К ним относятся:
- Тяжелые аллергические реакции на препарат – отеки и покраснения размером больше 8 см в области укола, повышение температуры до 40 ºС, анафилактический шок, судороги.
- Иммунодефицит. В этом случае возможна замена препаратов с живыми возбудителями инактивированными препаратами. Однако следует помнить, что эффективность последних может быть ниже.
К относительным факторам относят те, при которых вакцинация может быть небезопасной или не принесет эффекта:
- ОРВИ. Прививку рекомендуется перенести до выздоровления.
- Заболевания сердца, почек, диабет.
 Прививку можно проводить только после разрешения специалиста.
Прививку можно проводить только после разрешения специалиста. - Недоношенность. Обычно прививку можно проводить после набора ребенком нормального веса.
Следует иметь в виду, что такие реакции, как небольшое покраснение, болезненность и припухлость в места укола, повышение температуры, являются нормальными и проходят спустя несколько дней после процедуры. Также после прививок от кори и краснухи могут наблюдаться слабые симптомы, характерные для этих заболеваний – сыпь, насморк и кашель.
Почему же стоит сделать прививку малышу.
Гепатит B
Острое вирусное заболевание, поражающее печень. Оно опасно, прежде всего, своими осложнениями, такими, как цирроз. Прививка от гепатита обычно делается уже в первый день жизни. Препарат для вакцинации состоит из белков вируса гепатита B. На первом году жизни проводится от трех до четырех процедур, которые защищают организм вплоть до восьмилетнего возраста.
Есть две категории детей – те, которые находятся в группе риска, и все остальные.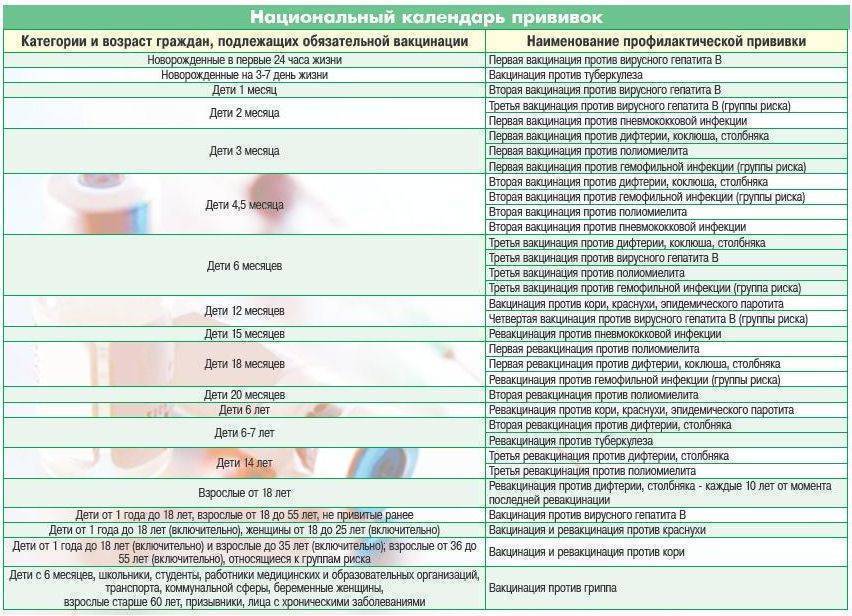 Обычно детям делают три процедуры. К группе риска относятся дети, чьи матери болеют гепатитом или являются вирусоносителями. Для них предусмотрен ускоренный график по сравнению с обычными детьми и добавлена дополнительная четвертая процедура.
Обычно детям делают три процедуры. К группе риска относятся дети, чьи матери болеют гепатитом или являются вирусоносителями. Для них предусмотрен ускоренный график по сравнению с обычными детьми и добавлена дополнительная четвертая процедура.
Туберкулез
Тяжелая хроническая болезнь, поражающая в первую очередь легкие и дающая осложнения на костные ткани и мозг. В препарате для вакцинации содержатся ослабленные бактерии бычьего туберкулеза, не вызывающие у человека заболевания. В первый год жизни проводится единственная прививка, которая дает иммунитет до семилетнего возраста. Недоношенным или имеющим малый вес детям проводится вакцинирование при помощи специальной педиатрической версии препарата, содержащей меньшее количество бактерий. В том случае, если иммунитет оказывается слишком слабым (что определяется при помощи пробы Манту), то после года проводится повторная прививка.
Коклюш, дифтерия и столбняк
Эти болезни опасны теми токсинами, которые вырабатывают микроорганизмы-возбудители. Смертность среди новорожденных от этих заболеваний чрезвычайно высока. Против этих болезней разработан комплексный препарат (АКДС), содержащий токсины дифтерии и столбняка в небольшой концентрации и инактивированную коклюшную палочку. Эти компоненты позволяют организму выработать иммунитет к болезням. Первая процедура вакцинации против этих заболеваний проводится в самом начале четвертого месяца жизни, а последняя – в возрасте шести месяцев. Всего в первый год жизни должно быть сделано три процедуры.
Смертность среди новорожденных от этих заболеваний чрезвычайно высока. Против этих болезней разработан комплексный препарат (АКДС), содержащий токсины дифтерии и столбняка в небольшой концентрации и инактивированную коклюшную палочку. Эти компоненты позволяют организму выработать иммунитет к болезням. Первая процедура вакцинации против этих заболеваний проводится в самом начале четвертого месяца жизни, а последняя – в возрасте шести месяцев. Всего в первый год жизни должно быть сделано три процедуры.
Гемофильная инфекция
Острое заболевание, вызываемое гемофильной палочкой. Оно поражает ЦНС, органы дыхания и может приводить к возникновению очагов гноя. Препарат для вакцинации от гемофильной инфекции содержит погибшие микроорганизмы, не вызывающие заболевания. В течение первого года делается три прививки от гемофильной инфекции.
Полиомиелит
Тяжелое инфекционное заболевание, поражающее центральную нервную систему, эндокринную систему, ЖКТ. Для болезни характерна высокая летальность. Одним из осложнений полиомиелита является паралич. Существует два варианта вакцины от полиомиелита. Один из них содержит живые, но ослабленные вирусы полиомиелита, а другой (инактивированный) – лишь белки вирусов. Первые две вакцинации проводятся инактивированным препаратом, а далее используется живая оральная полиовакцина. В течение первого года проводятся три процедуры вакцинации от полиомиелита, которые формируют иммунитет до десятилетнего возраста.
Для болезни характерна высокая летальность. Одним из осложнений полиомиелита является паралич. Существует два варианта вакцины от полиомиелита. Один из них содержит живые, но ослабленные вирусы полиомиелита, а другой (инактивированный) – лишь белки вирусов. Первые две вакцинации проводятся инактивированным препаратом, а далее используется живая оральная полиовакцина. В течение первого года проводятся три процедуры вакцинации от полиомиелита, которые формируют иммунитет до десятилетнего возраста.
Корь, краснуха, паротит
Протекают у детей в тяжелой форме и опасны своими осложнениями. В препарате для вакцинации содержатся ослабленные вирусы-возбудители. От них невозможно заразиться, но их введение вызывает полноценную ответную иммунную реакцию организма. Препарат вводится один раз в возрасте одного года. Действие продолжается до пяти лет.
Детская вакцинация
Для чего детям нужны прививки?
Вакцинация или прививка – это введение в организм ребенка антигенов микроорганизмов- возбудителей заболеваний. В ответ на это иммунная система активно вырабатывает антитела. Впоследствии при встрече с живым микробом организм встречает его «во всеоружии», а значит ребенок не заболеет вовсе или перенесет заболевание в легкой форме.
В ответ на это иммунная система активно вырабатывает антитела. Впоследствии при встрече с живым микробом организм встречает его «во всеоружии», а значит ребенок не заболеет вовсе или перенесет заболевание в легкой форме.
Сейчас национальный календарь включает в себя прививки против следующих заболеваний: вирусный гепатит В, гемофильная и пневмококковая инфекции, грипп, дифтерия, коклюш, корь, краснуха, полиомиелит, столбняк, туберкулез, эпидемический паротит (свинка).
Помимо профилактических существуют прививки постконтактные: те, которые делаются в первые часы или дни после доказанного контакта с инфекцией. Таким образом можно защититься от гепатита А и В, кори, столбняка и ветряной оспы.
Как подготовить ребенка к прививке?
Чтобы свести к минимуму риск возможных осложнений после проведения прививки нужно соблюдать несколько простых правил:
- Прививать допустимо только здорового ребенка. Убедитесь в том, что у ребенка не повышена температура, отсутствуют катаральные явления (насморк, кашель, покраснение горла), нет сыпи, поведение малыша не отличается от обычного (если ребенок капризен, плохо спит, отказывается от еды – это может быть первыми признаками начинающейся болезни).

- За несколько дней до прививки нужно сдать анализы крови и мочи.
- Если ребенок склонен к аллергии, за пару дней до прививки стоит начать давать ему антигистаминный препарат.
- Нежелательно делать прививку АКДС в жаркое время года.
- За сутки до вакцинации не давайте малышу аллергенных продуктов, грудничкам не вводите новые виды прикорма, соблюдайте питьевой режим. Не кормите ребенка за час до прививки.
- Попросите медсестру показать вам вакцину в нераспечатанном виде.
- Постарайтесь отвлечь малыша, возьмите с собой его любимую игрушку.
Что делать после прививки?
Несколько советов:
- Не уходите домой сразу после прививки, подождите полчаса, чтобы удостовериться, что у ребенка нет аллергической реакции. Лучше не сидеть в коридоре, а погулять это время рядом с клиникой.
- Не кормите ребенка хотя бы час после вакцинации, но обязательно давайте ему пить, лучше всего не соки, а обычную воду.

- Как минимум три дня воздержитесь от аллергенных продуктов, изменений в питании ребенка.
- В день прививки ограничьте контакт малыша с водой, в последующие дни купайте его как обычно.
- Гулять с ребенком можно и нужно!
- Желательно на несколько дней ограничить контакты ребенка с другими детьми. Если есть возможность, не водите его пару дней в детский сад.
Если возникли поствакцинальные осложнения
После проведения прививки у малыша могут появиться некоторые нежелательные реакции, в том числе:
- Боль, припухлость и покраснение в месте укола.
- Повышение температуры тела
- Общее недомогание
Такие симптомы считаются нормой, не требуют специального лечения и бесследно проходят спустя 2-3 дня.
Незамедлительно обратиться к врачу нужно, если:
- Краснота и отек в месте прививки увеличиваются день от дня.
- Температура выше 39 и плохо сбивается жаропонижающими.

- Ребенок жалуется на головную боль.
- Общее состояние малыша сильно нарушено.
- Эти симптомы сохраняются более трех дней.
При введении «живых» вакцин у ребенка могут наблюдаться так называемые отсроченные реакции:
- через 7-14 дней при введении вакцины от кори
- 11-23 дня от паротита (свинки)
- 7 дней от краснухи
При появлении таких реакций вы можете наблюдать у ребенка «мини-болезнь», то есть симптомы будут похожи на соответствующее заболевание, только слабо выраженное и проходящее без лечения в короткие сроки.
Более серьезные осложнения от введения вакцин бывают крайне редко (примерно 1 случай на миллион).
Случается, что за реакцию на прививку родители принимают самостоятельное заболевание. Здесь уместно вспомнить известное высказывание: «после» не значит «поэтому». Если через несколько дней после прививки ребенок заболел, это вовсе не обязательно связано с введением вакцины. В любом случае обратитесь к доктору за правильным диагнозом.
В любом случае обратитесь к доктору за правильным диагнозом.
В каких случаях вакцинация противопоказана
Перечень противопоказаний к прививкам невелик. Это, прежде всего, аллергия к компонентам вакцины, ранее уже возникавшая острая реакция на эту вакцину и заболевания в остром периоде.
Во всех остальных случаях вопрос о возможности вакцинации ребенка решает врач.
Чаще всего нежелательные реакции вызывает вакцина АКДС (коклюш, дифтерия, столбняк). Возможно, стоит подумать над заменой, например, использовать «Пентаксим».
И в заключение еще два совета:
- Постарайтесь найти врача, который отнесется к вашему ребенку со всем вниманием, как к личности, а не «человеку из очереди».
- Изучите информацию о вакцинах и примите осознанное решение о том, где, когда и какой вакциной привить вашего малыша.
Записаться на прививку
Здоровья вам и вашим детям!
Вакцинация БЦЖ у детей, инфицированных ВИЧ . Этот риск намного выше среди ВИЧ-инфицированных детей, а данные о защитной эффективности БЦЖ у ВИЧ-инфицированных детей отсутствуют. Недавние исследования безопасности вакцины БЦЖ для ВИЧ-инфицированных младенцев привели к изменениям в политике, но их реализация является сложной задачей.Необходимы новые подходы к профилактике туберкулеза среди младенцев и детей, особенно ВИЧ-инфицированных младенцев. В этом документе кратко рассматриваются вопросы безопасности и эффективности БЦЖ у ВИЧ-инфицированных младенцев и обсуждаются другие подходы к профилактике ТБ, включая новые противотуберкулезные вакцины и стратегии вакцинации.
Этот риск намного выше среди ВИЧ-инфицированных детей, а данные о защитной эффективности БЦЖ у ВИЧ-инфицированных детей отсутствуют. Недавние исследования безопасности вакцины БЦЖ для ВИЧ-инфицированных младенцев привели к изменениям в политике, но их реализация является сложной задачей.Необходимы новые подходы к профилактике туберкулеза среди младенцев и детей, особенно ВИЧ-инфицированных младенцев. В этом документе кратко рассматриваются вопросы безопасности и эффективности БЦЖ у ВИЧ-инфицированных младенцев и обсуждаются другие подходы к профилактике ТБ, включая новые противотуберкулезные вакцины и стратегии вакцинации.
1. Введение
По оценкам, во всем мире ежегодно вводится более 100 миллионов доз вакцины БЦЖ [1]. Однако точный характер защиты от туберкулеза после вакцинации БЦЖ полностью не выяснен.Эффективность и безопасность вакцины в контексте ВИЧ-инфекции вызывает споры и является предметом значительных недавних и текущих исследований. Такие исследования имеют большое значение для глобального общественного здравоохранения, поскольку эндемичные по ТБ районы часто совпадают с районами с высокой распространенностью ВИЧ, а коинфекция ВИЧ / ТБ распространена как среди взрослых, так и среди детей. В период с 2004 по 2006 год заболеваемость туберкулезом среди ВИЧ-инфицированных младенцев в Кейптауне, Южная Африка, составляла 1596 на 100 000 по сравнению с 66 на 100 000 среди младенцев, не инфицированных ВИЧ [2].Младенцы и дети раннего возраста, контактирующие с больными туберкулезом взрослых, подвержены высокому риску развития тяжелых и сложных форм туберкулеза. Диагностические трудности и сложность, связанные с клиническим ведением детей грудного и младшего возраста с сочетанной инфекцией, увеличивают масштабы педиатрической проблемы. Существует острая необходимость в безопасных и эффективных стратегиях профилактики туберкулеза у младенцев и детей, особенно у ВИЧ-инфицированных.
В период с 2004 по 2006 год заболеваемость туберкулезом среди ВИЧ-инфицированных младенцев в Кейптауне, Южная Африка, составляла 1596 на 100 000 по сравнению с 66 на 100 000 среди младенцев, не инфицированных ВИЧ [2].Младенцы и дети раннего возраста, контактирующие с больными туберкулезом взрослых, подвержены высокому риску развития тяжелых и сложных форм туберкулеза. Диагностические трудности и сложность, связанные с клиническим ведением детей грудного и младшего возраста с сочетанной инфекцией, увеличивают масштабы педиатрической проблемы. Существует острая необходимость в безопасных и эффективных стратегиях профилактики туберкулеза у младенцев и детей, особенно у ВИЧ-инфицированных.
2. Эффективность вакцины БЦЖ
Клиническая эффективность вакцины измеряется в процентах снижения заболеваемости среди вакцинированных лиц, связанного с вакцинацией.Эффективность представляет собой совокупный результат трех событий: (1) доля вакцины, «принятая», (2) степень защиты вакцины и (3) продолжительность защитного иммунитета [3].
Исследованию эффективности БЦЖ препятствовала невозможность определить надежный клинический или иммунологический параметр, указывающий на защиту от развития туберкулеза после вакцинации БЦЖ. Ни наличие рубца БЦЖ, ни реактивность кожной туберкулиновой пробы не коррелируют с защитой от туберкулеза [4].
В попытке лучше понять иммунитет, индуцированный БЦЖ, исследователи описали природу иммунных ответов после вакцинации БЦЖ и латентной инфекции ТБ. У многих людей вакцинация БЦЖ способна вызывать полифункциональный Т-клеточный ответ, в котором преобладают клетки, способные продуцировать цитокины 1 типа (включая интерферон- (IFN-) гамма, интерлейкин- (IL-) 2 и фактор некроза опухоли (TNF)) [ 5].
Были также попытки определить специфические иммунные дефекты у лиц, которые очень восприимчивы к развитию туберкулеза или осложнений после вакцинации живой ослабленной БЦЖ, включая ВИЧ-инфицированных лиц и младенцев с первичными иммунодефицитными расстройствами [3].Было показано, что среди ВИЧ-инфицированных младенцев, не получающих антиретровирусную терапию, БЦЖ вызывает гораздо более низкую частоту и качество специфических Т-лимфоцитов CD4, чем у ВИЧ-неинфицированных младенцев, и это сохраняется в течение первого года жизни [6].![]() Шестинедельные контактировавшие с ВИЧ (рожденные от ВИЧ-инфицированных матерей), но неинфицированные младенцы, получившие БЦЖ при рождении, имели более низкие ответы IFN-гамма, чем младенцы, не подвергавшиеся воздействию ВИЧ [7]. У детей, получающих антиретровирусную терапию, возможно восстановление антимикобактериального иммунного ответа [8].Лица с генетическими нарушениями пути цитокинов IFN-гамма особенно предрасположены к развитию активного ТБ [9].
Шестинедельные контактировавшие с ВИЧ (рожденные от ВИЧ-инфицированных матерей), но неинфицированные младенцы, получившие БЦЖ при рождении, имели более низкие ответы IFN-гамма, чем младенцы, не подвергавшиеся воздействию ВИЧ [7]. У детей, получающих антиретровирусную терапию, возможно восстановление антимикобактериального иммунного ответа [8].Лица с генетическими нарушениями пути цитокинов IFN-гамма особенно предрасположены к развитию активного ТБ [9].
Крупные рандомизированные клинические испытания предоставили данные об эффективности БЦЖ. Было показано, что у младенцев, не инфицированных ВИЧ, введение разовой дозы вакцины Bacillus Calmette-Guérin (БЦЖ) при рождении или вскоре после рождения обеспечивает примерно 80% защиту от диссеминированных форм ТБ (милиарный туберкулез и туберкулезный менингит) в младенчестве [ 10–12]. БЦЖ менее эффективна и вариабельна в профилактике легочного туберкулеза у младенцев и взрослых с эффективностью от 0% до 80%, о которой сообщалось в клинических испытаниях в прошлом веке [12]. Эти данные свидетельствуют о том, что БЦЖ вряд ли будет эффективна в предотвращении заражения M. tuberculosis , но может предотвратить прогрессирование инфекции в заболевание, особенно диссеминированные формы туберкулеза. Поскольку диссеминированное заболевание чаще встречается среди детей раннего возраста и связано с высокой заболеваемостью и смертностью, вакцинация новорожденных БЦЖ может быть рентабельной в качестве педиатрического вмешательства, но мало влияет на передачу ТБ среди взрослых [3]. Факторы, которые, как считается, влияют на вариабельность защиты, включают вариацию штамма БЦЖ, дозу вакцины, возраст пациента на момент вакцинации, статус питания, генетические факторы хозяина, микобактериальные и глистные инфекции окружающей среды и географическое положение [13–15].
Эти данные свидетельствуют о том, что БЦЖ вряд ли будет эффективна в предотвращении заражения M. tuberculosis , но может предотвратить прогрессирование инфекции в заболевание, особенно диссеминированные формы туберкулеза. Поскольку диссеминированное заболевание чаще встречается среди детей раннего возраста и связано с высокой заболеваемостью и смертностью, вакцинация новорожденных БЦЖ может быть рентабельной в качестве педиатрического вмешательства, но мало влияет на передачу ТБ среди взрослых [3]. Факторы, которые, как считается, влияют на вариабельность защиты, включают вариацию штамма БЦЖ, дозу вакцины, возраст пациента на момент вакцинации, статус питания, генетические факторы хозяина, микобактериальные и глистные инфекции окружающей среды и географическое положение [13–15].
Данные о защитной эффективности БЦЖ среди ВИЧ-инфицированных очень ограничены, поскольку большинство крупных исследований эффективности БЦЖ проводилось до начала пандемии ВИЧ. У ВИЧ-инфицированных взрослых вакцинация БЦЖ не показала статистически значимого эффекта в предотвращении легочного или диссеминированного туберкулеза [16]. Сообщалось о нескольких исследованиях с участием детей. В замбийском ретроспективном исследовании случай-контроль сообщалось об отсутствии защитного эффекта БЦЖ у 116 случаев ТБ и 154 контрольных больных без ТБ; напротив, защитный эффект 59% (OR 0.41, 95% ДИ 0,18–0,92) вакцинации БЦЖ было обнаружено у детей, не инфицированных ВИЧ [17]. Другое ретроспективное исследование, проведенное в Аргентине, показало, что у ВИЧ-инфицированных детей, вакцинированных БЦЖ, не было значительно более низкой заболеваемости ТБ по сравнению с невакцинированными детьми в течение 12-летнего периода наблюдения (Аннотация WeOa0104, третья конференция IAS по патогенезу и лечению ВИЧ, 2005 г., [ 18]).
Сообщалось о нескольких исследованиях с участием детей. В замбийском ретроспективном исследовании случай-контроль сообщалось об отсутствии защитного эффекта БЦЖ у 116 случаев ТБ и 154 контрольных больных без ТБ; напротив, защитный эффект 59% (OR 0.41, 95% ДИ 0,18–0,92) вакцинации БЦЖ было обнаружено у детей, не инфицированных ВИЧ [17]. Другое ретроспективное исследование, проведенное в Аргентине, показало, что у ВИЧ-инфицированных детей, вакцинированных БЦЖ, не было значительно более низкой заболеваемости ТБ по сравнению с невакцинированными детьми в течение 12-летнего периода наблюдения (Аннотация WeOa0104, третья конференция IAS по патогенезу и лечению ВИЧ, 2005 г., [ 18]).
Такие ретроспективные эпидемиологические исследования ограничены потенциальной систематической ошибкой из-за нестандартных критериев диагностики туберкулеза, потенциальных практик селективной вакцинации БЦЖ и плохой документации вакцинации БЦЖ или использования рубца БЦЖ для обозначения вакцинации БЦЖ, которая, как сообщается, реже у ВИЧ-инфицированных по сравнению с ВИЧ-неинфицированными детьми [19].
Перспектива проспективных рандомизированных исследований по оценке безопасности и эффективности вакцинации БЦЖ у ВИЧ-инфицированных и ВИЧ-инфицированных младенцев и детей осложняется описанными факторами: отсутствие клинических или иммунных коррелятов защиты, индуцированной БЦЖ, доказательства эффективности против диссеминированных форм туберкулеза у детей, не инфицированных ВИЧ, трудностей с диагностическими критериями заболевания туберкулезом у детей и того факта, что ВИЧ-статус младенцев неизвестен при рождении, то есть при введении вакцины БЦЖ в развивающихся странах.Дополнительной областью неопределенности является влияние раннего начала антиретровирусной терапии (АРТ) у младенцев на иммунитет, индуцированный БЦЖ, и потенциальная роль отсроченной вакцинации БЦЖ до наступления срока АРТ или ревакцинации.
3. Безопасность вакцины БЦЖ
Нормальное развитие местной кожной реакции после внутрикожной вакцинации БЦЖ включает развитие эритематозного пятна (через 3 недели после вакцинации), образование папулы (через 6 недель), неглубокую язву ( на 10 недель) и заживление (на 14 недель).
До пандемии ВИЧ БЦЖ имела хорошие показатели безопасности: сообщалось в основном о незначительных реакциях, а серьезные побочные эффекты, как правило, ограничивались младенцами с первичными иммунодефицитными расстройствами, включая тяжелый комбинированный иммунодефицит (ТКИД), хроническую гранулематозную болезнь (ХГБ), синдром ДиДжорджи, IFN дефицит гамма-рецепторов и дефицит IL-12 [19]. По оценкам, местные нежелательные явления у младенцев возникают у <0,04% реципиентов вакцины, а диссеминированная болезнь БЦЖ - у <0.002% реципиентов вакцины [20, 21].
Более серьезное заболевание БЦЖ было описано у ВИЧ-инфицированных младенцев и даже у взрослого ВИЧ-инфицированного человека через 30 лет после вакцинации [22]. Последующее многоцентровое исследование показало, что риск диссеминированного БЦЖ-заболевания у ВИЧ-инфицированных взрослых с ослабленным иммунитетом, получивших вакцинацию БЦЖ в младенчестве, был очень низким [23]. Однако риск как местного, так и диссеминированного заболевания БЦЖ среди ВИЧ-инфицированных младенцев и детей стал серьезной проблемой для общественного здравоохранения.
Два дозорных исследования в Южной Африке, хотя и ретроспективные серии случаев, показали гораздо более высокую распространенность подтвержденной посевом отдаленной или диссеминированной болезни БЦЖ среди ВИЧ-инфицированных младенцев с ослабленным иммунитетом, еще не получающих АРТ, чем считалось ранее. Первое исследование выявило одно важное объяснение непризнания болезни БЦЖ. Лабораторный посев респираторного секрета (включая образцы промывания желудка) на туберкулез идентифицирует M. tuberculosis complex (который включает M.tuberculosis и M. bovis среди других), и дальнейшее видообразование обычно не проводится. В этом исследовании ученые выполнили дальнейшее видообразование комплекса M. tuberculosis в 183 культивируемых изолятах от 49 ВИЧ-инфицированных детей с диагнозом «туберкулез» [24]. Датский штамм M. bovis BCG был изолирован от пяти младенцев, у каждого из которых была выраженная иммуносупрессия. В группе из пяти младенцев у четырех был подмышечный лимфаденит, ипсилатеральный по отношению к месту вакцинации БЦЖ, у двух были признаки легочной болезни БЦЖ, а у двух — регионарная и легочная БЦЖ болезнь.
Второе исследование представляло собой ретроспективный обзор подтвержденной посевом БЦЖ болезни у детей младше 13 лет, диагностированной в течение трех лет [25]. Среди 25 детей 88% имели местное заболевание, 32% — отдаленное или диссеминированное заболевание, а 20% — оба заболевания. Семнадцать из 25 детей были ВИЧ-инфицированы, а двое имели другие иммунодефициты. Все восемь детей с отдаленным или диссеминированным заболеванием имели тяжелый иммунодефицит (шесть были ВИЧ-инфицированы), а уровень смертности в этой группе составил 75%.
Подходы к математическому моделированию оценивают риск распространения БЦЖ у ВИЧ-инфицированных младенцев в контексте Южной Африки в пределах от 329 до 417 на 100 000 получателей вакцины, при условии 95% охвата вакциной БЦЖ, распространенности ВИЧ среди беременных женщин 12,4–15,4% и уровень вертикальной передачи ВИЧ составляет 5% [26]. Это очень много.
Еще одно важное наблюдение заключается в том, что БЦЖ является относительно частой ассоциацией с воспалительным синдромом восстановления иммунитета (ВСВИ) среди младенцев и детей раннего возраста, начинающих АРТ. IRIS относится к возникновению парадоксального инфекционного или воспалительного состояния у пациента, выздоравливающего после тяжелого иммунодефицита [27]. «Разоблачение» туберкулеза после начала АРТ — одна из наиболее распространенных форм ВСВИ, описываемых у взрослых, тогда как БЦЖ-ВСВИ, проявляющаяся как «парадоксальная» форма синдрома, отмечалась у 3–14,8% детей, начинающих АРТ на Юге. Африканские и тайские когорты [28–30]. Обычное клиническое проявление BCG-IRIS — воспалительный ипсилатеральный подмышечный или регионарный лимфаденит с воспалением или формированием абсцесса в месте вакцинации или без него.Более молодой возраст и более высокая исходная вирусная нагрузка ВИЧ были определены как факторы риска развития BCG-IRIS [29]. Хотя подозрение на отдаленное или диссеминированное заболевание, особенно с поражением легких или костей, было описано в контексте BCG-IRIS, неясно, может ли диссеминация происходить на ранней стадии после вакцинации при рождении, но проявляться клинически только после начала АРТ в возрасте нескольких месяцев.
IRIS относится к возникновению парадоксального инфекционного или воспалительного состояния у пациента, выздоравливающего после тяжелого иммунодефицита [27]. «Разоблачение» туберкулеза после начала АРТ — одна из наиболее распространенных форм ВСВИ, описываемых у взрослых, тогда как БЦЖ-ВСВИ, проявляющаяся как «парадоксальная» форма синдрома, отмечалась у 3–14,8% детей, начинающих АРТ на Юге. Африканские и тайские когорты [28–30]. Обычное клиническое проявление BCG-IRIS — воспалительный ипсилатеральный подмышечный или регионарный лимфаденит с воспалением или формированием абсцесса в месте вакцинации или без него.Более молодой возраст и более высокая исходная вирусная нагрузка ВИЧ были определены как факторы риска развития BCG-IRIS [29]. Хотя подозрение на отдаленное или диссеминированное заболевание, особенно с поражением легких или костей, было описано в контексте BCG-IRIS, неясно, может ли диссеминация происходить на ранней стадии после вакцинации при рождении, но проявляться клинически только после начала АРТ в возрасте нескольких месяцев. .
.
Следует ли отложить вакцинацию БЦЖ при рождении младенцам, контактировавшим с ВИЧ, и вообще избегать вакцинации ВИЧ-инфицированных младенцев?
Как обсуждалось выше, клинические и иммунологические доказательства защитной эффективности вакцинации БЦЖ у ВИЧ-инфицированных младенцев отсутствуют, и существуют серьезные опасения относительно безопасности вакцины БЦЖ у ВИЧ-инфицированных младенцев как до, так и после начала АРТ.В 2007 году Глобальный консультативный комитет по безопасности вакцин (GACVS) Всемирной организации здравоохранения (ВОЗ) опубликовал пересмотренные рекомендации, противопоказавшие вакцинацию БЦЖ детям с ВИЧ-инфекцией [31].
Более актуальным является вопрос о том, следует ли вводить вакцину БЦЖ всем младенцам, в том числе младенцам, рожденным от ВИЧ-инфицированных матерей при рождении, или же следует отложить вакцинацию БЦЖ для младенцев, контактировавших с ВИЧ, до тех пор, пока ВИЧ-инфекционный статус не будет окончательно установлен вирусологическое тестирование в возрасте около 6 недель. Увеличение охвата мерами по сокращению передачи ВИЧ от матери к ребенку (включая профилактические антиретровирусные препараты для матери и ребенка или антиретровирусную терапию для матери и безопасное вскармливание младенцев) приводит к тому, что большинство младенцев, рожденных от ВИЧ-инфицированных матерей, в конечном итоге не инфицированы. Ожидается, что этим младенцам принесет пользу вакцинация БЦЖ без риска диссеминированного заболевания БЦЖ, наблюдаемого у ВИЧ-инфицированных младенцев. Отсрочка вакцинации БЦЖ с рождения до 10-недельного возраста может привести к усилению Т-клеточного ответа памяти CD4, включая полифункциональные Т-клетки, экспрессирующие IFN-γ , TNF- α и IL-2, при измерении в возрасте 1 года у ВИЧ -неинфицированные младенцы [32].Это также может быть применимо к неинфицированным младенцам, контактировавшим с ВИЧ, но необходимы дальнейшие лабораторные и клинические исследования.
Увеличение охвата мерами по сокращению передачи ВИЧ от матери к ребенку (включая профилактические антиретровирусные препараты для матери и ребенка или антиретровирусную терапию для матери и безопасное вскармливание младенцев) приводит к тому, что большинство младенцев, рожденных от ВИЧ-инфицированных матерей, в конечном итоге не инфицированы. Ожидается, что этим младенцам принесет пользу вакцинация БЦЖ без риска диссеминированного заболевания БЦЖ, наблюдаемого у ВИЧ-инфицированных младенцев. Отсрочка вакцинации БЦЖ с рождения до 10-недельного возраста может привести к усилению Т-клеточного ответа памяти CD4, включая полифункциональные Т-клетки, экспрессирующие IFN-γ , TNF- α и IL-2, при измерении в возрасте 1 года у ВИЧ -неинфицированные младенцы [32].Это также может быть применимо к неинфицированным младенцам, контактировавшим с ВИЧ, но необходимы дальнейшие лабораторные и клинические исследования.
Есть опасения, что практика выборочной отсрочки вакцинации может поставить под угрозу преимущества высоких показателей охвата вакциной БЦЖ в результате того, что контактировавшие с ВИЧ, но неинфицированные дети пропускают последующую вакцинацию после 6-недельного возраста. Рабочая группа BCG Секции здоровья легких детей Международного союза борьбы с туберкулезом и легочными заболеваниями опубликовала консенсусное заявление о соответствующих критериях, которые должны учитываться программами по ВИЧ / ТБ при рассмотрении введения отсрочки селективной вакцинации БЦЖ [33].К ним относятся: высокая посещаемость материнского тестирования на ВИЧ в сочетании с эффективными стратегиями профилактики передачи от матери ребенку (ППМР), включая АРТ матери; ранняя вирусологическая диагностика ВИЧ-инфекции у младенцев в сочетании с учреждением АРТ; координация программ ППМР, вакцинации и борьбы с туберкулезом для сведения к минимуму потерь для последующего наблюдения, реализации альтернативных стратегий профилактики туберкулеза и проведения успешной вакцинации после выборочной невакцинации при рождении. В настоящее время реализация стратегий селективной вакцинации неосуществима в большинстве стран, которые являются высокоэндемичными по ВИЧ и туберкулезу, и всеобщая вакцинация младенцев БЦЖ, вероятно, будет продолжаться в течение некоторого времени.
Рабочая группа BCG Секции здоровья легких детей Международного союза борьбы с туберкулезом и легочными заболеваниями опубликовала консенсусное заявление о соответствующих критериях, которые должны учитываться программами по ВИЧ / ТБ при рассмотрении введения отсрочки селективной вакцинации БЦЖ [33].К ним относятся: высокая посещаемость материнского тестирования на ВИЧ в сочетании с эффективными стратегиями профилактики передачи от матери ребенку (ППМР), включая АРТ матери; ранняя вирусологическая диагностика ВИЧ-инфекции у младенцев в сочетании с учреждением АРТ; координация программ ППМР, вакцинации и борьбы с туберкулезом для сведения к минимуму потерь для последующего наблюдения, реализации альтернативных стратегий профилактики туберкулеза и проведения успешной вакцинации после выборочной невакцинации при рождении. В настоящее время реализация стратегий селективной вакцинации неосуществима в большинстве стран, которые являются высокоэндемичными по ВИЧ и туберкулезу, и всеобщая вакцинация младенцев БЦЖ, вероятно, будет продолжаться в течение некоторого времени.
4. Другие способы защиты ВИЧ-инфицированных младенцев от туберкулеза
Раннее начало АРТ (особенно в возрасте до 12 недель) у ВИЧ-инфицированных младенцев, независимо от клинических критериев или критериев подсчета CD4, значительно снижает смертность и заболеваемость туберкулезом [34] и может снизить частоту и тяжесть BCG-IRIS, вероятно, в результате сохранения иммунитета (Аннотация 600, четырнадцатая конференция по ретровирусам и оппортунистическим инфекциям, 2008 г., [35]).
Рутинная предэкспозиционная профилактика изониазидом для всех ВИЧ-инфицированных младенцев (младше 12 месяцев) в настоящее время не рекомендуется ВОЗ по результатам двойного слепого рандомизированного плацебо-контролируемого исследования с участием 452 младенцев, которые не показали никаких преимуществ (38, Abstract G2-1346a, 48-я международная конференция по антимикробным препаратам и химиотерапии, 2008 г., [36]).Ранее опубликованное исследование показало значительное сокращение смертности и заболеваемости туберкулезом среди ВИЧ-инфицированных младенцев и детей, получающих профилактику изониазидом [37].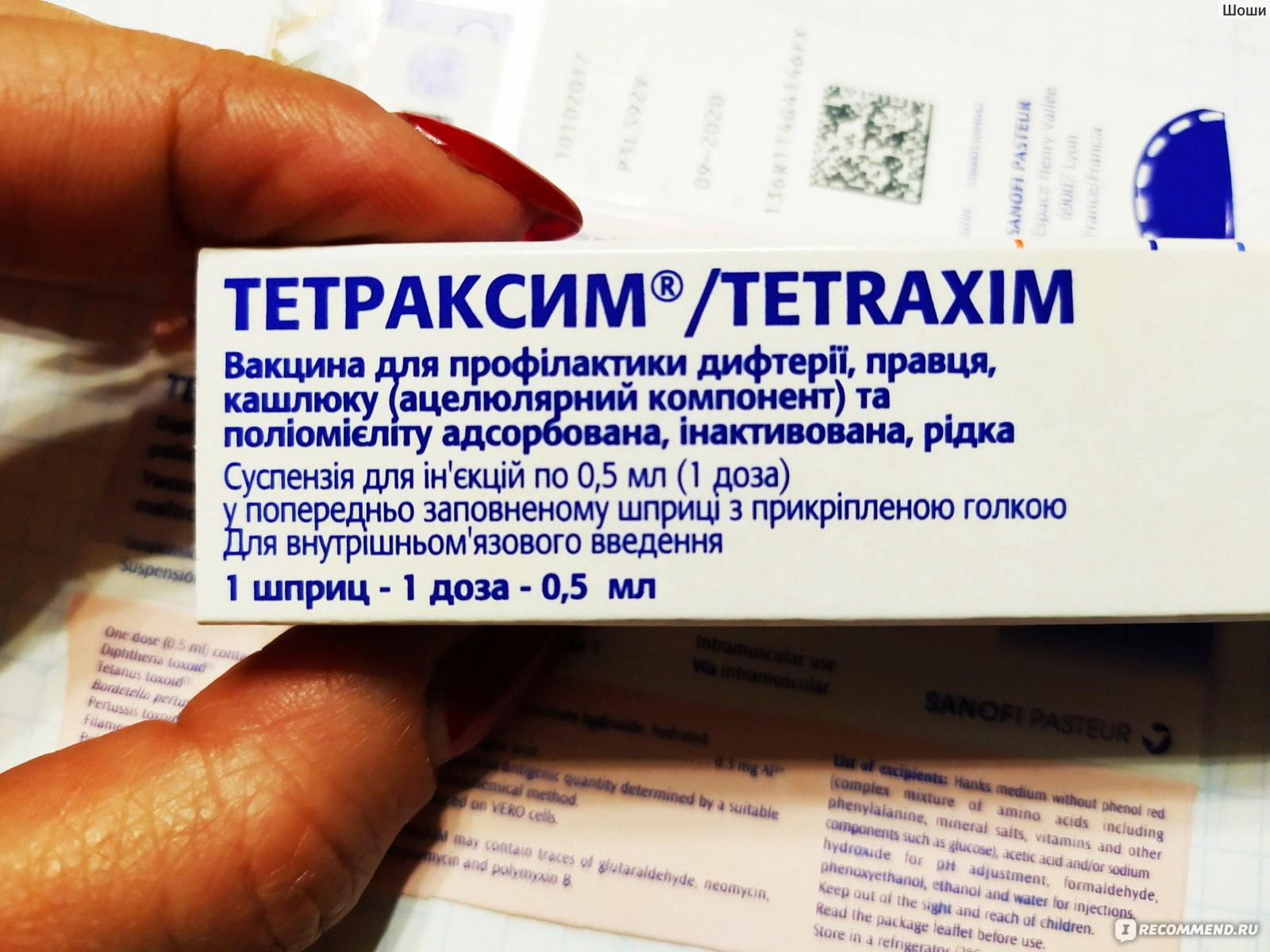 Недавние руководящие принципы ВОЗ рекомендуют шесть месяцев профилактической терапии изониазидом (ПЛИ) для ВИЧ-инфицированных детей любого возраста с контактом с источником инфекционного ТБ после исключения туберкулеза и шесть месяцев ПЛИ для ВИЧ-инфицированных детей в возрасте старше 12 месяцев. которые, как известно, не инфицированы туберкулезом [38].
Недавние руководящие принципы ВОЗ рекомендуют шесть месяцев профилактической терапии изониазидом (ПЛИ) для ВИЧ-инфицированных детей любого возраста с контактом с источником инфекционного ТБ после исключения туберкулеза и шесть месяцев ПЛИ для ВИЧ-инфицированных детей в возрасте старше 12 месяцев. которые, как известно, не инфицированы туберкулезом [38].
Введение вакцины БЦЖ ВИЧ-инфицированным младенцам или детям младшего возраста после начала АРТ и достижения некоторой степени восстановления иммунитета — еще один интересный подход, который еще не изучался подробно.Однако с учетом опасений по поводу безопасности живых вакцин в целом и БЦЖ в частности среди ВИЧ-инфицированных или лиц с иным ослабленным иммунитетом, а также пересмотренной рекомендации ВОЗ избегать применения БЦЖ у младенцев, контактировавших с ВИЧ, представляется маловероятным, что БЦЖ будет проходить проспективную оценку при ВИЧ. -инфицированные младенцы или дети.
Новые вакцины БЦЖ обладают значительными перспективами в среднесрочной и долгосрочной перспективе и могут в конечном итоге решить вопросы, связанные с эффективностью и безопасностью, на устойчивой основе. Достижения в области генетической технологии и секвенирования генома M. tuberculosis ( M. tb ) в 1990-е годы ускорили разработку новых кандидатных противотуберкулезных вакцин, и пять из них достигли стадии 1-й фазы испытаний на людях. Поскольку ВИЧ-инфицированные лица несут такую большую долю общего бремени ТБ, важной характеристикой идеальной противотуберкулезной вакцины является безопасность, иммуногенность и эффективность в профилактике ТБ у лиц с ВИЧ-инфекцией или СПИДом, включая детей.Живые аттенуированные микобактериальные вакцины, такие как БЦЖ, вероятно, будут вытеснены рекомбинантными векторными вакцинами или субъединичными вакцинами [39].
Достижения в области генетической технологии и секвенирования генома M. tuberculosis ( M. tb ) в 1990-е годы ускорили разработку новых кандидатных противотуберкулезных вакцин, и пять из них достигли стадии 1-й фазы испытаний на людях. Поскольку ВИЧ-инфицированные лица несут такую большую долю общего бремени ТБ, важной характеристикой идеальной противотуберкулезной вакцины является безопасность, иммуногенность и эффективность в профилактике ТБ у лиц с ВИЧ-инфекцией или СПИДом, включая детей.Живые аттенуированные микобактериальные вакцины, такие как БЦЖ, вероятно, будут вытеснены рекомбинантными векторными вакцинами или субъединичными вакцинами [39].
Новые вакцины необходимо тестировать на различных этапах естественного течения инфекции ТБ и развития болезни. Стратегии вакцинации включают прединфекционную вакцинацию, проводимую при рождении или вскоре после него (как в случае с БЦЖ), или в качестве ревакцинации после БЦЖ во время родов. Этот подход хорошо подходит для условий с тяжелым бременем ТБ, а метод бустинга имеет то преимущество, что потенциально повышает иммуногенность и эффективность БЦЖ, избегая при этом этической дилеммы полного отказа от БЦЖ. Недостатком метода повторной вакцинации после вакцинации БЦЖ является то, что сохраняются проблемы с безопасностью применения БЦЖ, особенно у ВИЧ-инфицированных младенцев.
Недостатком метода повторной вакцинации после вакцинации БЦЖ является то, что сохраняются проблемы с безопасностью применения БЦЖ, особенно у ВИЧ-инфицированных младенцев.
Другой подход — постинфекционная вакцинация после доказательства естественного заражения M. tb с целью повышения или повышения иммунитета и предотвращения прогрессирования туберкулеза. Этот подход, при условии, что вакцина безопасна, будет особенно актуален для ВИЧ-инфицированных, в том числе детей младшего возраста с высоким уровнем заражения и инфицирования ТБ и повышенным риском прогрессирования ТБ, включая тяжелые формы внелегочных заболеваний.Две рекомбинантные векторные вакцины (MVA85A и AERAS-402) исследуются для использования в качестве бустерных вакцин у лиц, примированных БЦЖ, и для постинфекционной вакцинации. Это наиболее вероятные вакцины-кандидаты и стратегии вакцинации, вокруг которых можно было бы разработать этически приемлемые клинические испытания среди младенцев и детей, в том числе тех, кто подвергается воздействию ВИЧ или инфицирован ВИЧ [39].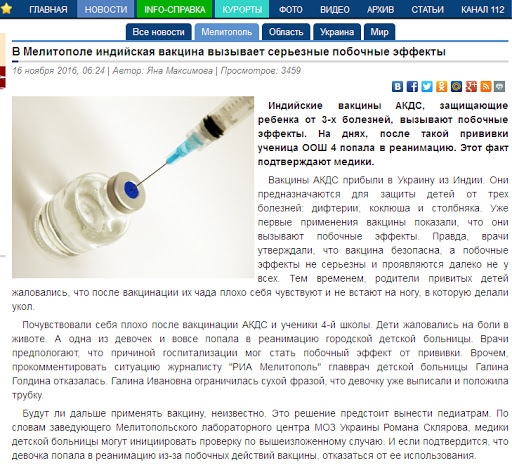
Лишь немногие из ведущих вакцин-кандидатов против туберкулеза до сих пор прошли клинические испытания на ВИЧ-инфицированных детях, однако эти две рекомбинантные векторные вакцины добились значительного прогресса в разработке вакцин.MVA85A состоит из модифицированной осповакцины Анкары (MVA), созданной с помощью генной инженерии для экспрессии M. tb антигена 85A [40]. Вакцины на основе MVA имеют хорошие показатели безопасности после широкого использования в эпоху искоренения оспы и в исследованиях кандидатных вакцин против ВИЧ [41, 42]. Ожидаются данные по безопасности и иммуногенности MVA85A у взрослых, инфицированных ВИЧ, инфицированных ТБ и ВИЧ-ТБ, а также у здоровых детей и младенцев (Хокридж А. в Proceedings of Tuberculosis Vaccines for the World Conference, 2006, см. [43]) .Вакцина AERAS-402 использует аденовирус серотипа 35, неспособный к репликации, но модифицированный для экспрессии слитого белка трех антигенов M. tb (85A, 85B и TB10.4). Она была разработана для использования в качестве бустерной вакцины у лиц, которым вводили БЦЖ, и вошла в клинические исследования на людях [39].
Субъединичная вакцина Mtb72F включает слитый белок двух иммуногенных белков M. tb , объединенный с адъювантом. Модификация, вакцина M72, оказалась безопасной и иммуногенной для здоровых взрослых добровольцев, хотя более реактогенна для людей, ранее подвергавшихся воздействию M.tb. Клинические испытания продолжаются в Европе и Южной Африке [39].
Проблемы, связанные с разработкой новых противотуберкулезных вакцин, включают ограниченное понимание защитных иммунных ответов против ТБ, трудности в выявлении латентной инфекции и дифференциации инфекции от болезни, трудности в определении клинических конечных точек испытаний и необходимость улучшения эпиднадзора за туберкулезом. заболеваемость и смертность в контексте крупных испытаний вакцины 3 фазы, проводившихся в течение многих лет [39].
Другая важная проблема связана с этическими проблемами, связанными с внедрением новой противотуберкулезной вакцины в контексте существующей, хотя и очень несовершенной вакцины (БЦЖ), которая обычно вводится всем новорожденным в эндемичных по ТБ странах. Вероятно, что немногие страны, если вообще какие-либо страны, успешно выполнили рекомендацию ВОЗ избегать вакцинации БЦЖ новорожденных, контактировавших с ВИЧ, до тех пор, пока окончательный ВИЧ-статус не будет установлен в возрасте 6 недель. С этической точки зрения, испытания вакцин с участием младенцев и детей, которые исключают вакцинацию БЦЖ в своей структуре, должны учитывать включение альтернативных мер профилактики ТБ, таких как обеспечение профилактической терапии изониазидом и рутинное раннее начало АРТ для ВИЧ-инфицированных младенцев и детей. , поскольку они, вероятно, станут стандартными вмешательствами.Поскольку новые противотуберкулезные вакцины, предназначенные для ВИЧ-инфицированных, вряд ли будут живыми аттенуированными вакцинами, ПЛИ вряд ли повлияет на меры иммуногенности вакцины, но может снизить риск развития активной формы ТБ у инфицированных ТБ лиц. Однако сохранение или восстановление иммунитета благодаря АРТ может повысить иммуногенность вакцины по сравнению с ВИЧ-инфицированными людьми, не получающими АРТ.
Вероятно, что немногие страны, если вообще какие-либо страны, успешно выполнили рекомендацию ВОЗ избегать вакцинации БЦЖ новорожденных, контактировавших с ВИЧ, до тех пор, пока окончательный ВИЧ-статус не будет установлен в возрасте 6 недель. С этической точки зрения, испытания вакцин с участием младенцев и детей, которые исключают вакцинацию БЦЖ в своей структуре, должны учитывать включение альтернативных мер профилактики ТБ, таких как обеспечение профилактической терапии изониазидом и рутинное раннее начало АРТ для ВИЧ-инфицированных младенцев и детей. , поскольку они, вероятно, станут стандартными вмешательствами.Поскольку новые противотуберкулезные вакцины, предназначенные для ВИЧ-инфицированных, вряд ли будут живыми аттенуированными вакцинами, ПЛИ вряд ли повлияет на меры иммуногенности вакцины, но может снизить риск развития активной формы ТБ у инфицированных ТБ лиц. Однако сохранение или восстановление иммунитета благодаря АРТ может повысить иммуногенность вакцины по сравнению с ВИЧ-инфицированными людьми, не получающими АРТ. Моральный императив включения таких вмешательств в испытания вакцин с участием ВИЧ-инфицированных младенцев и детей должен преобладать над другими соображениями.
Моральный императив включения таких вмешательств в испытания вакцин с участием ВИЧ-инфицированных младенцев и детей должен преобладать над другими соображениями.
5. Заключение
Вакцинация ВИЧ-инфицированных младенцев БЦЖ имеет неопределенную эффективность и связана со значительными проблемами безопасности у нелеченных младенцев и детей, получающих АРТ. Диагностика и лечение болезни БЦЖ сложны, что приводит к недооценке и неоптимальному уходу в условиях ограниченных ресурсов. Всеобщая иммунизация БЦЖ при рождении связана с высокими показателями охвата, тогда как выборочная отсрочка иммунизации БЦЖ до установления статуса ВИЧ-инфекции у младенцев создает риск значительного снижения охвата вакциной БЦЖ среди значительной части инфицированных ВИЧ, но не инфицированных младенцев.Универсальное раннее начало АРТ у ВИЧ-инфицированных младенцев в настоящее время может быть наиболее эффективным подходом к снижению риска как болезни БЦЖ, так и заболевания туберкулезом в этой группе. Профилактическая терапия изониазидом для младенцев и детей старшего возраста, контактировавших с ТБ, является важной дополнительной стратегией профилактики ТБ, в то время как новые вакцины БЦЖ с лучшими профилями безопасности и эффективности находятся в стадии исследования.
Профилактическая терапия изониазидом для младенцев и детей старшего возраста, контактировавших с ТБ, является важной дополнительной стратегией профилактики ТБ, в то время как новые вакцины БЦЖ с лучшими профилями безопасности и эффективности находятся в стадии исследования.
Дети, ВИЧ и СПИД | Avert
Во всем мире ежегодное число новых случаев инфицирования среди детей (0–14 лет) сократилось почти вдвое с 2010 года, при этом количество новых случаев ВИЧ-инфекции снизилось на 47%.С 1995 года, по оценкам, 1,6 миллиона новых случаев заражения ВИЧ среди детей было предотвращено благодаря предоставлению антиретровирусных препаратов (АРВ) женщинам, живущим с ВИЧ, во время беременности и кормления грудью. Подавляющее большинство этих инфекций (1,3 миллиона) удалось предотвратить в период с 2010 по 2015 год.
Несмотря на этот значительный прогресс, число детей, впервые инфицированных ВИЧ, остается неприемлемо высоким. В 2016 году 24% беременных женщин, живущих с ВИЧ, не имели доступа к АРВ-препаратам для предотвращения передачи инфекции их младенцам. В том же году около 160 000 детей заразились ВИЧ; это составляет 438 детей в день.
В том же году около 160 000 детей заразились ВИЧ; это составляет 438 детей в день.
В 2015 году в 21 стране с самым высоким бременем ВИЧ только 54% детей, инфицированных ВИЧ, прошли тестирование в течение рекомендованных двух месяцев. В следующем году около 1,8 миллиона детей жили с ВИЧ, но только 43% имели доступ к АРВ-препаратам. Хотя охват лечением улучшился с 2010 года, когда только 21% детей, живущих с ВИЧ, получали антиретровирусное лечение (АРТ), нынешняя ситуация означает, что около половины нуждающихся детей не имеют доступа.
Большинство детей, живущих с ВИЧ, живут в Африке, где СПИД остается основной причиной смерти среди подростков. В 2016 году во всем мире от болезней, связанных со СПИДом, умерло 120 000 детей. Это означает, что ежедневно умирает 328 человек. Фактически, дети в возрасте 0–4 лет, живущие с ВИЧ, имеют больше шансов умереть, чем люди, живущие с ВИЧ любого другого возраста. И это несмотря на сокращение на 62% случаев смерти от СПИДа среди этой возрастной группы во всем мире с 2000 года.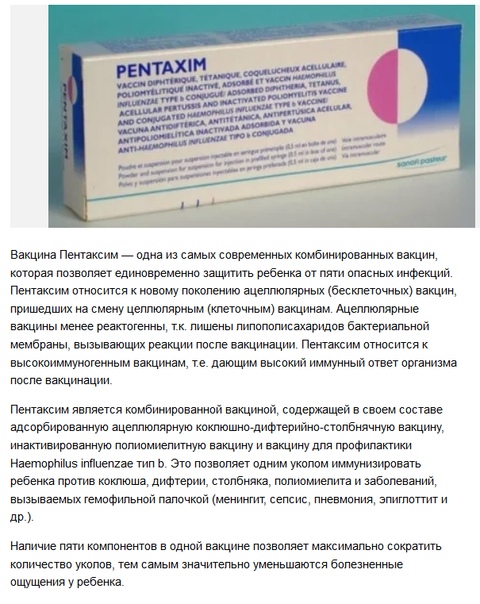
Кроме того, еще миллионы детей косвенно страдают от воздействия эпидемии ВИЧ на их семьи и сообщества.
Регулярное тестирование на ВИЧ, лечение, мониторинг и уход за детьми, живущими с ВИЧ, могут позволить им прожить долгую и полноценную жизнь. Однако отсутствие необходимых инвестиций и ресурсов для адекватного тестирования, педиатрических АРВ-препаратов и программ профилактики, ориентированных на детей, означает, что дети по-прежнему страдают от последствий эпидемии.
Передача от матери к ребенку (ПМР)
Большинство детей, живущих с ВИЧ, инфицированы в результате передачи от матери ребенку (ПМР), во время беременности, родов или кормления грудью.Иногда это называют «вертикальной передачей» или «передачей от родителей ребенку».
ПМР ВИЧ можно остановить, если будущие матери имеют доступ к услугам по профилактике передачи инфекции от матери ребенку (ППМР) во время беременности, родов и кормления грудью. Благодаря финансированию, обученному персоналу и ресурсам можно избежать новых инфекций среди многих тысяч детей.
Грудное вскармливание в настоящее время является причиной большинства ПМР. Когда кормление смесью не является жизнеспособным вариантом, женщины могут значительно снизить риск передачи ВИЧ своему ребенку на этой стадии, если они кормят исключительно грудью и получают АРТ.Однако в 2013 году только 49% женщин продолжали принимать АРВ-препараты во время грудного вскармливания по сравнению с 62% женщин, принимавших АРВ-препараты во время беременности и родов. Это подчеркивает острую необходимость в просвещении о важности продолжения послеродового лечения.
Без АРТ треть младенцев, заразившихся ВИЧ в результате ПМР, не доживет до первого дня рождения, а половина не доживет до второго дня рождения.
ВИЧ-инфекция в медицинских учреждениях / учреждениях здравоохранения
В настоящее время ВИЧ-инфекция встречается очень редко, но может возникнуть в медицинских учреждениях.Например, через иглы, которые не были стерилизованы, или через переливание крови, когда используется инфицированная кровь.
В 2012 году сообщалось, что за последнее десятилетие в Кыргызстане 270 детей были инфицированы ВИЧ в больницах в результате того, что врачи не соблюдали универсальные меры предосторожности во время медицинских процедур.
Сироты и уязвимые дети
Одно из самых разрушительных последствий ВИЧ — это потеря целых поколений людей в сообществах, наиболее пострадавших от эпидемии.В связи с этим чаще всего дети чувствуют наибольшее влияние потери родителей или старших родственников.
«Сирота» определяется Организацией Объединенных Наций как ребенок, который «потерял одного или обоих родителей». По оценкам, 13,4 миллиона детей и подростков (0-17 лет) во всем мире потеряли одного или обоих родителей из-за СПИДа по состоянию на 2015 год. Более 80% этих детей (10,9 миллиона) живут в странах Африки к югу от Сахары. В некоторых странах, сильно пострадавших от эпидемии, большой процент всех детей-сирот — например, 74% в Зимбабве и 63% в Южной Африке — стали сиротами из-за СПИДа.
Заметные успехи были достигнуты в смягчении экономического и социального воздействия ВИЧ и СПИДа на детей и семьи за последнее десятилетие. Тем не менее дети, осиротевшие из-за СПИДа или живущие с больными опекунами, по-прежнему сталкиваются с повышенным риском физического и эмоционального насилия по сравнению с другими детьми в странах Африки к югу от Сахары, включая других сирот. Это увеличивает уязвимость этих детей к ВИЧ.
Программы по борьбе с ВИЧ, ориентированные на сирот и уязвимых детей (иногда называемые OVC), являются жизненно важной стратегией для снижения уязвимости детей к ВИЧ.Эти программы нацелены на поддержку лиц, осуществляющих уход за детьми, часто старшего поколения, удержание детей в школе, защиту их юридических прав и прав человека и обеспечение удовлетворения их эмоциональных потребностей.
В июне 2011 года ЮНЭЙДС и Чрезвычайный план президента США по борьбе со СПИДом (PEPFAR) запустили «Глобальный план по искоренению новых случаев ВИЧ-инфекции среди детей к 2015 году и сохранению жизни их матерей» [pdf] вместе с 22 странами, которые: в то время на долю беременных женщин, живущих с ВИЧ, в мире приходилось 90%. Глобальный план стимулировал политическую волю и действия на глобальном и национальном уровнях, что привело к одним из самых впечатляющих и значительных достижений в истории борьбы с ВИЧ.
Глобальный план стимулировал политическую волю и действия на глобальном и национальном уровнях, что привело к одним из самых впечатляющих и значительных достижений в истории борьбы с ВИЧ.
Инициатива «Начни бесплатно, оставайся свободными, свободна от СПИДа», запущенная в 2016 году под руководством ЮНЭЙДС и ПЕПФАР, направлена на развитие прогресса, достигнутого в рамках Глобального плана по расширению услуг по профилактике, лечению, уходу и поддержке в связи с ВИЧ. для детей, подростков и молодых женщин. Инициатива направлена на усиление и усиление усилий, которые уже ускоряют прогресс, включая партнерство DREAMS, инициативу «Ускорение лечения детей от ВИЧ / СПИДа» и ALL-IN.
В этом подходе используется «подход жизненного цикла» к программированию, что означает, что он реагирует на меняющиеся контексты, с которыми люди сталкиваются в разном возрасте.
Инициатива «Начни бесплатно, оставайся свободными, свободна от СПИДа» состоит из трех частей:
- Start Free стремится завершить работу, начатую Глобальным планом, охватив 95% беременных женщин, живущих с ВИЧ, и обеспечить им пожизненное лечение от ВИЧ к 2018 году, а к 2018 году сократить число новых инфицированных детей до менее 40 000 и 20 000 к 2020 году.
 Цель
Цель - Stay Free — сделать так, чтобы дети, не инфицированные ВИЧ, на протяжении всего своего детства оставались свободными от ВИЧ. Он направлен на достижение этого путем усиления внимания к охвату и расширению прав и возможностей девочек-подростков и молодых женщин, а также на привлечении мужчин и мальчиков.
- AIDS Free нацелен на детей и подростков, живущих с ВИЧ, которые часто остаются позади из-за мер в ответ на ВИЧ. Инициатива направлена на обеспечение к 2018 году АРТ 1,6 миллиона детей (в возрасте от 0 до 14 лет) и 1,2 миллиона подростков (в возрасте от 15 до 19 лет), живущих с ВИЧ.
Профилактика передачи от матери ребенку (ППМР)
Для многих стран мира ППМР является наиболее успешным и важным приоритетом профилактики ВИЧ. Однако во всем мире существуют значительные пробелы в охвате.
По состоянию на июнь 2016 г., Армения, Беларусь, Куба и Таиланд были сертифицированы ВОЗ для ликвидации ПМР. К 2015 году в семи странах Восточной и Южной Африки охват услугами по ППМР превышал 90%. Это включает в себя Южную Африку, где проживает 25% беременных женщин в регионе, живущих с ВИЧ.Восточная и Южная Африка достигли самого большого сокращения ПМР в мире, снизившись с 18% младенцев, рожденных от матерей, живущих с ВИЧ, в 2010 году до 6% в 2015 году, т.е. в три раза меньше.
Это включает в себя Южную Африку, где проживает 25% беременных женщин в регионе, живущих с ВИЧ.Восточная и Южная Африка достигли самого большого сокращения ПМР в мире, снизившись с 18% младенцев, рожденных от матерей, живущих с ВИЧ, в 2010 году до 6% в 2015 году, т.е. в три раза меньше.
Ближний Восток и Северная Африка — это регион, в котором наблюдается наименьший прогресс, поскольку в 2015 году почти треть женщин, живущих с ВИЧ, передали вирус своим детям. Показатели ПМР в Азиатско-Тихоокеанском регионе, а также в западных и центральных регионах. Африка также была намного выше среднемирового показателя (10%).
По оценкам, 45% новых случаев заражения ВИЧ среди детей в 2015 году произошло в Западной и Центральной Африке. Несмотря на то, что в период с 2010 по 2015 год в регионе произошло 31% -ное сокращение числа новорожденных (иногда называемых педиатрическими) ВИЧ-инфекциями, это значительно ниже, чем 66% -ное сокращение в Восточной и Южной Африке. Ситуация особенно сложна в Нигерии, где в 2015 году была вторая по величине эпидемия ВИЧ в мире. В том же году в Нигерии было зарегистрировано самое большое количество новых случаев заражения ВИЧ среди детей в мире — приблизительно 41 000 человек, что примерно соответствует показателям следующих восьми стран вместе взятых.
В том же году в Нигерии было зарегистрировано самое большое количество новых случаев заражения ВИЧ среди детей в мире — приблизительно 41 000 человек, что примерно соответствует показателям следующих восьми стран вместе взятых.
С 2009 года число новых случаев инфицирования детей ВИЧ в стране снизилось только на 21% по сравнению со средним снижением на 60% среди других приоритетных стран Глобального плана.
Важным фактором успешного увеличения охвата лечением беременных женщин, живущих с ВИЧ, стало участие сообществ. Было показано, что поступление и удержание в медицинской помощи значительно улучшается благодаря вовлечению и поддержке сообщества, а также с помощью моделей предоставления услуг в сообществе.Сети и группы поддержки женщин, живущих с ВИЧ, сыграли особенно важную роль в расширении информационно-пропагандистской деятельности и предоставлении услуг по ППМР, консультировании, поддержке приверженности лечению, просвещению женщин об их репродуктивных правах, побуждении их обращаться за помощью и тестированием на ВИЧ, а также оказании психологической поддержки женщины смиряются с новым диагнозом ВИЧ.
В конце 2015 года более половины стран Африки к югу от Сахары использовали местных медицинских работников для предоставления и поддержки основных услуг в связи с ВИЧ, включая ППМР.
Несмотря на это, в 2013 году около 54% беременных женщин не прошли тест на ВИЧ и поэтому не знали о своем ВИЧ-статусе. Из тех, кто прошел тест и был поставлен положительный диагноз, 7 из 10 получили услуги по ППМР. Это помогло предотвратить 900 000 новых случаев инфицирования детей ВИЧ в период с 2009 по 2013 год.
Изменения в схемах лечения ППМР за последние пять лет сыграли важную роль в впечатляющем снижении показателей вертикальной передачи. В 2010 году большинство беременных женщин, живущих с ВИЧ, получали АРВ-препараты исключительно для предотвращения передачи инфекции ребенку, которого они вынашивали в то время.Но данные свидетельствуют о том, что немедленная и пожизненная АРТ для беременных женщин с диагнозом ВИЧ более эффективна, чем подходы «снова и снова». В 2015 году Всемирная организация здравоохранения (ВОЗ) рекомендовала предоставить всем беременным женщинам, живущим с ВИЧ, вариант B +, который включает немедленное предложение АРТ на протяжении всей жизни — помимо беременности, родов и грудного вскармливания — независимо от количества CD4 (который указывает уровень ВИЧ в организме). К 2015 году 91% из 1,1 миллиона женщин, получавших АРВ-препараты для предотвращения передачи инфекции от матери ребенку, получали АРТ всю жизнь в связи с глобальным развертыванием варианта B +.Это значительно повысило уровень подавления вируса, когда ВИЧ снижен до такого низкого уровня, что дальнейшая передача для этих женщин крайне маловероятна как в период кормления грудью, так и после него.
К 2015 году 91% из 1,1 миллиона женщин, получавших АРВ-препараты для предотвращения передачи инфекции от матери ребенку, получали АРТ всю жизнь в связи с глобальным развертыванием варианта B +.Это значительно повысило уровень подавления вируса, когда ВИЧ снижен до такого низкого уровня, что дальнейшая передача для этих женщин крайне маловероятна как в период кормления грудью, так и после него.
Определенные успехи были также достигнуты в усилиях по предотвращению нежелательной беременности в странах с большим числом случаев инфицирования детей ВИЧ, хотя во многих странах все еще сохраняется неудовлетворенная потребность в планировании семьи. Между периодами 2000–2004 и 2010–2014 годов неудовлетворенные потребности замужних женщин в планировании семьи сократились более чем на 10% в Эфиопии, Кении, Лесото, Малави и Руанде.Среди стран Африки к югу от Сахары, по которым имеются данные, в Зимбабве была самая низкая неудовлетворенная потребность в планировании семьи среди замужних женщин (10%).
Однако до сих пор отсутствует информация об использовании противозачаточных средств среди многих женщин в странах Африки к югу от Сахары, особенно на национальном уровне для женщин, живущих с ВИЧ. Некоторые более ранние исследования показали, что женщины, живущие с ВИЧ, могут быть более мотивированы использовать противозачаточные средства и, следовательно, иметь другие неудовлетворенные потребности, чем другие женщины, но все еще существует пробел в знаниях в этой области.
Также мало изменилось количество новых случаев инфицирования ВИЧ среди женщин. Еще 5,2 миллиона женщин репродуктивного возраста заразились ВИЧ в период с 2010 по 2015 год, в том числе 1,2 миллиона в Южной Африке. В результате в обозримом будущем потребность в услугах по ППМР для женщин репродуктивного возраста сохранится.
Когда младенец заражен ВИЧ, вероятность его смерти от заболевания, связанного со СПИДом, снижается на 75%, если он получает АРТ в течение первых 12 недель жизни.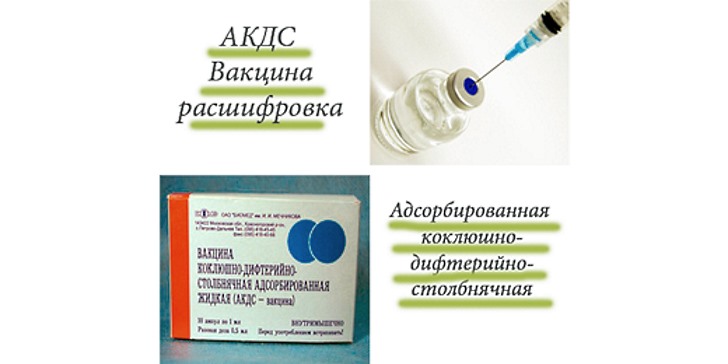
В результате в Руководстве ВОЗ по лечению от 2013 г. рекомендуется, чтобы младенцы, инфицированные ВИЧ, проходили тестирование при первом послеродовом посещении — обычно по достижении возраста четырех-шести недель — или при первой возможности после этого, и чтобы младенцы (и все дети младше в возрасте пяти лет) с положительным результатом теста на ВИЧ немедленно начинают лечение.
Несмотря на значительные инвестиции, только 54% детей, инфицированных ВИЧ, прошли тестирование на ВИЧ в течение первых восьми недель жизни в 2015 году (это называется «ранняя диагностика младенцев»), хотя это немного больше, чем в 2014 году, когда тестирование прошли 51%.
Охват ранней диагностикой грудных детей остается низким в большинстве приоритетных стран Глобального плана. Только Лесото, Южная Африка, Эсватини и Зимбабве предоставили тестирование на ВИЧ более чем половине младенцев, инфицированных ВИЧ в течение первых восьми недель жизни в 2015 году.
Младенцы, инфицированные в утробе матери (в утробе матери) или во время схваток и родов, имеют плохой прогноз по сравнению с младенцами, инфицированными во время грудного вскармливания, и им требуется срочная АРТ для предотвращения ранней смерти. Однако идентификация этих младенцев с помощью общего теста на антитела к ВИЧ представляет собой проблему из-за наличия материнских антител к ВИЧ, которые могут сохраняться в кровотоке ребенка до 18 месяцев.
Однако идентификация этих младенцев с помощью общего теста на антитела к ВИЧ представляет собой проблему из-за наличия материнских антител к ВИЧ, которые могут сохраняться в кровотоке ребенка до 18 месяцев.
Некоторые матери не приносят своих детей на тестирование к рекомендованному сроку шести недель, а другие дети, живущие с ВИЧ, могут умереть в течение первых шести недель. В целях обеспечения того, чтобы больше детей, живущих с ВИЧ, были диагностированы и начали лечение, Национальный департамент здравоохранения Южной Африки выпустил руководящие принципы, в которых содержится призыв ко всем младенцам, контактировавшим с ВИЧ, проходить тестирование при рождении и через 10 недель в 2015 году. Опыт Южной Африки с за тестированием при рождении внимательно следят, чтобы увидеть, можно ли преодолеть ключевые проблемы, например, матери, не приносящие своих детей на 10-недельный тест после того, как их дети при рождении не дали отрицательный результат на ВИЧ.
ВИЧ-отрицательных молодых матерей с высоким риском заражения ВИЧ также недостаточно тестируются во время кормления грудью. В результате на этой стадии младенцы неосознанно подвергаются воздействию ВИЧ. Изменение сроков передачи ВИЧ от матери к ребенку, которое перешло от беременности к грудному вскармливанию, создало новую необходимость сосредоточить внимание на приверженности новорожденных к АРВ-препаратах и удержании матерей и младенцев под присмотром до конца периода грудного вскармливания.
В результате на этой стадии младенцы неосознанно подвергаются воздействию ВИЧ. Изменение сроков передачи ВИЧ от матери к ребенку, которое перешло от беременности к грудному вскармливанию, создало новую необходимость сосредоточить внимание на приверженности новорожденных к АРВ-препаратах и удержании матерей и младенцев под присмотром до конца периода грудного вскармливания.
Несмотря на это, многие женщины, живущие с ВИЧ, не осознают, что им необходимо продолжать лечение во время грудного вскармливания своих младенцев, и возможности усилить призывы к соблюдению режима лечения и пополнить запасы АРВ-препаратов у женщин после рождения ребенка сокращаются, поскольку женщины сокращают их контакт с система здравоохранения.Очень важно, чтобы младенцы проходили повторное тестирование на ВИЧ, когда они прекращают кормить грудью, но, опять же, многие младенцы не проходят этот тест.
Доступ к тестированию на ВИЧ у детей старше 18 месяцев во многих странах остается ограниченным, что создает препятствия для расширения масштабов лечения.
Скрининг детей на ВИЧ в стационарах и клиниках питания, наряду с тестированием в контексте программ ППМР, предоставляет наилучшие возможности для диагностики ВИЧ-инфекций у детей, которые в противном случае могли бы остаться незамеченными.
Многие ВИЧ-инфицированные дети в странах с низким и средним уровнем доходов остаются невыявленными. Например, согласно одной из оценок из Кении, диагноз ставится только 40% детей с ВИЧ.
Для наиболее распространенных вирусологических тестов на ВИЧ для младенцев требуются сложные лабораторные инструменты и высокоспециализированный персонал, что затрудняет получение постоянных и своевременных результатов медицинскими работниками в сельских районах.
Во многих труднодоступных сельских районах тестирование на ВИЧ просто недоступно.Вместо этого медицинские работники должны использовать клинический диагноз для установления ВИЧ-положительного статуса ребенка. К сожалению, это приводит к тому, что многие инфекции остаются незамеченными.
В ответ на эту проблему был разработан ряд портативных систем тестирования в местах оказания медицинской помощи. По состоянию на 2016 год на рынке было три, которые могут работать от аккумуляторных блоков или от электросети и достаточно прочны для использования в мобильных лабораториях. Поскольку они маленькие и портативные, а также потому, что ими может управлять обученный персонал, не являющийся лаборантом, технологии в точках оказания медицинской помощи, вероятно, увеличат доступ к ранней диагностике младенцев и уменьшат вероятность последующего наблюдения.Оценка первых коммерчески доступных тестов в местах оказания медицинской помощи и у пациентов, проведенных во многих африканских странах, показывает, что эти тесты так же точны, как и лабораторные.
Даже когда дети и младенцы проходят тестирование, неэффективная транспортировка и плохие системы связи могут привести к увеличению времени цикла между сбором образцов крови в клиниках и получением результатов. Например, исследование, проведенное в Замбии, показало, что время от сбора образцов до возврата результатов лицу, осуществляющему уход, составляло 92 дня.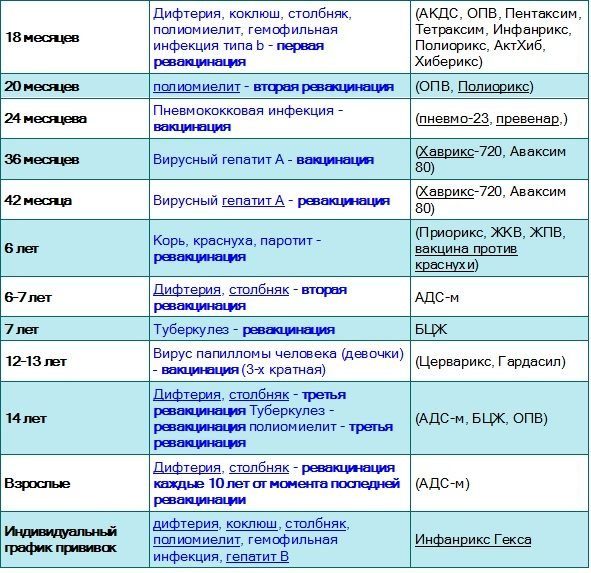 Это приводит к увеличению доли облученных младенцев и детей, которые теряются для последующего наблюдения, начинают лечение очень поздно или умирают, не успев начать лечение. Другие не имеют доступа к соответствующим педиатрическим препаратам.
Это приводит к увеличению доли облученных младенцев и детей, которые теряются для последующего наблюдения, начинают лечение очень поздно или умирают, не успев начать лечение. Другие не имеют доступа к соответствующим педиатрическим препаратам.
Жизненно важно, чтобы младенцы и дети раннего возраста, живущие с ВИЧ, получали лечение от ВИЧ как можно раньше и находились под постоянным наблюдением, поскольку их результаты лечения значительно хуже, чем у взрослых. Без лечения половина из них умрет к своему второму дню рождения.
Учитывая убедительные доказательства пользы, ВОЗ рекомендует лечение для всех детей и отдает предпочтение ему самых маленьких детей и детей с ослабленной иммунной функцией.
Несмотря на эту рекомендацию, низкие показатели тестирования на ВИЧ среди младенцев не позволяют тем, кто в нем нуждается, получить быстрый доступ к лечению от ВИЧ. В результате дети реже получают лечение, чем взрослые: только 43% получали лечение в 2016 году по сравнению с 54% взрослых.
Приверженность к антиретровирусному лечению
Лечение детей от ВИЧ работает.К сожалению, существует ограниченный диапазон соответствующих возрасту антиретровирусных препаратов, доступных в педиатрических формах, особенно альтернативы второй или третьей линии, что делает лечение еще более сложным.
Например, вкусовые качества лекарств могут быть сложными, поскольку некоторые из них сложно проглотить и они могут иметь неприятный вкус. Кроме того, объем лекарств, рекомендуемых для детей в возрасте до трех лет, представляет собой проблему, и некоторые из этих лекарств необходимо хранить в прохладном месте, что может быть проблемой в некоторых странах.
Тем не менее, в мае 2015 года произошел крупный прорыв, когда Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США дало предварительное одобрение на улучшенный педиатрический состав в виде небольших пероральных гранул. Эти гранулы поставляются упакованными в капсулы, которые легко открываются, что позволяет посыпать их пищей ребенка или, в случае младенцев меньшего размера, помещать их непосредственно в рот или над сцеживанием грудного молока. Ранее эти препараты были доступны только в форме таблеток, которые нельзя было разрушить, или в виде жидкости, которая требовала охлаждения и имела неприятный вкус, что делало ее чрезвычайно трудной для введения младенцам.
Ранее эти препараты были доступны только в форме таблеток, которые нельзя было разрушить, или в виде жидкости, которая требовала охлаждения и имела неприятный вкус, что делало ее чрезвычайно трудной для введения младенцам.
У детей иммунный ответ на ВИЧ отличается от иммунного ответа взрослых, поскольку их организм постоянно развивается, а их высокий уровень метаболизма делает прием лекарств против ВИЧ особенно трудным. Таким образом, педиатры, лечащие детей, живущих с ВИЧ, также должны знать специальные инструкции по дозировке.
В среднем людям, живущим с ВИЧ и живущим с ним с детства, придется принимать АРВ-препараты на 20 лет дольше, чем людям, заразившимся ВИЧ во взрослом возрасте, что усугубляет проблемы с приверженностью.По мере того, как все больше детей становятся старше с ВИЧ, становится очевидна неадекватность услуг в связи с ВИЧ для детей старшего возраста.
Сюда входит сложность соблюдения режима лечения для детей по мере того, как они становятся подростками, когда они могут хотеть свободы, а не строгих медицинских режимов, в сочетании с отсутствием соответствующих возрасту услуг и путаницей в отношении режимов АРВ при переходе от режима лечения для ребенка к режиму лечения для взрослых. .
.
Лекарственная устойчивость и стоимость лечения
Хотя стоимость первичной (или «первой линии») АРТ для детей резко снизилась из-за доступности непатентованных лекарств, если у ребенка разовьется лекарственная устойчивость и ему нужно будет начать лечение второй линией лекарств, лечение станет намного дороже.
Фактически, лекарственная устойчивость к ВИЧ (ЛУ-ВИЧ) к избранным лекарствам, приемлемым для детей, становится все более серьезной проблемой среди практикующих врачей, поскольку все больше детей развивают устойчивые к лечению штаммы вируса в результате расширения масштабов профилактики материнского программы передачи вируса от матери ребенку (ППМР). По оценкам ВОЗ, среди младенцев, участвующих в программах ППМР, распространенность ЛУ-ВИЧ составляет 21,6% по сравнению с 8,3% среди тех, кто не подвергался лечению.
В 2017 году результаты пятилетнего исследования эффективности лечения в Замбии показали, что 40% младенцев, у которых был поставлен диагноз ВИЧ в Лусаке, к 2014 году имели устойчивость по крайней мере к одному препарату АРТ по сравнению с 21,5% в 2009 году.
Несмотря на научные успехи, достигнутые в исследованиях и разработках новых лекарств от ВИЧ для взрослых, возможности для детей значительно отстают. В странах с высоким уровнем доходов рынок детских лекарств от ВИЧ практически исчез, поскольку новые случаи ВИЧ-инфекции среди детей практически ликвидированы.В результате стимулы для компаний разрабатывать составы для детей уменьшились, поскольку дети, живущие с ВИЧ, в странах с низким и средним уровнем доходов представляют собой менее жизнеспособный коммерческий рынок. Существует острая необходимость в усовершенствовании педиатрических АРВ-препаратов, в частности, для снижения их стоимости.
Отсутствие возможности наблюдения
Даже в тех случаях, когда лечение доступно и к нему есть доступ, удержание на лечении часто упоминается как ключевой вопрос во многих странах.
В 2014 году систематический обзор 30 000 детей, живущих с ВИЧ, в возрасте до 10 лет показал, что около 5–29% пациентов были потеряны для последующего наблюдения или умерли в течение 12 месяцев после начала лечения.
Аналогичное исследование с участием 13 611 детей из стран с низким уровнем дохода в Азии и Африке показало, что через 18 месяцев после начала АРТ 5,7% умерли, 12,3% были потеряны для последующего наблюдения и 8,6% были переведены в другие клиники. Потери для последующего наблюдения были намного больше в Западной Африке (21,8%) по сравнению с Азией (4,1%).
Дети более уязвимы для последующего наблюдения, чем взрослые, потому что они полагаются на своих родителей или опекунов, чтобы получить доступ к медицинским услугам. Некоторые из причин, по которым дети теряются для последующего наблюдения, включают отсутствие контактной информации о попечителях, стигматизацию и проблемы с консультированием, бремя, которое люди вынуждены возвращаться за результатами, и слабое последующее наблюдение в клиниках.
ПРАКТИЧЕСКИЙ ПРИМЕР: Улучшение сохранения ухода за младенцами в связи с ВИЧ в Уганде В некоторых районах Уганды менее 3% младенцев, рожденных женщинами, живущими с ВИЧ, в 2013 году, оставались под присмотром через один месяц. При поддержке PEPFAR Министерство здравоохранения работало с 22 медицинскими учреждениями, чтобы улучшить удержание матерей, живущих с ВИЧ, и их младенцев. Матери были опрошены, чтобы лучше понять их проблемы. Исследование показало, что 80% проблем с удержанием были вызваны забытыми встречами, конфликтами в расписании, отсутствием транспорта, проблемами конфиденциальности и страхом раскрытия информации своим партнерам.
При поддержке PEPFAR Министерство здравоохранения работало с 22 медицинскими учреждениями, чтобы улучшить удержание матерей, живущих с ВИЧ, и их младенцев. Матери были опрошены, чтобы лучше понять их проблемы. Исследование показало, что 80% проблем с удержанием были вызваны забытыми встречами, конфликтами в расписании, отсутствием транспорта, проблемами конфиденциальности и страхом раскрытия информации своим партнерам.
Информация была использована для улучшения качества медицинской помощи. Сверстники были приглашены для поиска других матерей и их детей из того же сообщества, которые были потеряны для последующего наблюдения. К февралю 2014 г., через 10 месяцев после базового исследования, все 22 медицинских учреждения добились значительных успехов, сохранив более 60% пар «мать – ребенок».
Многие национальные регистры здоровья до сих пор не отформатированы должным образом, чтобы облегчить долгосрочное наблюдение за младенцами, контактировавшими с ВИЧ, или парами мать-ребенок. Некоторые страны переходят на бумажные или электронные регистры, в которых фиксируются данные о младенцах, контактировавших с ВИЧ, и парах «мать-ребенок» во время многочисленных посещений врача, чтобы педиатры могли определить окончательный ВИЧ-статус младенца в конце грудного вскармливания. Электронная медицинская карта позволяет совместно отслеживать состояние матери и ее младенца с помощью одного инструмента, а также дает возможность обследовать и лечить младенцев, даже когда они доставляются в клинику для последующего наблюдения кем-то, кроме матери.
Некоторые страны переходят на бумажные или электронные регистры, в которых фиксируются данные о младенцах, контактировавших с ВИЧ, и парах «мать-ребенок» во время многочисленных посещений врача, чтобы педиатры могли определить окончательный ВИЧ-статус младенца в конце грудного вскармливания. Электронная медицинская карта позволяет совместно отслеживать состояние матери и ее младенца с помощью одного инструмента, а также дает возможность обследовать и лечить младенцев, даже когда они доставляются в клинику для последующего наблюдения кем-то, кроме матери.
Малави пилотирует использование службы коротких сообщений (SMS), широко доступной на мобильных телефонах, для отправки напоминаний матерям, которые пропустили послеродовой прием.SMS также используется в Кении, Южной Африке, Мозамбике, Зимбабве, Руанде и Замбии для отправки результатов тестов на ВИЧ младенцев из централизованных лабораторий на принтеры в медицинских учреждениях на уровне общины. Систематический обзор, сравнивающий бумажные системы и системы SMS, показал, что принтеры SMS ускорили доставку результатов испытаний в среднем на 17 дней.
В Кении с помощью системы отслеживания новорожденных, инфицированных ВИЧ (HITSystem), которая отправляет компьютерные предупреждения медицинскому персоналу и лабораторному персоналу, занимающемуся ранней диагностикой младенцев, наряду с SMS-предупреждениями матерям, увеличилась доля инфицированных ВИЧ младенцев, оставшихся под наблюдением через девять месяцев после рождения. ; сокращение времени между сбором образцов, результатами лабораторных исследований и уведомлением матерей; и увеличилась доля младенцев, живущих с ВИЧ, которые начинают АРТ.
ПОМОГИТЕ НАМ ПОМОГИТЕ ДРУГИМ
Avert.org помогает предотвратить распространение ВИЧ и улучшить сексуальное здоровье, предоставляя людям достоверную и актуальную информацию.
Мы предоставляем все это БЕСПЛАТНО, но для поддержания работы Avert.org нужны время и деньги.
Можете ли вы поддержать нас и защитить наше будущее?
Помогает каждый вклад, даже самый маленький.
Раскрытие информации о ВИЧ
Доводить до сведения маленьких детей или подростков важность лечения от ВИЧ может быть непросто. Многие лица, осуществляющие уход, откладывают сообщение ребенку о своем ВИЧ-положительном статусе по ряду причин. Они могут быть обеспокоены стигматизацией со стороны общества, чувством вины за передачу инфекции, неуверенностью в том, как раскрыть информацию, а также опасениями негативных реакций или сложных вопросов ребенка.
Многие лица, осуществляющие уход, откладывают сообщение ребенку о своем ВИЧ-положительном статусе по ряду причин. Они могут быть обеспокоены стигматизацией со стороны общества, чувством вины за передачу инфекции, неуверенностью в том, как раскрыть информацию, а также опасениями негативных реакций или сложных вопросов ребенка.
Однако для медицинского работника или опекуна важно раскрыть им статус ребенка, чтобы ребенок не чувствовал себя изолированным и не узнал о своем статусе случайно или публично. Имеющиеся данные также свидетельствуют о том, что у детей, которым были объяснены причины необходимости приема лекарств, было гораздо больше шансов улучшить подавление вируса, соблюдать режим лечения и оставаться на лечении дольше.
Исследование внедренной на национальном уровне меры по оказанию помощи медицинским работникам и лицам, обеспечивающим уход, в раскрытии информации о ВИЧ детям в Намибии показало, что среди детей, которые сообщили о неверных знаниях о том, почему они принимают АРВ, 83% показали улучшение знаний после вмешательства (определяемое как знание о ВИЧ. статус или принятие специального языка вмешательства). При зачислении только 11% знали свой статус, но еще 38% достигли полного раскрытия информации после вмешательства. Среднее время до полного раскрытия информации — 2.5 лет. Исследование показало, что это вмешательство помогло улучшить приверженность к АРТ, что улучшило подавление вируса.
статус или принятие специального языка вмешательства). При зачислении только 11% знали свой статус, но еще 38% достигли полного раскрытия информации после вмешательства. Среднее время до полного раскрытия информации — 2.5 лет. Исследование показало, что это вмешательство помогло улучшить приверженность к АРТ, что улучшило подавление вируса.
Психосоциальное благополучие
Многие дети, живущие с ВИЧ, переживают тяжелые жизненные события, которые могут повлиять на их психосоциальное благополучие, такие как потеря опекунов из-за болезней, связанных со СПИДом, стигматизация, шок из-за своего статуса и непонимание важности соблюдения режима лечения.
Чтобы смягчить эти события, важно побуждать детей иметь позитивный взгляд на жизнь, чему может помочь полное использование таких услуг, как группы поддержки.
Исследование семей, затронутых ВИЧ в Бангладеш в 2014 году, показало, что, хотя на жизнь детей влияет любое хроническое заболевание, которое может иметь их родители, когда это состояние подвергается стигматизации и несет в себе то, что исследование описывает как «социальные и моралистические коннотации», влияние на семья намного больше по интенсивности и последствиям. Исследование показало, что члены сообщества не любят общаться с ВИЧ-инфицированными людьми и их детьми из-за страха заразиться. Было обнаружено, что поддержка со стороны сверстников может быть эмоционально полезной для детей, затронутых ВИЧ, поскольку дети, как и взрослые, часто будут искать поддержки у друзей, чтобы справиться со стрессовыми ситуациями.
Исследование показало, что члены сообщества не любят общаться с ВИЧ-инфицированными людьми и их детьми из-за страха заразиться. Было обнаружено, что поддержка со стороны сверстников может быть эмоционально полезной для детей, затронутых ВИЧ, поскольку дети, как и взрослые, часто будут искать поддержки у друзей, чтобы справиться со стрессовыми ситуациями.
Маленькие дети слушают и учатся у сверстников и легко мотивируются друг другом, поэтому повышение осведомленности через сверстников, например создание групп сверстников или молодежных клубов в школах, может сыграть ключевую защитную роль в жизни детей, затронутых ВИЧ. В исследовании также рекомендуется, чтобы дети имели возможность информировать о разработке стратегий, которые позволят им справиться с жизнью в семьях, затронутых ВИЧ.
Раньше я сталкивался с проблемами в моем сообществе из-за ВИЧ.Люди думали, что, поскольку моя мать инфицирована ВИЧ, мы тоже инфицированы … Когда я был ребенком, меня спрашивали, у вашей матери СПИД? Тогда многие дети со мной не играли. Кто-то сказал: «У твоей матери харапрог [ВИЧ], у тебя тоже харапрог, не приходи к нам и не играй с нашими детьми». Наши соседи сказали, что наш отец был хараплоком. Как он делал харапкадж [плохие практики] в Индии, так он стал больным СПИДом.
Кто-то сказал: «У твоей матери харапрог [ВИЧ], у тебя тоже харапрог, не приходи к нам и не играй с нашими детьми». Наши соседи сказали, что наш отец был хараплоком. Как он делал харапкадж [плохие практики] в Индии, так он стал больным СПИДом.
— Рафик, 15-летний мальчик из Бангладеш, чья мать живет с ВИЧ, а отец умер от болезни, связанной со СПИДом
Право на образование
Все дети, живущие с ВИЧ, имеют право посещать школу, как и любой другой ребенок.Необходима политика, гарантирующая, что ребенок, живущий с ВИЧ, в школе не подвергается стигме, дискриминации или издевательствам, а также чтобы их статус оставался конфиденциальным.
Включение просвещения по вопросам секса и ВИЧ / СПИДа для детей младшего возраста имеет жизненно важное значение для борьбы со стигмой, окружающей ВИЧ, и для ознакомления других с фактами передачи ВИЧ. Программы информирования о ВИЧ важны для поощрения открытости о ВИЧ, а не для замалчивания.
Есть много способов связаться с молодежью; в том числе через социальные группы, средства массовой информации и работу со сверстниками — не только в школе.
Семейная поддержка детей, живущих с ВИЧ
Целостная поддержка семьи может быть лучшим способом обеспечить хорошее качество жизни для ребенка. Это должно включать схемы социальной защиты, которые предоставляют внешнюю помощь более бедным семьям в районах с высоким уровнем распространенности ВИЧ. Такие схемы сейчас рассматриваются как ценная часть улучшения жизни детей, затронутых ВИЧ.
ПРАКТИЧЕСКИЙ ПРИМЕР: Повышение устойчивости семей, затронутых ВИЧ, в РуандеИсследование семей, затронутых ВИЧ, в Руанде, проведенное в 2014 году, было сосредоточено на адаптированных к местным условиям домашних мероприятиях, направленных на улучшение функционирования семей и взаимоотношений между опекуном и ребенком, подключение уязвимых семей к доступным формальным и неформальным услугам в связи с ВИЧ и содействие эмоциональным поведенческое здоровье среди детей, затронутых ВИЧ.
В исследовании приняли участие тридцать девять детей и подростков (в возрасте от 7 до 17 лет) из 20 разных семей. Было обнаружено, что через шесть месяцев после проведения вмешательства лица, обеспечивающие уход, сообщили об улучшении поведения детей, и что семейные связи, хорошее воспитание и социальная поддержка были поддержаны и укреплены. У детей также улучшилась самооценка, а симптомы депрессии, беспокойства и раздражительности уменьшились.
Было обнаружено, что через шесть месяцев после проведения вмешательства лица, обеспечивающие уход, сообщили об улучшении поведения детей, и что семейные связи, хорошее воспитание и социальная поддержка были поддержаны и укреплены. У детей также улучшилась самооценка, а симптомы депрессии, беспокойства и раздражительности уменьшились.
Финансовая поддержка детей, живущих с ВИЧ
Снижение доходов семьи в сочетании с увеличением расходов (например, на лечение, транспорт и похороны) может подтолкнуть семьи, затронутые ВИЧ, к бедности, что имеет негативные последствия для детей с точки зрения питания, состояния здоровья, образования и эмоциональной поддержки.Например, исследование ежемесячного дохода семей, затронутых ВИЧ, в Камбодже, показало, что доход на 47% ниже, чем у здоровых семей. Аналогичным образом, в Китае доход подавляющего большинства семей, затронутых ВИЧ (93%), снизился более чем на 30% после постановки диагноза.
Предоставление семье возможности уйти от экономической уязвимости может привести к тому, что дети получат пользу от лучшего питания, возможности ходить в школу вместо работы и лучшего доступа к здравоохранению. Оценки национальных программ социальной защиты показали, что социальная защита (в частности, денежные переводы) способствует улучшению доступа к здравоохранению, образованию и питанию, укреплению социальных сетей, расширению доступа к лечению и профилактике, а также снижению уязвимости детей и подростков и снижению рискованности.
Оценки национальных программ социальной защиты показали, что социальная защита (в частности, денежные переводы) способствует улучшению доступа к здравоохранению, образованию и питанию, укреплению социальных сетей, расширению доступа к лечению и профилактике, а также снижению уязвимости детей и подростков и снижению рискованности.
Например, в Малави программа денежных трансфертов, предусматривающая особые условия для удержания девочек в школе, снизила процент отсева из школы на 35%. Это также привело к сокращению числа ранних браков на 40%, подростковой беременности на 30% и снижению риска заражения ВИЧ на 64% в течение 18 месяцев.
Благодаря эффективности этих мероприятий количество программ денежных переводов или денежных переводов в Африке удвоилось в период с 2000 по 2012 год, поддерживая за этот период трансферты на сумму 10 миллиардов долларов США.
Детские болезни
Детские болезни, такие как паротит и ветряная оспа, могут поражать всех детей, но дети, живущие с ВИЧ, могут обнаружить, что эти заболевания встречаются чаще, длятся дольше и хуже поддаются лечению.
В 2015 году около 40 000 детей, живущих с ВИЧ, умерли от туберкулеза (ТБ). Хотя смертность детей, живущих с ВИЧ, от туберкулеза снижается, составив 74 000 в 2012 г., многие страны указывают только ВИЧ как основную причину смерти, а туберкулез является сопутствующей причиной, а это означает, что это число может быть выше, чем зарегистрировано в настоящее время. .
Дети непропорционально сильно пострадали от эпидемии ВИЧ, и им по-прежнему не хватает жизненно необходимого лечения.
Вмешательства, отвечающие особым потребностям семей, основанные на опыте и рекомендациях детей, необходимы для того, чтобы 50% детей, живущих с ВИЧ, не имеющих лечения, могли получить к нему доступ. Без этого дети в возрасте 0–4 лет, живущие с ВИЧ, останутся возрастной группой, наиболее подверженной риску смерти в результате СПИДа.
Необходима совокупность усилий для предотвращения новых случаев ВИЧ-инфекции среди детей, обеспечения здоровья их матерей и улучшения диагностики и лечения детей с ВИЧ. Хотя огромные успехи были достигнуты в предотвращении передачи ВИЧ от матери ребенку, тот факт, что в период с 2010 по 2015 год еще 5,2 миллиона женщин репродуктивного возраста были инфицированы ВИЧ, означает, что в обозримом будущем потребность в услугах по ППМР сохранится.
Хотя огромные успехи были достигнуты в предотвращении передачи ВИЧ от матери ребенку, тот факт, что в период с 2010 по 2015 год еще 5,2 миллиона женщин репродуктивного возраста были инфицированы ВИЧ, означает, что в обозримом будущем потребность в услугах по ППМР сохранится.
Педиатрическая диагностика, тестирование и лечение ВИЧ необходимо расширить, чтобы привести их в соответствие со услугами для взрослых, и сделать их доступными ближе к тем местам, где живут дети, наиболее пострадавшие от ВИЧ.Медицинские работники должны быть обучены оказывать эффективные услуги в связи с ВИЧ детям, живущим с ВИЧ.
Системы поддержки сообществ бесценны и нуждаются в укреплении, чтобы они могли эффективно поддерживать детей и лиц, осуществляющих уход, чтобы поддерживать их здоровье и обеспечивать им доступ к необходимым услугам в связи с ВИЧ.
Необходимо разработать больше лекарств, специально адаптированных к потребностям детей, и сохранить их по доступной цене. Для этого требуются политическая воля и инвестиции со стороны отрасли.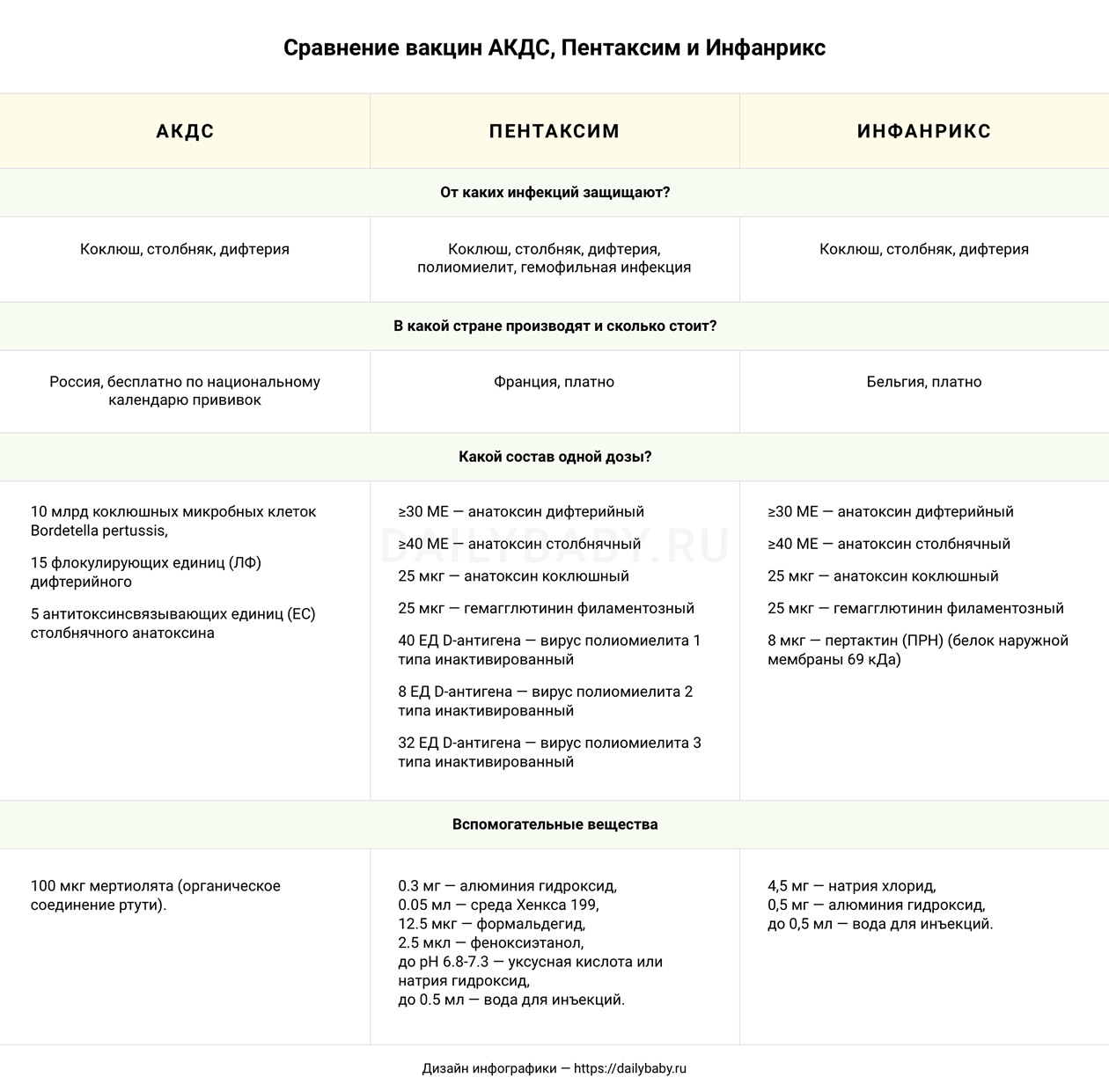 Правительству, неправительственным организациям, партнерам по исследованиям, экспертам в области здравоохранения и гражданскому обществу необходимо решительно выступать за разработку удобных для детей комбинаций с фиксированными дозами, чтобы простое и эффективное лечение стало быстро доступным и доступным для всех нуждающихся детей.
Правительству, неправительственным организациям, партнерам по исследованиям, экспертам в области здравоохранения и гражданскому обществу необходимо решительно выступать за разработку удобных для детей комбинаций с фиксированными дозами, чтобы простое и эффективное лечение стало быстро доступным и доступным для всех нуждающихся детей.
Наряду с этим необходимо усилить поддержку семей и сообществ, которые обеспечивают материальную, социальную и эмоциональную основу для развития ребенка.
Фото: © AVERT, Корри Вингейт.Фотографии используются в иллюстративных целях. Они не подразумевают никакого состояния здоровья или поведения со стороны людей на фотографии.
родителей о вакцинации детей-подростков от инфекций, передаваемых половым путем | Подростковая медицина | JAMA Педиатрия
Цели Оценить отношение родителей к вакцинации подростков в зависимости от характеристик вакцины, в том числе от того, предотвратила ли вакцина инфекцию, передаваемую половым путем (ИППП), и изучить возможные социально-демографические предикторы приемлемости вакцин против ИППП.
Дизайн В нем приняли участие 278 родителей, которые сопровождали своих детей (69,1% девочек в возрасте от 12 до 17 лет) на приемы в медицинские клиники. С помощью компьютерных анкет родители оценили 9 гипотетических сценариев вакцинации, каждый из которых определялся по 4 параметрам: способ передачи (ИППП или не ИППП), тяжесть инфекции (излечимая, хроническая или летальная), эффективность вакцины (50 %, 70% или 90%), а также наличие поведенческих методов профилактики (доступных или недоступных).Готовность родителей вакцинировать своих подростков в соответствии с каждым сценарием вакцинации оценивалась по шкале от 0 до 100. Для определения относительного вклада каждого параметра в рейтинги использовался совместный анализ.
Результаты Средняя оценка сценария вакцины составила 81,3. Вакцины против инфекций, передаваемых половым путем (среднее значение 81,3) не оценивались иначе, чем вакцины, не связанные с ИППП (среднее значение 80,0). Совместный анализ показал, что серьезность инфекции и эффективность вакцины оказали самое сильное влияние на оценки, за которыми следует доступность поведенческой профилактики.Способ передачи имел незначительное влияние на рейтинг. Возраст ребенка ( P = 0,08) и пол ( P = 0,77), возраст родителей ( P = 0,32) и образование ( P = 0,34), страховой статус ( P =. 08) и сайт сбора данных ( P = 0,48) не были существенно связаны с приемлемостью вакцины против ИППП.
Совместный анализ показал, что серьезность инфекции и эффективность вакцины оказали самое сильное влияние на оценки, за которыми следует доступность поведенческой профилактики.Способ передачи имел незначительное влияние на рейтинг. Возраст ребенка ( P = 0,08) и пол ( P = 0,77), возраст родителей ( P = 0,32) и образование ( P = 0,34), страховой статус ( P =. 08) и сайт сбора данных ( P = 0,48) не были существенно связаны с приемлемостью вакцины против ИППП.
Выводы Родители соглашались с идеей вакцинации своих детей-подростков от ИППП. Наиболее существенными проблемами были тяжесть инфекции и эффективность вакцины, а не передача инфекции половым путем.Родители также отдавали предпочтение вакцинам от инфекций, для которых не существовало методов поведенческой профилактики.
Несколько вакцин для профилактики инфекций, передаваемых половым путем (ИППП), находятся на разных стадиях разработки. Среди них профилактические вакцины против Neisseria gonorrhoeae , Chlamydia trachomatis , вируса простого герпеса 2 типа (основная причина генитального герпеса), вируса папилломы человека (ВПЧ) и вируса иммунодефицита человека. 1 -4 На основе анализа экономической эффективности Институт медицины предположил, что многие вакцины от ИППП могут привести к значительной экономии затрат на здравоохранение. 5 В идеале эффективная программа иммунизации от ИППП была бы нацелена на молодых подростков и подростков, желательно до того, как они станут сексуально активными. 5 -7 Стратегии иммунизации против инфекций, передаваемых половым путем, направленные на детей и подростков, возлагают большую часть бремени принятия решений на родителей.Например, исследование вакцинации подростков против гепатита В показало, что лучшим предиктором принятия подростками является их вера в то, что вакцинация считается важной для родителей.
Среди них профилактические вакцины против Neisseria gonorrhoeae , Chlamydia trachomatis , вируса простого герпеса 2 типа (основная причина генитального герпеса), вируса папилломы человека (ВПЧ) и вируса иммунодефицита человека. 1 -4 На основе анализа экономической эффективности Институт медицины предположил, что многие вакцины от ИППП могут привести к значительной экономии затрат на здравоохранение. 5 В идеале эффективная программа иммунизации от ИППП была бы нацелена на молодых подростков и подростков, желательно до того, как они станут сексуально активными. 5 -7 Стратегии иммунизации против инфекций, передаваемых половым путем, направленные на детей и подростков, возлагают большую часть бремени принятия решений на родителей.Например, исследование вакцинации подростков против гепатита В показало, что лучшим предиктором принятия подростками является их вера в то, что вакцинация считается важной для родителей. 8 Это открытие предполагает, что успех этих программ иммунизации будет в значительной степени зависеть от принятия родителями иммунизации от ИППП для подростков и подростков. Более того, было высказано предположение, что педиатры могут неохотно рекомендовать вакцинацию от ИППП 9 , что отчасти может быть связано с ожиданием негативных реакций родителей.
8 Это открытие предполагает, что успех этих программ иммунизации будет в значительной степени зависеть от принятия родителями иммунизации от ИППП для подростков и подростков. Более того, было высказано предположение, что педиатры могут неохотно рекомендовать вакцинацию от ИППП 9 , что отчасти может быть связано с ожиданием негативных реакций родителей.
Хотя в нескольких исследованиях изучались детерминанты приемлемости гипотетических вакцин против ИППП, включая убеждения людей в отношении здоровья 10 -16 и отношение к характеристикам вакцины, 6 , 17 , 18 относительно мало опубликовано, связанных с родительские установки. 19 -21 В одном исследовании изучали отношение матерей в Мексике к идее вакцинации против ВПЧ / рака шейки матки для своих дочерей-подростков.Результаты показали, что более 83% матерей разрешили бы сделать вакцину своим дочерям. 19 Однако многие участники, возможно, не понимали, что ВПЧ — это ИППП. Второе качественное исследование включало глубинные интервью, проведенные с 34 родителями из США. 20 Анализ содержимого показал, что большинство родителей одобрили описанные вакцины от ИППП (от гонореи, генитального герпеса, ВПЧ и вируса иммунодефицита человека). Родители, выступавшие против вакцинации одной или несколькими вакцинами, обычно считали, что их дети подвержены меньшему риску заражения.Другое недавно опубликованное исследование первоначально показало, что родители в меньшей степени одобряют вакцину против ВПЧ (55%), но продемонстрировали увеличение до 75% поддержки вакцинации после краткого образовательного вмешательства. 21
Второе качественное исследование включало глубинные интервью, проведенные с 34 родителями из США. 20 Анализ содержимого показал, что большинство родителей одобрили описанные вакцины от ИППП (от гонореи, генитального герпеса, ВПЧ и вируса иммунодефицита человека). Родители, выступавшие против вакцинации одной или несколькими вакцинами, обычно считали, что их дети подвержены меньшему риску заражения.Другое недавно опубликованное исследование первоначально показало, что родители в меньшей степени одобряют вакцину против ВПЧ (55%), но продемонстрировали увеличение до 75% поддержки вакцинации после краткого образовательного вмешательства. 21
Основная цель настоящего исследования заключалась в оценке того, как различные характеристики, связанные с вакцинацией (например, передача инфекции половым путем, серьезность инфекции, эффективность вакцины и доступность поведенческих методов профилактики) могут влиять на готовность родителей к сделайте прививки своим детям. Дополнительная исследовательская цель заключалась в том, чтобы изучить, повлияет ли возраст и пол ребенка на приемлемость вакцинации от ИППП родителями. Не исключено, что родители с большей готовностью вакцинируют детей младшего возраста (поскольку потенциальное начало половой жизни более отдаленное и, следовательно, менее опасное) и девочек (поскольку девочки и женщины обычно испытывают более серьезные неблагоприятные последствия из-за ИППП). Наша основная цель исследования заключалась в том, чтобы определить, будут ли на приемлемость вакцин против ИППП влиять следующие характеристики: (1) половая передаваемость предотвращаемой инфекции, (2) тяжесть инфекции, (3) эффективность вакцины, и (4) доступны ли поведенческие методы предотвращения инфекции.
Дополнительная исследовательская цель заключалась в том, чтобы изучить, повлияет ли возраст и пол ребенка на приемлемость вакцинации от ИППП родителями. Не исключено, что родители с большей готовностью вакцинируют детей младшего возраста (поскольку потенциальное начало половой жизни более отдаленное и, следовательно, менее опасное) и девочек (поскольку девочки и женщины обычно испытывают более серьезные неблагоприятные последствия из-за ИППП). Наша основная цель исследования заключалась в том, чтобы определить, будут ли на приемлемость вакцин против ИППП влиять следующие характеристики: (1) половая передаваемость предотвращаемой инфекции, (2) тяжесть инфекции, (3) эффективность вакцины, и (4) доступны ли поведенческие методы предотвращения инфекции.
Данные были собраны у родителей или опекунов, которые сопровождали своих детей (в возрасте 12-17 лет) на приемы к врачу в городских поликлиниках первичной медико-санитарной помощи для подростков и в частных педиатрических учреждениях по месту жительства. Участники-родители были набраны из залов ожидания клиники научными сотрудниками и ориентированы на исследовательский проект. Из подходящих потенциальных участников обратились 62 человека (понимающие английский язык, у которых был ребенок в возрасте 12-17 лет).8% согласились участвовать. Из 37,2% отказавшихся от участия 67,4% отказались из-за нехватки времени. Как только анкета была запущена, все участники адекватно заполнили инструмент.
Участники-родители были набраны из залов ожидания клиники научными сотрудниками и ориентированы на исследовательский проект. Из подходящих потенциальных участников обратились 62 человека (понимающие английский язык, у которых был ребенок в возрасте 12-17 лет).8% согласились участвовать. Из 37,2% отказавшихся от участия 67,4% отказались из-за нехватки времени. Как только анкета была запущена, все участники адекватно заполнили инструмент.
Данные были собраны посредством анонимных, аудио, компьютерных интервью, проводимых самостоятельно. Использовались ноутбуки с сенсорными экранами, что позволяло респондентам отвечать на вопросы, касаясь экрана пластиковым стилусом. Исследование было одобрено Наблюдательным советом университета, и все участники получили письменное информированное согласие.Составление содержания аудио, компьютеризированных и самостоятельных интервью было основано на предшествующих исследованиях вакцины против ИППП 6 , 13 , 17 , 22 и предварительных полуструктурированных интервью, проведенных с родителями. 20 Перед проведением аудио-, компьютеризированных и самостоятельных собеседований было заполнено 20 пилотных вопросников в бумажно-карандашном формате с опросными интервью, чтобы гарантировать понимание вопросов и рассмотрение соответствующих вопросов.
20 Перед проведением аудио-, компьютеризированных и самостоятельных собеседований было заполнено 20 пилотных вопросников в бумажно-карандашном формате с опросными интервью, чтобы гарантировать понимание вопросов и рассмотрение соответствующих вопросов.
Оцениваемые фоновые переменные включали возраст и пол родителей и детей, местонахождение клиники (городская поликлиника для подростков или частная практика), страховой статус и образование родителей.
Чтобы оценить приемлемость вакцины, участники ответили на 9 вопросов. Пункты были представлены компьютером в случайном порядке, чтобы исключить возможное влияние эффектов упорядочения.Каждый пункт описывал гипотетический сценарий вакцины, однозначно определяемый по следующим 4 параметрам: способ передачи (ИППП или не ИППП), тяжесть инфекции (излечимая антибиотиками, хроническая и неизлечимая или обычно летальная), эффективность вакцины (50%, 70%). %, или 90%), а также наличие поведенческих методов профилактики (да или нет). Например, один из сценариев гласил: «Эта вакцина защищает людей от болезней, которые могут передаваться половым путем. Заболевание можно вылечить антибиотиками.Вакцина действует у 9 из 10 человек, которые ее получают. Использование презервативов убережет человека от заболевания ». В таблице приведены описания 9 сценариев вакцинации. Родителей спросили: «Если бы эта вакцина была доступна сегодня и у вас было время, вы бы разрешили сделать прививку своему ребенку?» Был предоставлен 11-балльный формат ответов от 0 («Я бы никогда не позволил своему ребенку получить эту вакцину») до 100 («Я бы определенно позволил своему ребенку получить эту вакцину») с интервалом в 10. Эти 9 пунктов позволили нам для оценки относительного воздействия передачи ИППП, тяжести инфекции, эффективности вакцины и доступности поведенческих мер профилактики на приемлемость вакцины.
%, или 90%), а также наличие поведенческих методов профилактики (да или нет). Например, один из сценариев гласил: «Эта вакцина защищает людей от болезней, которые могут передаваться половым путем. Заболевание можно вылечить антибиотиками.Вакцина действует у 9 из 10 человек, которые ее получают. Использование презервативов убережет человека от заболевания ». В таблице приведены описания 9 сценариев вакцинации. Родителей спросили: «Если бы эта вакцина была доступна сегодня и у вас было время, вы бы разрешили сделать прививку своему ребенку?» Был предоставлен 11-балльный формат ответов от 0 («Я бы никогда не позволил своему ребенку получить эту вакцину») до 100 («Я бы определенно позволил своему ребенку получить эту вакцину») с интервалом в 10. Эти 9 пунктов позволили нам для оценки относительного воздействия передачи ИППП, тяжести инфекции, эффективности вакцины и доступности поведенческих мер профилактики на приемлемость вакцины.
Таблица.
Представленные сценарии вакцины
Приемлемость вакцины против инфекций, передаваемых половым путем, в целом оценивалась путем создания шкалы баллов, основанной на среднем значении по 6 из 9 пунктов, касающихся вакцин, предотвращающих ИППП (коэффициент α = 0,92).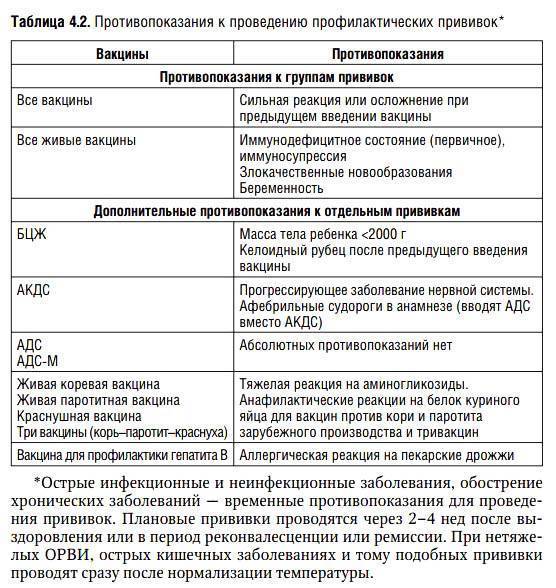 Приемлемость вакцин, не связанных с ИППП, оценивалась путем создания шкалы баллов на основе среднего значения по 3 оставшимся пунктам (коэффициент α = 0,77). Неравное количество вакцин против ИППП по сравнению с вакцинами, не связанными с ИППП, было неизбежным результатом дробного факторного дизайна, созданного для метода совместного анализа (см. Подраздел «Анализ данных» этого раздела для получения дополнительной информации), и, похоже, не повлияло на анализ.
Приемлемость вакцин, не связанных с ИППП, оценивалась путем создания шкалы баллов на основе среднего значения по 3 оставшимся пунктам (коэффициент α = 0,77). Неравное количество вакцин против ИППП по сравнению с вакцинами, не связанными с ИППП, было неизбежным результатом дробного факторного дизайна, созданного для метода совместного анализа (см. Подраздел «Анализ данных» этого раздела для получения дополнительной информации), и, похоже, не повлияло на анализ.
Парный тест t использовался для сравнения среднего балла для 6 сценариев вакцинации ИППП со средним баллом для 3 сценариев вакцинации, не относящейся к ИППП. Связи непрерывных фоновых переменных (возраст родителей и детей) с показателем приемлемости вакцины от ИППП из 6 пунктов оценивались с помощью корреляций моментов продукта Пирсона. Для оценки связи каждой категориальной переменной (пол ребенка, место сбора данных, страховой статус и образование родителей) с приемлемостью вакцины против ИППП использовался односторонний дисперсионный анализ.
Для оценки влияния параметров сценария вакцинации на готовность родителей разрешить вакцинацию детей использовался совместный анализ на основе полнопрофильных рейтингов. Этот основанный на регрессии аналитический метод часто используется в маркетинговых исследованиях для оценки того, как характеристики продукта влияют на его приемлемость. 23 В течение последних нескольких лет совместные аналитические методы все чаще применялись для изучения предпочтений в области здравоохранения, 24 -27 , включая предпочтения, связанные с гипотетическими вакцинами против вируса иммунодефицита человека. 6 , 28 Как отмечалось ранее, в этом исследовании оценивались 4 измерения (передача инфекции половым путем, серьезность инфекции, эффективность вакцины и доступность поведенческой профилактики), каждый из которых имел 2 или 3 уровня атрибутов (например, передача половым путем имела 2 уровня, тогда как эффективность вакцины — 3 уровня).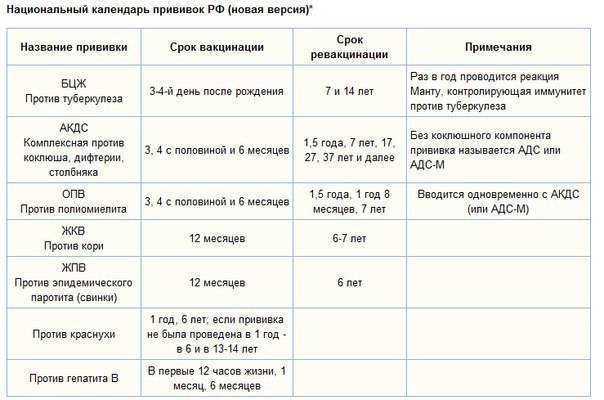 Для представления всех возможных комбинаций характеристик (например, полного факторного плана) участников попросили бы оценить 36 отдельных сценариев вакцинации, что потребовало бы повторяемости и затрат времени.Поэтому мы решили использовать дробный факторный план с репрезентативным подмножеством из 9 сценариев, который был построен с использованием процедуры (Conjoint) из коммерчески доступной программы (SPSS). 29 Использование дробного факторного плана делает задачу рейтинга более выполнимой, но ограничивает анализ основными эффектами каждого измерения.
Для представления всех возможных комбинаций характеристик (например, полного факторного плана) участников попросили бы оценить 36 отдельных сценариев вакцинации, что потребовало бы повторяемости и затрат времени.Поэтому мы решили использовать дробный факторный план с репрезентативным подмножеством из 9 сценариев, который был построен с использованием процедуры (Conjoint) из коммерчески доступной программы (SPSS). 29 Использование дробного факторного плана делает задачу рейтинга более выполнимой, но ограничивает анализ основными эффектами каждого измерения.
Совместный анализ 9 вакцин привел к разработке описательной модели, которая предоставила информацию об относительных предпочтениях каждого субъекта в отношении атрибутов в каждом измерении (например, предпочтение вакцины от ИППП по сравнению с вакциной, не связанной с ИППП, в пределах половой передачи. размер).В совместном анализе эти относительные предпочтения называются частичной полезностью. Чем больше респонденты предпочитают различать атрибуты, тем шире диапазон частичной стоимости коммунальных услуг. Например, если вакцина от ИППП была сильно предпочтительна по сравнению с вакциной, не связанной с ИППП, атрибут ИППП имел бы высокую положительную частичную полезность, а атрибут не-ИППП имел бы столь же сильную, но отрицательную, частичную полезность. ценность. Для каждого измерения сумма частных полезностей равна 0.Степень вклада каждого параметра в рейтинги вакцины измерялась баллами важности, которые отражают относительные диапазоны полезности неполной ценности по 4 параметрам. При таком подходе к совместному анализу сумма оценок важности по измерениям всегда равна 100.
Например, если вакцина от ИППП была сильно предпочтительна по сравнению с вакциной, не связанной с ИППП, атрибут ИППП имел бы высокую положительную частичную полезность, а атрибут не-ИППП имел бы столь же сильную, но отрицательную, частичную полезность. ценность. Для каждого измерения сумма частных полезностей равна 0.Степень вклада каждого параметра в рейтинги вакцины измерялась баллами важности, которые отражают относительные диапазоны полезности неполной ценности по 4 параметрам. При таком подходе к совместному анализу сумма оценок важности по измерениям всегда равна 100.
Из 278 родителей или опекунов, принявших участие в этом исследовании, 92,8% составляли женщины в возрасте от 24 до 66 лет (в среднем 40,9 года; стандартное отклонение 7.2 года). Их дети составляли 69,1% девочек в возрасте от 12 до 17 лет (в среднем 14,4 года; стандартное отклонение 1,5 года). 66,5% детей были набраны из городских клиник подростковой медицины и 33,5% — из частных практик.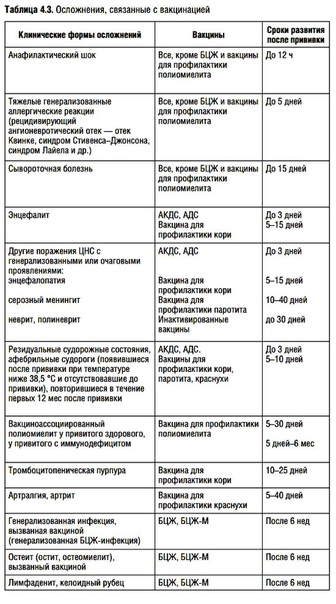 56,1% родителей назвали себя белыми, а 39,6% назвали себя афроамериканцами. Менее 2% сообщили о латиноамериканской этнической принадлежности. Что касается уровня образования родителей, участники разделились довольно поровну: 26,3% указали, что образование ниже среднего, 25.2% сообщили о среднем образовании, 30,6% указали, что они получили некоторое высшее образование, и 18,0% сообщили о 4-летнем образовании. 65,7% родителей сообщили, что они либо получали Медикейд, либо самостоятельно оплачивали медицинское обслуживание, тогда как остальные 34,3% сообщили, что имеют частную страховку.
56,1% родителей назвали себя белыми, а 39,6% назвали себя афроамериканцами. Менее 2% сообщили о латиноамериканской этнической принадлежности. Что касается уровня образования родителей, участники разделились довольно поровну: 26,3% указали, что образование ниже среднего, 25.2% сообщили о среднем образовании, 30,6% указали, что они получили некоторое высшее образование, и 18,0% сообщили о 4-летнем образовании. 65,7% родителей сообщили, что они либо получали Медикейд, либо самостоятельно оплачивали медицинское обслуживание, тогда как остальные 34,3% сообщили, что имеют частную страховку.
По 9 сценариям вакцинации общая готовность родителей принять вакцинацию для своих детей-подростков варьировалась от 0 до 100 (среднее значение 81,3; стандартное отклонение 21,1). Наименее приемлемый сценарий вакцины («Эта вакцина предохраняет людей от болезней, не передающихся половым путем.Болезнь нельзя вылечить, но люди от нее не умирают. Вакцина эффективна для 5 из 10 человек, получивших ее. Мытье рук несколько раз в день предотвратит заражение человека ».) Получил средний балл 74,9 (стандартное отклонение, 27,6), тогда как наиболее приемлемый сценарий вакцины (« Эта вакцина предохраняет людей от заболевания, не передаваемого половым путем. В большинстве случаев люди умирают от этой болезни. Вакцина работает для 9 из 10 заболевших. Мытье рук несколько раз в день не убережет человека от заражения.”) Получил средний балл 88,6 (СО, 20,2). В таблице перечислены средние баллы и стандартные отклонения для всех 9 сценариев вакцинации. Парный тест t показал, что средний балл для 6 сценариев вакцинации ИППП (балл 81,3) был выше, хотя и незначительно, по сравнению со средним баллом для 3 сценариев вакцинации не-ИППП (балл 80,0) ( t = 1,9, P = 0,06). Возраст родителей и детей не имел значительной корреляции с приемлемостью вакцины против ИППП ( r = 0.06 [ P = 0,32] и r = 0,11 [ P = 0,08] соответственно). Приемлемость вакцины против инфекций, передаваемых половым путем, также не была существенно связана с полом ребенка (F = 0,09, P = 0,77, η 2 <0,001), место сбора данных (F = 0,49, P = 0,48, η ).
Мытье рук несколько раз в день предотвратит заражение человека ».) Получил средний балл 74,9 (стандартное отклонение, 27,6), тогда как наиболее приемлемый сценарий вакцины (« Эта вакцина предохраняет людей от заболевания, не передаваемого половым путем. В большинстве случаев люди умирают от этой болезни. Вакцина работает для 9 из 10 заболевших. Мытье рук несколько раз в день не убережет человека от заражения.”) Получил средний балл 88,6 (СО, 20,2). В таблице перечислены средние баллы и стандартные отклонения для всех 9 сценариев вакцинации. Парный тест t показал, что средний балл для 6 сценариев вакцинации ИППП (балл 81,3) был выше, хотя и незначительно, по сравнению со средним баллом для 3 сценариев вакцинации не-ИППП (балл 80,0) ( t = 1,9, P = 0,06). Возраст родителей и детей не имел значительной корреляции с приемлемостью вакцины против ИППП ( r = 0.06 [ P = 0,32] и r = 0,11 [ P = 0,08] соответственно). Приемлемость вакцины против инфекций, передаваемых половым путем, также не была существенно связана с полом ребенка (F = 0,09, P = 0,77, η 2 <0,001), место сбора данных (F = 0,49, P = 0,48, η ).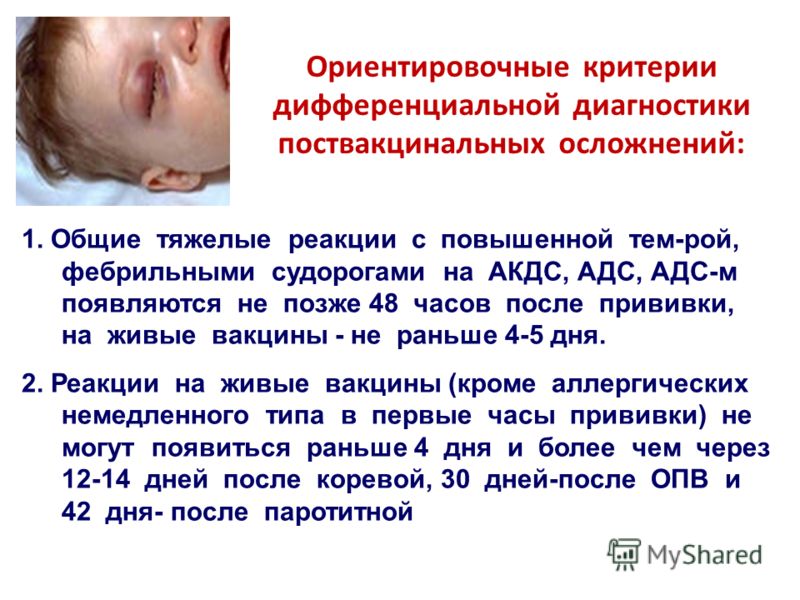 2 = 0,002), страховой статус (F = 3,2, P = 0,08, η 2 = 0,011) или образование родителей (F = 1,13, P = 0,34, η 2 = 0.012).
2 = 0,002), страховой статус (F = 3,2, P = 0,08, η 2 = 0,011) или образование родителей (F = 1,13, P = 0,34, η 2 = 0.012).
Восемьдесят один родитель (29,1%) дал каждому из 9 сценариев совместной вакцины одинаковую оценку. Из этих 81 респондентов двое дали оценку 0 по всем вакцинам, что означает, что они не нашли ни одну из вакцин приемлемой. Пять родителей дали всем вакцинам оценку 50. Семьдесят четыре родителя (26,6% от общей выборки) дали оценку 100 каждой вакцине, что свидетельствует о том, что они сочли все вакцины приемлемыми для их детей. Используя дисперсионный анализ и логистическую регрессию, мы исследовали, отличаются ли эти высокоактивные участники вакцинации (n = 74) от остальных участников (n = 204) с точки зрения социально-демографических показателей, описанных ранее.Возраст родителей не отличался значимо для высоких и низких акцепторов (F = 0,59, P = 0,44, η 2 = 0,002). В группе с высоким акцептором были дети, которые были значительно, но незначительно старше (средний возраст 14,7 года), чем группа с низким уровнем акцептора (средний возраст 14,2 года) (F = 4,55, P = 0,03, η 2 = 0,016). Пол ребенка не был связан с акцепторной группой (отношение шансов [OR], 1,08; 95% доверительный интервал [CI], 0,60–1,93). Тем не менее, родители, набранные из городских клиник, с большей вероятностью будут склонны принимать активное участие, чем те, кто был набран в условиях частной практики (OR, 2.20; 95% ДИ, 1,18-4,09). Точно так же родители, сообщавшие о самостоятельной оплате медицинского обслуживания или страховании Medicaid, с большей вероятностью были более активными сторонниками, чем те, кто имел частную страховку (OR, 2,31; 95% ДИ, 1,24–4,30). Наконец, родители, не окончившие среднюю школу (OR, 4,30; 95% ДИ, 1,62-11,43), и родители с аттестатом о среднем образовании (OR, 3,36; 95% ДИ, 1,25-9,06) с большей вероятностью соглашались чем те, кто закончил колледж.
Пол ребенка не был связан с акцепторной группой (отношение шансов [OR], 1,08; 95% доверительный интервал [CI], 0,60–1,93). Тем не менее, родители, набранные из городских клиник, с большей вероятностью будут склонны принимать активное участие, чем те, кто был набран в условиях частной практики (OR, 2.20; 95% ДИ, 1,18-4,09). Точно так же родители, сообщавшие о самостоятельной оплате медицинского обслуживания или страховании Medicaid, с большей вероятностью были более активными сторонниками, чем те, кто имел частную страховку (OR, 2,31; 95% ДИ, 1,24–4,30). Наконец, родители, не окончившие среднюю школу (OR, 4,30; 95% ДИ, 1,62-11,43), и родители с аттестатом о среднем образовании (OR, 3,36; 95% ДИ, 1,25-9,06) с большей вероятностью соглашались чем те, кто закончил колледж.
Учитывая, что 81 участник не продемонстрировал различий в предпочтениях по сценариям вакцинации, по необходимости они были исключены из совместного анализа, который предназначен для выявления детерминант предпочтений. Таким образом, общая совместная модель была основана на оставшихся 197 респондентах.
Таким образом, общая совместная модель была основана на оставшихся 197 респондентах.
В результате совместного анализа были получены следующие результаты. Различия в приемлемости для родителей ИППП по сравнению с вакциной, не связанной с ИППП, были незначительны. Тем не менее, родители выразили явное и решительное предпочтение вакцины, предотвращающей потенциально смертельную инфекцию, по сравнению с вакцинами, предотвращающими хроническую или излечимую инфекцию. Кроме того, было относительно сильное предпочтение вакцины с эффективностью 90% по сравнению с вакцинами с эффективностью 70% и 50%.Наконец, родители выразили умеренное относительное предпочтение вакцине, которая предотвращала инфекцию, для которой не было доступной поведенческой профилактики, по сравнению с вакциной, для которой существовала стратегия поведенческой профилактики. На рисунке показаны значения полезности частичной стоимости по всем измерениям. Как отмечалось ранее, оценки важности совместного анализа выводятся из диапазона полезностей с частичной стоимостью и отражают степень, в которой каждый параметр способствовал родительским оценкам сценариев вакцинации. Эффективность вакцины оказала наибольшее влияние на рейтинг вакцины (оценка важности 44.5), затем следует серьезность инфекции (оценка важности 31,4) и доступность поведенческой профилактики (оценка важности 17,7). Передача инфекции половым путем оказала незначительное влияние на родительские оценки (оценка значимости 6,4). Общая модель совместного анализа продемонстрировала превосходное соответствие с данными, что отражено в моменте произведения Пирсона r , равном 0,99.
Эффективность вакцины оказала наибольшее влияние на рейтинг вакцины (оценка важности 44.5), затем следует серьезность инфекции (оценка важности 31,4) и доступность поведенческой профилактики (оценка важности 17,7). Передача инфекции половым путем оказала незначительное влияние на родительские оценки (оценка значимости 6,4). Общая модель совместного анализа продемонстрировала превосходное соответствие с данными, что отражено в моменте произведения Пирсона r , равном 0,99.
Рисунок.
Неполные полезные значения по измерениям.
Несмотря на то, что сексуальная трансмиссия не была важной проблемой для родителей в целом, она была важным фактором в рейтинге для подгруппы участников. Используя пороговое значение частичной полезности 7,0 или -7,0 (что указывает на умеренно сильные предпочтения в контексте данного исследования), 31 родитель (11,2% от общей выборки) указали на относительно сильное предпочтение вакцины от ИППП (неполная полезность). ,> 7,0), тогда как 16 родителей (5,8% выборки) указали на относительно сильное противодействие вакцине от ИППП (частичная оплата коммунальных услуг, <−7.0). Для этих 47 участников половая передаваемость как параметр оказала большое влияние на оценку вакцины, при этом оценка важности варьировалась от 12,0 до 55,6 (среднее значение 29,2; стандартное отклонение 10,4).
,> 7,0), тогда как 16 родителей (5,8% выборки) указали на относительно сильное противодействие вакцине от ИППП (частичная оплата коммунальных услуг, <−7.0). Для этих 47 участников половая передаваемость как параметр оказала большое влияние на оценку вакцины, при этом оценка важности варьировалась от 12,0 до 55,6 (среднее значение 29,2; стандартное отклонение 10,4).
В этом исследовании оцениваются факторы, связанные с готовностью родителей вакцинировать своих детей-подростков. В данном конкретном исследовании мы сосредоточили внимание на следующих характеристиках ситуации с вакцинацией: передача инфекции половым путем, тяжесть инфекции, эффективность вакцины и доступность методов поведенческой профилактики.Мы также были заинтересованы в изучении возможных демографических предикторов приемлемости вакцины против ИППП. Основным выводом этого исследования было желание большинства родителей рассмотреть вопрос о вакцинации от ИППП для своих детей-подростков, независимо от возраста родителей, возраста ребенка, пола ребенка, места сбора данных, статуса страховки или образования родителей. Более четверти выборки указали на 100% готовность вакцинировать своих детей любой из 9 описанных вакцин. Эти люди с высоким уровнем допуска с большей вероятностью были набраны из городских клиник, с меньшей вероятностью имели частную страховку и с большей вероятностью имели среднее или меньшее образование.Наши результаты в целом согласуются с недавним исследованием, в ходе которого был проведен опрос 315 родителей детей младше 18 лет с использованием случайного набора номера (Николь Лиддон, доктор философии, письменное сообщение, 1998). В этом исследовании 69% родителей указали, что они будут вакцинировать своего ребенка против вируса герпеса человека 2.
Более четверти выборки указали на 100% готовность вакцинировать своих детей любой из 9 описанных вакцин. Эти люди с высоким уровнем допуска с большей вероятностью были набраны из городских клиник, с меньшей вероятностью имели частную страховку и с большей вероятностью имели среднее или меньшее образование.Наши результаты в целом согласуются с недавним исследованием, в ходе которого был проведен опрос 315 родителей детей младше 18 лет с использованием случайного набора номера (Николь Лиддон, доктор философии, письменное сообщение, 1998). В этом исследовании 69% родителей указали, что они будут вакцинировать своего ребенка против вируса герпеса человека 2.
Отсутствие значимой корреляции приемлемости вакцины от ИППП с возрастом ребенка в настоящем исследовании указывает на то, что эти родители не дифференцировали необходимость вакцинации от ИППП в зависимости от возраста своих детей.Этот вывод, в свою очередь, предполагает, что родители не могут принимать решения о вакцинации на основании относительной временной близости их детей к началу половой жизни. Однако, учитывая, что подросткам в этом исследовании было от 12 до 17 лет, в будущих исследованиях будет важно расширить возрастной диапазон вниз, чтобы полностью изучить этот вопрос.
Однако, учитывая, что подросткам в этом исследовании было от 12 до 17 лет, в будущих исследованиях будет важно расширить возрастной диапазон вниз, чтобы полностью изучить этот вопрос.
Было высказано предположение, что педиатры и другие поставщики медицинских услуг для подростков (например, семейные врачи и медсестры) могут неохотно рекомендовать вакцины от ИППП родителям подростков, возможно, отчасти из-за опасений по поводу того, как родители могут отреагировать на эту рекомендацию. 9 Высокие оценки приемлемости, о которых сообщают большинство родителей в этом исследовании, предполагают, что большинство родителей не отреагируют отрицательно на предложение иммунизировать своих детей от ИППП. Как и следовало ожидать, эффективность вакцины и тяжесть инфекции существенно повлияли на оценку родителями сценариев вакцинации. Этот результат согласуется с предыдущими исследованиями вакцинации против ИППП и вируса иммунодефицита человека с участием подростков, студентов колледжей и других взрослых, которые показали, что эффективность иммунизации и тяжесть инфекции являются важными детерминантами приемлемости. 6 , 17 , 18,20 , 30 Мы также обнаружили, что родители с большей вероятностью одобрили вакцины, предотвращающие инфекции, для которых не было доступного поведенческого метода профилактики. Предварительное качественное исследование также показало, что некоторые родители говорили о том, как на их отношение к вакцинации от ИППП в некоторой степени повлияла степень, в которой человек может предотвратить заражение посредством поведения (например, воздержания или использования презервативов). 20 По мере появления новых вакцин против ИППП может быть важно обратить внимание родителей на то, что методы профилактики поведения не всегда работают, что вакцинация не устраняет необходимость в поведенческой профилактике ИППП и что, следовательно, вакцинация против ИППП будет способ обеспечения дополнительной защиты от инфекции.
6 , 17 , 18,20 , 30 Мы также обнаружили, что родители с большей вероятностью одобрили вакцины, предотвращающие инфекции, для которых не было доступного поведенческого метода профилактики. Предварительное качественное исследование также показало, что некоторые родители говорили о том, как на их отношение к вакцинации от ИППП в некоторой степени повлияла степень, в которой человек может предотвратить заражение посредством поведения (например, воздержания или использования презервативов). 20 По мере появления новых вакцин против ИППП может быть важно обратить внимание родителей на то, что методы профилактики поведения не всегда работают, что вакцинация не устраняет необходимость в поведенческой профилактике ИППП и что, следовательно, вакцинация против ИППП будет способ обеспечения дополнительной защиты от инфекции.
Наши результаты не подтверждают мнение о том, что родители будут более неохотно вакцинировать своих детей вакциной от ИППП, чем вакциной, не связанной с ИППП. Этот результат относительно согласуется с предварительными исследованиями, которые показали, что большинство родителей сосредоточены на защите здоровья своих детей и не очень обеспокоены источником инфекции. 20 Очевидно, что тяжесть заболевания и эффективность вакцины были для этих родителей гораздо более важными аспектами, чем половая передача.Однако была небольшая группа родителей (5,8%), которые выражали относительно сильную антипатию к вакцине от ИППП. В будущих исследованиях важно будет более конкретно сосредоточиться на этой группе родителей, чтобы лучше понять источник их нежелания рассматривать возможность вакцинации своих детей от ИППП.
Этот результат относительно согласуется с предварительными исследованиями, которые показали, что большинство родителей сосредоточены на защите здоровья своих детей и не очень обеспокоены источником инфекции. 20 Очевидно, что тяжесть заболевания и эффективность вакцины были для этих родителей гораздо более важными аспектами, чем половая передача.Однако была небольшая группа родителей (5,8%), которые выражали относительно сильную антипатию к вакцине от ИППП. В будущих исследованиях важно будет более конкретно сосредоточиться на этой группе родителей, чтобы лучше понять источник их нежелания рассматривать возможность вакцинации своих детей от ИППП.
Это исследование имеет несколько ограничений, поэтому к результатам следует относиться с осторожностью. Во-первых, выборка родителей была неслучайной удобной выборкой, основанной на клинике, что указывает на то, что результаты не могут быть распространены на всех родителей.Более того, учитывая их присутствие на посещениях подростками медицинских учреждений, эти родители, возможно, представляли собой избранную выборку с особенно позитивным отношением к иммунизации. Тем не менее, образец является подходящим, поскольку вакцины от ИППП, скорее всего, будут вводиться в клинических условиях и, вероятно, потребуют разрешения родителей в течение определенного периода времени после их введения. Тем не менее, в будущих исследованиях будет важно изучить более репрезентативную выборку родителей, чтобы более полно понять детерминанты поддержки и противодействия вакцинации от ИППП.Второе ограничение заключается в том, что реакция родителей на гипотетические сценарии вакцинации вряд ли будет полностью предсказывать фактическое принятие решения. Кроме того, некоторые из наших выводов (например, что родители с меньшим образованием, те, у кого есть страховка Medicaid и те, кто посещает городскую клинику, с большей вероятностью будут активно соглашаться), контрастируют с сообщениями в литературе, которые указывают на то, что эти же факторы связано с недостаточной иммунизацией маленьких детей. 31 , 32 Это несоответствие может быть отражением некоторых ограничений, связанных с реакцией родителей на гипотетические вакцины.Однако использование гипотетических сценариев является неизбежной частью любого исследования, направленного на намерение попробовать продукты, которые еще не доступны. Кроме того, маркетинговые исследования и исследования поведения в отношении здоровья показывают, что намерение выполнить поведение является разумным, хотя и несовершенным, предиктором выполнения поведения. 33 , 34 Наконец, это исследование было сосредоточено на характеристиках сценария вакцинации и на социально-демографических факторах. В будущих исследованиях приемлемости вакцины против ИППП необходимо будет изучить другие вопросы, включая, помимо прочего, убеждения родителей в отношении здоровья, религиозные убеждения, относящиеся к вакцинации и ИППП, поведенческие факторы риска, а также соответствующий родительский анамнез и опыт (например, история ИППП в родитель).
Таким образом, серьезность инфекции, эффективность вакцины и, в меньшей степени, отсутствие доступной поведенческой профилактики были связаны с большей готовностью родителей принять вакцинацию для своих детей-подростков. Передача целевой инфекции половым путем не была важной проблемой для большинства родителей, но вызывала беспокойство у небольшой группы. Кроме того, возраст ребенка не имел значительной корреляции с приемлемостью вакцины против ИППП. Эти результаты позволяют предположить, что родители не возражают против вакцинации своих детей-подростков от ИППП.Если эти результаты будут воспроизведены на других выборках родителей, будет важно проинформировать педиатров, других врачей и медсестер о том, что большинство родителей, скорее всего, примут рекомендации относительно вакцинации ИППП.
Для корреспонденции: Грегори Д. Зимет, доктор философии, кафедра педиатрии, Медицинский факультет Университета Индианы, 575 N West Dr, комната 070, Индианаполис, IN 46202 ([email protected]).
Принята к публикации: 7 сентября 2004 г.
Финансирование / поддержка: Это исследование было поддержано грантом U19 AI31494 Национального института аллергии и инфекционных заболеваний, Бетесда, штат Мэриленд,
Благодарности: Мы благодарим Freddie Harris, BA, за его помощь во вводе данных и управлении.
2.Stanberry Л. Р. Бернштейн DI Заболевания, передаваемые половым путем: вакцины, профилактика и контроль .Сан-Диего, Калифорнийская академическая пресса 2000;
3.Коутский LAAult KAWheeler СМ и другие. Контролируемое испытание вакцины против вируса папилломы человека типа 16. N Engl J Med 2002; 3471645-1651PubMedGoogle ScholarCrossref 4.Stanberry LRSpruance SLCunningham AL и другие. Гликопротеин-D-адъювантная вакцина для профилактики генитального герпеса. N Engl J Med 2002; 3471652-1661PubMedGoogle ScholarCrossref 5.Институт медицины, Вакцины для 21 века .Вашингтон, округ Колумбия, Национальная академия Press2000;
6.Zimet GDBlythe MJFortenberry JD Характеристики вакцины и приемлемость иммунизации против ВИЧ среди подростков. Int J STD AIDS 2000; 11143-149PubMedGoogle ScholarCrossref 7.Zimet GDMays RMFortenberry JD Вакцины против инфекций, передаваемых половым путем: перспективы и проблемы волшебной палочки для профилактики и контроля. Sex Transm Dis 2000; 2749-52Google ScholarCrossref 8.Розенталь SLKottenhahn РКБиро FMSuccop Принятие вакцины против гепатита В среди подростков и их родителей. J Здоровье подростков 1995; 17248-254PubMedGoogle ScholarCrossref 9.Schrag SJSchuchat Ащулькин J Вакцина против вируса папилломы человека типа 16 [письмо]. N Engl J Med 2003; 3481402-1403PubMedGoogle ScholarCrossref 10.Gagnon М-Пгодин G Молодые люди и вакцина против ВИЧ: факторы, определяющие намерение пройти вакцинацию. Can J Public Health 2000; 91432- 434PubMedGoogle Scholar11.Rosenthal SLLewis LMSuccop П.А.Бернштейн DIStanberry Отношение студентов колледжа LR к вакцинации для предотвращения генитального герпеса. Sex Transm Dis 1999; 26438-443Google ScholarCrossref 12.Lewis LMStanberry LRRosenthal SLStewart DASuccop П.А.Бернштейн Д.И. Отношение к вакцинации от ЗППП и других болезней. Int J STD AIDS 2000; 11170-172PubMedGoogle ScholarCrossref 13.Zimet GDFortenberry JDBlythe MJ Отношение подростков к иммунизации против ВИЧ. J Pediatr Psychol 1999; 2467-75Google ScholarCrossref 14.Liau AZimet GD Восприятие иммунизации от ВИЧ студентами: отношение и поведение как определяющие факторы. Int J STD AIDS 2000; 11445-450PubMedGoogle ScholarCrossref 15.Kahn Я. Розенталь SLHamann TBernstein Д.И. Отношение к вакцине против вируса папилломы человека у молодых женщин. Int J STD AIDS 2003; 14300-306PubMedGoogle ScholarCrossref 16.Boehner CWHowe SRBernstein ДИРозенталь SL Приемлемость вакцины против вирусных заболеваний, передаваемых половым путем, среди студентов колледжей. Sex Transm Dis 2003; 30774-778Google ScholarCrossref 17.Zimet GDMays RMWinston YKee RDickes JSu L Приемлемость иммунизации против вируса папилломы человека. J Womens Health Gend Based Med 2000; 947-50Google ScholarCrossref 18.Ляу AZimet GD Приемлемость иммунизации против ВИЧ: изучение характеристик вакцины как определяющих факторов. AIDS Care 2001; 13643-650PubMedGoogle ScholarCrossref 19.Lazcano-Ponce ERivera Ларилло-Сантильян ESalmeron JHernandez-Avila MMunoz N Приемлемость пробной вакцины против вируса папилломы человека (ВПЧ) среди матерей подростков в Куэрнаваке, Мексика. Arch Med Res 2001; 32243-247PubMedGoogle ScholarCrossref 20.Май RMSturm LAZimet GD Перспективы родителей по вакцинации детей от инфекций, передаваемых половым путем. Soc Sci Med 2004; 581405-1413PubMedGoogle ScholarCrossref 21. Дэвис К.Дикман EDFerris DDias JK Приемлемость вакцины против вируса папилломы человека родителями подростков от 10 до 15 лет. Obstet Gynecol Surv 2004; 59820-822PubMedGoogle ScholarCrossref 22.Zimet GDFortenberry JDFife KHTyring SKHerne К.Дуглас JM Приемлемость иммунизации против генитального герпеса: роль убеждений в отношении здоровья и поведения в отношении здоровья. Sex Transm Dis 1997; 24555-560Google ScholarCrossref 23.Churchill GA Маркетинговые исследования: методологические основы . 5-е изд. Чикаго, Илл Драйден Пресс, 1991;
24. Сингх JCuttler Лшин MSilvers JNeuhauser D Принятие медицинских решений и пациент: понять предпочтения в отношении терапии гормоном роста с помощью совместного анализа. Med Care 1998; 36 ((Suppl)) AS31- AS45PubMedGoogle ScholarCrossref 25.Филлипс КАМаддала Т.Джонсон FR Измерение предпочтений медицинских вмешательств с использованием совместного анализа: приложение к тестированию на ВИЧ. Health Serv Res 2002; 371681-1705PubMedGoogle ScholarCrossref 27.Ryan MHughes J Использование совместного анализа для оценки предпочтений женщин в отношении ведения выкидыша. Health Econ 1997; 6261-273PubMedGoogle ScholarCrossref 28.Liau AZimet GDFortenberry JD Отношение к иммунизации против вируса иммунодефицита человека: влияние убеждений в отношении здоровья и характеристик вакцины. Sex Transm Dis 1998; 2576-81Google ScholarCrossref 29.SPSS Inc, SPSS Conjoint 8.0 . Чикаго, штат Иллинойс, SPSS Inc1997;
30. Веб-сайт PMZimet GDMays RMFortenberry JD иммунизация против ВИЧ: приемлемость и ожидаемое влияние на сексуальное поведение среди подростков. J Adolesc Health 1999; 25320-322PubMedGoogle ScholarCrossref 31.Bates А.С.Фицджеральд JFDittus RSWolinsky FD Факторы риска недостаточной иммунизации у бедных городских младенцев. JAMA 1994; 2721105-11110PubMedGoogle ScholarCrossref 32.Prislin RDyer JABlakely Ч.Джонсон Статус иммунизации CD и социально-демографические характеристики: посредническая роль убеждений, взглядов и предполагаемого контроля. Am J Public Health 1998; 881821-1826PubMedGoogle ScholarCrossref 33.Jamieson LBass F Корректировка заявленных мер намерения покупки для прогнозирования пробной покупки новых продуктов. J Market Res 1989; 26336-345Google ScholarCrossref 34.Терри DGallois CMcCamish M Теория разумных действий и заботливого поведения. Терри DJGallois CMcCamish Meds. Теория разумных действий: ее применение к профилактике СПИДа Оксфорд, Англия Пергамон 1993; 1-27 Google Scholarвакцин для младенцев, детей и подростков
Вакцины помогают защитить младенцев, детей и подростков от серьезных заболеваний. Получение детских вакцин означает, что у вашего ребенка может развиться иммунитет (защита) от болезней еще до того, как он с ними соприкоснется.
А знаете ли вы, что вакцинация вашего ребенка также защищает других? Из-за иммунитета сообщества вакцины помогают уберечь младших братьев и сестер вашего ребенка, старших членов семьи и друзей от болезней. Узнайте больше об иммунитете сообщества.
В этом разделе вы найдете информацию о вакцинах и расписания для:
Почему вакцинация начинается так рано?
Маленькие дети подвергаются повышенному риску инфекционных заболеваний, потому что их иммунная система еще не построила необходимую защиту для борьбы с серьезными инфекциями и заболеваниями.В результате такие заболевания, как коклюш или пневмококковая инфекция, могут быть очень серьезными и даже смертельными для младенцев и маленьких детей. Вакцинация начинается в раннем возрасте, чтобы защитить детей, прежде чем они столкнутся с этими заболеваниями.
Могут ли вакцины перегрузить иммунную систему моего ребенка?
Нет, вакцины не перегружают иммунную систему. Иммунная система вашего ребенка успешно борется с тысячами микробов каждый день. Даже если вашему ребенку делают несколько прививок в день, вакцины составляют лишь небольшую часть микробов, с которыми борется их организм.
Узнайте больше о том, как вакцины помогают иммунной системе бороться с болезнями.
Почему моему ребенку нужно более 1 дозы вакцины?
Детям — и взрослым — требуется более 1 дозы некоторых вакцин. Это потому, что для выработки иммунитета против болезни может потребоваться более одной дозы. Защита вакцины также может со временем исчезнуть.
Вот почему важна каждая доза вакцины.
Защищают ли некоторые вакцины более чем от 1 болезни?
Да.Во многих случаях ваш ребенок может получить комбинированные вакцины или вакцины, которые защищают его от более чем одного заболевания. Это означает меньшее количество вакцин для них и меньшее количество посещений врача. Подробнее о комбинированных вакцинах (PDF — 401 КБ).
Могу ли я отложить вакцинацию моего ребенка или распространить их на более длительный период времени?
Эксперты не рекомендуют распространять вакцины для вашего ребенка или откладывать их. Распространение вакцинации бесполезно, а соблюдение рекомендованного графика защищает младенцев и детей, обеспечивая иммунитет в раннем возрасте.Если ваш ребенок пропустит вакцинацию или получит ее с опозданием, он подвергнется риску серьезных заболеваний, которые можно предотвратить.
Можно ли сделать прививку моему ребенку, если он заболел?
Возможно, но сначала спросите педиатра вашего ребенка. Дети обычно могут получить вакцины, если у них легкое заболевание — например, простуда, низкая температура, ушная инфекция или диарея (водянистые фекалии). Узнайте больше о вакцинах, когда ваш ребенок заболел (PDF — 606 КБ).
Родители, не принимающие вакцину,
Родители хотят делать то, что лучше всего для их ребенка, даже те, кто задает вопросы.Хотя все родители разные, и не все методы общения работают для каждого родителя или врача, ниже приводится краткий обзор отношения родителей к иммунизации и методов общения, которые помогли успокоить родителей в некоторых обстоятельствах. Для начала:
Выслушайте опасения родителей и признайте их без конфронтации. Позволив родителям выразить свою обеспокоенность, повысится их желание прислушиваться к мнению педиатра.
Поощрять партнерские отношения с родителями в процессе принятия решений и персонализировать эти отношения.Сначала предоставьте важную информацию. Убедитесь, что родитель понимает информацию. Уточните и подтвердите правильные представления родителей об иммунизации и измените заблуждения
Обсудите преимущества вакцин и возможность побочных эффектов. Будьте открыты в отношении того, что известно об иммунизации, а что неизвестно. Предоставьте родителям информационные сообщения о вакцинах, образовательные ресурсы и надежные веб-сайты. Персонализируйте информацию, предоставляемую родителям, на основе культурных убеждений, проблем, связанных с вакцинами, и уровня грамотности.
Подчеркните количество жизней, спасенных с помощью иммунизации, в качестве позитивного подхода, а не сосредотачивайтесь на количестве смертей в результате отказа от иммунизации.
Обсудите законы штата о поступлении в школу и их обоснование. Некоторые родители не согласны с обязательной иммунизацией и сопротивляются иммунизации, потому что считают, что их права как родителей отнимаются. Объясните, что вакцины приносят пользу отдельным детям и общинам благодаря коллективному иммунитету.
Отношение и убеждения поставщиков в отношении безопасности вакцин были связаны с охватом вакцинацией детей дошкольного возраста.Большинство родителей считают, что иммунизация важна, и доверяют педиатрам как наиболее важному источнику информации о вакцинации.
Kimmel SR, Wolfe RM. Информирование о преимуществах и рисках вакцин. Журнал семейной практики. 2005; 54: S51-S57
Чжан Дж., Ю К.Ф. Каков относительный риск? Метод корректировки отношения шансов в когортных исследованиях общих исходов. JAMA. 1998; 280: 1690-1691

 В клинике «СМ-Доктор» доступны современные препараты импортного и отечественного производства.
В клинике «СМ-Доктор» доступны современные препараты импортного и отечественного производства. Она проводится по желанию родителей и создает стойкий иммунитет, сохраняющийся на протяжении 7-20 лет. В клинике «СМ-Доктор» всегда доступны современные и безопасные для детей вакцины против гепатита А, которые можно использовать уже с 12 месяцев.
Она проводится по желанию родителей и создает стойкий иммунитет, сохраняющийся на протяжении 7-20 лет. В клинике «СМ-Доктор» всегда доступны современные и безопасные для детей вакцины против гепатита А, которые можно использовать уже с 12 месяцев. Комплекс из нескольких введений препарата входит в обязательный календарь вакцинации по всему миру. В клинике «СМ-Доктор» имеются безопасные и эффективные вакцины, которые помогут сформировать стойкий иммунитет к заболеванию.
Комплекс из нескольких введений препарата входит в обязательный календарь вакцинации по всему миру. В клинике «СМ-Доктор» имеются безопасные и эффективные вакцины, которые помогут сформировать стойкий иммунитет к заболеванию. Только благодаря этому удается держать заболевание под контролем и избегать масштабных эпидемий. Клиника «СМ-Доктор» приглашает всех детей сделать прививку от кори качественной вакциной, помните, цена пренебрежения может быть очень высокой.
Только благодаря этому удается держать заболевание под контролем и избегать масштабных эпидемий. Клиника «СМ-Доктор» приглашает всех детей сделать прививку от кори качественной вакциной, помните, цена пренебрежения может быть очень высокой. Заражение вполне может привести к тяжелейшим последствиям вплоть до летального исхода в течение нескольких часов. В клинике «СМ-Доктор» всегда есть в наличии качественные и безопасные вакцины, которые надежно защитят малыша от опасности.
Заражение вполне может привести к тяжелейшим последствиям вплоть до летального исхода в течение нескольких часов. В клинике «СМ-Доктор» всегда есть в наличии качественные и безопасные вакцины, которые надежно защитят малыша от опасности. Ее введение не является обязательным, но многочисленные исследования доказали, что своевременная вакцинация надежно защищает малыша от тяжелого гастроэнтерита, вызванного вирусом.
Ее введение не является обязательным, но многочисленные исследования доказали, что своевременная вакцинация надежно защищает малыша от тяжелого гастроэнтерита, вызванного вирусом. 4ая вакцинация против вирусного гепатита В.
4ая вакцинация против вирусного гепатита В.

