Врожденный гипотиреоз тип наследования – Врожденный гипотиреоз: симптомы, лечение, диагностика, причины
Врождённый гипотиреоз — Википедия
Материал из Википедии — свободной энциклопедии
Врождённый гипотирео́з — гетерогенная по этиологии группа заболеваний щитовидной железы, проявляющихся сразу после рождения и характеризующихся частичным или полным выпадением её функции. Врождённый и приобретённый гипотиреоз в детском возрасте имеет сходную клиническую картину — преобладает торможение всех функций организма: ослаблена деятельность ряда органов и систем, отмечается вялость обменных процессов и наличие трофических расстройств[2].
Врождённый гипотиреоз — заболевание, которое регистрируется с частотой от 1 на 4 000—5 000 новорожденных в Европе и Северной Америке до 1 на 6 000—7 000 — в Японии. При этом у девочек данная патология встречается в 2—2,5 раза чаще, чем у мальчиков. В 90% случаев развитие врождённого гипотиреоза носит спорадический характер, а в 10% — является вторичным, связанным с врождёнными нарушениями синтеза, секреции и утилизации гормонов щитовидной железы[3]
Причины врождённой тиреоидной недостаточности весьма разнообразны и обусловлены не только непосредственным анатомическим повреждением щитовидной железы во внутриутробном периоде развития, но и морфофункциональной незрелостью гипоталамо-гипофизарной системы. Значительную роль в развитии врождённого гипотиреоза отводят вредным факторам, влияющим на женщину во время беременности: неудовлетворительное питание, инфекции и токсические вредности (М. Юлес и И. Холло, 1963). Немаловажную роль отводят генетически обусловленным нарушениям и недостаточному поступлению йода в организм (в районах йодной эндемии)[2].
Многочисленные этиологические факторы ведут к нарушению процессов биосинтеза тиреоидных гормонов, что вызывает усиление стимуляции работы щитовидной железы тиреотропным гормоном гипофиза с последующим развитием гипертрофии и гиперплазии щитовидной железы, не способной компенсировать развившуюся тиреоидную недостаточность
Согласно международной классификации болезней (10-й пересмотр) различают:
- E0000. — синдром врождённой йодной недостаточности, неврологическая форма. Эндемический кретинизм, неврологическая форма;
- E00.100.1 — синдром врождённой йодной недостаточности, микседематозная форма. Эндемический кретинизм:
- гипотиреоидный;
- микседематозная форма.
- E00.900.9 — синдром врождённой йодной недостаточности неуточнённый. Врождённый гипотиреоз вследствие йодной недостаточности. Эндемический кретинизм.
- E03.003.0 — врождённый гипотиреоз с диффузным зобом. Зоб (нетоксический) врождённый.
- E03.103.1 — врождённый гипотиреоз без зоба. Аплазия щитовидной железы (с микседемой). Врождённая(ый):
- атрофия щитовидной железы;
- гипотиреоз.
На передний план выступает задержка физического, интеллектуального (умственного) и полового развития ребёнка — выраженость клинических проявлений напрямую зависит от степени выраженности тиреоидной недостаточности и срока заболевания. Если гипотиреоз остался нераспознанным, то согласно L. Wilkins, к 5—6 месяцу постнатального развития выявляется классическая клиническая картина с тремя основными группами симптомов: задержка психофизического развития, функциональные изменения многих органов и систем, трофические нарушения кожи и её придатков
Диагностика клинически выраженного гипотиреоза не вызывает затруднений, сложно выявить гипотиреоз у детей первых недель и даже месяцев жизни. Неспецифичность ранних клинических проявлений у детей первых недель жизни, наличие лёгких и стёртых форм врождённого гипотиреоза требуют применения лабораторных методов диагностики[2].
С целью дифференциальной диагностики форм и стадий гипотиреоза применяют функциональные пробы. Наиболее достоверной является проведение пробы с тиреотропин-рилизинг гормоном (ТРГ)
Основная цель лечения — устранение расстройств обмена веществ и компенсация недостаточности щитовидной железы. Основной метод лечения гипотиреоза — пожизненная заместительная терапия препаратами тиреоидных гормонов. Необходим подбор индивидуальной адекватной дозы препаратов для каждого ребёнка: на первом этапе лечения — с целью достижения эутиреоидного («равновесного») состояния, а на втором — обеспечение сохранения компенсации заболевания[2].
При своевременно распознанном заболевании и квалифицированной медицинской помощи (пожизненная заместительная терапия тиреоидными гормонами) — благоприятный[4]. Если заболевание не распознано вовремя и лечение не начато своевременно развивается кретинизм — необратимое поражение головного мозга.
- ↑ Disease Ontology release 2019-08-22 — 2019-08-22 — 2019.
- ↑ 1 2 3 4 5 6 7 Жуковский М. А. Детская эндокринология. — 3-е изд. — М.: Медицина, 1995. — С. 206-228. — 656 с. — (Руководство для врачей). — 8000 экз. — ISBN 5-225-01167-5.
- ↑ Природжений гіпотиреоз. Клініка. Діагностика. Лікування (Врождённый гипотиреоз. Клиника. Диагностика. Лечение., укр.) / Моисеенко Р. О., Гречанина Е. Я. — 1-е изд. —
- ↑ Малая энциклопедия врача-эндокринолога / Ефимов А. С. — 1-е изд. — К.: Медкнига, ДСГ Лтд, Киев, 2007. — С. 114-119. — 360 с. — («Библиотечка практикующего врача»). — 5000 экз. — ISBN 966-7013-23-5.
- Врождённый гипотиреоз у детей (ранняя диагностика и лечение). Метод. рекоменд./Дедов И. И., Петеркова В. А., Безлепкина О. Б. — М., 1999. — 23 с.
- Гречанина Е. Я., Степанец А. П., Белаш Н. Н. Массовый скрининг новорожденных на гипотиреоз//VI съезд Украинского общества генетиков и селекционеров им. Н. И. Вавилова. — Тез. докл.: в 3 т. —
ru.wikipedia.org
Врожденный гипотиреоз — причины, симптомы, диагностика и лечение
Врожденный гипотиреоз – комплекс клинических и лабораторных проявлений, возникающих у ребенка с рождения при недостаточности гормонов щитовидной железы или невосприимчивости к ним тропных органов. Симптомы включают в себя отставание в психофизическом развитии, микседему, трофические нарушения кожи и ее придатков, угнетение работы сердца, снижение основного обмена. Диагностика базируется на характерной клинике, данных рентгенодиагностики, УЗИ щитовидной железы, ЭКГ, лабораторных исследований, в том числе измерения тиреотропного гормона и тироксина в плазме крови. Лечение подразумевает пожизненную заместительную терапию искусственными аналогами гормонов щитовидной железы.
Общие сведения
Врожденный гипотиреоз – это полиэтиологическое заболевание, характеризующееся клиническими проявлениями недостаточности щитовидной железы. Является наиболее распространенной эндокринной патологией в педиатрии. Чаще всего заболевание возникает на фоне изменений непосредственно в щитовидной железе, реже является результатом патологии гипоталамо-гипофизарной системы или дефектного строения рецепторного аппарата тропных органов. В 90% случаев носит спорадический характер. Заболеваемость – 1:3,7-4 тыс. новорожденных в Европе и США, в Японии – 1:6-7 тыс. Женский пол болеет в 2-2,5 раза чаще мужского. Первые скрининг-тесты на врожденный гипотиреоз были выполнены в 1973 г. канадцами J. Dussault, С. Laberge. На данный момент неонатальный скрининг проводится с целью максимально быстрой постановки диагноза и при необходимости — проведения своевременного лечения.
Врожденный гипотиреоз
Причины врожденного гипотиреоза
В 80-90% случаев возникает первичная форма врожденного гипотиреоза. Причины – аномалии развития щитовидной железы, чаще всего – дистопия в загрудинное или подъязычное пространство, реже – гипоплазия, атиреоз. Факторами риска могут выступать аутоиммунные и инфекционные заболевания матери, токсическое влияние медикаментов, химических средств, радиоактивное облучение, недостаточность йода во время беременности. Порядка 2% случаев пороков развития железы – наследственные формы. Основная их причина – мутации в генах TITF1, TITF2, FOXE1, PAX8. Как правило, генетические обусловленные формы сопровождают другие аномалии развития: врожденные пороки сердца, «волчья пасть» и т. п.
От 5 до 10% детей с врожденным гипотиреозом имеют нарушения синтеза, выделения или взаимодействия самих гормонов щитовидной железы. Передача, как правило, происходит по аутосомно-рецессивному типу. Самые частые варианты – дефекты органификации йода и тиреоидных гормонов (частота – 1:40000), синдром Пендреда (1:50000). Другие формы встречаются крайне редко.
Примерно 5% всех случаев врожденного гипотиреоза – центральные (вторичные или третичные) формы. Наиболее распространенный вариант – сочетанный дефицит гормонов аденогипофиза, в том числе ТТГ. Изолированный дефицит встречается редко. Причины поражения гипоталамо-гипофизарной системы – аномалии развития головного мозга, кисты, злокачественные и доброкачественные опухоли, родовая травма новорожденных, асфиксия во время родов, редко – аплазия гипофиза.
Причиной развития клинических симптомов гипотиреоза может быть аномалия структуры рецепторов в органах-мишенях, вызванная генными мутациями. Невозможность взаимодействия достаточного количества гормонов с рецепторами тропных тканей провоцирует развитие так называемого «синдрома резистентности». Как правило, это наследственная патология, передающаяся по аутосомно-доминантному типу. При ней уровень ТТГ в плазме крови нормальный, Т3 и Т4 – в переделах нормы или умеренно повышены.
Классификация врожденного гипотиреоза
Врожденный гипотиреоз имеет несколько классификаций, основывающихся на локализации нарушения, тяжести симптомов и уровне тироксина, компенсации на фоне лечения и длительности заболевания. По происхождению заболевания выделяют следующие формы гипотиреоза:
- Первичный, или тиреогенный. Патологические изменения возникают непосредственно в тканях щитовидной железы.
- Вторичный. Развиваются нарушения работы аденогипофиза, при которых возникает дефицит синтеза тиреотропного гормона (ТТГ).
- Третичный. Недостаточность щитовидной железы, возникающая при дефиците одного из гормонов гипоталамуса – тиролиберина. Вместе с вторичной формой относится к центральным гипотиреозам.
- Периферический. Недостаточность эффекта гормонов обусловлена дефектом или отсутствием рецепторов в тропных тканях или нарушением конверсии тироксина (Т4) в трийодтиронин (Т3).
По степени выраженности клинических симптомов и уровню Т4 в плазме гипотиреоз может быть латентным, манифестным и осложненным. Латентный, или субклинический гипотиреоз характеризуется нормальным уровнем Т4 на фоне повышения ТТГ. Клинических проявлений не возникает или они неспецифичны и малозаметны. При манифестной форме на фоне высокой концентрации ТТГ уровень Т4 несколько снижен. Развивается классическая клиническая картина гипотиреоза. Осложненный гипотиреоз протекает с высоким уровнем ТТГ, резким дефицитом Т4. Помимо тяжелой степени гипотиреоза возникают нарушения других органов и систем: сердечная недостаточность, полисерозит, кретинизм, кома, редко – аденома гипофиза.
В зависимости от эффективности лечения выделяют врожденный гипотиреоз:
- компенсированный
- декомпенсированный — даже на фоне адекватного лечения имеются клинические и лабораторные проявления гипотиреоза.
По продолжительности врожденный гипотиреоз разделяют на:
- транзиторный — заболевание развивается на фоне воздействия антител матери к ТТГ ребенка. Длительность – от 7 дней до 1 месяца.
- перманентный — требует проведения пожизненной заместительной терапии.
Симптомы врожденного гипотиреоза
В зависимости от формы и степени тяжести нарушений первые признаки первичного врожденного гипотиреоза могут манифестировать в разном возрасте. Резкая гипоплазия или аплазия железы проявляется в первые 7 дней жизни ребенка. Дистопия или несильная гипоплазия может вызывать клинические проявления в возрасте от 2 до 6 лет.
Первичные признаки, указывающие на врожденный гипотиреоз: вес ребенка при рождении свыше 4 кг; незрелость при доношенной или переношенной (более 40 недель) беременности; запоздалое отхождение мекониальных масс; длительная желтуха новорожденных; диспепсические явления; медленная прибавка массы тела; апатичность; макроглоссия; метеоризм и запоры; мышечная слабость; гипорефлексия; цианоз и эпизоды апноэ во время кормления. Кожные покровы ребенка холодные, возникают отеки конечностей и половых органов. Часто наблюдаются увеличенные роднички, несращение швов костей черепа, дисплазии тазобедренных суставов. Грудное вскармливание способно уменьшать выраженность клинических проявлений гипотиреоза.
Первичный врожденный гипотиреоз развивается поэтапно. Ярко выраженная клиника наблюдается в возрасте 3-6 месяцев. Возникает микседема. Кожные покровы уплотненные, желтушно-серые, сухие. Потоотделение резко уменьшено. Развивается атрофия ногтевых пластинок и волос. Голос ребенка низкий, хриплый и грубый. Возникает отставание в психомоторном и физическом развитии, зубы прорезываются и сменяются с задержкой. При дальнейшем развитии наблюдается умственная отсталость. Это проявляется скудностью словарного запаса и снижением интеллекта, которое склонно к прогрессированию вплоть до олигофрении.
Центральный врожденный гипотиреоз имеет нечеткую клиническую картину. Часто сочетается с аномалиями лицевого черепа («заячья губа», «волчья пасть») и недостаточностью других гормонов гипофиза (соматотропного, лютеинизирующего и фолликулостимулирующего) с характерной для этого симптоматикой.
Диагностика врожденного гипотиреоза
Диагностика врожденного гипотиреоза включает в себя сбор анамнестических данных, объективное обследование ребенка педиатром или неонатологом, инструментальные исследования, общие и специфические лабораторные тесты. В анамнезе можно выявить предрасполагающие факторы – отягощенную наследственность, заболевания матери во время беременности, нарушение питания, использование акушерских пособий во время родов и пр. При физикальном обследовании ребенка выявляется снижение ЧСС, АД, умеренная гипотермия, гипорефлексия, отставание в развитии.
На рентгенограмме конечностей определяют запоздание и нарушение очередности формирования ядер окостенения, их несимметричность и специфический признак – эпифизарный дисгенез. На ЭКГ – синусовая брадикардия, снижение амплитуды зубцов, расширение комплекса QRS. УЗИ щитовидной железы позволяет выявить дистопию, гипоплазию или отсутствие этого органа.
В ОАК – нормохромная анемия. В биохимическом анализе крови выявляется повышение липопротеидов и холестерина. При подозрении на центральное происхождение гипотиреоза проводится КТ и МРТ гипофиза. Специфические лабораторные тесты – измерение уровня Т4 и ТТГ в плазме крови. Данные тесты используются в качестве неонатального скрининга. В зависимости от формы гипотиреоза концентрации данных гормонов в крови могут быть увеличены или снижены. Редко применяют молекулярно-генетическое исследование с целью идентификации мутации генов.
Лечение врожденного гипотиреоза
Лечение врожденного гипотиреоза начинается немедленно с момента постановки диагноза и продолжается пожизненно. Препарат выбора – L-тироксин. Данное средство являет собой синтетический аналог гормонов щитовидной железы и используется в качестве заместительной терапии. Дозировка подбирается индивидуально. При необходимости препарат можно смешивать с грудным молоком. Эффективность проводимого лечения оценивается по уровню ТТГ и Т4 в крови, исчезновению симптомов гипотиреоза. При необходимости дополнительно назначаются поливитаминные комплексы, симптоматические препараты.
Прогноз при врожденном гипотиреозе зависит от адекватности и своевременности лечения. При ранней диагностике и вовремя начатой терапии, нормализации уровня ТТГ и Т4 – прогноз для психофизического развития благоприятный. При отсутствии лечения на протяжении первых 3-6 месяцев жизни прогноз сомнительный даже при правильной дальнейшей терапевтической тактике. При адекватном подборе дозы лекарственных средств скорость психофизического развития достигает физиологической нормы, однако отставание в интеллекте остается. Профилактика заключается в антенатальной защите плода, медико-генетической консультации при планировании беременности, рациональной диете и адекватном употреблении йода при вынашивании ребенка.
www.krasotaimedicina.ru
Врожденный гипотиреоз — описание болезни
Врожденный гипотиреоз — гетерогенная группа заболеваний, проявляющаяся врожденным дефицитом тиреоидных гормонов, развивающимся вследствие дисгенезии щитовидной железы или гипофизарной системы, а также вследствие врожденных дефектов синтеза тиреоидных гормонов и различных экзогенных воздействий (медикаменты, материнские блокирующие антитела и прочее). Другими словами, термином «врожденный гипотиреоз» обозначается гипотиреоз любого генеза, который манифестирует и диагностируется при рождении.
Возникновение болезни Врожденный гипотиреоз
Врожденный гипотиреоз примерно в 85 % случаев является спорадическим и в подавляющем большинстве случаев развивается вследствие дисгенезии щитовидной железы. Примерно в 15 % случаев причиной врожденного гипотиреоза является наследование дефектов синтеза Т4 или воздействие материнских антител к щитовидной железе (блокирующие антитела, циркулирующие у женщин с аутоиммунной патологией щитовидной железы). Для отдельных форм врожденного гипотиреоза в настоящее время известны генетические мутации, приводящие к его развитию.
Основные причины врожденного гипотиреоза.
I. Дисгенезия щитовидной железы:
1. агенезия (22-42 %)
2. гипоплазия (24-36 %)
3. дистопия (35-43 %)
II. Врожденные дефекты синтеза Т4:
1. дефект тиреоидной перокидазы
2. дефект тиреоглобулина
3. дефект натрий-йодидного симпортера
4. синдром Пендреда
5. дефект дейодиназ тиреоидных гормонов
III. Центральный (гипоталамо-гипофизарный) врожденный гипотиреоз
IV. Врожденный гипотиреоз, обусловленный материнскими антителами
Течение болезни Врожденный гипотиреоз
Внутриутробное развитие плода, у которого по тем или иным причинам не функционирует или отсутствует щитовидная железа, осуществляется за счет материнских тиреоидных гормонов, проникающих через плаценту. После рождения уровень материнских тиреоидных гормонов в крови у плода быстро падает. В неонатальном периоде, особенно раннем, тиреоидные гормоны критически необходимы для развития ЦНС новорожденного, особенно для продолжающихся процессов миелинизации нейронов коры головного мозга. При дефиците тиреоидных гормонов в этот период формируется необратимое недоразвитие коры головного мозга ребенка, клинически проявляющееся различной степенью умственной отсталости вплоть до кретинизма. При своевременном начале заместительной терапии (в идеале первая неделя жизни) развитие ЦНС практически соответствует норме. Наряду с развитием патологии ЦНС при несвоевременно компенсированном врожденным гипотиреозом страдает формирование скелета и других внутренних органов.
Симптомы болезни Врожденный гипотиреоз
Клинические симптомы в большинстве случаев не помогают в ранней диагностике врожденного гипотиреоза. Только в 5 % случаев врожденного гипотиреоза может быть сразу заподозрен у новорожденных на основании данных клинической картины. К ранним симптомам относятся пролонгированная гипербилирубинемия (> 7 дней), низкий голос, вздутый живот, пупочная грыжа, гипотония, увеличенный задний родничок, макроглоссия и увеличение щитовидной железы. Если лечение не начато, в дальнейшем, на 3-4 месяцев жизни, появляются такие симптомы, как сниженный аппетит, затруднение при глотании, плохая прибавка массы тела, метеоризм, запоры, сухость и бледность кожи, гипотермия, мышечная гипотония. После 5-6 месяца на первый план выступает задержка психомоторного и физического развития ребенка, а также диспропорциональный рост: широкая запавшая переносица, гипертелоризм, позднее закрытие родничков.
Диагностика болезни Врожденный гипотиреоз
В основе диагностики врожденного гипотиреоза лежит неонатальный скрининг. Стоимость скрининга и стоимость лечения ребенка-инвалида в поздно диагностируемых случаях врожденного гипотиреоза соотносится как 1:7-1:11. Наиболее принятый вариант скрининга подразумевает определение уровня ТТГ в высушенных пятнах крови на фильтровальной бумаге, взятой на 4-5 день жизни ребенка, когда происходит снижение уровня ТТГ, который в раннем неонатальном периоде ив норме значительно повышен.
Проведение скрининга на более ранних сроках приводит к увеличению числа ложноположительным результатов. В том случае, если уровень ТТГ по данным неонатального скрининга превышает 100 мЕд/л, диагноз врожденного гипотиреоза не вызывает сомнений, и ребенку показано назначение заместительной терапии L-T4. При исходном уровне ТТГ 20-50 мЕд/л проводится повторное определение его уровня в сухом пятне цельной крови; если он повторно превышает 20 мЕд/л проводится определение ТТГ и свободного Т4 в сыворотке крови. Определение этиологии врожденного гипотиреоза в неонатальном периоде не является первоочередной задачей в силу ургентной необходимости проведения заместительной терапии, которая позволит сохранить приемлемый уровень развития интеллекта.
Дифференциальная диагностика
Врожденный гипотиреоз необходимо дифференцировать от транзиторной гипертиротропинемии, под которой подразумевают преходящее повышение уровня ТТГ, выявляемое при неонатальном скриниге на врожденный гипотиреоз. В случае если наряду с этим имеет место транзиторное снижение уровня Т4, говорят отранзиторном гипотиреозе. Причинами транзиторной гипертиротропинемии могут быть: йодный дефицит, недоношенность, низкий вес при рождении, внутриутробная гипотрофия, внутриутробные инфекции, прием матерью тиреостатиков во время беременности, аутоиммунные заболевания щитовидной железы у матери. Наиболее частой и изученной причиной транзиторной неонатальной гипертиротропинемии является дефицит йода. По мере утяжеления йодного дефицита увеличивается доля детей, у которых при скрининге на врожденный гипотиреоз выявляется транзиторная гипертиротропинемия.
Лечение болезни Врожденный гипотиреоз
Целью заместительной терапии является скорейшая нормализация уровня Т4 в крови, а в дальнейшем подбор дозы L-T4, которая обеспечит стойкое поддержание нормального уровня Т4 и ТТГ. Рекомендуемая начальная доза L-T4 составляет 10-15 мкг на кг массы тела вдень. В дальнейшем необходимо проведение регулярных контрольных обследований для подбора адекватной дозы L-T4.
Прогноз
В первую очередь зависит от времени начала заместительной терапии L-T4. Если это происходит на первой-второй неделе жизни — нарушения психического и физического развития практически полностью предотвращаются. Далее по мере увеличения времени от рождения ребенка до назначения заместительной терапии увеличивается риск развития и тяжесть олигофрении вплоть до тяжелейших форм.
Гипотиреоз достаточно просто лечится приемом препаратов тиреоидного гормона. Наиболее эффективным и надежным из препаратов, используемых для заместительной терапии при гипотиреозе, является синтетический (получаемый искусственно) тиреоидный гормон. После начала лечения вам потребуется регулярно посещать врача с целью подбора точной дозы препарата.
В большинстве случаев регресс симптомов гипотиреоза начинается уже в первую неделю приема препарата. Полное исчезновение симптомов обычно происходит на протяжении нескольких месяцев. Грудным и более старшим детям с гипотиреозом лечение необходимо в обязательном порядке. Пожилые больные и люди с ослабленным здоровьем могут реагировать на прием препарата медленнее.
— Если гипотиреоз был спровоцирован лучевой терапией или возник вследствие удаления щитовидной железы, лечение скорее всего будет пожизненным. Пожизненное лечение может потребоваться и тогда, когда гипотиреоз возникает на фоне болезни Хашимото. В некоторых случаях, однако, функция щитовидной железы при тиреоидите Хашимото самопроизвольно восстанавливается.
— Если гипотиреоз возник на фоне другой серьезной патологии, функция щитовидной железы чаще всего нормализуется по мере излечения основного заболевания.
— Гипотиреоз может быть вызван приемом некоторых лекарственных средств. В таких случаях деятельность щитовидной железы нормализуется после отмены препарата.
— При латентной (субклинической) форме гипотиреоза лечение может не требоваться, однако больной нуждается во врачебном наблюдении, цель которого – не пропустить признаков прогрессирования заболевания. На сегодня нет точных данных в пользу необходимости заместительного лечения при латентном гипотиреозе, и мнения ученых на этот счет расходятся. Принимая решение о необходимости лечения в подобных случаях, вы и ваш врач должны обсудить вопрос соразмерности пользы от приема препаратов и потенциальных рисков и финансовых затрат на лечение и контроль состояния. Люди, страдающие сердечными заболеваниями, нуждаются в особо тщательном подборе доз препаратов, так как избыточный прием гормона повышает риск возникновения загрудинных болей (стенокардии) или нарушения сердечного ритма (мерцательной аритмии).
Начало лечения
Ваш врач назначит вам препарат, содержащий действующий компонент под названием “левотироксин натрий” (например, Синтроид, Левоксил или Левотроид). Принимайте его в точности так, как назначено. Через 6-8 недель после начала приема необходимо показаться врачу, чтобы убедиться в адекватности назначенной дозы.
Если получаемая доза слишком мала, у вас могут сохраняться признаки гипотиреоза: запоры, зябкость, вялость, увеличение массы тела. Признаками завышенной дозы может быть нервозность, нарушение сна, дрожь (тремор). При наличии заболеваний сердца избыточная доза гормона может вызывать нарушения сердечного ритма и боль за грудиной. Пациентов с сердечной недостаточностью вначале обычно ведут на небольшой дозе левотироксина, постепенно увеличивая ее по мере необходимости.
Если на момент постановки диагноза гипотиреоз имеет тяжелое течение, лечение должно быть начато немедленно. Тяжелый нелеченный гипотиреоз может привести к редко встречающемуся, но опасному для жизни осложнению — гипотиреоидной (микседематозной) коме.
Лечение микседематозной комы проводится в условиях палаты интенсивной терапии. Препарат тиреоидного гормона вводят внутривенно. При нарушении дыхания используют аппарат для искусственной вентиляции легких. Больного обследуют на наличие сопутствующих нарушений работы сердца (в том числе инфаркта миокарда) и назначают соответствующее лечение.
Лечение гипотиреоза во время беременности имеет особенно важное значение, так как нелеченный гипотиреоз может приводить к повреждению развивающегося плода.
— Если гипотиреоз возникает во время беременности, лечение следует начинать незамедлительно. Если же гипотиреоз был выявлен до наступления беременности, необходим контроль уровня тиреоидного гормона с соответствующей коррекцией принимаемой дозы препарата. При беременности потребность в дозе гормона может повышаться на 25-50%.
— Лечение может требоваться и в тех случаях, когда гипотиреоз возникает после рождения ребенка (послеродовой гипотиреоз). При наступлении каждой новой беременности вам будет рекомендовано обследование на гипотиреоз. В некоторых случаях послеродовой гипотиреоз проходит сам по себе; в других случаях он остается на всю жизнь и требует пожизненного лечения.
Поддерживающее лечение
Лечение гипотиреоза чаще всего бывает пожизненным, поэтому важно принимать назначенный препарат в точном соответствии с рекомендациями. У некоторых людей гипотиреоз носит прогрессирующий характер, так что дозировка получаемого гормона требует постепенного увеличения по мере затухания функции щитовидной железы.
У большинства больных, находящихся на лечении препаратами тиреоидного гормона, при отмене этих препаратов вновь развиваются признаки гипотиреоза. В таких случаях прием препарата должен быть возобновлен.
Если гипотиреоз возникает как осложнение инфекции или другого тяжелого заболевания, то после выздоровления функция щитовидной железы в большинстве случаев восстанавливается. Для проверки работоспособности щитовидной железы прием препаратов тиреоидного гормона временно прерывают. У большинства пациентов такая отмена препаратов приводит к кратковременному возврату симптомов гипотиреоза (организм зачастую подает щитовидной железе сигнал о необходимости возобновить работу с некоторым запаздыванием). Если железа в состоянии вырабатывать достаточное количество гормона самостоятельно, дальнейшее лечение не требуется. Если же уровень гормона остается низким, прием препарата следует возобновить.
При приеме препаратов тиреоидного гормона следует раз в полгода или год посещать лечащего врача для плановой проверки. Вам предложат сдать анализ на тиреотропный гормон (ТТГ), который покажет, соответствует ли уровень гормона норме.
Лечение при ухудшении состояния
Иногда симптомы гипотиреоза (вялость, запоры, зябкость, ухудшение памяти и способности к концентрации внимания) сохраняются, несмотря на лечение. Это происходит, когда доза принимаемого гормона недостаточна или препарат плохо всасывается из желудочно-кишечного тракта. Действие тиреоидного гормона может блокироваться при заболеваниях кишечника или приеме некоторых других медикаментов. Если вы принимаете карбонат кальция, холестирамин, сукральфат, гидроксид алюминия, сульфат железа или эстроген, врач может порекомендовать увеличение дозы тиреоидного гормона. Пищевые добавки с кальцием следует принимать не менее чем за 4 часа до (или через 4 часа после) очередного приема гормона.
Избыточные дозы тиреоидного гормона могут вызывать нарушения сердечного ритма, а со временем – и остеопороз. При наличии сопутствующих заболеваний сердца завышенная доза гормона может вызывать стенокардию (боль за грудиной) или аритмию. Ваш лечащий врач будет контролировать содержание тиреоидного гормона в вашем организме по результатам анализа крови на тиреотропный гормон (ТТГ). В случае необходимости врач порекомендует снижение дозы.
Профилактика болезни Врожденный гипотиреоз
Профилактика врожденного гипотиреоза предполагает обязательное медико-генетическое консультирование будущих родителей в том случае, если кто-нибудь из них происходит из семьи с повышенным риском развития гипотиреоза.
К каким докторам следует обращаться при болезни Врожденный гипотиреоз
Эндокринолог
znaniemed.ru
Врожденный гипотиреоз: причины, патогенез, последствия, прогноз
Исход врожденной формы гипотиреоза зависит от своевременной диагностики патологии и времени начала заместительной гормональной терапии. Если лечение было начато в первые месяцы жизни, то интеллектуальные способности и психофизическое развитие ребенка не нарушаются. Лечение малышей старше 3-6 месяцев позволяет остановить отставания в развитии, но имеющиеся нарушения интеллекта останутся навсегда.
- Если патология вызвана болезнью Хашимото, лучевой терапией или отсутствием щитовидки, то пациента ждет пожизненная терапия.
- Если гипотиреоз вызван другими заболеваниями и нарушениями организма, то после устранения причинных факторов состояние пациента нормализуется.
- При болезни вызванной медикаментозными препаратами, синтезирование гормонов восстанавливается после отмены приема лекарств.
- Если патология протекает в латентной, то есть субклинической форме, то лечение может не проводиться. Но пациент нуждается в регулярном посещении врача для контроля общего состояния и выявления признаков прогрессирования болезни.
Если заболевание было поздно диагностировано, время начала заместительной терапии упущено или прием препаратов так и не начинается, то прогноз врожденного гипотиреоза ухудшается. Существует риск развития тяжелых осложнений болезни: олигофрения, кретинизм и инвалидизация.
[20], [21], [22], [23], [24], [25], [26], [27], [28]
Инвалидность
Согласно медицинской статистике, инвалидность при врожденном гипотиреозе составляет 3-4%. Частичная или полная потеря работоспособности наблюдается на запущенных стадиях болезни и при тяжелых формах патологии, которые мешают вести полноценный образ жизни.
Пациент с нарушениями функционирования щитовидной железы становится гормонозависимым, что накладывает негативный отпечаток не только на состояние здоровья, но и на образ жизни. Кроме того, определенные стадии болезни осложняются сопутствующими патологиями, что еще больше усугубляет состояние больного.
Для установления инвалидности пациента направляют на медицинскую социальную экспертизу и врачебную консультационную комиссию. Основными показаниями для прохождения медкомиссии выступают:
- Гипотиреоз 2 или 3 степени тяжести.
- Эндокринная кардиомиопатия.
- Паратиреоидная недостаточность.
- Выраженные психические изменения и расстройства.
- Перикардиальный выпот.
- Снижение работоспособности.
- Необходимость изменений условий труда.
Для подтверждения инвалидности, пациенту необходимо пройти ряд диагностических процедур:
- Гормональные анализы крови на ТТГ, ТГ.
- Анализ на электролиты и триглециды.
- УЗИ и электромиография.
- Исследование антител к тиреоглобулину.
- Уровень сахара и холестерина в крови.
По результатам проведенных анализов, пациент получает удостоверение по инвалидности.
Инвалидизация имеет несколько категорий, каждая из которых свои особенности:
Степень | Особенности нарушений | Ограничения | Группа инвалидности | Запрещенная работа |
I | Легкие соматические нарушения. Повышенная утомляемость и сонливость. Незначительное снижение психомоторного развития. Задержка роста. Уровни гормонов в норме или немного повышены. | Ограничений жизнедеятельности нет | Ограничение по линии ВКК |
|
II | Умеренные соматические нарушения. Утомляемость и сонливость. Отечность. Лабильность АД. Неврозоподобный симптомокомплекс. Нейропатия, задержка роста. Легкая степень слабоумия. Уровни гормонов умеренно снижены. | I степень ограничений:
| III группа |
|
III | Выраженные соматические нарушения. Брадикардия и миопатия. Нарушение половой функции. Длительные запоры. Гипотиреоидный полисерозит. Умственная отсталость. Выраженные гормональные нарушения. | II степень ограничений:
| II группа | Недееспособность |
IV | Тяжелые соматические нарушения. Выраженные патологии сердечно-сосудистой системы. ЖКТ нарушения. Нарушения мочевыделительной системы. Нервно-психические патологии. Задержка роста. Умственная отсталость тяжелой или средней степени. Значительные гормональные нарушения. | III степень ограничений:
| I группа | Недееспособность |
Врожденный гипотиреоз является серьезной патологией эндокринной системы, которая без своевременной медицинской помощи грозит многочисленными осложнениями и ухудшением качества жизни. При тяжелых формах заболевания, инвалидность выступает необходимой мерой для облегчения состояния пациента и улучшения качества его жизни.
[29], [30]
ilive.com.ua
Врожденный гипотиреоз: симптомы у детей
В этой статье вы узнаете:
Врожденный гипотиреоз чаще диагностируется в детском возрасте и его причина обычно необратима. Однако, грамотно подобранная доза левотироксина для заместительной терапии, полностью устраняет влияние врожденного гипотиреоза на организм.
Причины врожденного гипотиреоза
Основные из них:
- Отсутствие/недоразвитие щитовидной железы, обусловленное генетически;
- Генетические нарушения биосинтеза щитовидных гормонов;
- Нехватка или избыток йода в питании беременной способны привести к гипотиреозу у новорожденного;
- Чрезмерное количество в рационе тио- и изоционатов, а также цианогенных гликозидов. Эти вещества во врачебной среде принято называть струмогенными и они содержатся в обычной, брюссельской и цветной капусте, рапсе, турнепсе, сладком картофеле… Список можно продолжить, но это вовсе не значит, что при беременности указанные продукты надо из диеты исключить. Достаточно лишь не употреблять их в очень больших количествах;
- Достаточно редко – воздействие употребляемого беременной радиоактивного йода. Примерно с 10–12 недели щитовидка плода уже накапливает йод, в том числе и радиоактивный;
- Самая редкая и наименее перспективная в отношении лечения причина врожденного гипотиреоза – это патология рецепторов к щитовидным гормонам. В этом случае в крови много и ТТГ, и Т3, и Т4, но все равно наблюдается гипотиреоз. Описано всего две сотни семей с этой разновидностью врожденного гипотиреоза.
Врожденный гипотиреоз, если он установлен у ребенка, принято называть кретинизмом. Действительно, недостаток щитовидных гормонов замедляет психоэмоциональное развитие человека. О микседеме говорят при тяжелом гипотиреозе, в том числе и врожденном, когда развиваются характерные гипотиреоидные или микседематозные отеки.
Диагностика
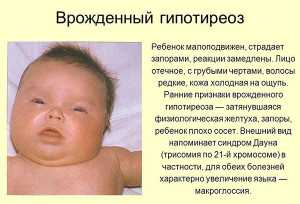 Внешний вид новорожденного настолько характерный, что опытный неонатолог предполагает диагноз уже на основании простого осмотра:
Внешний вид новорожденного настолько характерный, что опытный неонатолог предполагает диагноз уже на основании простого осмотра:
- Масса новорожденного выше нормы или на ее верхней границе;
- Наблюдается отечность стоп, кистей, личика. Бросается в глаза по сравнению с другими новорожденными более плотная кожа ребенка;
- При прикосновении ощущается неожиданно низкая температура тела;
- Ребенок с врожденным гипотиреозом вялый, мало плачет, сосательный рефлекс слабый, что нередко путают с ослабленным аппетитом;
- Однако, при этом ребенок интенсивно набирает вес. Масса тела растет не за счет жира, а из-за нарастающих отеков. При врожденном гипотиреозе и у новорожденного, и у ребенка, и у взрослого в подкожном жире скапливаются вещества в целом безвредные, но имеющие неприятное свойство задерживать жидкость. Из-за этого отеки при любом гипотиреозе такие плотные, а кожа кажется утолщенной.
Более достоверные лабораторные данные можно получить не раньше, чем на 4–5 день, поскольку до этого в крови новорожденного можно обнаружить еще материнские гормоны. Есть тест-полоски, на них наносится капелька крови, которую у новорожденных берут из пяточек. Если таким образом выявляется избыток ТТГ, то диагноз установлен.
Следующий этап – установить причину врожденного гипотиреоза, поскольку от нее во многом зависит лечение. Врожденный гипотиреоз в случае если он «центральный», сочетается с врожденной же надпочечниковой недостаточностью. Это объясняется тем, что проблема в гипоталамусе (часть мозга, центральной нервной системы), который при этой болезни не стимулирует ни надпочечники, ни щитовидку. В этом случае лучше назначать не щитовидные гормоны, а ТТГ и непременно в комбинации с гормонами надпочечников, которые назначают первыми. К счастью, врожденный центральный гипотиреоз встречается казуистически редко.
Нелеченный врожденный гипотиреоз
Казалось бы, все просто: характерный внешний вид младенца, анализ и можно лечить. Но гораздо чаще встречаются субклинические формы врожденного гипотиреоза, которые установить нелегко. Указанные симптомы у новорожденного, разумеется, присутствуют, но выражены гораздо слабее, не бросаются в глаза и обычно остаются незамеченными, а ребенок – не вылеченным. Чаще всего из причин врожденного гипотиреоза встречается недоразвитие щитовидки, а в этом случае развивается как раз субклинический, слабовыраженный гипотиреоз.
Ребенок растет вялым и флегматичным, плотного телосложения, зачастую отстает в развитии. Это вызвано угнетением развития головного мозга. Физическое развитие тоже замедлено: позже закрываются роднички, прорезываются первые зубы. Склонность к запорам, общая отечность тоже характерны для таких деток. Отек распространяется и на носоглотку, и часто ребенок дышит ртом. Формируется аденоидный тип лица с маленьким подбородком и постоянно приоткрытым ртом. Аналогично поражается и слуховой аппарат, ухудшается слух.
Симптомы у взрослых в целом аналогичны, но добавляются проблемы с сердцем: рано появляется атеросклероз и следующая за ним ИБС. Волосы выпадают, ногти ломаются, человек склонен к депрессиям, но попытки суицида редки. Обычно этому стандартному для врожденного гипотиреоза набору присоединяется анемия. Поэтому цвет лица у человека характерного бледновато-желтоватого оттенка из-за сочетания анемии с общей отечностью.
Лишь анализы на гормоны могут указать на верный диагноз. Значительно повышается ТТГ, а щитовидные гормоны снижены. Если сделать УЗИ, то можно обнаружить уменьшение, изменение формы щитовидки.
Лечение
Симптомы врожденного гипотиреоза успешно купируются назначением щитовидных гормонов, причем лечение должно быть начато не позднее 5–17 дня после рождения человека.
Что касается детей с поздно установленным субклиническим гипотиреозом, то их состояние очень быстро отвечает на правильное лечение. Педиатры зовут это явление «катастрофическим выздоровлением». Быстро уходят отеки, ребенок активизируется, растет любознательность, развитие идет обычным темпом. Все это происходит за считанные дни, хотя гормоны в анализах крови все еще не в норме.
Сложность лечения детей щитовидными гормонами в том, что по мере роста потребность в них меняется и дозу, соответственно, подбирают заново. Что касается взрослых, то лечение в целом аналогично, дозы меняются редко (беременность, большие стрессы, менопауза и др.), а результат более предсказуем. С годами присоединяется сопутствующая патология, врачу приходится подбирать лекарства, сочетающиеся с назначаемыми постоянно щитовидными гормонами, которые человеку жизненно необходимы и не отменяются никогда.
Сегодня наиболее популярен левотироксин натрия, но и комбинированные (Т3+Т4 или Т3+Т4+йод) препараты также иногда назначают. Начальная доза всегда минимальная (50-150 мкг/сутки для взрослого, 5-15 мкг/кг для новорожденного и не менее 2 мкг/кг для ребенка), ее медленно повышают до индивидуально подходящей. Врач-эндокринолог ориентируется на уровень ТТГ: если он повышен, то и дозу надо повышать, а если понижен, то передозировка. Если человек старше 55, то строго контролируют холестерин и работу сердца, есть особенности подбора доз (см. таблицу).
У взрослых ТТГ проверяют на 1-1, 3-1 и 6-й месяцы после его нормализации, потом в первые несколько лет анализы повторяют раз в полгода, а потом не реже года. Дети быстрее отвечают на лечение нормализацией ТТГ – уже на 2–3 неделю. Если хоть в одном анализе ТТГ не в норме, то заново начинают подбор дозы.
Врожденный гипотиреоз обычно требует постоянного, длительного приема лекарств. Однако на продолжительность, качество жизни назначаемые врачом щитовидные гормоны в правильной дозировке влияют только положительно.
Регулярный прием щитовидных гормонов в правильной дозе позволяет ребенку поддерживать тот же темп развития, что и у его сверстников.
endokrinplus.ru
Массовое обследование новорожденных на наследственные болезни. Врожденный гипотиреоз — Красноярский краевой медико-генетический центр

Прочтите и возьмите себе на заметку, особенно если вы молодые люди
В России уже много лет проводится массовое обследование новорожденных для выявления у них нескольких наследственных заболеваний. Такое обследование проводится во многих странах и называется скринингом новорожденных или неонаталъным скринингом.
Целью скрининга новорожденных является, конечно, не само выявление новорожденных с еще не проявившимися наследственными заболеваниями, а их лечение, которое позволяет предотвратить появление клинических симптомов, во многих случаях весьма тяжелых, или даже фатальных. В результате рано начатого и аккуратно проводимого лечения вместо тяжело больных детей, а затем подростков и взрослых, получаются здоровые люди, полноценные члены общества, нередко являющиеся гордостью семьи.
Скрининг новорожденных в России ведется в отношении 5 наследственных и врожденных заболеваний: фенилкетонурии, гипотиреоза, галактоземии, адрено-гениталъного синдрома и муковисцидоза.
ЧТО ТАКОЕ ВРОЖДЕННЫЙ ГИПОТИРЕОЗ?
Врожденный гипотиреоз, как следует из его названия, проявляется с рождения и обусловлен полным или частичным нарушением функции щитовидной железы. Щитовидная железа производит содержащие йод гормоны. Эти гормоны очень важны для нормального роста, развития мозга и многих других функций организма любого человека, так как они влияют на скорость обмена веществ. В большинстве случаев врожденный гипотиреоз обусловлен либо отсутствием щитовидной железы, либо ее недоразвитием, либо неправильным положением. Примерно в 15-20% случаев врожденный гипотиреоз возникает из-за того, что щитовидная железа не способна образовывать в нужном количестве гормоны. Если врожденный гипотиреоз не лечить, то у ребенка резко замедляется рост, развивается умственная отсталость и появляются другие клинические признаки заболевания. Болезнь все время прогрессирует и может привести к пожизненной инвалидности. Однако если лечение начато в первый месяц после рождения, то в абсолютном большинстве случаев ребенок развивается нормально.
КАК ЧАСТО ВСТРЕЧАЕТСЯ ВРОЖДЕННЫЙ ГИПОТИРЕОЗ?
Врожденный гипотиреоз встречается повсеместно с примерно одинаковой частотой — 1 больной на 3000-4000 новорожденных. Такая же частота врожденного гипотиреоза и в России. У девочек по невыясненным причинам врожденный гипотиреоз обнаруживается вдвое чаще, чем у мальчиков.
КАК НАСЛЕДУЕТСЯ ГИПОТИРЕОЗ?
Примерно 80-85% случаев врожденного гипотиреоза ненаследственные, они возникают случайно и обычно обусловлены нарушением развития щитовидной железы, причины которого остаются неизвестными. Однако в оставшихся 15-20% случаях гипотиреоз наследуется, как правило, как аутосомно-рецессивное состояние, когда больные накапливаются в одном поколении. Схема такого наследования приведена на рисунке, на котором изображен фрагмент родословной семьи, в которой родился ребенок, больной наследственным гипотиреозом. На родословной мужчины обозначены квадратиком, а женщины — кружочком. Внутри этих квадратиков и кружочков нарисована только одна хромосома из 23 пар, имеющихся у человека. Она имеет нормальный или дефектный (мутантный) ген гипотиреоза, последний помечен черной точкой.
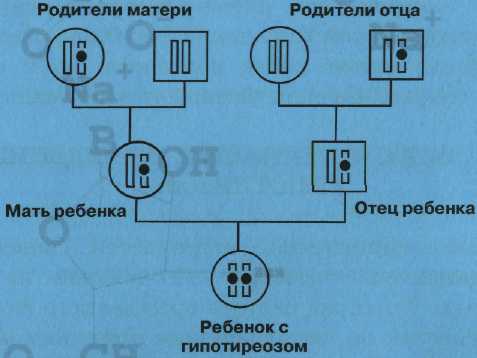
На рисунке для простоты изображена только хромосома, содержащая ген, изменения (мутации) в котором вызывают гипотиреоз. У ребенка в обеих хромосомах содержится мутантный ген и поэтому он болен. У каждого из родителей мутантный ген содержится только в одной хромосоме, а вторая хромосома нормальная и поэтому они здоровы. Такие люди, имеющие нормальный и измененный ген, называются носителями мутантного гена.У бабки по матери мутантный ген также имеется только в одной хромосоме, как и у деда со стороны отца. Они, как и родители больного ребенка, здоровы, но передали хромосомы, содержащие мутантный ген, своим детям. У вторых деда и бабки обе хромосомы содержат только нормальный ген. Таким образом, при рецессивном наследовании болен только тот член семьи, который получил от своих родителей обе хромосомы, несущие мутантный ген. Все остальные члены семьи здоровы, в том числе и те, кто является носителем мутантного гена.
На рисунке видно, что у родителей больного ребенка могут еще появиться больные дети. Вероятность появления больного ребенка в семьях, в которых родители являются носителями мутантного гена, составляет 1/4 или 25%. Эта вероятность не меняется от числа больных или здоровых детей в семье: для каждого, следующего ребенка риск, что он будет болен, составляет 25%. Вероятность рождения нормального ребенка, обе хромосомы которого содержат только нормальный ген, так же равна 25%. Вероятность появления детей, у которых имеется один нормальный и один мутантный ген, составляет 50%. У человека известно, по меньшей мере, 7 генов, мутации которых ведут к гипотиреозу. Поэтому молекулярно-генетический анализ при врожденном гипотиреозе сложный и не всегда эффективный. Однако, поскольку врожденный гипотиреоз, как наследственной природы, так и не наследственной, при раннем выявлении хорошо лечится, в таком генетическом анализе нет особой нужды.
ЧТО ТАКОЕ СКРИНИНГ НОВОРОЖДЕННЫХ НА ГИПОТИРЕОЗ?
Для того чтобы избежать развития тяжелых клинических проявлений гипотиреоза, надо, чтобы новорожденный в первые дни жизни был тестирован на гипотиреоз. В России скрининг новорожденных на гипотиреоз проводится в абсолютном большинстве территорий. Он заключается в том, что у новорожденного на 4 — 5 день жизни перед выпиской из родильного дома берут из пятки несколько капель крови, которую наносят на специальную фильтровальную бумагу. Кровь высушивается, и такой бланк, на котором указана фамилия новорожденного и ряд других сведений, необходимых для его идентификации, переправляется в лабораторию региональной медико-генетической консультации. В лаборатории определяют содержание в ней уровня гормонов щитовидной железы. Если их уровень оказывается нормальным, то это означает, что у ребенка нет гипотиреоза. Если же уровень гормонов щитовидной железы в крови низкий, то возникает подозрение на гипотиреоз. Таких детей лаборатория через врача педиатра, так как новорожденный к этому времени уже выписан из родильного дома, вызывает на повторное исследование. Обычно в это время родители узнают, что первый тест на гипотиреоз у их ребенка оказался ненормальным. У них появляется повод для беспокойства. Повторное тестирование образца крови является решающим. В ряде случаев при повторном исследовании уровень гормонов щитовидной железы оказывается нормальным. Это означает, что результат первого исследования был неверный (его называют ложноположительным). Причины этого могут быть связаны как с состоянием младенца на момент взятия крови, так и с какой-то ошибкой лаборатории. Этот результат, свидетельствующий о том, что у ребенка нет гипотиреоза, сразу же сообщается родителям, и они могут успокоиться.
ЧТО ДЕЛАТЬ, ЕСЛИ ДИАГНОЗ ГИПОТИРЕОЗА НА СКРИНИНГЕ ПОДТВЕРДИЛСЯ?
Если и при втором тестировании у ребенка уровень гормонов щитовидной железы в крови остается низким, то это означает, что ребенок болен гипотиреозом. В этом случае семья немедленно приглашается в медико-генетическую консультацию. Здесь родителям объясняют, что собой представляет гипотиреоз, и направляют больного к эндокринологу, который назначает лечение и будет наблюдать за ребенком в дальнейшем. Врожденный гипотиреоз лечится ежедневным приемом гормонов щитовидной железы. Если лечение начато рано, то клинические симптомы врожденного гипотиреоза у ребенка не проявятся, и он будет расти здоровым, не отличаясь от сверстников. Периодически семья должна будет посещать эндокринолога и осуществлять лабораторный контроль за лечением ребенка.
krasmgc.ru
Врожденный гипотиреоз у новорожденных: симптомы, лечение
Эндокринные заболевания, которые с рождения характеризуются пониженной функциональностью щитовидной железы, классифицируются, как врожденный гипотиреоз.

Заболевание у младенцев встречается достаточно редко (1: 5000). Опасность заболевания заключается в гормональной недостаточности, что значительно затормаживает формирование психомоторики и нервно-психического формирования у детей. Среди младенцев женского пола врожденный гипотиреоз отмечается значительно чаще.
Роль щитовидной железы
Щитовидная железа — это основной орган эндокринной системы человека, который играет в организме следующую роль:
- Контролирование основных обменных процессов и температурного режима.
- Нормализация обменных кальциевых процессов.
- Влияние на формирование интеллектуального развития больного.
- У детей щитовидная железа формирует скелетную мускулатуру и отвечает за развитие нервных функций.
В нормальном состоянии тип гормонов, производимых щитовидной железой определяется тироксином и трийодтиронином. Если подтверждена диагностика заболевания, то врожденный гипотиреоз способен вызвать у детей заторможенность нервно-психического развития.
Факторы развития заболевания
- Главной причиной появления гипотиреоза является поражение непосредственно самой железы. При этом заболевание определяется, как первичный врожденный гипотиреоз. Иногда может развиться вторичный гипотиреоз, обусловленный поражением гипоталамуса или гипофиза. Это может сопровождаться серьезными нарушениями эндокринной системы.
- Кроме того, причины развития врожденной формы заболевания определяются наследственным фактором. Генетика играет важную роль для наследования заболевания на стадии внутриутробного развития ребенка, что объясняется генетическими мутациями.

- Причины заболевания могут напрямую зависеть от сниженной чувствительности щитовидной железы к йодсодержащим препаратам, что приводит к нарушению транспортной функции по доставке веществ, которые требуются для обеспечения гормонального синтеза.
- Наиболее часто диагностика показывает снижение восприимчивости к гормонам тироидного ряда. Нередко такое явление возникает при употреблении беременной женщиной специальной антитироидной терапии.
Патогенез заболевания
Причины заболевания при внутриутробном развитии плода заключаются в недостаточной функциональности щитовидной железы, что приводит к восполнению тироидного гормона, который преодолевает плацентарный барьер, из организма матери.
После родоразрешения уровень этих гормонов у новорожденного резко понижается, а они крайне необходимы для формирования нервной системы у новорожденных. Особенно нуждаются в них дети с хроническими патологиями.
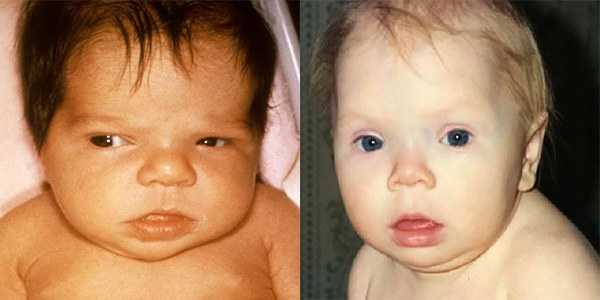
В том случае, когда диагностика подтверждает предварительный диагноз, возникает формирование необратимых процессов в коре головного мозга у детей. В критической степени ребенок может страдать умственной отсталостью, а при наиболее тяжелом развитии симптоматики, возможно такое осложнение, как кретинизм.
Однако при своевременно начатых терапевтических мероприятиях (наиболее оптимальным считается 1 неделя жизни малыша), симптомы нарушения ЦНС могут отсутствовать.
Диагностика врожденного гипотириоза
В первую очередь диагностика заболевания предполагает неонатальный скрининг, который подразумевает выявление уровня тиреотропного гормона (ТГТ) в пятнах крови, предварительно нанесенных на фильтрованный лист бумаги и высушенных. Неонатальный скрининг проводится на пятый день жизни малыша, когда снижается ТГТ. Обследование которое проводится в нарушении этих сроков, приводит к ложноположительным результатам.

Если ТГТ после проведенного исследования более 100 мЕд/л, этиология врожденной формы гипотиреоза не вызывает сомнения. Если показатели ТГТ от 20 до 50 мЕд/л рекомендуется провести повторный анализ.
Важно понимать, что этиология гипотиреоза в период новорожденности — это первоочередная задача для формирования дальнейшей терапии.
Проведение дифференциальной диагностики
Врожденный гипотиреоз следует отличать от транзиторной формы гипертиротропинемии, что предполагает нестойкое изменение уровня ТГТ, определяемого при скрининге на врожденный гипотиреоз. Если присоединяется транзиторное понижение ТГТ, можно предполагать транзиторный гипотиреоз.
Факторами, провоцирующими развитие транзиторной формы гипертиротропинемии у новорожденных, являются:
- значительный дефицит йода;
- низкий вес при рождении;
- преждевременные роды;
- внутриутробное инфицирование и гипотрофия;
- прием беременной женщиной тиреостатических препаратов;

- аутоиммунные нарушения у беременной женщины.
По мере тяжести симптоматики у детей, может проводиться повторный скрининг на врожденный гипотиреоз и определение транзиторной гипертиротропинемии.
Симптоматика заболевания
Как правило, врожденный гипотиреоз практически никак не дает о себе знать в первых 7-10 дней жизни малышей. Негативная симптоматика в это время способна возникнуть лишь у 1-2% малышей. Первые характерные симптомы появляются через 2-3 месяца, когда становятся заметны незначительные отклонения в развитии детей.
Наиболее типичные симптомы заболевания у новорожденных заключаются в следующем:
- если дети рождаются с массой тела более 3500 кг;
- пастозный тип лица и приоткрытый рот при дыхании;
- образование отеков в надключичной ямке;
- у новорожденных во время плача отмечается сиплый голос;
- возможна длительно не проходящая желтуха новорожденных;
- нередко дыхательная недостаточность сопровождается цианозом носогубной области.

С 3-4 месяца жизни ребенка симптомы заболевания проявляются:
- снижением (или полным отсутствием) аппетита;
- у грудных детей возможны частые запоры;
- кожа сухая и отмечается ее шелушение;
- достаточно часто у новорожденных наблюдается гипотермия.
Характерная симптоматика заболевания детей от 6 месяцев:
- задержка в физическом развитии;
- несвоевременное появление молочных зубов;

- у некоторых малышей возможны задержки психосоматики.
Важно учитывать, что врожденный гипотиреоз в первые несколько дней от рождения малыша можно выявить, опираясь только на симптоматику заболевания. Эта задача успешно решается при помощи скрининга, поэтому ранний неонатальный скрининг должен быть проведен у малышей сразу после рождения. От своевременно начатых терапевтических процедур (не позднее 1 месяца от рождения) зависит дальнейшее развитие малыша, так как недостаточное присутствие гормонов в первые 2-3 недели жизни малыша способно спровоцировать необратимые последствия в дальнейшем.
Лечение гипотириоза
Заболевание у детей, а также у взрослых пациентов лечится методом заместительной терапии с применением тиреоидной гормональной терапии.
- Наиболее часто назначается прием таблеток Эутирокса (тироксина), которые практически ничем не отличаются от тироксина, образующегося естественным путем в человеческом организме. Реже назначается комплексная терапия Эутироксом и Трийодтиронином. Такой тип лечения считается более физиологичным;
- лечение врожденного гипотиреоза Эутироксом назначается с минимальной дозировки (от 12,5 до 25 мкг) с постепенным полным замещением гормонов. Спустя 15-20 дней дозировка препарата должна составлять от 100 до 150 мкг ежедневно;
- взрослым пациентам и малышам с гипотиреозом нередко назначается Левотироксин. Начальная дозировка препарата зависит от степени тяжести симптоматики, длительности нелеченого заболевания и общего состояния сердечной системы. У взрослых пациентов начальная доза Левотирексина составляет 75-100 мкг в сутки с постепенным увеличением. Левотироксин следует принимать натощак за 30 минут до приема пищи;
- кроме того, до начала лечения необходимо проведение диагностики не менее 1 раза в полгода для определения количества ТГТ. Это позволит оценить правильность принимаемой дозировки препарата и предупредить возможные осложнения. Важно помнить, что при гипотиреозе гормонотерапия проводится на протяжении жизни больного, потому что организм не способен восстановить естественную выработку гормонов щитовидки;
- у большого количества пациентов, находящихся на гормональной терапии при резкой отмене этих лекарственных средств развивается острый приступ, именно поэтому специфическое лечение не следует прерывать.
Основная задача при лечении гипотиреоза заключается в ежедневном употреблении лекарственных препаратов. Прерывать курс категорически запрещено!
У определенного числа пациентов симптомы гипотиреоза постепенно прогрессируют, поэтому требуется постоянное наблюдение эндокринолога и корректировка гормональной дозировки. Когда заболевание возникает в результате инфекционного осложнения, то, как правило, после проведенной терапии функциональность щитовидной железы восстанавливается. Для подтверждения работоспособности проводится обязательная диагностика. Если отмена гормональных препаратов провоцирует повторные симптомы заболевания, следует возобновить терапию.
Профилактические мероприятия
Профилактика врожденного гипотиреоза предусматривает обязательную медико-генетическую консультацию взрослых пациентов, которые готовятся стать родителями, особенно если у них отягощенный наследственностью анамнез.
Достаточно часто у беременных женщин врожденный гипотиреоз провоцирует мутацию генов и аномалии формирования щитовидной железы, но при соблюдении определенных правил вполне возможно предотвратить развитие последствий у новорожденных.
- Обязательно должна быть проведена диагностика будущей матери на этапе подготовки к зачатию. В первую очередь определяется уровень тиреоидов в крови пациентки и концентрация антител по отношению к АТ-ТПО (тиреопероксидазе) и АТ-ТГ (тиреоглобулину).
 В норме эти тела должны отсутствовать в крови или составлять не более 18 Ед./мл (АТ-ТГ) и 5,6 Ед./мл (АТ-ТПО). Превышение этих антител указывает на развитие аутоиммунного воспаления щитовидной железы. Оно, как правило, прогрессирует достаточно медленно и чаще всего приводит к пожизненному заболеванию. Помимо всего вышеперечисленного, высокий уровень антител способен привести к появлению злокачественных новообразований в щитовидной железе.
В норме эти тела должны отсутствовать в крови или составлять не более 18 Ед./мл (АТ-ТГ) и 5,6 Ед./мл (АТ-ТПО). Превышение этих антител указывает на развитие аутоиммунного воспаления щитовидной железы. Оно, как правило, прогрессирует достаточно медленно и чаще всего приводит к пожизненному заболеванию. Помимо всего вышеперечисленного, высокий уровень антител способен привести к появлению злокачественных новообразований в щитовидной железе. - Если заболевание выявлено до беременности женщины, рекомендуется немедленное лечение Левотироксином, по специально разработанной индивидуальной схеме.
- Когда диагностика показала предрасположенность к заболеванию уже после наступления зачатия, тиреоидные гормоны назначаются в усиленной дозировке до устранения их недостатка в организме будущей матери.
- Пациенткам с подтвержденным гипотиреозом рекомендуется дополнительное употребление йода и йодсодержащих продуктов вместе с пищей. Это условие касается и абсолютно здоровых пациенток при беременности, потому что в это время наблюдается резкое падение гормонального уровня.
 У детей это может сопровождаться аномалиями при закладке органов и систем. Наиболее опасен такой дефицит до 12 недель беременности, так как именно на этом сроке происходит закладка всех основных физиологических функций у малыша.
У детей это может сопровождаться аномалиями при закладке органов и систем. Наиболее опасен такой дефицит до 12 недель беременности, так как именно на этом сроке происходит закладка всех основных физиологических функций у малыша. - Присутствие естественного количества тироидных гормонов в организме беременной женщины и у будущего малыша чрезвычайно важно, так как при их недостатке дети могут испытывать сильнейшую гормональную нагрузку, плоть до прерывания беременности. Поэтому во избежание такого осложнения со стороны гормональной системы назначается длительное и сложное лечение.
Необходимо помнить, что для получения эффективного и продолжительного результата категорически запрещено самостоятельное употребление гормональных препаратов, особенно когда диагноз заболевания сомнительный или не подтвержден. Это может спровоцировать тяжелые осложнения.
moyazheleza.ru

 В норме эти тела должны отсутствовать в крови или составлять не более 18 Ед./мл (АТ-ТГ) и 5,6 Ед./мл (АТ-ТПО). Превышение этих антител указывает на развитие аутоиммунного воспаления щитовидной железы. Оно, как правило, прогрессирует достаточно медленно и чаще всего приводит к пожизненному заболеванию. Помимо всего вышеперечисленного, высокий уровень антител способен привести к появлению злокачественных новообразований в щитовидной железе.
В норме эти тела должны отсутствовать в крови или составлять не более 18 Ед./мл (АТ-ТГ) и 5,6 Ед./мл (АТ-ТПО). Превышение этих антител указывает на развитие аутоиммунного воспаления щитовидной железы. Оно, как правило, прогрессирует достаточно медленно и чаще всего приводит к пожизненному заболеванию. Помимо всего вышеперечисленного, высокий уровень антител способен привести к появлению злокачественных новообразований в щитовидной железе. У детей это может сопровождаться аномалиями при закладке органов и систем. Наиболее опасен такой дефицит до 12 недель беременности, так как именно на этом сроке происходит закладка всех основных физиологических функций у малыша.
У детей это может сопровождаться аномалиями при закладке органов и систем. Наиболее опасен такой дефицит до 12 недель беременности, так как именно на этом сроке происходит закладка всех основных физиологических функций у малыша.