Внутриутробная гипоксия плода что это: Гипоксия плода: симптомы, признаки и последствия
Гипоксия плода: симптомы, признаки и последствия
Во время ожидания ребенка будущая мама иногда сталкивается с диагнозами, которые вызывают тревогу. Один из них – гипоксия плода, достаточно распространенное состояние у беременных, при котором нужна квалифицированная помощь врача. Что такое гипоксия плода, чем она опасна и каковы особенности лечения?
пятница, июня 15th, 2018
Присоединяйтесь к Клубу Заботливых Мам NestleBaby®!
Зарегистрируйся сегодня
Получайте полезные советы и принимайте участие в тестировании продукции
Причины гипоксии плода
Гипоксия плода – состояние, при котором ребенок в утробе испытывает сильный дефицит кислорода. Хроническая гипоксия бывает при беременности, острая – во время родов.
Существует много факторов, приводящих к патологии. К ним относятся следующие причины:
- Заболевания беременной, которые появились еще до зачатия: гипертония, болезни сердца и почек, сахарный диабет, бронхиты (острого и хронического течения), бронхиальная астма.

- Патологии вынашивания: гестоз, эклампсия, многоводие, фетоплацентарная недостаточность, токсикозы, переношенная беременность.
- Заболевания плода, при котором нарушается внутриутробное развитие, наследственно-генетические отклонения (часто гипоксия плода наблюдается при гемолитической болезни).
- Вынашивание двух и больше детей.
- Стремительные или затяжные роды, отслойка плаценты, обвитие пуповиной.
Гипоксию плода иногда вызывают внешние факторы: неудовлетворительная экология, прием некоторых лекарств, химическое отравление. Риск патологии еще выше у будущих мам, которые курят и злоупотребляют алкоголем.
Каковы симптомы дефицита кислорода у ребенка?
Важно распознать признаки гипоксии плода на ранней стадии, чтобы вовремя начать лечение и предупредить развитие тяжелых нарушений.
Ярких симптомов нехватки кислорода не существует. Поэтому будущая мама должна ориентироваться на количество шевелений ребенка. Согласно нормам, он должен давать о себе знать 3 – 10 раз в день.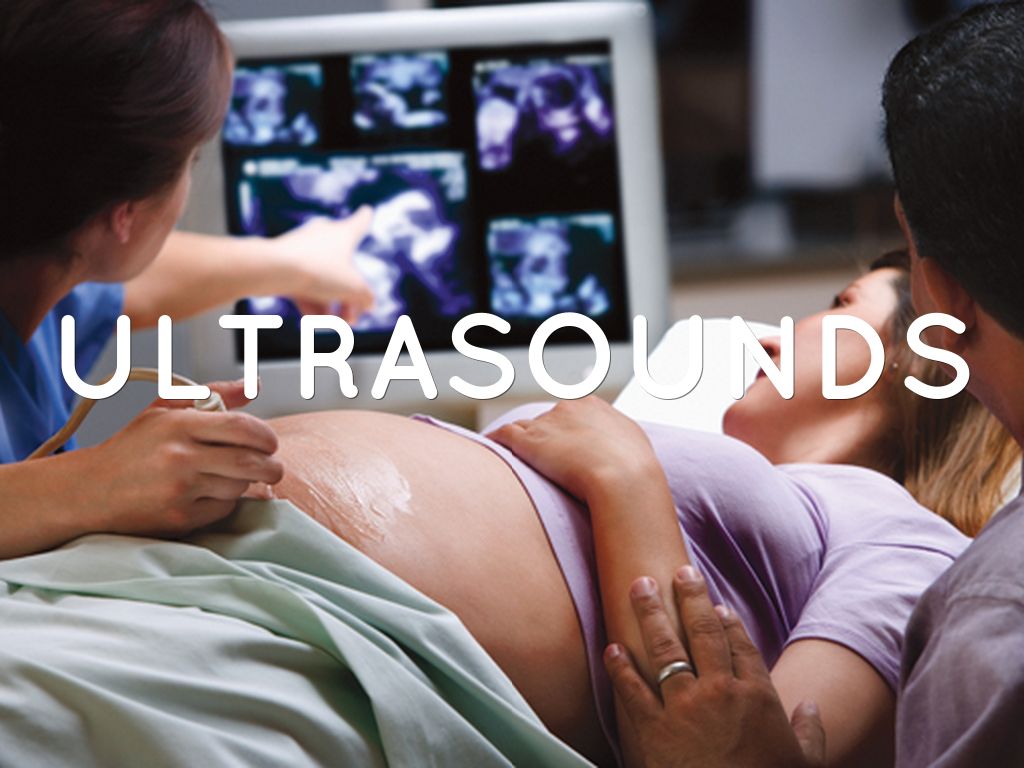 Чем больше срок вынашивания, тем интенсивнее должны быть движения. Если же малыш в утробе затих или, наоборот, слишком активен, следует срочно обратиться в поликлинику.
Чем больше срок вынашивания, тем интенсивнее должны быть движения. Если же малыш в утробе затих или, наоборот, слишком активен, следует срочно обратиться в поликлинику.
Гипоксия плода: последствия и осложнения
Дефицит кислорода имеет тяжелые последствия для плода. На ранних сроках вынашивания закладываются органы и системы маленького человека. В этот период гипоксия может нарушить образование нервной системы, сердца, головного мозга, почек.
Во второй половине беременности дефицит кислорода – частая причина отклонения в развитии сердца, легких, мозга, задержки роста малыша. У новорожденного возможен маленький вес, неврологические и психические заболевания.
Гипоксия плода тяжелого течения иногда приводит к внутриутробной гибели ребенка или его смерти в первые сутки жизни. Поэтому важно знать, что делать при гипоксии плода во время беременности.
Как диагностируют патологию?
Если ближе к концу беременности женщина может следить за количеством шевелений ребенка, то в первом и начале второго триместра трудно заподозрить гипоксию. Это значит, что будущей маме следует регулярно показываться врачу.
Это значит, что будущей маме следует регулярно показываться врачу.
При подозрении на гипоксию плода, акушер прослушивает частоту сердцебиения малыша. Для этого используется стетоскоп. Затем назначает следующие методики диагностирования:
- УЗ-исследование. С его помощью врач изучает состав и объем околоплодных вод. Слишком большое количество жидкости, также как и недостаточное, указывает на риск развития гипоксии плода.
- Допплерометрия. Позволяет узнать скорость движения крови в сосудах плаценты и пуповины.
- Кардиотокография. С ее помощью оценивается, как часто двигается плод, и количество сокращений его сердца.
- Амниоскопия. Состояние плода определяется по цветовым характеристикам и прозрачности околоплодной жидкости.
Что делать при гипоксии плода во время беременности?
Будущей маме, в зависимости от степени патологии, назначают амбулаторное или стационарное лечение. Оно направлено на устранение причины состояния и профилактику возможных последствий.
Коррекция образа жизни
Беременной необходим полный покой. Для улучшения кровотока в матке, обеспечения отдыха назначается постельный режим.
После улучшения состояния будущей маме обычно рекомендуются физические занятия, направленные на активизацию кровотока. Хороший эффект оказывает дыхательная гимнастика, аквааэробика. Все упражнения следует делать под контролем медицинского специалиста.
Лекарственная терапия
При необходимости врач назначает беременной лекарственные средства для улучшения обменных процессов. Прием их предупреждает гипоксию плода. Обычно применяются следующие лекарства:
- Гинипрал, Магне В6 – для снижения тонуса матки;
- Но-шпа, Эуфиллин – для расширения и улучшения состояния сосудов плаценты;
- Актовегин, Трентал – для нормализации показателей крови.
Если состояние ребенка не улучшилось после проведенного консервативного лечения, на сроке после семи месяцев делают кесарево сечение.
Зная, что такое гипоксия плода, каковы ее признаки, можно вовремя заподозрить патологию. Это позволит срочно обратиться к врачу, поможет улучшить состояние ребенка, и в результате, – предупредить серьезные последствия.
Похожие статьи:
Шевеление ребенка
Первые шевеления
Алкоголь и курение на ранних сроках беременности
Подробнее
УЗИ с доплером при беременности
Своевременная диагностика нарушений состояния плода позволяет вовремя провести соответствующее лечение, определить тактику ведения беременности. Однако обычными клиническими методами достоверно установить эти состояния не всегда можно. В настоящее время разработаны специальные методы диагностики состояния плода во время беременности. Из них одним из основных является УЗИ при беременности, обладающее высокой информативностью, а так же безвредностью для матери и плода.
С помощью УЗИ при измерении плода можно выявить несоответствие измеряемых размеров плода нормативным для данного срока беременности, что свидетельствует о нарушении жизнедеятельности плода и наличии синдрома задержки развития.
При благоприятном течение беременности у здоровых женщин обычно проводится 3 плановых сеанса УЗИ, соответственно триместрам беременности. В случаях выявления отклонений от нормы, развития осложнений беременности, а также у женщин с тяжелыми заболеваниями (сахарный диабет, заболевания почек, сердца и т.п.) УЗИ при беременности выполнятся чаще, что позволяет своевременно обнаружить отклонения от нормы и отследить динамику выявленных изменений. При проведении планового УЗИ в 30-34 недели обязательным компонентом обследования является допплерометрия (доплер).
Известно, что одним из основных факторов, приводящих к нарушению внутриутробного развития плода, являются нарушения кровообращения в системе мать-плацента-плод. Доплер дает возможность оценить реальное состояние кровоснабжения плаценты и матки, то есть маточно-плацентарный кровоток, и состояние плода. При допплерометрии обычно изучают состояние кровообращения в сосудах матки, пуповины и плода (аорта, среднемозговая артерия).
Как правило, плановый доплер назначают в начале третьего триместра. Однако важно помнить, что важным преимуществом УЗИ с доплером при беременности является возможность прогнозировать развитие таких серьезных осложнений как гестоз, СЗРП, внутриутробная гипоксия плода. А это, соответственно, позволяет провести своевременную адекватную профилактику в каждом конкретном случае.
Поэтому в группах риска первое проведение УЗИ с допплером желательно на сроках 20 — 24 недели беременности. Обследование на этих сроках необходимо проводить в группах риска по развитию таких осложнений беременности, как гестоз, внутриутробная гипоксия и задержка развития плода. Если есть необходимость, допплер может быть назначена в любые сроки беременности.
Показания к проведению УЗИ с доплером при беременности:
- Со стороны матери (сахарный диабет, артериальная гипертензия, заболевания почек, седечно-сосудистой системы, гестоз)
- Со стороны плода (многоплодная беременность, маловодие, синдром задержки внутриутробного развития плода — СЗРП, преждевременное созревание плаценты)
-
Отягощенный акушерский анамнез (сведения, полученные от женщины о предыдущих беременностях) – внутриутробная гибель плода, СЗРП, гестоз.

Акушеры-гинекологи ГС-клиники могут предложить Вам весь комплекс современного обследования плода при беременности.
Главная
25 февраля 16:58
Конгресс, посвященный Всемирному дню борьбы с ожирением3–5 марта 2021 года состоится Конгресс, посвященный Всемирному дню борьбы с ожирением. Мероприятие пройдет в онлайн-формате. В Конгрессе примут участие постоянные авторы журнала «Доктор.Ру» – Аметов А.С., Анциферов М.Б., Арутюнов Г.П., Баранов И.И., Лила А.М., Петеркова В.А., Сухих Г.Т., Шабунин А.В., Юренева С.В., Ходжаева З.С., Ярмолинская М.И.
25 февраля 10:58
Онлайн-семинар «GOLD 2021 и COVID-19: актуальные вопросы»25 февраля в 15:00 (мск) приглашаем на
онлайн-семинар постоянных авторов журнала «Доктор.Ру» Лещенко Игоря Викторовича,
д. м. н., профессора кафедры фтизиатрии и пульмонологии ФГБОУ ВО «Уральский
государственный медицинский университет» Минздрава России, и Визеля Александра
Андреевича, д. м. н., профессора, заведующего кафедрой фтизиопульмонологии
ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России
м. н., профессора кафедры фтизиатрии и пульмонологии ФГБОУ ВО «Уральский
государственный медицинский университет» Минздрава России, и Визеля Александра
Андреевича, д. м. н., профессора, заведующего кафедрой фтизиопульмонологии
ФГБОУ ВО «Казанский государственный медицинский университет» Минздрава России
25 февраля 10:56
Стратегия и тактика терапии атопического дерматитаВебинар постоянного автора журнала «Доктор.Ру» Ревякиной Веры Афанасьевны, д. м. н., профессора, заведующей отделением аллергологии ФГБУН ФИЦ питания и биотехнологии, пройдет 25 февраля в 17:00 (мск)
20 февраля 15:11
Атопический дерматит и ихтиоз: особенности ухода за кожей24 февраля в 13:00 (мск) приглашаем на вебинар автора журнала «Доктор.Ру» Корсунской Ирины Марковны, д. м. н., профессора, заведующей лабораторией физико-химических и генетических проблем дерматологии ФГБУН «Центр теоретических проблем физико-химической фармакологии Российской академии наук»
Все новостиСовременные методы диагностики гипоксии плода в родах с применением прямой ЭКГ плода
При внедрении кардиотокограммы плода (КТГ) в клиническую практику 30 лет назад было сделано предположение, что электронный мониторинг плода в родах позволяет улучшить диагностику внутриутробной гипоксии плода. Это привело к увеличению количества необоснованных оперативных вмешательств путем кесарева сечения. Однако увеличение процента кесаревых сечений не улучшает перинатальные показатели. В связи с этим возникла необходимость применения дополнительных методов исследования плода — прямая ЭКГ плода. В наше время в США, Англии и Швеции с целью регистрации прямой ЭКГ плода используется прямой скальпель-электрод, который позволяет фиксировать ЭКГ плода в родах.
Это привело к увеличению количества необоснованных оперативных вмешательств путем кесарева сечения. Однако увеличение процента кесаревых сечений не улучшает перинатальные показатели. В связи с этим возникла необходимость применения дополнительных методов исследования плода — прямая ЭКГ плода. В наше время в США, Англии и Швеции с целью регистрации прямой ЭКГ плода используется прямой скальпель-электрод, который позволяет фиксировать ЭКГ плода в родах.
С помощью системы STAN осуществляется непрерывное предоставление информации о состоянии плода в родах. Эта система сочетает в себе измерение интервала RR и оценку изменений ST сегмента. Отношение высоты зубца Т и амплитуды комплекса QRS называется ТQRS соотношением, которое используется для точной оценки изменений высоты Т — зубца. Увеличение амплитуды зубца Т является классической реакцией плода на гипоксию и указывает на наличие хороших компенсаторных возможностей у плода. Степень увеличения амплитуды зубца Т зависит от количества утилизируемой глюкозы, необходимой для обеспечения энергетического баланса в миокарде.
Двухфазный интервал ST может наблюдаться в двух ситуациях: действие гипоксии на кардиомиоциты при отсутствии адекватных компенсаторных возможностей плода, а также при пороках сердца и инфекции.
Информация о характере интервала ST должна анализироваться с учетом данных КТГ. В случае изменения характера КТГ при анализе интервала ST можно получить подробную информацию о тяжести состояния плода.
Нами проведено 185 родов с параллельной оценкой КТГ и прямой ЭКГ плода на базе родильного дома № 2. Показаниями для применения STAN явились признаки интранатального дисстресса плода при гестозе второй половины беременности, анемии беременных, перенашивании беременности, роды крупным плодом, аномалиях родовой деятельности.
Контрольную группу составили 30 рожениц, роды у которых велись без применения системы STAN.
При анализе исходов родов отмечено уменьшение процента кесарева сечения в основной группе до 27%. В контрольной группе — 34%. Вакуум-экстракция плода в основной группе выполнена в четырех случаях в связи с интранатальной гипоксией плода в период изгнания. В контрольной группе — 12 случаев. Все дети имели оценку по шкале Апгар 7-10 баллов. В реабилитации нуждались 8 детей в группе применения системы STAN — вдвое меньше, чем в контрольной группе.
В контрольной группе — 12 случаев. Все дети имели оценку по шкале Апгар 7-10 баллов. В реабилитации нуждались 8 детей в группе применения системы STAN — вдвое меньше, чем в контрольной группе.
Таким образом, применение прямого ЭКГ плода в родах, с помощью системы STAN, позволяет снизить процент оперативного родоразрешения (кесарево сечение, вакуум экстракция плода) и улучшить перинатальные показатели.
Борисов А.В., Каплун И.Б.
Другие статьи
Беременность и роды после 35
Желание осуществить мечту материнства будет до тех пор, пока существует мир. Женщина 21 века стоит на одной ступени с мужчиной в достижении карьерного роста. Лишь достигнув полного совершенства в деловой сфере, большинство пар задумываются о рождении ребенка.
Бифидо и лактофлора в гинекологии
Для чего нужен приём препаратов содержащих бифидо и лактобактерии в гинекологии? Ответ можно дать коротким предложением: для восстановления микрофлоры полового канала после лечения воспалительных заболеваний и дисбактериоза.
Советы эксперта: все о визите к гинекологу
Как правило, все мы хотим от врача любой специальности одного и того же: аккуратного подробного осмотра, грамотного подхода к диагностике и лечению заболевания, доступного объяснения ситуации, информации о методах профилактики проблем со здоровьем. Особое значение эти моменты приобретают у такого врача как акушер-гинеколог.
Гипоксия победима!
Сегодня половине (!) беременных женщин, проживающих в крупных городах, гинекологи ставят диагноз «гипоксия плода». Мы привыкли считать знакомое нестрашным. Если же потратить 15 минут на самообразование в проблеме гипоксии, можно понять:
1) насколько она опасна,
2) ее можно избежать,
3) недуги ребенка, рожденного даже в тяжелой степени гипоксии, поддаются лечению (все зависит от усердия родителей).
О проблеме гипоксии нас консультирует заведующая отделением патологи беременности роддома N7 Ирина Хабировна Байрамова.
КАК ВОЗНИКАЕТ ГИПОКСИЯ
Кислород и питательные вещества поступают к плоду через маточно-плацентарный кровоток. При нарушениях этого кровотока плод получает недостаточно питательных веществ и кислорода. Этот недостаток и называют гипоксией.
Гипоксия всегда является результатом плацентарной недостаточности (нарушения функций и раннего старения плаценты). Поэтому поиск причин гипоксии — в причинах плацентарной недостаточности. А их немало:
— Инфекционные заболевания, особенно протекающие в острой форме или обостряющиеся во время беременности. В особой группе риска — женщины, не пролечившие до беременности инфекции, передающиеся половым путем.
— Различные хронические заболевания, имеющиеся у беременной (заболевания сердечнососудистой системы, почек, печени, легких).
— Гормональные нарушения в организме беременной.
— Иммунологические проблемы (например, иммунологический конфликт между мужем и женой).
Совет по избежанию этой группы причин — обследоваться до наступления беременности и пролечивать все свои недуги, дабы они не повлияли на здоровье будущего малыша. Если не получилось до беременности — в крайнем случае, в первом триместре.
Если не получилось до беременности — в крайнем случае, в первом триместре.
— Угроза прерывания беременности тоже вызывает гипоксию плода. Это состояние характеризуется повышенным сокращением мускулатуры матки, а это опять же вызывает ухудшение кровотока в матке и плаценте, и, следовательно, ограничивает приток кислорода и питательных веществ к плоду.
— Гестоз — коварное осложнение беременности, при котором питательные вещества и кислород проходят «мимо» плода (выводятся выделительной системой женщины). Даже легкий гестоз, незаметный внешне в виде отеков на теле беременной, вызывает отек плаценты и, как следствие, гипоксию.
Совет: если врач ставит вам эти диагнозы и предлагает лечение в стационаре, не отказывайтесь. Не думайте, что отеки или тянущие боли внизу живота — это только «ваши» проблемы. Данные патологии неизбежно ведут к гипоксии плода, которая обуславливает различные пороки его развития.
Для большей убедительности напомним, что в хронической форме гипоксия оказывает влияние на отклонения в развитии плода, в острой — на его жизнь. Острая форма гипоксии, вызванная повышенным тонусом матки, проявляется как одномоментный спазм сосудов маточно-плацентарного кровотока, при котором доступ кислорода к плоду прерывается. Без немедленного оказания медицинской помощи жизнь плода — под угрозой. Острая форма гипоксии, вызванная тяжелым гестозом, проявляется как отслойка плаценты. Жизнь плода в этом случае может спасти только экстренное родоразрешение.
Острая форма гипоксии, вызванная повышенным тонусом матки, проявляется как одномоментный спазм сосудов маточно-плацентарного кровотока, при котором доступ кислорода к плоду прерывается. Без немедленного оказания медицинской помощи жизнь плода — под угрозой. Острая форма гипоксии, вызванная тяжелым гестозом, проявляется как отслойка плаценты. Жизнь плода в этом случае может спасти только экстренное родоразрешение.
КАК ПРОЯВЛЯЕТСЯ ГИПОКСИЯ У НОВОРОЖДЕННОГО
В первые минуты жизни новорожденного неонатолог оценивает пять показателей его жизнеспособности по шкале Апгар:
— сердцебиение
— дыхание
— цвет кожных покров
— мышечный тонус
— наличие врожденных рефлексов
За каждый показатель в норме выставляется по 2 балла. Малыш на 9-10 баллов полностью здоров: розовенький, мышцы в тонусе (ручки и ножки прижаты к животу, голова — к груди, есть сосательный и хватательный рефлексы, крик громкий, свидетельствующий о нормальном запуске дыхательной системы, сердечный тон четкий, ясный. 8 баллов свидетельствуют о легкой степени гипоксии плода (может наблюдаться, например, незначительная синюшность кожных покровов). О средней степени гипоксии говорят, когда ребенок рождается с немного синенькими ладошками, стопами, лицом, ручки в суставах слегка разогнуты, сосет ребенок слабо, кричит тоже слабо (6 баллов). Тяжелая степень гипоксии проявляется в том, что кожные покровы новорожденного бледные, ручки и ножки разогнуты, крика нет, сосание очень слабое или отсутствует, сердцебиение есть (4 балла).
8 баллов свидетельствуют о легкой степени гипоксии плода (может наблюдаться, например, незначительная синюшность кожных покровов). О средней степени гипоксии говорят, когда ребенок рождается с немного синенькими ладошками, стопами, лицом, ручки в суставах слегка разогнуты, сосет ребенок слабо, кричит тоже слабо (6 баллов). Тяжелая степень гипоксии проявляется в том, что кожные покровы новорожденного бледные, ручки и ножки разогнуты, крика нет, сосание очень слабое или отсутствует, сердцебиение есть (4 балла).
ПОСЛЕДСТВИЯ ГИПОКСИИ
Доказано, что наиболее кислородозависимыми являются нервные клетки, поэтому от гипоксии в первую очередь страдает центральная нервная система плода. В зависимости от степени гипоксии неврологические нарушения новорожденного варьируются от функциональных (обратимых) расстройств (например, пониженный мышечный тонус, снижение активности врожденных рефлексов) до тяжелых нарушений психического развития.
Интересно, что организм плода обладает огромными компенсаторными способностями, поэтому при первых проявлениях гипоксии организм малыша начинает работать в усиленном режиме, перераспределяя кислородные потоки на критически важные для жизни органы и системы: головной мозг, сердце, надпочечники. Естественно, при этом лишаются своей «нормальной порции» кислорода и питательных веществ другие органы — легкие, почки, желудочно-кишечный тракт, кожные покровы. В них-то и могут возникнуть патологии развития в том случае, если организм плода справляется с задачей спасения от пороков развития центральной нервной системы. Однако возможности компенсаторных механизмов имеют предел, и при длительной гипоксии эта защита ослабевает.
У детей, рожденных со средней или тяжелой степенью гипоксии в период новорожденности могут наблюдаться следующие нарушения развития:
- гипотрофия (недостаточный вес),
- снижение мышечного тонуса и угнетение физиологических рефлексов (сосание, хватание),
- синдром дыхательных расстройств,
- аномалии развития — дисплазия тазобедренных суставов, кривошея, пороки сердца и др.

В будущем при отсутствии лечения дети, страдавшие гипоксией в период внутриутробного развития, могут испытывать:
- задержку развития физических и психических навыков,
- повышенное внутричерепное давление,
- частые ОРВИ и кишечные расстройства,
- синдром повышенной возбудимости.
Любые состояния гипоксии, зафиксированные на момент рождения ребенка, лечатся, — успокаивает Ирина Хабировна Байрамова. — Если в течение первого года жизни ребенка приложить все усилия для устранения последствий гипоксии, то к году ваш малыш не будет отличаться по психофизическому развитию от своих сверстников. Последствия легкой гипоксии хорошо лечатся с помощью массажей и упражнений для отдельных групп мышц. Особенно хорошо помогают упражнения в воде, поскольку они стимулируют психо-эмоциональную сферу ребенка, восстанавливая тем самым поврежденные в результате гипоксии участки мозга. Более тяжелые формы гипоксии лечат непосредственно в роддоме медикаментозными методами. Даже при хороших результатах лечения родителям важно знать, что теперь их ребенку особенно важно регулярно наблюдаться у врачей разных специальностей, главными из которых являются педиатр и невролог. Они будут осуществлять контроль за развитием психического здоровья малыша, исключать поздние проявления пороков развития нервной системы.
Даже при хороших результатах лечения родителям важно знать, что теперь их ребенку особенно важно регулярно наблюдаться у врачей разных специальностей, главными из которых являются педиатр и невролог. Они будут осуществлять контроль за развитием психического здоровья малыша, исключать поздние проявления пороков развития нервной системы.
ПОБЕДИТЬ ГИПОКСИЮ
Еще лучше лечить гипоксию плода внутриутробно, чтобы предотвратить знакомство с описанными выше неприятными диагнозами у своего малыша.
Диагноз «гипоксия плода» ваш акушер-гинеколог может поставить не ранее 28 недели беременности. Он делает это, выслушивая сердцебиение плода стетоскопом. Нормальное сердцебиение плода — 120-160 ударов в минуту. Если оно больше или меньше, можно подозревать о наличии гипоксии. Чтобы сказать наверняка, врачу необходимы результаты исследований КТГ (электрокардиограмма плода), УЗИ (смотрится степень зрелости плаценты и качество околоплодных вод). В некоторых случаях для уточнения диагноза необходимо проведение допплеровского исследования (показывает наличие или отсутствие проблем сосудистого кровотока в матке и плаценте).
В некоторых случаях для уточнения диагноза необходимо проведение допплеровского исследования (показывает наличие или отсутствие проблем сосудистого кровотока в матке и плаценте).
Если данные исследования указывают на наличие средней и тяжелой степени гипоксии, беременной обязательно нужно ложиться в стационар. Без уточняющих вопросов «А обязательно ли это?». » Я рекомендую полежать в стационаре и пройти курс лечения даже беременным с легкой гипоксией плода, — говорит Ирина Хабировна Байрамова. — Для преодоления легкой гипоксии, как правило, достаточно просто отдохнуть от забот и перестать нервничать. Но обычно этот совет гинеколога женщины либо игнорируют, либо у них просто нет возможности дома устроить себе полноценный отдых. Прибрать, приготовить, помыть, а еще есть старший ребенок, муж… Планы «полежать отдохнуть вечерком» как правило, срываются…
При лечении гипоксии в условиях стационара проводится терапия, направленная на улучшение снабжения плода кислородом и нормализацию процесса обмена веществ. Если у пациентки с тяжелой гипоксией плода не наблюдается улучшений в течение трех дней, это может свидетельствовать о наличии необратимых изменений в системе «мать-дитя» (например, об отслойке плаценты), и врачи могут принять решение о досрочном родоразрешении на любом сроке беременности (напомним, диагноз «гипоксия» ставится не ранее 28 недели) с целью сохранения жизни ребенка.
Если у пациентки с тяжелой гипоксией плода не наблюдается улучшений в течение трех дней, это может свидетельствовать о наличии необратимых изменений в системе «мать-дитя» (например, об отслойке плаценты), и врачи могут принять решение о досрочном родоразрешении на любом сроке беременности (напомним, диагноз «гипоксия» ставится не ранее 28 недели) с целью сохранения жизни ребенка.
— Здоровье большинства женщин, к сожалению, сегодня далеко не идеально, — констатирует Ирина Хабировна Б.айрамова. — Различные хронические заболевания, стрессы, усталость, чрезмерная нагрузка на работе провоцируют различные осложнения беременности. В результате диагноз «плацентарная недостаточность» ставят сегодня каждой второй беременной женщине, «угроза прерывания беременности» — каждой третьей. А если есть плацентарная недостаточность или повышенный тонус матки, значит, есть гипоксия плода. Этот диагноз встречается у 50-70% беременных женщин. Но это не означает, что можно успокоиться тем, что «у всех сейчас так». Ни в коем случае! Напоминания врачей о том, что беременной женщине нужны достаточный сон, отдых, прогулки на свежем воздухе не менее трех часов в день, хорошее питание и витамины, противопоказаны физические, умственные и эмоциональные перегрузки — не пустые слова! Даже имея отклонения в собственном здоровье, женщина может выносить здорового ребенка, если будет придерживаться этих советов. И еще — обследоваться до наступления беременности, чтобы подлечить свои хронические заболевания, исключить или пролечить заболевания, передающиеся половым путем. Крутясь, как белка в колесе в бешеном темпе нашей жизни, остановитесь на секунду и подумайте, что вам важнее — ваша работа (к которой вы еще успеете вернуться, когда малыш подрастет), чистота в доме (к которой можно попробовать относиться проще) или здоровье будущего ребенка? Ведь здоровый или практически здоровый малыш — это огромная экономия жизненных сил, денег и счастье для любой семьи. А девять месяцев — не такой долгий отрезок времени, на который можно попытаться снизить свои нагрузки на любимой работе (например, воспользоваться правом нашего законодательства о сокращении рабочего дня беременной женщины на один час), переложить на кого-нибудь часть забот по дому (или просто забыть о них!) и освоить новое увлечение — медитацию, которое позволит вам расслабляться и успокаиваться, когда эмоции зашкаливают.
Ни в коем случае! Напоминания врачей о том, что беременной женщине нужны достаточный сон, отдых, прогулки на свежем воздухе не менее трех часов в день, хорошее питание и витамины, противопоказаны физические, умственные и эмоциональные перегрузки — не пустые слова! Даже имея отклонения в собственном здоровье, женщина может выносить здорового ребенка, если будет придерживаться этих советов. И еще — обследоваться до наступления беременности, чтобы подлечить свои хронические заболевания, исключить или пролечить заболевания, передающиеся половым путем. Крутясь, как белка в колесе в бешеном темпе нашей жизни, остановитесь на секунду и подумайте, что вам важнее — ваша работа (к которой вы еще успеете вернуться, когда малыш подрастет), чистота в доме (к которой можно попробовать относиться проще) или здоровье будущего ребенка? Ведь здоровый или практически здоровый малыш — это огромная экономия жизненных сил, денег и счастье для любой семьи. А девять месяцев — не такой долгий отрезок времени, на который можно попытаться снизить свои нагрузки на любимой работе (например, воспользоваться правом нашего законодательства о сокращении рабочего дня беременной женщины на один час), переложить на кого-нибудь часть забот по дому (или просто забыть о них!) и освоить новое увлечение — медитацию, которое позволит вам расслабляться и успокаиваться, когда эмоции зашкаливают.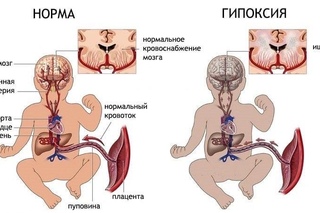
Александра Медведева
Гипоксия плода — обзор
Неонатальная асфиксия
Хроническая внутриутробная асфиксия влияет на кровоток в плаценте, а инфаркт плаценты отрицательно влияет на рост плода. В случае хронической внутриутробной асфиксии роды могут плохо переноситься, и может потребоваться реанимация новорожденных. Когда требуется реанимация новорожденных, первичные или вторичные последствия асфиксии, включая ацидоз, судороги, преходящую сердечную дисфункцию (например, кардиомиопатию или трикуспидальную недостаточность), легочную гипертензию, почечную недостаточность (например.g., острый тубулярный некроз), желудочно-кишечные / печеночные инсульты (например, некротический энтероколит [NEC]) или нарушения свертывания крови .
Послеродовая асфиксия часто является результатом ряда внутриутробных событий, но она также может быть вызвана событиями, происходящими во время родов. Механизмы контроля дыхания у незрелых детей могут предрасполагать новорожденных, особенно недоношенных, к опасным для жизни реакциям на асфиксию. Например, реакция на гипоксию в течение первых 3-4 недель жизни может быть парадоксальной, поскольку гипоксия вызывает короткий период гиперпноэ, за которым следует брадипноэ (Cross and Oppe, 1952; Brady and Ceruti, 1966).Гипотермия и гиперкапноэ притупляют начальное гиперпноэ (Ceruti, 1966; Rigatto et al., 1975). Респираторная реакция на углекислый газ усиливается как в постнатальном, так и в гестационном возрасте (см. Главу 3, Респираторная физиология у младенцев и детей) (Rigatto et al., 1975).
Например, реакция на гипоксию в течение первых 3-4 недель жизни может быть парадоксальной, поскольку гипоксия вызывает короткий период гиперпноэ, за которым следует брадипноэ (Cross and Oppe, 1952; Brady and Ceruti, 1966).Гипотермия и гиперкапноэ притупляют начальное гиперпноэ (Ceruti, 1966; Rigatto et al., 1975). Респираторная реакция на углекислый газ усиливается как в постнатальном, так и в гестационном возрасте (см. Главу 3, Респираторная физиология у младенцев и детей) (Rigatto et al., 1975).
Хотя гипоксия может иметь долгосрочные последствия для плода и новорожденного, гипероксия также может вызывать серьезные осложнения, особенно у недоношенных детей. Например, гипероксия поражает недоношенных детей, особенно рожденных до 32 недель ‘ беременность, к значительному риску ретинопатии недоношенных (ROP; см. ниже) и, в некоторых случаях, слепоты (см. главу 27, Анестезия для офтальмологической хирургии) (Sylvester, 2008).В норме Pao 2 плода составляет от 20 до 30 мм рт. После рождения Pao 2 60 мм рт. Ст., Вероятно, является гипероксичным для младенцев, рожденных в возрасте от 24 до 36 недель ‘; беременность. Чтобы избежать последствий окислительного стресса у новорожденных, сатурация кислорода для недоношенных детей обычно поддерживается в пределах от 88% до 93% (Pao 2 от 45 до 60 мм рт. уместно в операционной. Непрерывное измерение Sao 2 облегчает поддержание желаемого насыщения кислородом.Следует отметить одного недоношенного ребенка, у которого никогда не было повышенного Pao 2 , кроме как в операционной, но у которого развилась ROP после операции (Betts et al., 1977).
После рождения Pao 2 60 мм рт. Ст., Вероятно, является гипероксичным для младенцев, рожденных в возрасте от 24 до 36 недель ‘; беременность. Чтобы избежать последствий окислительного стресса у новорожденных, сатурация кислорода для недоношенных детей обычно поддерживается в пределах от 88% до 93% (Pao 2 от 45 до 60 мм рт. уместно в операционной. Непрерывное измерение Sao 2 облегчает поддержание желаемого насыщения кислородом.Следует отметить одного недоношенного ребенка, у которого никогда не было повышенного Pao 2 , кроме как в операционной, но у которого развилась ROP после операции (Betts et al., 1977).
(PDF) Причины и механизмы внутриутробной гипоксии и ее влияние на сердечно-сосудистую систему плода: обзор
International Journal of Pediatrics 7
с сердечными заболеваниями, Circulation, vol. 105, нет. 18, pp. 2179–
2184, 2002.
[48] S.C.Siu, M.Sermer, J.M.Colmanetal., «Проспективное многоцентровое исследование исходов беременности
у женщин с сердечными заболеваниями
», Circulation, vol. 104, нет. 5, pp. 515–521, 2001.
104, нет. 5, pp. 515–521, 2001.
[49] А. Хамид, И. С. Караалп, П. П. Туммала и др. «Влияние
порока сердца на исход беременности
у матери и плода», Журнал Американский колледж кардиологии, т.
37, вып. 3, pp. 893–899, 2001.
[50] П. Пресбитеро, Дж. Сомервилль, С. Стоун, Э. Арута, Д. Шпигельхал —
тер и Ф. Рабайоли, «Беременность при синюшном врожденном сердце
Болезнь: исход матери и плода // Кровообращение.89,
нет. 6, pp. 2673–2676, 1994.
[51] Дж. С. Селлман и Р. Л. Холман, «Тромбоэмболия во время беременности
: риски, проблемы и рекомендации», Пост-
Медицина, вып. 108, нет. 4, pp. 71–84, 2000.
[52] «Технический бюллетень ACOG. Заболевания легких при беременности.
Номер 224 — июнь 1996 г. Американский колледж акушеров
и гинекологов, Международный журнал гинекологии и
акушерства, т.54, нет. 2, стр. 187–196, 1996.
[53] Р. Кумар, «Пренатальные факторы и развитие астмы»,
Current Opinion in Pediatrics, vol. 20, нет. 6, pp. 682–687,
20, нет. 6, pp. 682–687,
2008.
[54] Э. С. Гай, А. Кирумаки и Н. А. Ханания, «Острая астма при беременности
», Critical Care Clinics, vol. 20, нет. 4, pp. 731–745,
2004.
[55] Л. Д. Инге и Дж. У. Уилсон, «Последние сведения о лечении туберкулеза
», American Family Physician, vol.78, No 4, с.
457–470, 2008.
[56] С. М. Роу, С. Миллер, Э. Дж. Соршер, «Кистозный фиброз», Медицинский журнал Новой Англии
, вып. 352, нет. 19, pp. 1992–
2001, 2005.
[57] EY Cheng, CH Goss, EF McKone et al., «Агрессивный пренатальный уход
приводит к успешным исходам плода у CF
женщин», Journal of Cystic Фиброз, т. 5, вып. 2, pp. 85–91,
2006.
[58] I. degaard, B. Stray-Pedersen, K.Hallberg, O.C. Haanaes,
O. T. Storrøsten и M. Johannesson, «Заболеваемость матери и
плода при беременности у норвежских и шведских
женщин с кистозным фиброзом», Acta Obstetricia et Gynecologica,
Sc. 81, нет. 8, pp. 698–705, 2002.
81, нет. 8, pp. 698–705, 2002.
[59] А. Розенберг, «IUGR новорожденный», Семинары по перинатолии,
,, т. 32, нет. 3, pp. 219–224, 2008.
[60] CH Goss, GD Rubenfeld, K. Otto, и ML Aitken,
«Влияние беременности на выживаемость у женщин с кистозным фиброзом
», Chest, vol. .124, вып. 4, стр. 1460–1468, 2003.
[61] Д.С. Хардин, Дж. Райс, Р.К. Коэн, К.Дж. Эллис и Дж. А.
Ник, «Метаболические эффекты беременности при кистозном фиброзе»,
Акушерство и гинекология, vol. . 106, нет. 2, стр. 367–375, 2005.
[62] С. В. Макколгин, Л. Гли и Б. А. Брайан, «Легочное заболевание
приказов, осложняющих беременность», Акушерство и гинекология
Клиники Северной Америки, вып. 19, нет. 4, pp. 697–717, 1992.
[63] Дж. М.Шапиро, «Критическая помощь акушерскому пациенту», Journal
of Intensive Care Medicine, vol. 21, нет. 5, pp. 278–286, 2006.
[64] С. Махаджан, Р. Аалинкил, П. Шах, С. Сингх и Н. Кочупил —
lai, «Нутритивная анемия нарушает регуляцию эндокринного контроля
плода. рост », British Journal of Nutrition, vol. 100, нет. 2, pp.
рост », British Journal of Nutrition, vol. 100, нет. 2, pp.
408–417, 2008.
[65] PN Singla, M. Tyagi, A. Kumar, D. Dash, R. Shankar,
«Рост плода при материнской анемии», Journal of Tropical
Педиатрия, т.43, нет. 2, pp. 89–92, 1997.
[66] PN Baker, SJ Wheeler, TA Sanders et al., «Проспективное исследование
статуса микронутриентов у подростков при беременности»,
American Journal of Clinical Nutrition, vol. .89, No 4, стр.
1114–1124, 2009.
[67] Л. Х. Аллен, «Беременность и дефицит железа: нерешенные проблемы
», Nutrition Reviews, vol. 55, нет. 4, pp. 91–101, 1997.
[68] DJP Barker, AR Bull, C. Osmond, and SJ Simmonds,
«Размер плода и плаценты и риск гипертонии в жизни взрослого
», British Medical Journal , т.301, нет. 6746, pp. 259–262,
1990.
[69] Т. Т. Лао и В. М. Вонг, «Плацентарное соотношение — его связь
с легкой материнской анемией», Плацента, том 18, № 7, стр.
593–596, 1997.
[70] Л.А. Уильямс, С.Ф. Эванс и Дж. П. Ньюнхэм, «Проспективное когортное исследование
факторов, влияющих на относительный вес плаценты
и новорожденного», British Medical Journal,
об. 314, нет. 7098, стр. 1864–1868, 1997.
[71] С. К. Дэвис, Э. Кронин, М. Гилл, П. Грингросс, М. Хикман,
и К. Норманд, «Скрининг серповидноклеточной анемии и лассемии
: систематический обзор с дополнительными исследованиями. , ”
Health Technology Assessment, vol. 4, вып. 3, pp. 1–87, 2000.
[72] А. Г. Мотульски, «Частота серповидных расстройств у чернокожих в США
», Медицинский журнал Новой Англии, вып. 288, нет.
1, стр. 31–33, 1973 г.
[73] «Практический бюллетень ACOG, №78: гемоглобинопатии при беременности
, Акушерство и гинекология, т. 109, нет. 1, pp.
229–238, 2007.
[74] П.М. Сан, У. Уилберн, Б.Д. Рейнор и Д. Джеймисон, «Серповидноклеточная болезнь
у беременных: двадцать лет опыта в Grady
Memorial. Больница, Атланта, Джорджия », Американский журнал
Больница, Атланта, Джорджия », Американский журнал
акушерства и гинекологии, т. 184, нет. 6, pp. 1127–1130,
2001.
[75] M.Koshy, L.Burd, D.Wallace, A.Moawad, andJ.Барон,
«Профилактические переливания эритроцитов беременным с серповидно-клеточной анемией
». Рандомизированное совместное исследование », The New
England Journal of Medicine, vol. 319, нет. 22, pp. 1447–1452,
1988.
[76] Х. Казазян-младший, «Синдромы талассемии: молекулярная основа
и пренатальная диагностика в 1990 году», Семинары по гематологии
ogy, vol. 27, нет. 3, pp. 209–228, 1990.
[77] A. Aessopos, F. Karabatsos, D.Фармакис и др., «Беременность у
пациенток с хорошо пролеченной β-талассемией: исход для моли
и новорожденных», Американский журнал акушерства и
гинекологии, т. 180, нет. 2, часть 1, стр. 360–365, 1999.
[78] CE Jensen, SM Tuck и B. Wonke, «Фертильность при большой βtha-
лассемии: отчет о 16 беременностях, предварительная оценка
и обзор литературы », Британский журнал
акушерства и гинекологии, вып. 102, нет. 8, pp. 625–629,
102, нет. 8, pp. 625–629,
1995.
[79] Х. К. Онг, Дж. К. Уайт и Т. А. Синнатур, «Гемоглобин
БолезньH и беременность у малазийской женщины», Acta
Haematologica, vol. 58, нет. 4, pp. 229–233, 1977.
[80] JERamsay, F.Stewart, IAGreer, and N.Sattar,
«Дисфункция микрососудов: связь между преэклампсией
и ишемической болезнью сердца матери». BJOG, т. 110, нет. 11,
pp. 1029–1031, 2003.
[81] B.Дж. Уилсон, М. С. Уотсон, Г. Дж. Прескотт и др., «Гипертоническая болезнь
беременных и риск гипертонии и инсульта в
более позднем возрасте: результаты когортного исследования», British Medical Journal,
vol. 326, нет. 7394, pp. 845–849, 2003.
[82] Л. Хауккамаа, М. Салминен, Х. Лайвуори, Х. Лейнонен,
В. Хиилесмаа и Р. Каая, «Риск для последующей коронарной
артерии. болезнь после преэклампсии », American Journal of Cardi-
ology, vol.93, нет. 6, pp. 805–808, 2004.
[83] Д. Дж. П. Баркер, «Рост в утробе матери и ишемическая болезнь сердца»,
Дж. П. Баркер, «Рост в утробе матери и ишемическая болезнь сердца»,
Nutrition Reviews, vol. 54, нет. 2, pp. S1 – S7, 1996.
клинических последствий и терапевтических перспектив
Исследования и отчеты в области неонатологии, 2015: 5
представьте свою рукопись | www.dovepress.com
Dovepress
Dovepress
88
Thompson et al
43. Laresgoiti-Servitje E, Gomez-Lopez N.Патофизиология преелькампсии
включает измененные уровни ангиогенных факторов, которые усиливаются гипоксией и механизмами, опосредованными аутоантителами. Биол Репрод.
2012; 87 (2): 36.
44. Huppertz B, Kingdom J, Caniggia I, et al. Гипоксия способствует некротическому выделению
по сравнению с апоптитным выделением синцитиотрофобласта плаценты в кровоток матери
. Плацента. 2003. 24: 181–190.
45. Американский колледж акушеров и гинекологов; Целевая группа
по гипертонии при беременности.Гипертония при беременности. Отчет
Отчет
Американской коллегии акушеров и гинекологов по задаче
Force on Hypertension in Pregnancy. Obstet Gynecol. 2013; 122 (5):
1122–1131.
46. Сибай Б.М., Рамадан МК, Уста I, Салама М., Мерсер Б.М., Фридман С.А.
Материнская заболеваемость и смертность при 442 беременностях с гемолизом,
повышенных ферментов печени и низком уровне тромбоцитов (HELLP-синдром). Am J
Obstet Gynecol. 1993; 169: 1000–1006.
47. Postma IR, Slager S, Kremer HP, de Groot JC, Zeeman GG.
отдаленных последствий синдрома задней обратимой энцефалопатии в
эклампсии и преэклампсии: обзор акушерской и неакушерской
литературы. Obstet Gynecol Surv. 2014; 69 (5): 287–300.
48. Сиркар М., Тадхани Р., Каруманчи С.А. Патогенез преэклампсии.
Curr Opin Nephrol Hypertens. 2015; 24 (2): 131–138.
49. Бомбрис А.Е., Бартон Дж. Р., Хабли М., Сибай Б.М.Ожидаемое ведение
тяжелой преэклампсии на сроке беременности от 27 (0/7) до 33 (6/7) недель: материнское
и перинатальные исходы в зависимости от гестационного возраста по неделям на момент начала
выжидательной тактики. Am J Perinatol. 2009. 26 (6): 441–446.
Am J Perinatol. 2009. 26 (6): 441–446.
50. Одегард Р.А., Ваттен Л.Дж., Нильсен С.Т., Салвесен К.А., Аустгулен Р.
Преэклампсия и рост плода. Obstet Gynecol. 2000; 96: 950–955.
51. Хаддад Б., Деис С., Гоффнет Ф., Паниэль Б.Дж., Каброл Д., Сибай Б.М.Материнские
и перинатальные исходы во время выжидательной тактики 239 тяжелых
прекламптических женщин на сроке от 24 до 33 недель беременности. Am J Obstet
Gynecol. 2004. 190 (6): 1590–1595; обсуждение 1595–1597.
52. Рис Э.А., Визницер А., Ле Э, Хомко С.Дж., Берман Х., Спенсер Э.М.
Связь между ростом плода человека и уровнями в крови плода
инсулиноподобных факторов роста I и II, их связывающих белков и
рецепторов.Obstet Gynecol. 1994; 84: 88–95.
53. Meschia G, Battaglia FC, Hay WW, Sparks JW. Утилизация субстратов
плацентой овцы in vivo. Fed Proc. 1980; 39: 245–249.
54. Ригано С, Боццо М, Феррацци Е, Беллатти М, Баттагли ФК, Галан Х. Л.
Л.
Раннее и стойкое снижение кровотока в пупочной вене у плода с задержкой роста
: продольное исследование. Am J Obstet Gynecol.
2001; 185: 834–838.
55.Леви Р., Смит С.Д., Чендлер К., Садовский Ю., Нельсон Д.М. Апоптоз
в культивируемых трофобластах человека усиливается гипоксией и ослабляется
эпидермальным фактором роста. Am J Physiol Cell Physiol. 2000; 278:
C982 – C988.
56. Ниши Х., Накада Т., Кио С., Иноуэ М., Шай Дж. У., Исака К. Гипоксия-
-индуцированный фактор 1 опосредует повышенную регуляцию теломеразы (hTERT). Mol
Cell Biol. 2004. 24 (13): 6076–6083.
57. Trudinger B, Song JZ, Wu ZH, Wang J.Плацентарная недостаточность
характеризуется активацией тромбоцитов у плода. Obstet Gynecol.
2003; 101: 975–981.
58. Башат А.А., Гембрух Ю., Рейсс И., Кортнер Л., Вайнер С.П., Харман С.Р.
Отсутствие конечной диастолической веолии пупочной артерии у плодов с задержкой роста
: фактор риска неонатальной тромбоцитопении. Obstet Gynecol.
Obstet Gynecol.
2000; 96: 162–166.
59. Дэвис Н., Снайдер Р., Николаидес К.Х. Внутриутробное голодание и количество лейкоцитов у плода
.Fetal Diagn Ther. 1991; 6: 107–112.
60. аль-Газали В., Чита С.К., Чапман М.Г., Аллан Л.Д. Свидетельства
перераспределения сердечного выброса при асимметричной задержке роста.
Br J Obstet Gynaecol. 1989. 96 (6): 697–704.
61. Риццо Дж., Ардуини Д., Романини К. Допплерэхокардиографическая оценка —
сердечной функции плода. Ультразвуковой акушерский гинекол. 1992; 2 (6):
434–445.
62. Soothill PW, Nicolaides KH, Campbell S.Пренатальная асфиксия, гипер-
лактикемия, гипогликемия и эритробластоз с задержкой роста
плодов. Br Med J (Clin Res Ed). 1987. 294 (6579): 1051–1053.
63. Маккартон С.М., Уоллес И.Ф., Дивон М., Воган Х.Г. Младший. Когнитивное и
неврологическое развитие недоношенных, маленьких для гестационного возраста ребенка
— до 6 лет: сравнение по массе при рождении и гестационном возрасте. Pedi-
Pedi-
atrics. 1996. 98 (6 Pt 1): 1167–1178.
64. Гардози Дж., Мадурасингхе В., Уильямс М., Малик А., Фрэнсис Ф.Mater-
Факторы риска мертворождения у плода и плода: популяционное исследование. BMJ.
2013; 346: f108.
65. Баркер DJ. Фетальное происхождение гипертонии у взрослых. J Hypertens Suppl.
1992; 10 (7): S39 – S44.
66. Бонами А.К., Бендито А., Мартин Х., Андольф Э., Седин Г., Норман М.
Преждевременные роды способствуют повышению сосудистого сопротивления и повышению кровяного давления
у девочек-подростков. Pediatr Res. 2005. 58 (5): 845–849.
67. Сяо CC, Tsao LY, Chen HN, Chiu HY, Chang WC. Изменение клинических проявлений
и выживаемости при трисомии 18. Pediatr Neonatol.
2009; 50: 147–151.
68. Харрингтон К., Карпентер Р.Г., Голдфрад С., Кэмпбелл С. Трансвагинальное
Допплеровское ультразвуковое исследование маточно-плацентарного кровообращения в ранней предэклампсии и задержке внутреннего роста до
. Br J Obstet
Br J Obstet
Gynaecol. 1997. 104: 674–681.
69.Papageorghiou AT, Yu CK, Nicolaides KH. Роль маточной артерии
Допплерография в прогнозировании неблагоприятного исхода беременности. Best Practices Clin
Obstet Gynaecol. 2004. 18 (3): 383–396.
70. Морроу Р.Дж., Адамсон С.Л., Булл С.Б., Ричи Дж.В. Влияние эмболизации плаценты
на форму волны скорости пупочной артерии у плодов овцы.
Am J Obstet Gynecol. 1989; 161: 1055–1060.
71. Башат А.А., Хечер К. Ограничение роста плода из-за плацентарной болезни
.Семин Перинатол. 2004. 28 (1): 67–80.
72. Николаидес К. Х., Билардо С. М., Сотилл П. У., Кэмпбелл С. Отсутствие конечных диастолических частот
в пупочной артерии: признак гипоксии плода
и ацидоза. BMJ. 1988. 297 (6655): 1026–1027.
73. Weiner CP. Взаимосвязь между систолическим соотношением пупочной артерии / диастолическим
и измерениями газов в пуповинной крови у мужчин с образцом
, полученными с помощью кордоцентеза. Am J Obstet Gynecol.1990; 162:
Am J Obstet Gynecol.1990; 162:
1198–1202.
74. Gramellini D, Folli MC, Raboni S, Vadora E, Merialdi A. Cerebral-
Коэффициент пупочного допплера как предиктор неблагоприятного перинатального исхода.
Акушерский гинекол. 1992; 79: 416–420.
75. Хечер К., Кэмпбелл С., Дойл П., Харрингтон К., Николайдес К.
Оценка компромисса плода с помощью ультразвукового допплера
кровообращения плода. Артериальный, внутрисердечный и венозный кровоток
исследования.Тираж. 1995. 91: 129–138.
76. Карвалью Ф.Х., Морон А.Ф., Маттар Р. и др. Венозный проток Doppler
Велосиметрия в прогнозе ацидемии при рождении: какой параметр
является лучшим? Prenat Diagn. 2005. 25 (13): 1212–1216.
77. Schwarze A, Gembruch U, Krapp M, Katalinic A, Germer U,
Axt-Fliedner R. Качественный анализ формы волны венозного допплера
у недоношенных плодов с ограниченным внутриутробным развитием с ARED-потоком в
пупочной артерии — корреляция с краткосрочным результатом. УЗИ
УЗИ
Акушерский гинекол. 2005. 25 (6): 573–579.
78. Укомплектование персоналом FA. Биофизический профиль плода. Obstet Gynecol Clin North
Am. 1999; 26: 557–577, v.
79. Рибберт Л.С., Николаидес К.Х., Виссер Г.Х. Прогнозирование ацидемии плода при задержке внутриутробного развития
: сравнение количественной оценки активности плода
с баллами биофизического профиля. Br J Obstet Gynaecol. 1993; 100 (7):
653–656.
80. Винцилеос AM, Femiling AD, Scorza WE, et al.Связь между
биофизической активностью плода и значениями газов пуповинной крови. Am J
Obstet Gynecol. 1991; 165: 707–713.
81. Кримминз С., Десаи А., Блок-Абрахам Д., Берг С., Гембрух У.,
Башат А.А.
Сравнение доплеровских и биофизических данных между живорожденными и мертворожденными плодами с задержкой роста. Am J Obstet
Gynecol. 2014; 211 (6): e1 – e10.
82. Башат А.А., Косми Э., Билардо С.М. и др.Предикторы неонатального исхода
относятся к ранней плацентарной дисфункции. Obstet Gynecol. 2007; 109:
Obstet Gynecol. 2007; 109:
253–261.
83. Туран С., Миллер Дж., Башат А.А. Комплексное тестирование и управление
ограничения роста плода. Семин перинатальный. 2008. 32: 194–200.
Антиоксиданты | Бесплатный полнотекстовый | Пренатальная гипоксия и оксидативный стресс плаценты: выводы от животных моделей к клиническим доказательствам
Пренатальная гипоксия — это состояние, ответственное за заболевание и гибель плода или новорожденного [18].Плацента — важный орган для общения беременной женщины и плода. Правильное функционирование этого органа важно для развития плода. Гипоксия определяется как снижение O 2 , необходимого для физиологических функций тканей [19]. Повышение уровней ROS, вызванное неполным восстановлением O 2 , является одним из наиболее распространенных механизмов, вызывающих гипоксию. Обычно плацента производит такие АФК, как супероксид-анион (O 2 — ), гидроксильный радикал (HO — ) и перекись водорода (H 2 O 2 ) [20]. Эти молекулы очень нестабильны и обладают сильной химической реакционной способностью из-за наличия неспаренных электронов на внешней орбитали [21]. Из-за этой нестабильности АФК склонны отдавать или приобретать электрон от других электрически нестабильных молекул, чтобы достичь стабильного энергетического состояния. Таким образом, они проводят серию окислительно-восстановительных реакций, важных для клеточного выживания. Нормальное производство АФК обеспечивается балансом между производством этих молекул и системой антиоксидантной защиты.Основная антиоксидантная система обеспечивается за счет активности антиоксидантных ферментов, таких как супероксиддисмутаза (SOD), глутатионпероксидаза (GPx) и каталаза (CAT). Неферментативные антиоксиданты, такие как тиолы (например, глутатион, GSH), протеиновые тиолы; витамины A, B6, B12, C и E; селен; фолиевая кислота; и β-каротиноиды, билирубин и мочевая кислота, представляют собой еще один защитный механизм, способный уменьшить чрезмерную продукцию ROS [22].
Эти молекулы очень нестабильны и обладают сильной химической реакционной способностью из-за наличия неспаренных электронов на внешней орбитали [21]. Из-за этой нестабильности АФК склонны отдавать или приобретать электрон от других электрически нестабильных молекул, чтобы достичь стабильного энергетического состояния. Таким образом, они проводят серию окислительно-восстановительных реакций, важных для клеточного выживания. Нормальное производство АФК обеспечивается балансом между производством этих молекул и системой антиоксидантной защиты.Основная антиоксидантная система обеспечивается за счет активности антиоксидантных ферментов, таких как супероксиддисмутаза (SOD), глутатионпероксидаза (GPx) и каталаза (CAT). Неферментативные антиоксиданты, такие как тиолы (например, глутатион, GSH), протеиновые тиолы; витамины A, B6, B12, C и E; селен; фолиевая кислота; и β-каротиноиды, билирубин и мочевая кислота, представляют собой еще один защитный механизм, способный уменьшить чрезмерную продукцию ROS [22]. Во время беременности нормальные уровни АФК могут участвовать в пролиферации и дифференцировке трофобластов и в модуляции сосудистых ответов плаценты [19].Однако повышение уровня АФК отвечает за функциональные изменения плаценты. После гипоксии плода низкие уровни O 2 приводят к снижению активности митохондриальной цепи переноса электронов. Таким образом, это снижение способствует увеличению процентного содержания не полностью восстановленного O 2 с последующим образованием ROS, таких как O 2 — [20,23]. Митохондриальная электронная транспортная цепь представляет собой основной продуцент АФК. Другой источник АФК — НАДФН-оксидаза, ответственная за эндогенную продукцию O 2 — [24].В эндотелии сосудов цитохром P450 — еще один фермент, ответственный за продукцию OH – и O 2 – [25]. Металлофлавопротеин ксантиноксидаза — еще один фермент, который после окисления гипоксантина до ксантина и мочевой кислоты приводит к образованию O 2 — [26].
Во время беременности нормальные уровни АФК могут участвовать в пролиферации и дифференцировке трофобластов и в модуляции сосудистых ответов плаценты [19].Однако повышение уровня АФК отвечает за функциональные изменения плаценты. После гипоксии плода низкие уровни O 2 приводят к снижению активности митохондриальной цепи переноса электронов. Таким образом, это снижение способствует увеличению процентного содержания не полностью восстановленного O 2 с последующим образованием ROS, таких как O 2 — [20,23]. Митохондриальная электронная транспортная цепь представляет собой основной продуцент АФК. Другой источник АФК — НАДФН-оксидаза, ответственная за эндогенную продукцию O 2 — [24].В эндотелии сосудов цитохром P450 — еще один фермент, ответственный за продукцию OH – и O 2 – [25]. Металлофлавопротеин ксантиноксидаза — еще один фермент, который после окисления гипоксантина до ксантина и мочевой кислоты приводит к образованию O 2 — [26]. В плаценте в условиях гипоксии потребление кислорода митохондриями снижается. Это приводит к уменьшению запасов высокоэнергетических фосфатов, генерирующих высокие уровни ксантина, гипоксантина, NADH, FADH, ионов водорода (H + ) и молочной кислоты [27].Гипоксия вызывает снижение ферментативной активности насосов АТФ-ази-зависимых мембран, снижение мембранного потенциала и повышение уровня цитозольного кальция (Ca 2+ ). В условиях гипоксии увеличение внутриклеточного Ca 2+ из-за активации потенциал-зависимых каналов и высвобождения митохондриями и эндоплазматическим ретикулумом создает петлю, которая запускает механизм апоптоза и некроза нейронов [28]. Поступление Ca 2+ , особенно в нейронные клетки, способствует накоплению глутамата.Глутамат, взаимодействуя с рецепторами N-метил-D аспартата (NMDA), усиливает внутриклеточный ток Ca 2+ , дополнительно способствуя повреждению нейронов [29]. Кроме того, Ca 2+ отвечает за активацию синтазы оксида азота ( NOS), участвующий в производстве оксида азота (NO).
В плаценте в условиях гипоксии потребление кислорода митохондриями снижается. Это приводит к уменьшению запасов высокоэнергетических фосфатов, генерирующих высокие уровни ксантина, гипоксантина, NADH, FADH, ионов водорода (H + ) и молочной кислоты [27].Гипоксия вызывает снижение ферментативной активности насосов АТФ-ази-зависимых мембран, снижение мембранного потенциала и повышение уровня цитозольного кальция (Ca 2+ ). В условиях гипоксии увеличение внутриклеточного Ca 2+ из-за активации потенциал-зависимых каналов и высвобождения митохондриями и эндоплазматическим ретикулумом создает петлю, которая запускает механизм апоптоза и некроза нейронов [28]. Поступление Ca 2+ , особенно в нейронные клетки, способствует накоплению глутамата.Глутамат, взаимодействуя с рецепторами N-метил-D аспартата (NMDA), усиливает внутриклеточный ток Ca 2+ , дополнительно способствуя повреждению нейронов [29]. Кроме того, Ca 2+ отвечает за активацию синтазы оксида азота ( NOS), участвующий в производстве оксида азота (NO). Среди трех известных изоформ NOS эндотелиальная синтаза оксида азота (eNOS) представляет собой Ca 2+ -зависимый флавоэнзим, который генерирует NO [30]. В этом процессе Ca 2+ играет важную роль в активации eNOS, регулируя связывание eNOS с кальмодулином [31]. NO является мощным эндотелиальным вазодилататором, участвующим в регуляции сосудистого тонуса, в контроле кровотока в тканях и в агрегации тромбоцитов.В плаценте NO играет ключевую роль в расширении сосудов маточно-плацентарных артерий, важном механизме, который определяет инвазию трофобластов и ремоделирование эндотелия [32]. Следовательно, измененный баланс NO и ROS играет решающую роль в модулировании функции сосудов пуповины и плаценты в различных пренатальных условиях. Следовательно, высокие уровни ROS ответственны за повреждение нескольких клеточных компонентов, таких как ДНК, белки и липиды, с последующим нарушением. нормальных клеточных функций [33].Во время беременности в течение 10–12 недель беременности наблюдается усиление притока материнской крови к плаценте, что приводит к локальному увеличению кислорода и, как следствие, к повышению активности антиоксидантных ферментов.
Среди трех известных изоформ NOS эндотелиальная синтаза оксида азота (eNOS) представляет собой Ca 2+ -зависимый флавоэнзим, который генерирует NO [30]. В этом процессе Ca 2+ играет важную роль в активации eNOS, регулируя связывание eNOS с кальмодулином [31]. NO является мощным эндотелиальным вазодилататором, участвующим в регуляции сосудистого тонуса, в контроле кровотока в тканях и в агрегации тромбоцитов.В плаценте NO играет ключевую роль в расширении сосудов маточно-плацентарных артерий, важном механизме, который определяет инвазию трофобластов и ремоделирование эндотелия [32]. Следовательно, измененный баланс NO и ROS играет решающую роль в модулировании функции сосудов пуповины и плаценты в различных пренатальных условиях. Следовательно, высокие уровни ROS ответственны за повреждение нескольких клеточных компонентов, таких как ДНК, белки и липиды, с последующим нарушением. нормальных клеточных функций [33].Во время беременности в течение 10–12 недель беременности наблюдается усиление притока материнской крови к плаценте, что приводит к локальному увеличению кислорода и, как следствие, к повышению активности антиоксидантных ферментов. Однако чрезмерное увеличение ROS, которому не может противодействовать антиоксидантный ответ, вызывает условия окислительного стресса. Окислительный стресс плаценты, особенно на этой стадии беременности, отвечает за снижение инвазии трофобластов. Этот каскад событий вызывает различные состояния, которые могут быть связаны с изменениями развития плода, а в серьезных случаях даже с преждевременной неудачей беременности [34,35].Мозг более чувствителен к изменениям уровня O 2 . Окислительный стресс является основным фактором, вызывающим гибель нейрональных клеток в незрелом мозге [36]. Во время эмбриогенеза гипоксическое повреждение также задерживает миграцию нейронов и изменяет экспрессию многочисленных нейротрансмиттеров [37,38]. Эти механизмы повышают риск врожденных дефектов нервной системы, повреждения головного мозга и долгосрочных когнитивных нарушений в обучении и памяти [39,40]. Более того, он также может предрасполагать потомство к будущему возникновению эпилептических состояний [41].
Однако чрезмерное увеличение ROS, которому не может противодействовать антиоксидантный ответ, вызывает условия окислительного стресса. Окислительный стресс плаценты, особенно на этой стадии беременности, отвечает за снижение инвазии трофобластов. Этот каскад событий вызывает различные состояния, которые могут быть связаны с изменениями развития плода, а в серьезных случаях даже с преждевременной неудачей беременности [34,35].Мозг более чувствителен к изменениям уровня O 2 . Окислительный стресс является основным фактором, вызывающим гибель нейрональных клеток в незрелом мозге [36]. Во время эмбриогенеза гипоксическое повреждение также задерживает миграцию нейронов и изменяет экспрессию многочисленных нейротрансмиттеров [37,38]. Эти механизмы повышают риск врожденных дефектов нервной системы, повреждения головного мозга и долгосрочных когнитивных нарушений в обучении и памяти [39,40]. Более того, он также может предрасполагать потомство к будущему возникновению эпилептических состояний [41].
Внутриутробная гибель плода может быть удалена от провоцирующего инсульта на животной модели гипоксии-ишемии
H-I плода в результате ишемии матки в течение 40 минут на 22-й день беременности (E22) привело к смеси мертворожденных и выживших с гипертонией и без после доставки (10). Сначала мы определили, является ли фиктивная ишемия матки причиной смерти. В контрольных хирургических группах, которым проводили H – I плода в течение 30 минут, умер только один плод, и 96% плодов дожили до срока (25 из 26). Это показало, что эффекты хирургического вмешательства были незначительными, поскольку эти результаты не отличались от контрольных наивных кроликов.
Впоследствии мы сравнили 40-минутную ишемию матки на трех разных сроках гестации, E22, E25 и E29, что соответствует 70, 79 и 92% срока беременности, соответственно. Количество наборов живых новорожденных кроликов уменьшалось с ростом H – I с увеличением гестационного возраста ( Рисунок 1 ) из группы E22 в группу E29. Число доношенных мертворождений увеличивалось соответственно с H – I с увеличением гестационного возраста, с E22 до E29 ( Рисунок 1 ).Число преждевременных мертворождений также увеличилось с E22 до E25. Сравнения между E22 и E25 были более достоверными, чем сравнения с E29. Немедленная и острая умершая популяция, которая составляет раннюю перинатальную смерть после гипоксии E29, вероятно, была недостаточно представлена по сравнению с группами E22 и E25, потому что было только 2 дня после E29, чтобы подсчитать их согласно нашему определению родов до E31. Процент живорожденных с тяжелой формой гипертонии на ст. E22, E25 и E29 составлял 30, 88 и 42% соответственно.Всего в трех пометах наборов E29 остались выжившие.
Число доношенных мертворождений увеличивалось соответственно с H – I с увеличением гестационного возраста, с E22 до E29 ( Рисунок 1 ).Число преждевременных мертворождений также увеличилось с E22 до E25. Сравнения между E22 и E25 были более достоверными, чем сравнения с E29. Немедленная и острая умершая популяция, которая составляет раннюю перинатальную смерть после гипоксии E29, вероятно, была недостаточно представлена по сравнению с группами E22 и E25, потому что было только 2 дня после E29, чтобы подсчитать их согласно нашему определению родов до E31. Процент живорожденных с тяжелой формой гипертонии на ст. E22, E25 и E29 составлял 30, 88 и 42% соответственно.Всего в трех пометах наборов E29 остались выжившие.
Результаты выполнения. Исходы на 32-й день беременности (E32) показаны в процентах от контрольных животных и гипоксии-ишемии плода в течение 40 минут на E22, E25 и E29. Наборы живорожденных обозначены белой областью и черным числом.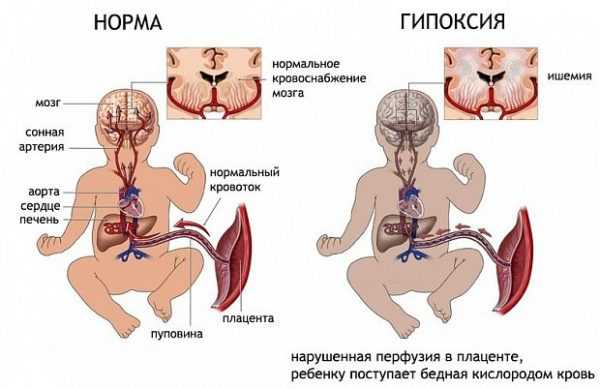 Ранняя перинатальная смерть (обозначена серой областью и светло-серым числом) — это плоды, которые умирают в утробе матери и рожают до E31 (E22 20%, E25 36% и E29 10%). Поздняя перинатальная смерть (черная область и серое число) — это все кролики, найденные мертвыми на E32 после нормальных родов или кесарева сечения (E22 21%, E25 37%, E29 71%).Разница между группами по точному критерию Фишера очень значима ( P <0,0001). Группы с гипоксией также значительно различаются, и каждая группа с гипоксией значительно отличается от других групп с гипоксией (тау-b Кендалла).
Ранняя перинатальная смерть (обозначена серой областью и светло-серым числом) — это плоды, которые умирают в утробе матери и рожают до E31 (E22 20%, E25 36% и E29 10%). Поздняя перинатальная смерть (черная область и серое число) — это все кролики, найденные мертвыми на E32 после нормальных родов или кесарева сечения (E22 21%, E25 37%, E29 71%).Разница между группами по точному критерию Фишера очень значима ( P <0,0001). Группы с гипоксией также значительно различаются, и каждая группа с гипоксией значительно отличается от других групп с гипоксией (тау-b Кендалла).
Нормальный рост плода у кроликов был установлен в популяции наивных животных, полученной путем гистеротомии на E22, E25 или E29, или путем спонтанных родов в срок. Рост у кроликов на поздних сроках беременности линейный ( Рисунок 2 ).Линия регрессии была рассчитана по графику веса и гестационного возраста, и корреляция была высокозначимой ( R = 0,9554, P <0,01).
Масса плода в зависимости от срока гестации. Вес плода кролика в граммах показан по сроку беременности. Наивные плоды на 22-й день беременности (E22), E25 и E29 были доставлены путем гистеротомии и взвешены. Наборы новорожденных кроликов взвешивали после рождения (стрелка) на E32. Рост линейный: R = 0.9554. Линия регрессии — это сплошная черная линия, а 95% доверительные интервалы — серые пунктирные линии.
Далее мы исследовали все выкидыши ( Рисунок 3a ). Линия регрессии и доверительные интервалы веса выкидышей до E32 после H – I на E22, E25 и E29 были почти идентичны таковым для наивных контролей. Это означает, что смерть была очень близка к первоначальному оскорблению H – I. В отличие от выкидышей, мертворожденные имели в среднем больший вес, но разница в весе была выше ( Рисунок 3b ).После E22 и E25 H – I наблюдалось бимодальное распределение: животные с меньшим весом были похожи на выкидыши, а более крупные животные — на живорожденные. Более четкое представление этого бимодального распределения показано в частотном распределении весов мертворожденных из групп E22, E25 и E29 ( Рисунок 3c ). Негипертонические наборы для новорожденных после H – I (E22 62,8 ± 2,7, E25 58,2 ± 3,6, E29 53,0 ± 9,0 г) существенно не отличаются от контрольных наборов постнатального дня (P) 1 (55.6 ± 0,5 г). Наборы для лечения гипертонии (E22 52,6 ± 3,4, E25 52,0 ± 2,1, E29 46,0 ± 0,8 г) были незначительно меньше, чем группа негипертоников или контрольная группа.
Более четкое представление этого бимодального распределения показано в частотном распределении весов мертворожденных из групп E22, E25 и E29 ( Рисунок 3c ). Негипертонические наборы для новорожденных после H – I (E22 62,8 ± 2,7, E25 58,2 ± 3,6, E29 53,0 ± 9,0 г) существенно не отличаются от контрольных наборов постнатального дня (P) 1 (55.6 ± 0,5 г). Наборы для лечения гипертонии (E22 52,6 ± 3,4, E25 52,0 ± 2,1, E29 46,0 ± 0,8 г) были незначительно меньше, чем группа негипертоников или контрольная группа.
Выкидыши и мертворождения. ( a ) Линия регрессии и доверительные интервалы (обозначены черными пунктирными линиями) веса выкидыша (белые кружки). Эти линии почти идентичны наивной линии регрессии и доверительным полосам (показаны серыми сплошными линиями), что означает, что выкидыши умерли во время инсульта H – I плода.( b ) Линия регрессии и доверительные интервалы (изображены черными пунктирными линиями) мертворожденных наборов отличаются от выкидышей (серые сплошные линии). Средний вес значительно превышает вес наивных плодов в этом возрасте. Это подразумевает продолжающийся рост плода и отсроченную смерть некоторых животных. ( c ) Бимодальное распределение мертворождений становится очевидным, когда аналогичные частотные распределения (сплайновые кривые серого цвета) построены для 22 дней беременности (E22) (белые столбцы) и E25 (серые столбцы), но не для E29 (черные столбцы). бары) группа.Большинство мертворожденных пережили первоначальное оскорбление, продолжили расти и умерли позже. Ось z показывает возраст в H – I. H – I, гипоксия – ишемия.
Средний вес значительно превышает вес наивных плодов в этом возрасте. Это подразумевает продолжающийся рост плода и отсроченную смерть некоторых животных. ( c ) Бимодальное распределение мертворождений становится очевидным, когда аналогичные частотные распределения (сплайновые кривые серого цвета) построены для 22 дней беременности (E22) (белые столбцы) и E25 (серые столбцы), но не для E29 (черные столбцы). бары) группа.Большинство мертворожденных пережили первоначальное оскорбление, продолжили расти и умерли позже. Ось z показывает возраст в H – I. H – I, гипоксия – ишемия.
Чтобы получить более точное время смерти, мы использовали нормальную скорость роста плода, показанную на Рисунок 2 для генерации времени смерти с помощью линии регрессии ( Рисунок 4a вставка), учитывая предположение, что H – I не оказал большого влияния на рост плода.Затем мы построили кривые выживаемости Каплана – Мейера для группы мертворожденных. Это предположение, вероятно, справедливо для E22 H – I, поскольку масса живорожденных наборов была такой же, как и контрольных наборов. После E22 H – I популяция с ранней перинатальной смертью, вероятно, умерла в течение полутора дней после H – I плода ( Рисунок 4a ), и это составляет четверть смертей мертворожденных. Наборы, представляющие остальную часть перинатальной смерти, начали умирать через 4 дня и продолжались до последней части беременности.Это показывает, что первоначальный эпизод приводит к немедленной и острой смерти части помета, и 78% этой популяции с ранней перинатальной смертью родятся преждевременно до E31.
Это предположение, вероятно, справедливо для E22 H – I, поскольку масса живорожденных наборов была такой же, как и контрольных наборов. После E22 H – I популяция с ранней перинатальной смертью, вероятно, умерла в течение полутора дней после H – I плода ( Рисунок 4a ), и это составляет четверть смертей мертворожденных. Наборы, представляющие остальную часть перинатальной смерти, начали умирать через 4 дня и продолжались до последней части беременности.Это показывает, что первоначальный эпизод приводит к немедленной и острой смерти части помета, и 78% этой популяции с ранней перинатальной смертью родятся преждевременно до E31.
Расчетное время смерти для ранней и поздней перинатальной смерти. Время смерти ранней (серая линия) и поздней перинатальной смерти (черная линия) оценивалось по весам и рассчитанному наклону регрессии для наивных контрольных плодов и новорожденных наборов ( Рисунок 2 ) и процесс, показанный на вставке пунктирной стрелкой. Ордината показывает в порядке убывания процент животных, погибших каждый день. ( a ) На 22 день беременности (E22) все ранние перинатальные смерти, вероятно, произошли в течение полутора дней после H – I. Около четверти поздних перинатальных смертей также произошло в течение полутора дней после H – I, но остальные плоды начали умирать через 4 дня. ( b ) На ст. E25 все ранние перинатальные смерти также произошли в течение 2 дней после H – I; Поздняя перинатальная смерть произошла на протяжении оставшейся части беременности, при этом 47% поздних перинатальных смертей приходились на роды (стрелка).( c ) На E29 было несколько случаев ранней перинатальной смерти. Поздняя перинатальная смерть была преобладающей формой смерти. H – I, гипоксия – ишемия.
Ордината показывает в порядке убывания процент животных, погибших каждый день. ( a ) На 22 день беременности (E22) все ранние перинатальные смерти, вероятно, произошли в течение полутора дней после H – I. Около четверти поздних перинатальных смертей также произошло в течение полутора дней после H – I, но остальные плоды начали умирать через 4 дня. ( b ) На ст. E25 все ранние перинатальные смерти также произошли в течение 2 дней после H – I; Поздняя перинатальная смерть произошла на протяжении оставшейся части беременности, при этом 47% поздних перинатальных смертей приходились на роды (стрелка).( c ) На E29 было несколько случаев ранней перинатальной смерти. Поздняя перинатальная смерть была преобладающей формой смерти. H – I, гипоксия – ишемия.
Для E25 H – I популяция с ранней перинатальной смертью вела себя так же, как после гипоксии E22, поскольку все ранние перинатальные смерти произошли в течение 2 дней после H – I плода. Только 15% поздних перинатальных смертей произошло в первые 2 дня, и большая часть группы E25 H – I умерла впоследствии ( Рисунок 4b ). 82% населения, умершего в течение 2 дней, родились до E31.Отличие от гипоксии E22 состояло в том, что значительная часть поздних перинатальных смертей (47%) произошла около рождения (начиная с E31 и далее). Даже с учетом того факта, что после H – I последовало небольшое ограничение роста, процент поздних перинатальных смертей остается неизменным и составляет 47%.
82% населения, умершего в течение 2 дней, родились до E31.Отличие от гипоксии E22 состояло в том, что значительная часть поздних перинатальных смертей (47%) произошла около рождения (начиная с E31 и далее). Даже с учетом того факта, что после H – I последовало небольшое ограничение роста, процент поздних перинатальных смертей остается неизменным и составляет 47%.
Для гипоксии E29 ( Рисунок 4c ) оценки времени смерти простираются от H – I до времени рождения. Из-за близости H – I оскорбления ко времени рождения трудно различить раннюю и позднюю перинатальную смерть.
Чтобы подтвердить время острой смерти после H – I, мы выполнили гистеротомию через 24 часа после H – I на E22 или E25. Затем мы сравнили эти «фактические» показатели острой смертности с ранее оцененными показателями в первые 24 часа. Как после E22 ( n = 29), так и после E25 ( n = 21) H – I процент плодов, фактически обнаруженных мертвыми, определяемый отсутствием частоты сердечных сокращений плода (30 и 42% соответственно), не был достоверно отличается от предполагаемой смерти по весовым критериям (22 и 35% соответственно). Число фактических смертей через 24 часа после гипоксии E22 существенно не отличалось от числа смертей после гипоксии E25 (χ 2 P = 0,0769, мощность = 25%). У выживших в обеих группах была нормальная частота сердечных сокращений плода. Эти исследования также подтверждают наше первоначальное предположение о нормальном росте плода после H – I для оценки времени смерти, поскольку фактический уровень смертности, хотя и не отличался, был немного выше, чем расчетный уровень смертности, и с учетом того факта, что при некоторой задержке внутриутробного развития плода , фактические показатели смертности должны были быть ниже расчетных значений.
Число фактических смертей через 24 часа после гипоксии E22 существенно не отличалось от числа смертей после гипоксии E25 (χ 2 P = 0,0769, мощность = 25%). У выживших в обеих группах была нормальная частота сердечных сокращений плода. Эти исследования также подтверждают наше первоначальное предположение о нормальном росте плода после H – I для оценки времени смерти, поскольку фактический уровень смертности, хотя и не отличался, был немного выше, чем расчетный уровень смертности, и с учетом того факта, что при некоторой задержке внутриутробного развития плода , фактические показатели смертности должны были быть ниже расчетных значений.
Магнитно-резонансная томография
Магнитно-резонансная томография (МРТ) диагностировала умершие плоды путем визуализации сердца ( Рисунок 5a ). Мы также исследовали изменения кажущегося коэффициента диффузии в головном мозге плода (ADC) в пометах, подвергшихся H – I под магнитом на E22, E25 или E29, а также получили значения ADC через 4, 24 и 72 часа после H – I в подгруппе беременных самок E25. Положение матки подтверждено кесаревым сечением на E31.Острая реакция на H – I показала, что в более позднем гестационном возрасте начало наступало раньше и наблюдалось более глубокое падение ADC ( Рисунок 5d ). Нам также удалось получить и проанализировать динамику ADC у 41 плода, умершего при кесаревом сечении (12 плодов). Немедленная смерть могла быть диагностирована, если ADC головного мозга плода не восстановился выше 0,7 мкм 2 / мс к 20 мин реперфузии и оставался ниже этого порога на сеансе МРТ через 4 часа после H – I ( Рисунок 5e ).ADC в мозге мертвого плода остается низким в течение как минимум 24 часов после смерти. Эти исследования показывают, что время смерти можно определить по динамическим изменениям ADC вокруг инсульта.
Положение матки подтверждено кесаревым сечением на E31.Острая реакция на H – I показала, что в более позднем гестационном возрасте начало наступало раньше и наблюдалось более глубокое падение ADC ( Рисунок 5d ). Нам также удалось получить и проанализировать динамику ADC у 41 плода, умершего при кесаревом сечении (12 плодов). Немедленная смерть могла быть диагностирована, если ADC головного мозга плода не восстановился выше 0,7 мкм 2 / мс к 20 мин реперфузии и оставался ниже этого порога на сеансе МРТ через 4 часа после H – I ( Рисунок 5e ).ADC в мозге мертвого плода остается низким в течение как минимум 24 часов после смерти. Эти исследования показывают, что время смерти можно определить по динамическим изменениям ADC вокруг инсульта.
Изменения МРТ головного мозга плода. ( a ) Нормально бьющееся сердце плода создает гипоинтенсивные области на T2-взвешенных изображениях из-за потери сигнала МРТ из-за движения крови (пунктирная стрелка). Стрелка показывает печень плода. ( b ) Потеря гипоинтенсивности в области сердца показана у того же плода через 20 минут реперфузии (пунктирная стрелка), что свидетельствует о прекращении кровообращения и гибели плода.Для сравнения, в печени плода изменений интенсивности не наблюдается (стрелка). ( c ) Через 72 часа после H – I потеря структуры мозга может наблюдаться у мертвых плодов на T2-взвешенных изображениях, что свидетельствует о разложении ткани (стрелка) по сравнению с мозгом живого плода (пунктирная стрелка). ( d ) Острые изменения кажущегося коэффициента диффузии головного мозга плода (ADC) с H – I сравнивали на разных сроках беременности, 22 дня беременности (E22) (белые кружки, пунктирная линия) и E25 (темные кружки, сплошная линия) с 40-минутным H – I и E29 (серые квадраты, пунктирная линия) с 32-минутным H – I.( e ) ADC головного мозга плода у мертворожденных плодов (белые квадраты, пунктирная линия). Ход времени сравнивали с фиктивным контролем (светлые кружки, сплошная линия) и выжившими с гипертонией (черные ромбы, сплошная линия).
Стрелка показывает печень плода. ( b ) Потеря гипоинтенсивности в области сердца показана у того же плода через 20 минут реперфузии (пунктирная стрелка), что свидетельствует о прекращении кровообращения и гибели плода.Для сравнения, в печени плода изменений интенсивности не наблюдается (стрелка). ( c ) Через 72 часа после H – I потеря структуры мозга может наблюдаться у мертвых плодов на T2-взвешенных изображениях, что свидетельствует о разложении ткани (стрелка) по сравнению с мозгом живого плода (пунктирная стрелка). ( d ) Острые изменения кажущегося коэффициента диффузии головного мозга плода (ADC) с H – I сравнивали на разных сроках беременности, 22 дня беременности (E22) (белые кружки, пунктирная линия) и E25 (темные кружки, сплошная линия) с 40-минутным H – I и E29 (серые квадраты, пунктирная линия) с 32-минутным H – I.( e ) ADC головного мозга плода у мертворожденных плодов (белые квадраты, пунктирная линия). Ход времени сравнивали с фиктивным контролем (светлые кружки, сплошная линия) и выжившими с гипертонией (черные ромбы, сплошная линия). Время смерти определялось как немедленное, если ADC головного мозга плода не восстанавливалась выше 0,7 мкм 2 / мс к 20 мин реперфузии и оставалась ниже этого порога через 4 часа после H – I. H – I, гипоксия – ишемия; МРТ, магнитно-резонансная томография.
Время смерти определялось как немедленное, если ADC головного мозга плода не восстанавливалась выше 0,7 мкм 2 / мс к 20 мин реперфузии и оставалась ниже этого порога через 4 часа после H – I. H – I, гипоксия – ишемия; МРТ, магнитно-резонансная томография.
Внутриутробная гипоксия (антенатальный период) — Адвокат по детским и родовым травмам
Внутриутробная гипоксия (ВГ) возникает, когда плод не получает достаточного количества кислорода перед родами.ИГ может быть результатом различных состояний, таких как пролапс пуповины, окклюзия пуповины и инфаркт плаценты. IH, если его вовремя не распознать и не лечить, может привести к гипоксической ишемической энцефалопатии, которая представляет собой клеточное повреждение центральной нервной системы. Такие органы, как мозг, сердце и легкие, могут быть необратимо повреждены из-за IH.
Каковы симптомы внутриутробной гипоксии?
До рождения у ребенка может быть слабое дыхание или низкая частота сердечных сокращений. При рождении у ребенка может быть пурпурная кожа, слабый мышечный тонус и рефлексы или низкая частота сердечных сокращений.Во время родов артериальное давление у матери также может быть низким.
При рождении у ребенка может быть пурпурная кожа, слабый мышечный тонус и рефлексы или низкая частота сердечных сокращений.Во время родов артериальное давление у матери также может быть низким.
Что вызывает внутриутробную гипоксию?
Длительный, стрессовый или сложный родовой процесс может вызвать внутриутробную гиперемию, а также выпадение пуповины. У младенца может быть анемия или инфекция. Во время родов могут возникнуть неотложные медицинские состояния, например разрыв матки. У матери могут быть проблемы с дыханием, связанные с анестезией. По этим причинам медицинские работники должны проявлять необходимую заботу, необходимую для обеспечения безопасности как матери, так и ребенка во время родов.Устройство, известное как кардиомонитор плода, полезно для отслеживания частоты сердечных сокращений ребенка, и за ним можно внимательно наблюдать, чтобы предупредить медицинский персонал, если уровень крови или кислорода ребенка нарушается.
Какие методы лечения используются при внутриутробной гипоксии?
В экстренных случаях ребенок будет доставлен через кесарево сечение. Если симптомы появляются до начала родов, матери можно предоставить дополнительный кислород. Могут вводиться лекарства для контроля артериального давления. Артериальная кровь пуповины может быть проверена на неправильный уровень кислоты.Необходимость принятия соответствующих и немедленных мер является критической при появлении признаков или симптомов внутриутробной гипоксии. Эти меры необходимы, чтобы избежать возможных серьезных или необратимых травм ребенка.
Если симптомы появляются до начала родов, матери можно предоставить дополнительный кислород. Могут вводиться лекарства для контроля артериального давления. Артериальная кровь пуповины может быть проверена на неправильный уровень кислоты.Необходимость принятия соответствующих и немедленных мер является критической при появлении признаков или симптомов внутриутробной гипоксии. Эти меры необходимы, чтобы избежать возможных серьезных или необратимых травм ребенка.
Гипоксия плода — Дуган, Бабидж, Толлей и Колер
Во время беременности приток кислорода и питательных веществ к ребенку, а также удаление углекислого газа и других отработанных газов из ребенка осуществляется через плаценту.
Плацента — чрезвычайно сложный орган, который состоит из систем кровообращения матери и плода.
Адекватный кровоток к плаценте и от плаценты, а также в кровотоке матери и плода необходим для того, чтобы ребенок получал достаточно кислорода и мог выводить углекислый газ и другие отходящие газы.
Любое изменение функции плаценты может привести к снижению доставки кислорода ребенку — состоянию, известному как гипоксия плода.
Поскольку гипоксия плода может быть результатом многих заболеваний или состояний матери или плода, которые снижают функцию плаценты, безопасные и осторожные акушеры будут тщательно обследовать своих пациентов, которые подвержены риску развития гипоксии плода.
Гипертензивные расстройства у матери во время беременности, включая преэклампсию и синдром HELLP, если их не диагностировать или не лечить, они могут напрямую привести к нарушению функции плаценты и, как следствие, к гипоксии плода.
Геморрагические заболевания матери, включая геморрагическое предлежание плаценты или отслойку плаценты, при которых плацента преждевременно отрывается от матки, могут непосредственно и остро привести к гипоксии плода.
Плохо управляемый сахарный диабет также связан со значительно повышенным риском маточно-плацентарной недостаточности, которая может напрямую привести к гипоксии плода.
Пониженный уровень околоплодных вод, также известный как олигогидрамнион, может привести к соударению или выпадению пуповины ребенка, тем самым напрямую перекрывая поток насыщенной кислородом крови от плаценты к ребенку, что приводит к гипоксии плода.
Если гипоксия или недостаток кислорода являются легкими или преходящими, ребенок обычно сможет компенсировать это без каких-либо постоянных травм.
Однако длительная или тяжелая гипоксия может привести к асфиксии плода.В таких случаях компенсаторные механизмы ребенка выходят из строя или иным образом нарушаются, что напрямую ведет к риску необратимого повреждения мозга и состояния, известного как гипоксически-ишемическая энцефалопатия.
У тех пациентов, которые признаны подверженными риску гипоксии плода, безопасный и внимательный акушер инициирует режим наблюдения за плодами для регулярной оценки состояния ребенка.
Такие тесты для наблюдения за плодами обычно включают нестрессовые тесты, так называемые стресс-тесты, также известные как тесты с провокацией окситоцина и тестирование биофизического профиля.
Давно признано, что вариации частоты сердечных сокращений плода, определяемые непрерывным электронным мониторингом сердца плода, могут отражать как гипоксию плода, так и наличие у ребенка ацидоза, то есть накопление кислот в крови, как и в результате нарушенного газообмена.
Таким образом, у младенцев, которые подвержены риску развития гипоксии плода, безопасные и внимательные акушеры изучат вариабельность сердечного ритма плода и оценят, есть ли какие-либо замедления сердечного ритма плода по сравнению с нормальным исходным уровнем.
Вариабельность от минимальной до «отсутствующей» и / или наличие «поздних» замедлений во время родов многие безопасные и осторожные акушеры считают зловещими признаками потенциальной гипоксии плода.
Безопасные и внимательные акушеры и акушерские медсестры оперативно отреагируют на любые признаки гипоксии плода.
Во многих случаях обнаружение гипоксии плода требует своевременных родов путем кесарева сечения.
К сожалению, во многих случаях, когда гипоксия плода не диагностируется или если родоразрешение путем кесарева сечения неоправданно откладывается, продолжительная гипоксия плода приводит к необратимому и необратимому повреждению мозга, также известному как гипоксически-ишемическая энцефалопатия.
Таким образом, своевременная оценка гипоксии плода и родоразрешение посредством кесарева сечения во многих случаях будет единственным способом предотвратить потенциально разрушительные повреждения ребенка, такие как повреждение головного мозга и церебральный паралич.
Во время беременности приток кислорода и питательных веществ к ребенку, а также удаление углекислого газа и других отработанных газов из ребенка осуществляется через плаценту.
Плацента — чрезвычайно сложный орган, который состоит из систем кровообращения матери и плода.
Адекватный приток крови к плаценте и от плаценты, а также в кровотоке матери и плода необходим для того, чтобы ребенок получал достаточно кислорода и мог выводить углекислый газ и другие отходящие газы.
Любое изменение функции плаценты может привести к снижению доставки кислорода ребенку — состоянию, известному как гипоксия плода.
Поскольку гипоксия плода может быть результатом многих заболеваний или состояний матери или плода, которые снижают функцию плаценты, безопасные и осторожные акушеры будут тщательно обследовать своих пациентов, которые подвержены риску развития гипоксии плода.
Гипертензивные расстройства у матери во время беременности, включая преэклампсию и синдром HELLP, если их не диагностировать или не лечить, они могут напрямую привести к нарушению функции плаценты и, как следствие, к гипоксии плода.
Геморрагические заболевания матери, включая геморрагическое предлежание плаценты или отслойку плаценты, при которых плацента преждевременно отрывается от матки, могут непосредственно и остро привести к гипоксии плода.
Плохо управляемый сахарный диабет также связан со значительно повышенным риском маточно-плацентарной недостаточности, которая может напрямую привести к гипоксии плода.
Пониженный уровень околоплодных вод, также известный как олигогидрамнион, может привести к соударению или выпадению пуповины ребенка, тем самым напрямую перекрывая поток насыщенной кислородом крови от плаценты к ребенку, что приводит к гипоксии плода.
Если гипоксия или недостаток кислорода являются легкими или преходящими, ребенок обычно сможет компенсировать это без каких-либо постоянных травм.
Однако длительная или тяжелая гипоксия может привести к асфиксии плода.В таких случаях компенсаторные механизмы ребенка выходят из строя или иным образом нарушаются, что напрямую ведет к риску необратимого повреждения мозга и состояния, известного как гипоксически-ишемическая энцефалопатия.
У тех пациентов, которые признаны подверженными риску гипоксии плода, безопасный и внимательный акушер инициирует режим наблюдения за плодами для регулярной оценки состояния ребенка.
Такие тесты для наблюдения за плодами обычно включают нестрессовые тесты, так называемые стресс-тесты, также известные как тесты с провокацией окситоцина и тестирование биофизического профиля.
Давно признано, что вариации частоты сердечных сокращений плода, определяемые непрерывным электронным мониторингом сердца плода, могут отражать как гипоксию плода, так и наличие у ребенка ацидоза, то есть накопление кислот в крови, как и в результате нарушенного газообмена.
Таким образом, у младенцев, которые подвержены риску развития гипоксии плода, безопасные и внимательные акушеры изучат вариабельность сердечного ритма плода и оценят, есть ли какие-либо замедления сердечного ритма плода по сравнению с нормальным исходным уровнем.
Вариабельность от минимальной до «отсутствующей» и / или наличие «поздних» замедлений во время родов многие безопасные и осторожные акушеры считают зловещими признаками потенциальной гипоксии плода.
Безопасные и внимательные акушеры и акушерские медсестры оперативно отреагируют на любые признаки гипоксии плода.
Во многих случаях обнаружение гипоксии плода требует своевременных родов путем кесарева сечения.



