Перибронхит что это у детей: что такое, причины, симптомы, диагностика, лечение
что такое, причины, симптомы, диагностика, лечение
Органы дыхания в здоровом состоянии позволяют спокойно получать необходимое количество кислорода и выдыхать ненужный углекислый газ. Многие люди сталкиваются с различными респираторными заболеваниями. Часто они болеют насморком, ОРВИ, ларингитом. Не редкостью становится бронхит, который при затяжном течении переходит в хроническую форму. Однако если бронхит воспаляет слизистую поверхность бронхов, то перибронхит поражает наружную оболочку.
Что это за болезнь? Все о перибронхите будет идти речь на vospalenia.ru.
Что это такое – перибронхит?
Что это такое – перибронхит? Это воспаление наружного слоя клетчатки бронха, который соединяет орган с близлежащими частями. Часто заболевание развивается на фоне хронического бронхита, который характеризуется обильным воспалением слизистой бронхов.
По путям проникновения инфекции разделяют виды:
- Аэрогенный – через просвет бронхов;
- Лимфагенный – через лимфу из лимфатических узлов.

По формам развития разделяют:
- Острый перибронхит с ярко выраженной симптоматикой;
- Хронический перибронхит, который развивается в результате недолеченного или нелечимого острого перибронхита. Характеризуется периодическими ремиссиями и обострениями.
Выделяют три стадии развития перибронхита:
- Компенсаторная – когда внутренние ресурсы организма позволяют компенсировать недостаток дыхательной недостаточности. Проявляется в кашле, одышке.
- Субкомпенсаторная – грудная клетка расширяется, одышка возникает даже в спокойном состоянии. Все больше нарастает дыхательная недостаточность. Утомляемость возникает практически мгновенно.
- Декомпенсаторная – когда дыхательная недостаточность настолько высока, что человек не имеет сил для активного движения.
Причины перибронхита клетчатки бронхов
Основной причиной перибронхита клетчатки бронхов является проникновение инфекции, которая попадает через воздух из просвета бронхов или от других органов организма, которые воспалены и через лимфу распространяют вредность.
При отсутствии лечения инфекция может распространиться на близлежащие альвеолы и ткани, провоцируя возникновение болезней бронхов (например, бронхит или бронхоэктатическая болезнь) и легких (например, пневмония).
Вредностями, которые поражают клетчатку бронхов, являются:
- Инфекции от других болезней: корь, грипп, коклюш, туберкулез и пр.
- Химические вещества, вдыхаемые через воздух.
- Застойные явления в легких из-за плохой работы сердца.
Симптомы и признаки
Признаки и симптомы воспаления клетчатки бронхов возникают на фоне разрастания соединительной ткани вдоль бронхов и их рубцевания. Какие это симптомы?
- Повышение температуры до 39ºС;
- Ухудшение здоровья, что происходит очень резко;
- Выделяется обильное количество гнойной мокроты;
- Слышны шумы во время дыхания;
- Появляются симптомы бронхоэктатической болезни, которая начинает развиваться на фоне основного заболевания: снижение аппетита, потоотделение, одышка, кашель, кровохарканье, упадок сил;
- Повышенная утомляемость;
- Грудная клетка обретает округлую форму.

При кашле отходит зловонная гнойная мокрота, которая слегка улучшает общее состояние. Больному кажется, что он выздоравливает. На самом деле это не так. Перибронхит сам не излечится. Последующие приступы будут указывать лишь на развитие хронической болезни, которая будет лечиться более долго и серьезно.
Перибронхит у детей
Перибронхит у детей развивается на фоне хронического бронхита, кори, гриппа, коклюша. Таким образом, следует вовремя лечить инфекционные болезни, которые провоцируют воспаление клетчатки бронхов.
перейти наверхПерибронхит у взрослых
перейти наверхПерибронхит у взрослых проявляется достаточно часто, если больной пренебрегает лечением других респираторных болезней нижних отделов дыхательной системы. Вредность на работе также сказывается на развитии воспаления, соответственно, часто он встречается у мужчин, нежели у женщин.
Диагностика
Симптоматика перибронхита настолько неуникальна, что ее часто путают с другими респираторными заболеваниями, например, бронхит или альвеолит.
- Делается анализ крови;
- Проводится бактериологический анализ мокроты, которая отходит вместе с кашлем;
- Проводится рентгенография, КТ и МРТ дыхательных путей;
- Проверяется аллергическая реакция на различные вещества.
Лечение
Лечение перибронхита начинается с устранения основного заболевания, которое привело к развитию воспаления клетчатки бронхов. Часто данной болезнью является хронический бронхит. Лечение одной и той же области дает качественные результаты. Комплекс процедур практически одинаков.
перейти наверхЧем лечить перибронхит?
Лекарствами:
- Антибиотиками, противовирусными или противогрибковыми препаратами, в зависимости от причины возникновения.

- Противоаллергическими препаратами, если причиной стала аллергия.
- Йодистыми препаратами, фибролизином и рассасывающими средствами.
- Мочегонными препаратами для снятия отека.
- Сульфаниламидами.
В качестве диеты выступает питание, полное углеводов. Дается больше теплой жидкости, чтобы способствовать разжижению мокроты.
В домашних условиях лечение не проводится, поскольку речь часто идет о двух заболеваниях одновременно – то, которое спровоцировало перибронхит, и само воспаление клетчатки бронхов. Здесь проводятся различные прогревающие процедуры (компрессы, аппликации, грелки, ванны), которые способствуют выздоровлению.
перейти наверхПродолжительность жизни
Сколько живут при перибронхите? В совокупности с другими болезнями он дает неутешительный прогноз. При отсутствии должного лечения продолжительность жизни составляет несколько лет, в зависимости от осложнений, которые развиваются, и симптомов, которые они вызывают. Осложнениями являются:
- Гангрена легкого.

- Бронхит в обструктивной форме.
- Пневмония.
- Бронхоэктатическая болезнь.
- Дыхательная недостаточность.
| Воспаления
Раздражительный человек – это звучит как диагноз. Раздражительность является реакцией психики на то, от чего человек устал, на что у него не хватает душевных сил и энергии реагировать спокойно.
Постоянная раздражительность может свидетельствовать об эмоциональном выгорании, о хронической усталости. В такой ситуации человек нуждается в отдыхе, в смене обстановки. Но если ситуация не изменится и после отдыха, то однозначно требуется помощь специалиста.
Однако сейчас я хочу поговорить не о болезненной раздражительности, а о раздражении, которое время от времени возникает у, в общем-то, благополучных и спокойных людей.
Если мы понаблюдаем за собой, то обнаружим, что у нас вызывают раздражение определенные черты характера, определенные ситуации и определенный тип людей.
К примеру, нас может раздражать безответственность или человек, разговаривающий с превосходством. Давайте попробуем вспомнить, какая черта нас больше всего раздражает в людях.
Отдельная и довольно своеобразная категория людей — это пожилые люди и старики, требующие ухода. В силу ограничивающих их обстоятельств они капризны и раздражительны, нуждаются в постоянном внимании и заботе, на которые у нас порой не хватает времени, желания и сил, соответственно вызывают у нас повышенное раздражение. Самый оптимальный выход из подобной ситуации это помощь профессиональной сиделки, которая в силу своей профессии обучена общению с такой категорией людей и которая существенно облегчит жизнь и сбережет ваши нервы. Такую помощь можно найти на https://sidelka-myliza.ru/
Под большим секретом хочется сообщить, что раздражительность — это черта характера, присущая нам самим.
Заранее предвижу, как многие люди будут возмущаться, что это, дескать, абсурд, полная чушь!!!!
А речь идет именно о том, что мы считаем эту черту слишком постыдной, слишком отрицательной, поэтому не позволяем вести себя подобным образом ни при каких обстоятельствах. Мы бессознательно боимся, что если будем вести себя «неподобающим» образом, то нас могут осудить, отвергнуть.
Мы бессознательно боимся, что если будем вести себя «неподобающим» образом, то нас могут осудить, отвергнуть.
Считая, что эта черта слишком «плохая» мы стараемся все время (а происходит это бессознательно!) следить за собой, прикладывать усилия, тратить свободную энергию, чтобы не быть «такими», всегда, так сказать, соответствовать. А в случае, когда в жизни сталкиваемся с подобными проявлениями, возникают отрицательные чувства: непримиримость, осуждение, раздражительность, агрессия.
Чаще всего это убеждение у человека возникает в детстве: этому ребенка учили родители или другие значимые для него люди, в семье это убеждение было негласным правилом, или это убеждение было почерпнуто из книг или правил социальной морали.
А ведь самый здоровый подход к жизни – это принятие. Принятие, что подобные чувства и черты характера существуют и что нам они тоже присущи в той или иной степени. Если мы примем, что нам тоже присуща эта «плохая» черта, это не означает, что мы начнем ее проявлять. К примеру, мы не станем тут же вести себя эгоистично или грубо. Мы уже воспитаны, приучены быть «хорошими» и от этого уже никуда не денемся. Это умение навсегда остается нашим. Просто принятие себя автоматически снизит уровень раздражительности и агрессии, а как следствие, отношения с людьми станут более комфортными и приятными, более дружелюбными, поскольку люди и без слов чувствуют симпатию и расположение или неприятие и осуждение.
К примеру, мы не станем тут же вести себя эгоистично или грубо. Мы уже воспитаны, приучены быть «хорошими» и от этого уже никуда не денемся. Это умение навсегда остается нашим. Просто принятие себя автоматически снизит уровень раздражительности и агрессии, а как следствие, отношения с людьми станут более комфортными и приятными, более дружелюбными, поскольку люди и без слов чувствуют симпатию и расположение или неприятие и осуждение.
Для того, чтобы легче было принять в себе это «плохое», можно попробовать отважиться на эксперимент и позволить себе немножечко проявить эту черту (безусловно, в той степени, и в той ситуации, когда это не принесет вреда окружающим.) Можно попробовать поозорничать и побыть, к примеру, чуточку высокомерным или шутливо-неграмотным. При условии, что вы себя не осуждаете за подобное поведение, это может принести ощущение легкости и веселья. Окружающих это может удивить, может даже возникнуть сопротивление такому новшеству в вас, поскольку вы стали несколько непредсказуемым, что не очень удобно и привычно. Но со временем они привыкнут и общаться с вами теперь будет легче, интереснее и безопаснее (ведь вы уже не будете их осуждать!). А вам позволит избавиться от агрессии и раздражительности, что даст возможность часть свободной энергии, которая до сих пор тратилась на негативные эмоции, потратить на что-то более приятное.
Но со временем они привыкнут и общаться с вами теперь будет легче, интереснее и безопаснее (ведь вы уже не будете их осуждать!). А вам позволит избавиться от агрессии и раздражительности, что даст возможность часть свободной энергии, которая до сих пор тратилась на негативные эмоции, потратить на что-то более приятное.
Хочется сказать, что все вышесказанное относится и к тем чертам характера, которыми мы восхищаемся в других людях. Чем больше мы этими чертами восхищаемся, тем в большей степени они принадлежат нам.
Осложнения коронавируса: страдают легкие, сердце, почки и мозг. Это надолго или навсегда?
Автор фото, Getty Images
Вот уже полгода ученые и медики пытаются оценить вред, который наносит человеческому организму Covid-19, однако, несмотря на более чем 400 тыс. летальных исходов, миллионы переболевших и тысячи исследований и отчетов, картина так до конца и не прояснилась.
Данные, полученные британскими исследователями, свидетельствуют, что первичные симптомы заболевания могут проявляться, исчезать и вновь проявляться в течение 30 и более дней, что заметно дольше официального двухнедельного периода, обозначенного экспертами ВОЗ.
А для кого-то болезнь может означать лишь начало долгой и мучительной борьбы с вирусом, которая может обернуться новым «посткоронавирусным синдромом».
По данным авторитетного журнала Science, этот коронавирус «творит такие вещи, какие не творила ни одна болезнь, известная человечеству».
Пока власти принимали одну меру за другой в попытке остановить распространение инфекции, а медики (тщетно) искали лекарство или вакцину, способные побороть болезнь, мы узнавали о коронавирусе все новые подробности, и наше представление о нем менялось, причем в некоторых аспектах — в корне.
Поначалу казалось, что это обычное респираторное заболевание вроде SARS или птичьего гриппа, однако позже выяснилось, что коронавирус (его официальное название SARS-CoV-2) может затронуть легкие, мозг, носоглотку, глаза, сердце, кровеносные сосуды, печень, почки и кишечник, то есть буквально все жизненно важные органы.
По результатам уже проведенных исследований, Covid-19 сопровождается целым набором самых разнообразных симптомов, и для тех, кто переболел в тяжелой форме, долговременные последствия могут быть самыми серьезными: от рубцевания легочной ткани и отказа почек до воспаления сердечной мышцы, аритмии, повреждения печени, когнитивных нарушений, психозов, сопровождающихся резкой сменой настроения, и многого другого.
То, как заболевание отразится на людях в долгосрочной перспективе, еще предстоит выяснить в полной мере, однако уже сейчас есть много указаний на то, что последствия этого заболевания продолжают испытывать даже те, кто переболел коронавирусом в достаточно легкой форме.
Есть и еще один важный вопрос: может ли вирус SARS-CoV-2 сохраняться в человеческом организме в дормантном состоянии, и не проявит ли он себя через несколько лет в том или ином виде?
Ничего удивительного в этом не будет, говорят медики, ведь известны вирусы, которые ведут себя именно так. К примеру, после того, как человек переболел ветрянкой, вирус герпеса, который ее вызвал, никуда не исчезает, он может тихо прятаться десятилетиями, а потом при удобном случае вылиться в болезненный опоясывающий лишай.
А вирус, вызывающий гепатит B, через много лет может привести к раку печени.
Даже вирус Эбола, обнаруженный спустя много месяцев у выживших пациентов в глазной жидкости, впоследствии вызывает слепоту у 40% инфицированных.
Поэтому, учитывая тот факт, что SARS-CoV-2 предпочитает легкие, врачи заподозрили, что именно там в первую очередь вирус способен вызывать необратимые изменения.
Легкие
Еще в марте специалисты Уханьского технологического университета сообщали, что у 66 из 70 пациентов, переживших пневмонию на фоне Covid-19, компьютерная томография обнаружила видимые повреждения в легких.
Автор фото, Getty Images
Подпись к фото,У некоторых пациентов функции легких могут не восстановиться полностью
Эти повреждения варьировались от закупорки кровеносных сосудов в альвеолах до рубцевания легочной ткани. Такое рубцевание, или утолщение ткани, называется легочным фиброзом и может привести к одышке. В настоящее время не существует способов остановить или повернуть вспять этот процесс.
«Фиброз может стабилизироваться и не меняться со временем, это верно. У некоторых пациентов функции легких могут не восстановиться полностью, однако последствия этого не будут столь уж существенными, — поясняет профессор Лестерского университета Луиза Уэйн.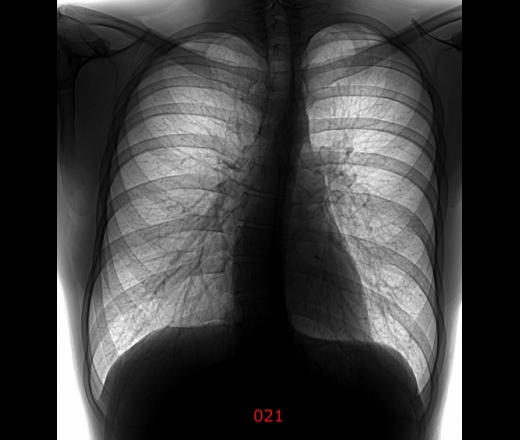 — Но бывают и случаи прогрессирующего фиброза, а это по-настоящему опасно, потому что рано или поздно он убивает».
— Но бывают и случаи прогрессирующего фиброза, а это по-настоящему опасно, потому что рано или поздно он убивает».
Кроме того, еще до введения в Британии жесткого карантина Факультет медицины интенсивной терапии (FICM) — профессиональная медицинская организация, отвечающая за подготовку британских врачей-реаниматологов, предупреждал, что пациенты с тяжелой формой Covid-19 могут получить столь сильные повреждения легких, что на восстановление им понадобится до 15 лет.
FICM подчеркивал, что у многих пациентов, поступивших в отделения реанимации, развивался острый респираторный дистресс-синдром (ОРДС) — сильнейшее воспаление легких, при котором жидкость из крови попадает в альвеолы, что делает дыхание невозможным без специального аппарата.
Учитывая историю повреждения легочной ткани у пациентов, переболевших SARS и MERS, группа медиков под руководством радиолога Мелины Хоссейни из Калифорнийского университета в Лос-Анджелесе настоятельно рекомендует вести мониторинг пациентов, переболевших Covid-19, и проверять их легкие «на предмет оценки долгосрочного или перманентного повреждения, включая фиброз».
Сердце и кровеносные сосуды
По мере того, как врачи пытаются оценить ущерб, нанесенный различным органам пациентов, переболевших Covid-19, они сталкиваются с вполне ожидаемой проблемой: люди, страдающие заболеваниями легких, сердца, почек или крови, как правило, и становились первыми жертвами коронавируса, и в их случае болезнь чаще всего протекала тяжело. Поэтому не всегда можно определить, к чему привел вирус, а что уже было повреждено до него.
Однако ясно одно: когда симптомы инфекции начинают проявляться, функции многих органов нарушаются, и отказ одного ведет за собой отказ других.
Свою роль играет и острый воспалительный процесс, который приводит к инсультам и инфарктам.
Автор фото, Getty Images
Подпись к фото,Коронавирус может вызывать повреждение сердечной мышцы и образование тромбов в крови
Как говорится в отчете за март, опубликованном в специализированном медицинском журнале JAMA Cardiology, повреждения сердечной мышцы были отмечены почти у 20% из 416 обследованных пациентов в уханьских больницах.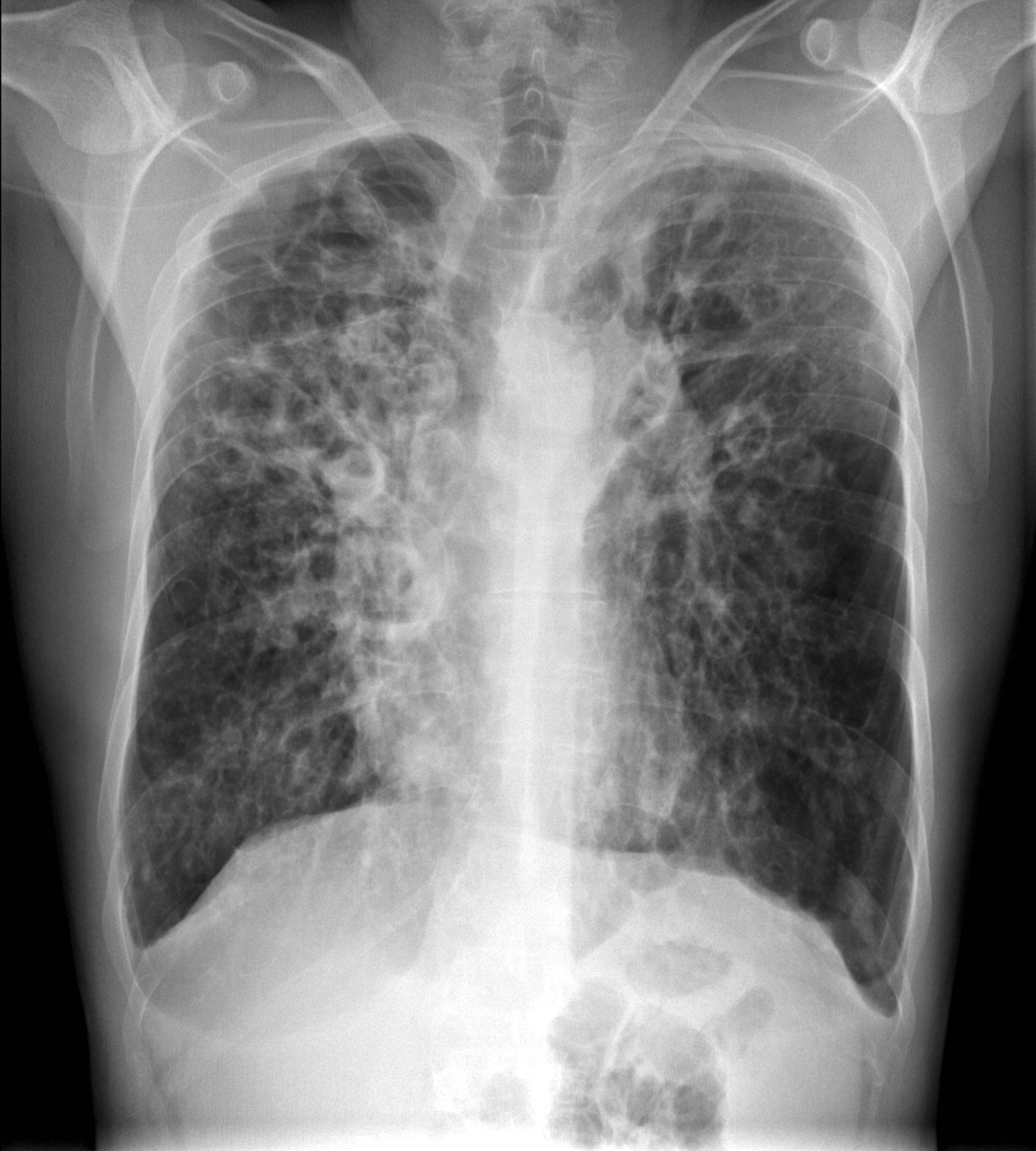
Там же, но уже в реанимационных отделениях, аритмия была отмечена у 44% из 36 пациентов.
Медики связывают это с гиперцитокинемией, или цитокиновым штормом, потенциально смертельной реакцией организма, который запускает неконтролируемую активацию иммунных клеток, что ведет к разрушению тканей очага воспаления. Такая реакция наблюдалась у некоторых больных коронавирусом.
В частности, возникает воспаление сердечной мышцы (миокардит), что сбивает электрические импульсы, ведет к артимии и нарушает циркуляцию крови, вызывая одышку.
Осложнения на сердечно-сосудистую систему характерны не только для Covid-19: миокардит могут вызывать многие вирусные заболевания. И хотя большинство пациентов выздоравливает, у некоторых повреждения сердечной мышцы носят необратимый характер.
Более того, Covid-19 негативно влияет и на саму кровь. У 38% из 184 пациентов с коронавирусом, попавших в реанимацию в Голландии, была выявлена повышенная свертываемость крови, и почти у трети из них обнаружились тромбы.
Почки
Хотя коронавирус поражает в первую очередь легкие, у некоторых пациентов инфекция переходила и на почки.
Согласно проведенным в Китае выборочным исследованиям, у 27% из 85 пациентов, попавших в уханьские больницы с коронавирусом, были отмечены проблемы с почками.
По результатам другого исследования, у 59% из почти 200 пациентов, госпитализированных в провинциях Хубэй и Сычуань, в моче наблюдался белок, свидетельствующий об инфекции, а у 44% присутствовала и кровь, что говорит о серьезном поражении почек.
Причем у пациентов с острой почечной недостаточностью (ОПН) риск летального исхода был в 5 раз выше, чем у обычных больных коронавирусом.
Мозг
Автор фото, Getty Images
Подпись к фото,Ученые еще не установили, как именно коронавирус воздействует на мозг
Из 214 исследованных пациентов с Covid-19 треть продемонстрировала неврологические симптомы, включая головокружение, головную боль и когнитивные расстройства.
Пока что ученые лишь гадают, что именно вызвало эти симптомы. Однако существующие теории сфокусированы на том, как вирус воздействует на нейроны — нервные клетки. Упоминается и потеря вкуса и запаха, и воспалительные процессы (таким образом на вирус реагирует наша иммунная система), и нехватка кислорода, которую ощущали некоторые больные.
Когнитивные расстройства могут быть связаны с пребыванием пациентов в реанимации, это еще называют временным помутнением рассудка, или делирием, когда у человека возникают галлюцинации, впрочем, чаще это наблюдается у пожилых людей.
И хотя симптомы, как правило, со временем пропадают, некоторые из них могут сохраняться. По словам врачей, восстановление когнитивных функций у переболевших коронавирусом сильно зависит от возраста, коморбидности (то есть сосуществования у пациента двух или более заболеваний или расстройств) и тяжести течения самой болезни.
Как указывает профессор реабилитационной медицины Королевского колледжа Лондона Линн Тернер-Стокс, вирус может затрагивать мозг даже тех пациентов, которые переболели в достаточно легкой форме.
А по словам профессора Кембриджского университета Эда Буллмора, у нас уже есть достаточно оснований полагать, что SARS-CoV-2 вызывает «нейротоксическое заболевание», которое приводит к «своего рода изменению ментального состояния пациента».
«Мы точно не знаем, что именно вызывает эту нейротоксичность, — признается профессор Буллмор. — Может быть, вирус заражает мозг, может быть, реакция нашей иммунной системы на вирус ведет к повреждению нейронов, или все дело в крови, которая поступает в мозг. На данный момент возможны все эти варианты».
В статье использованы материалы Independent, Los Angeles Times и Mail Online.
Острый бронхит: лечение народными средствами
Лечение народными средствами этой болезни нередко оказывается достаточно эффективным. Это не удивительно, ведь бронхит относится к распространенным заболеваниям дыхательной системы, и народная медицина давно нашла лекарства от этой хвори. Как именно справляться с бронхитом сидя дома рассказывает портал Medaboutme.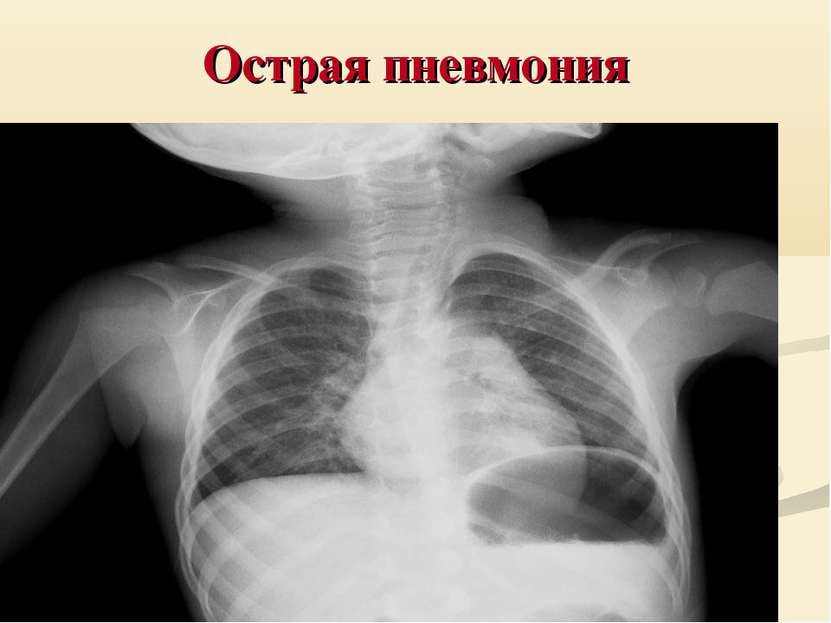 ru.
ru.Источник: MedAboutMe.Ru © Medaboutme.ru
Воспаление слизистой оболочки бронхов может развиться как самостоятельное заболевание, вызванное инфекцией или неблагоприятными факторами среды. Иногда острый бронхит становится осложнением на фоне другой болезни: кори, ОРВИ, ветрянки. Бронхитом часто страдают курильщики. Некоторые вредные производства также способствуют появлению предрасположенности к бронхиту.
Симптомы острого бронхита развиваются быстро. Сначала больной начинает чувствовать недомогание, у него поднимается температура, в груди появляется ощущение, словно кто-то прошелся по дыхательным путям грубой наждачкой. Дыхание становится хриплым, шумным. Через некоторое время появляется сухой кашель, не приносящий облегчения. Вскоре начинается отделение мокроты и кашель становится влажным, с большим количеством отделяемого неприятного серовато-желтого или зеленоватого цвета. Если не запускать острый бронхит, народное лечение может дать отличный результат и не даст болезни перейти в хроническую форму.
Рецепты народного лечения бронхита
Foto: Shutterstock
Если симптомы указывают на острый бронхит, лечение народными средствами нужно начинать немедленно. В начале заболевания состояние больного может облегчить использование потогонных средств: отвара из сушеной малины, цветков липы, шалфея или мяты. Хорошо помогает также имбирный чай с медом, можно добавить немного лимонного сока, если нет аллергии.
Иногда помогает компресс из натертого хрена, но с этим средством нужно быть очень осторожным: можно ненароком добавить к бронхиту ожог и раздражение на коже.
Детям можно делать на ночь компресс из разогретого натурального меда, смешанного с топленым свиным салом.
Когда появляется сухой кашель, облегчить состояние помогут отхаркивающие средства. Одно из наиболее эффективных — сок черной редьки, смешанный с медом. В северных регионах для лечения бронхита готовят сироп из сосновых почек, с добавлением меда и спиртового раствора прополиса. Для приготовления этого средства килограмм сосновых почек мелко нарезают, кипятят в 3 л воды в течение 15 минут. В процеженный отвар добавляют 1 кг меда и 10 мл спиртовой настойки прополиса. Все хорошо перемешивают, разливают по стеклянным бутылкам и хранят состав в холодильнике. Курс лечения — до 3 недель, в течение которых нужно принимать по 5 мл состава за 30 минут до еды 2-3 раза в день.
Для приготовления этого средства килограмм сосновых почек мелко нарезают, кипятят в 3 л воды в течение 15 минут. В процеженный отвар добавляют 1 кг меда и 10 мл спиртовой настойки прополиса. Все хорошо перемешивают, разливают по стеклянным бутылкам и хранят состав в холодильнике. Курс лечения — до 3 недель, в течение которых нужно принимать по 5 мл состава за 30 минут до еды 2-3 раза в день.
Когда бронхит переходит в последнюю фазу, можно переходить к лечению соком алоэ. Для лекарства потребуется 10 зрелых листьев алоэ. Растение должно быть не моложе 3 лет, и перед срезанием листьев его не поливают в течение недели. Срезанные листья выдерживают в холодильнике 1-2 дня, потом их измельчают в мясорубке или блендере. В получившуюся массу добавляют 0,5 л меда и 1 л кагора, все хорошо перемешивают и дают настояться в течение недели в темном месте. После этого состав нужно процедить и хранить в холодильнике. Пьют лекарство по столовой ложке перед едой, трижды в день, курс составляет 30 дней.
У этого средства есть противопоказания:
- Детям оно не подходит из-за значительного содержания алкоголя.
- Нельзя принимать состав беременным и кормящим женщинам.
- Не рекомендуется применение при наличии заболеваний печени и почек.
Диагностика и лечение респираторного микоплазмоза Текст научной статьи по специальности «Клиническая медицина»
и ОБЗОРЫ
поз. с участием иностранных уч-х. — Ленинград, 1974. — С. 77-82.
17. Дильман, В.М. Корреляция между иммунологической реактивностью и эндо-углеводным обменом. Влияние фен-формина //Вопросы онкологии.-1976.- №2.- С. 13-17.
18. Иванов, С.Г. Стимулирующее влияние заместительной гормональной терапии на опиоидную систему больных с климактерической миокардиодистрофией как один из возможных механизмов кардиопротекторного действия терапии / С. Г. Иванов, Н.Е. Гальцова, А.А. Зозуля.- M.,
Г. Иванов, Н.Е. Гальцова, А.А. Зозуля.- M.,
2002.- 40 с.
19. Коваленко, В.Н. Анализ взаимосвязи вегетативных расстройств и изменений сердечно-сосудистой системы в климактерический период / В.Н. Коваленко, А.Д. Старцева, Л.А. Шумленский. — Днепропетровск, 1999.- 4 с.
20. Козинец, Г.И. Физиологические аспекты старения организма человека, основные показатели / Г.И. Козинец. -Санкт-Петербург, 2000. — C. 23-38.
21. Колесник, Ю.М. Взаимоотношения гипоталамо-гипофи-зарно-надпочечниковой системы у женщин с экспериментальным сахарным диабетом / Ю.М. Колесник, А.В. Абримов, О.В. Мельникова //Проблемы эндокриноло-гии.-1996.- Т.42, №1.- С.34-37.
22. Кретова, Н.Е. Климактерическая миокардиодистрофия. Клиника, диагностика и лечение: дис. …докт. мед. наук.
…докт. мед. наук.
— М., 1989.- 330 с.
23. Куликова, Н.Г. К вопросу о социально-гигиенических и клинических аспектах климактерической миокардио-дистрофии // Проблемы социальной медицины и история медицины.-1997.-№1.-С. 39-40.
24. Куликова, Н.Г. Социально-гигиенические и клинические подходы в дифференциальной диагностике климактерической миокардиодистрофии / Н.Г. Куликова.- М., 1998.6 с .- Деп. журн. Тер. архив, №25838.
25. Коробкеев, А.А. Сосуды и околососудистое русло сердца людей старших возрастных групп. Дисс. …канд.мед. наук. / А.А. Коробкеев.- Ставрополь, 1992.-222 с.
26. Меерсон, Ф.З. Феномен адаптационной стабилизации структур и защита организма / Ф.З. Меерсон, И.Ф. Малышев. — М.: Наука., — 1993. — 158 с.
27. Меерсон, Ф.З. Адаптация к стрессовым ситуациям и физическим нагрузкам / Ф.З. Меерсон, М.Г Пшенникова.
Меерсон, Ф.З. Адаптация к стрессовым ситуациям и физическим нагрузкам / Ф.З. Меерсон, М.Г Пшенникова.
— М., 1988.- 45 с.
28. Метелица, В.И. Нарушение ритма / В.И. Метелица, Е.В. Копурина, Е.В. Бочкарева [и др.] // Кардиология.-1996.-№2.- С. 4-16.
29. Орехов, К.В. Онтогенез человека и цивилизации / К.В. Орехов // Бюллетень СО АМН СССР. — 1982.- №3.- 45 с.
30. Разумов, А.Н. Здоровье здорового человека / А.Н. Разумов. — М.: Медицина, 1999.-39 с.
31. Разумов, А.Н. Гомеостатическая адаптация человека /
A.Н. Разумов, В.А. Матихин. — М., 1999.-C. 45-76.
32. Разумов, А.Н. Здоровье здорового человека. (Основы восстановительной медицины) / А. Н. Разумов, В.А. Пономаренко, В.А. Пискунов, В.С. Шинкаренко.- М., 1996.
Н. Разумов, В.А. Пономаренко, В.А. Пискунов, В.С. Шинкаренко.- М., 1996.
— C. 59-64.
33. Фролькис, В.В. Физиологические механизмы старения /
B.В.Фролькис, Д.Ф. Чеботарев.- Л.: Наука,1979.-679 с.
34. Фролькис, В.В. Кровообращение и старение / В.В. Фролькис, В.В. Безруков, В.Г. Шевчук. — Л.: Наука, 1984.-215 с.
35. Хмельницкий, О.К. Функциональная морфология эндокринной системы при атеросклерозе и старении / О.К. Хмельницкий, А.С. Ступина.- М.,1989.-53 с.
36. Arab, D. Magnetic stimulation of the human brain and peripheral nervous system / D. Arab, A. Lopes-Candales, V. Valeti., H.J. Shunemann // Am. J. Cardiol.-2000.-Vol.85.-P.764-766.
37. Arcaro, G. Balneotherapie — new Aspekte / G. Arcaro, M. Zenere, D. Travia [et al.] // Eur. J. clin. Invest. — 1993. — Vol. 231. — P. 116 — 118.
Arcaro, G. Balneotherapie — new Aspekte / G. Arcaro, M. Zenere, D. Travia [et al.] // Eur. J. clin. Invest. — 1993. — Vol. 231. — P. 116 — 118.
38. Bos, J.D. Bioelectric Responses of Smooth and skeletal Muscles to a Double Stimuli Pulsed Magnetic Field / J.D. Bos // Clin. exp. — 1997. — Vol. 93., Suppl. — P. 35-39.
39. Boesgaard, S. Ambulatory cardiology diseases / S. Boesgaard, J. Alderskvite, E. Poulsen [et al.] — // Circ. Res. — 1994. -Vol.74. — P. 115-120.
40. Bellossi, M. Ultrasound diagnosis / M. Bellossi, V. Gullien, M. Rocker Ruellossi //Abstracts 3-rd. International Bioelectric congress of European. — Nancy. — 1996. — P. 15-17.
41. Okin, P.M. Progression of chronic discase. Mechanisms, risc factors, and testing of interventions/ P.M. Okin, R.B. Devereenx, B.V. Howard [et al. ] //Circulation.-2000.-Vol.101. — P. 61-66.
] //Circulation.-2000.-Vol.101. — P. 61-66.
42. Vincent, G.M. Long-term effects of hormone therapy / G.M. Vincent, K. Fimothy, J. Fox., L. Zhang // Cardiol. Rev.-1999.- Vol.92, №7. — P. 44-45.
© В.А. Батурин, Е.В. Щетинин, 2007 УДК 616.99: 579.88 (075)
ДИАГНОСТИКА И ЛЕЧЕНИЕ РЕСПИРАТОРНОГО МИКОПЛАЗМОЗА
В.А. Батурин, Е.В. Щетинин
Ставропольская государственная медицинская академия
Одними из основных проблемных возбудителей с середины прошлого столетия стали считать представителей так называемых атипичных заболеваний. Термин “атипичный” появился впервые в пульмонологии, а затем укоренился в других областях медицины. Им обозначали заболевания, протекающие без привычной клинической симптоматики — со скудными клиническими, рентгенологическими, аускультативными и лабораторными показателями, без выраженного лейкоцитоза и не поддающиеся обычной терапии антибиотиками пенициллинового ряда. Определенную роль в изучении данных инфекций сыграли также многочисленные попытки выделить возбудителей и опыты по заражению различных видов животных и эмбрионов, а также посевы на известные среды, которые не давали положительных результатов. Поэтому вполне справедливо возникало предположение о вирусной природе этих возбудителей. Однако по мере пополнения и накопления сведений была определена их структура и морфология, выявлены факторы патогенности, исследовано таксономическое положение, изучены клинические варианты течения, принципы терапии. К таким заболеваниям в первую очередь были отнесены хламидиозы, микоплазмозы, легионеллезы, пневмоцистозы.
Определенную роль в изучении данных инфекций сыграли также многочисленные попытки выделить возбудителей и опыты по заражению различных видов животных и эмбрионов, а также посевы на известные среды, которые не давали положительных результатов. Поэтому вполне справедливо возникало предположение о вирусной природе этих возбудителей. Однако по мере пополнения и накопления сведений была определена их структура и морфология, выявлены факторы патогенности, исследовано таксономическое положение, изучены клинические варианты течения, принципы терапии. К таким заболеваниям в первую очередь были отнесены хламидиозы, микоплазмозы, легионеллезы, пневмоцистозы.
Поскольку изучение “атипичных” инфекций началось с микоплазм, вполне естественно, что на сегодняшний день накопился огромный клинический опыт, освещены основные этапы диагностики и лечения заболеваний ими вызванных.
Эпидемиология
Микоплазма является внутриклеточным паразитом и в прежние годы наиболее часто рассматривалась в связи со способностью вызывать вялотекущее поражение урогенитального тракта, а также верхних или нижних дыхательных путей.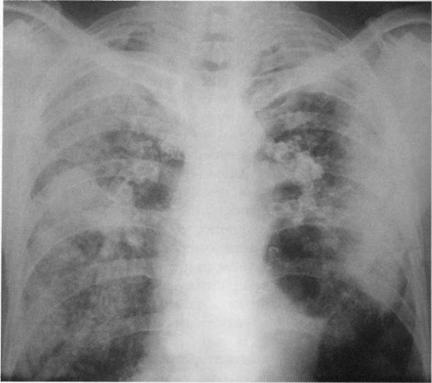 Сегодня микоплазменная инфекция прочно заняла ведущее место в спектре возбудителей пневмоний после пневмококка. При этом пневмонии, вызываемые M. pneumoniae, нередко имеют тенденцию к хронизации (74%) и тяжелому течению с летальными исходами (12,9%) [5,9]. M. pneumoniae инфицирует детей всех возрастов, но инфекции нижних дыхательных путей встречаются в основном у школьников и у взрослых молодого возраста. Серологическое обследование дошкольников продемонстрировало
Сегодня микоплазменная инфекция прочно заняла ведущее место в спектре возбудителей пневмоний после пневмококка. При этом пневмонии, вызываемые M. pneumoniae, нередко имеют тенденцию к хронизации (74%) и тяжелому течению с летальными исходами (12,9%) [5,9]. M. pneumoniae инфицирует детей всех возрастов, но инфекции нижних дыхательных путей встречаются в основном у школьников и у взрослых молодого возраста. Серологическое обследование дошкольников продемонстрировало
наличие инфекции при отсутствии анамнеза, который позволял бы заподозрить заболевание нижних дыхательных путей [10,22]. Этиологическая значимость M. pneumoniae возрастает у детей школьного возраста, достигая приблизительно 20% при внебольничной пневмонии у школьников и 50% — у студентов и военнослужащих [10,12,13]. Эпидемиологические исследования у военнослужащих продемонстрировали, что перенесенная инфекция обеспечивает по крайней мере краткосрочную защиту от последующих M. pneumoniae-инфекций и что иммунитет после пневмонии длится дольше, чем после бессимптомного течения заболевания. Вероятность развития инфекций увеличивается в 2-3 раза при неблагоприятных социально-экономических условиях, в 4-5 раз при циркуляции возбудителя в семье и рецидивирующем их течении.
pneumoniae-инфекций и что иммунитет после пневмонии длится дольше, чем после бессимптомного течения заболевания. Вероятность развития инфекций увеличивается в 2-3 раза при неблагоприятных социально-экономических условиях, в 4-5 раз при циркуляции возбудителя в семье и рецидивирующем их течении.
Эпидемические вспышки M. pneumoniae встречаются с интервалом 3 — 7 лет. Они начинаются осенью и могут длиться в течение нескольких месяцев. Источником M. pneumoniae-инфекции в семьях часто являются дети. Инкубационный период длится около 3-4 недель.
Наиболее частым клиническим синдромом M. pneumoniae-инфекции является трахеобронхит с гриппоподобными системными проявлениями. Системные признаки заболевания, как правило, умеренно выраженные. Менее 2% детей с пневмонией требуют госпитализации.
Эрадикация M. pneumoniae из респираторного тракта может происходить через несколько недель или месяцев после начала симптомов заболевания. Анти-биотикотерапия, по мнению некоторых специалистов, более полезна для облегчения симптомов заболевания, чем для эрадикации микрорганизма [11].
Анти-биотикотерапия, по мнению некоторых специалистов, более полезна для облегчения симптомов заболевания, чем для эрадикации микрорганизма [11].
Патогенез
M. pneumoniae поражает эпителиальную ткань респираторного тракта. Экспериментальные модели на животных показывают перибронхиальную воспалительную инфильтрацию. Микроорганизм передается аэрозольно-капельным путем. Происходит специфическое взаимодействие между эпителиальными клеточными рецепторами и связывающим протеином Р1 микроорганизма — поверхностным антигеном M. pneumoniae. Происходит накопление цитотоксических продуктов (пероксид водорода и супероксид-анион), которые, вероятно, определяют клеточную токсичность патогена. Паралич ресничек респираторного тракта, другие пос-
ледствия M. pneumoniae-инфекции могут вызывать кашель, который часто персистирует в течение нескольких недель после полного выздоровления [10,15].
В прошлом невозможность выделить M. pneumoniae культуральным способом из нереспираторных клинических образцов приводила к мнению, что распространения микроорганизма вне респираторного тракта не происходит. Предполагалось, что экстрапульмональные осложнения могут быть результатом накопления пере-крестно-реагирующих антител, приводящих к аутоиммунным феноменам. Однако использование ПЦР позволило подтвердить диссеминацию микроорганизма: M. pneumoniae обнаружили в ликворе и сыворотке крови. Эффекты перекрестно-реагирующих антител предположительно объясняют механизм развития гемолиза и кожных проявлений.
Клиническая картина заболевания
В начале заболевания больные обычно предъявляют жалобы на общее недомогание, миалгии, боли в горле, ретробульбарную головную боль и повышение температуры тела. Боль и напряжение в области параназальных синусов, оталгия описывается у подростков и у взрослых. Вышеуказанные симптомы не отличаются от таковых при респираторных вирусных инфекциях. Часто затянувшийся кашель на фоне трахеобронхита (ми-коплазменной этиологии) при отсутствии пневмонии иногда симулирует коклюш.
Вышеуказанные симптомы не отличаются от таковых при респираторных вирусных инфекциях. Часто затянувшийся кашель на фоне трахеобронхита (ми-коплазменной этиологии) при отсутствии пневмонии иногда симулирует коклюш.
Заболевание респираторного тракта
Бронхопневмония — наиболее часто распознаваемый клинический синдром, ассоциированный с M. pneumoniae- инфекцией [10,22]. Обычно начало заболевания постепенное, проявляется недомоганием, головной болью, лихорадкой, фарингитом. При дальнейшем прогрессировании заболевания и вовлечении в патологический процесс нижних дыхательных путей отмечается осиплость голоса и кашель. Проявления острого ринита не характерны для микоплазменной пневмонии и обычно позволяют заподозрить вирусную этиологию.
Хотя клиническое течение заболевания у пациентов, не получавших лечение, вариабельно, отмечается усиление кашля в течение 2 недель заболевания, затем все симптомы постепенно разрешаются в течение 3-4 недель. В начальной стадии кашель непродуктивный, но у старших детей и у подростков выделяется пенистая белая мокрота. Степень выраженности жалоб обычно выше по сравнению с объективными клиническими признаками, которые проявляются позже. Сухие и влажные хрипы выслушиваются хорошо и похожи на одноименные аускультативные феномены при бронхиальной астме и бронхиолите. С прогрессированием заболевания повышается температура тела, кашель становится мучительным и у некоторых пациентов может возникнуть диспноэ.
В начальной стадии кашель непродуктивный, но у старших детей и у подростков выделяется пенистая белая мокрота. Степень выраженности жалоб обычно выше по сравнению с объективными клиническими признаками, которые проявляются позже. Сухие и влажные хрипы выслушиваются хорошо и похожи на одноименные аускультативные феномены при бронхиальной астме и бронхиолите. С прогрессированием заболевания повышается температура тела, кашель становится мучительным и у некоторых пациентов может возникнуть диспноэ.
Рентгенологические признаки микоплазменной пневмонии неспецифичны. Пневмония обычно описывается как интерстициальная или бронхопневмония; в большинстве случаев вовлекаются нижние доли; унила-теральная пневмония с более выраженным уплотнением в центре инфильтрата описывается в 75% случаев. Реже описываются лобарные пневмонии. Выраженный плевральный выпот не характерен, но у больных с большим плевральным выпотом, вызванным M. pneumoniae, заболевание протекает тяжелее и дольше по сравнению с пациентами без экссудативного плеврита. Количество лейкоцитов и лейкоцитарная формула обычно в пределах нормы, СОЭ, как правило, повышается.
Количество лейкоцитов и лейкоцитарная формула обычно в пределах нормы, СОЭ, как правило, повышается.
Имеются сообщения о тяжелой и фатальной пневмонии, вызванной M. pneumoniae, как у детей, так и у взрослых [21,23]. Фоновая патология в виде иммунодефицита (особенно гипогаммаглобулинемия), синдром Down, серповидноклеточная гемоглобинопатия, сердечно-легочная патология предрасполагают к повышенной восприимчивости к M. pneumoniae. При гистопатоло-гическом анализе фатальных случаев обнаруживается десквамативная интерстициальная пневмония, иногда сопровождающаяся фокальным альвеолярным поражением и облитерирующим бронхиолитом. У большинства пациентов с тяжелыми легочными проявлениями отмечается поражение ЦНС и гемолиз с холодовыми агглютининами.
Имеются некоторые отличительные признаки и детали, позволяющие дифференцировать микоплаз-менную пневмонию от вирусного или бактериального поражения легочной паренхимы. Типичны пятнистый, односторонний, сегментарный или субсегментарный варианты консолидации, но может быть диффузное, двустороннее интерстициальное поражение.
Типичны пятнистый, односторонний, сегментарный или субсегментарный варианты консолидации, но может быть диффузное, двустороннее интерстициальное поражение.
M. pneumoniae может вызывать ОРЗ, фарингит, синусит, круп и бронхиолит. M. pneumoniae часто выступает в роли триггера приступов бронхиальной астмы у детей [10, 22]. Средний отит, вызванный M. pneumoniae, как правило, ассоциируется с инфекцией нижних дыхательных путей.
У детей M. pneumoniae-инфекция неотличима от ОРВИ, возможна микст-инфекция. У детей, инфицированных M. pneumoniae, могут отсутствовать клинические проявления; возможны ринорея, фарингит, средний отит. Рентген-подтвержденная пневмония обнаруживается у 60%-85% проконтактировавших членов семьи младше 15 лет, клиническое течение легкое. Хотя исследования в США продемонстрировали низкую частоту встречаемости инфекций нижних дыхательных путей, вызванных M. pneumoniae, у детей младше 5 лет в исследованиях, проведенных в Японии, показано более высокая частота встречаемости M. pneumoniae в аналогичных возрастных группах, у которых свистящее дыхание было основным проявлением [18,19].
pneumoniae в аналогичных возрастных группах, у которых свистящее дыхание было основным проявлением [18,19].
Внелегочные поражения
Внелегочные осложнения, ассоциированные с M. pneumoniae, представлены в таблице.
Случайное выделение M. pneumoniae из крови, лик-вора, синовиальной жидкости и из участков кожного поражения (у больных с иммунодефицитом) указывает на диссеминацию микроорганизма. Молекулярная идентификация микроорганизма методом ПЦР подтверждает роль M. pneumoniae в следующих патологических состояниях: энцефалит и поперечный миелит, плевральный выпот и бактериемия. Вовлечение головного мозга в патологический процесс может проявляться тяжелой дистонией и двигательными нарушениями. Неврологические осложнения включают менингоэнцефалит, поперечный миелит, асептический менингит, мозжечковую атаксию, паралич Белла, глухоту, синдром поражения ствола мозга, острый демиелинизирующий энцефалит и синдром Гийена-Барре. Неврологические осложнения возникают на 3-28 дни (в среднем на 10 день) после респираторного заболевания, но могут и предшествовать ему в 20% случаев. Энцефалит, возникающий в течение 5 дней от начала продромальных симптомов, может вызываться прямой инвазией M. pneumoniae в ЦНС; в случае проявления энцефалита в сроки более 7 дней от начала продрормальных признаков более вероятен аутоиммунный механизм. Причиной от 1 до 15%
Неврологические осложнения возникают на 3-28 дни (в среднем на 10 день) после респираторного заболевания, но могут и предшествовать ему в 20% случаев. Энцефалит, возникающий в течение 5 дней от начала продромальных симптомов, может вызываться прямой инвазией M. pneumoniae в ЦНС; в случае проявления энцефалита в сроки более 7 дней от начала продрормальных признаков более вероятен аутоиммунный механизм. Причиной от 1 до 15%
Таблица
Внелегочные заболевания, ассоциированные с Mycoplasma pneumoniae
Заболевание Характеристики
Экзантема/энантема Дискретный макулопапулез Полиформная эритема Синдром Stevens-Johnson Крапивница Кореподобная экзантема Везикулы/буллы Язвенный стоматит Erythema marginatum
Гемолиз Комплемент-зависимый, Coombs-положительный, анти-I антиген, Ig M антитела
Заболевания ЦНС Энцефалит/менингоэнцефалит Поперечный миелит Синдром Guillain-Barm Фокальный энцефалит Полирадикулит Паралич Белла Асимметричный паралич Мозжечковая атаксия Психоз Инфаркт мозга
Артрит Острого/хронического течения Моно-/мигрирующий/полиартрит
Заболевания сердца Перикардит Миокардит Нарушение проводимости Инфаркт миокарда Застойная сердечная недостаточность
Печеночная дисфунция Умеренное повышение печеночных ферментов
Панкреатит Острое воспаление
Заболевания глаз Конъюнктивит Отек диска зрительного нерва Ирит
всех форм энцефалита у детей, судорог, задержки умственного развития, дефицитом лицевой мимики, атаксии является M. pneumoniae.
pneumoniae.
Диагноз устанавливается на основании положительных результатов ПЦР ликвора и мазка из зева или диагностического титра антител. На МРТ определя-
ются фокальные ишемические изменения, вентрикуло-мегалия, диффузный отек или мультифокальное воспалительное поражение белого вещества, совпадающие с демиелинизирующим энцефаломиелитом. Неврологические осложнения встречаются у 20-30% больных.
По современным данным, некоторые внелегочные
заболевания развиваются по инфекционному механизму (т.е. за счет прямого действия микрорганизма), в то время как другие — за счет иммунных механизмов.
Поражения кожи включают различные экзантемы, из них наиболее часто встречаются макулопапулез-ная сыпь, многоформная эритема и синдром StevensJohnson [11].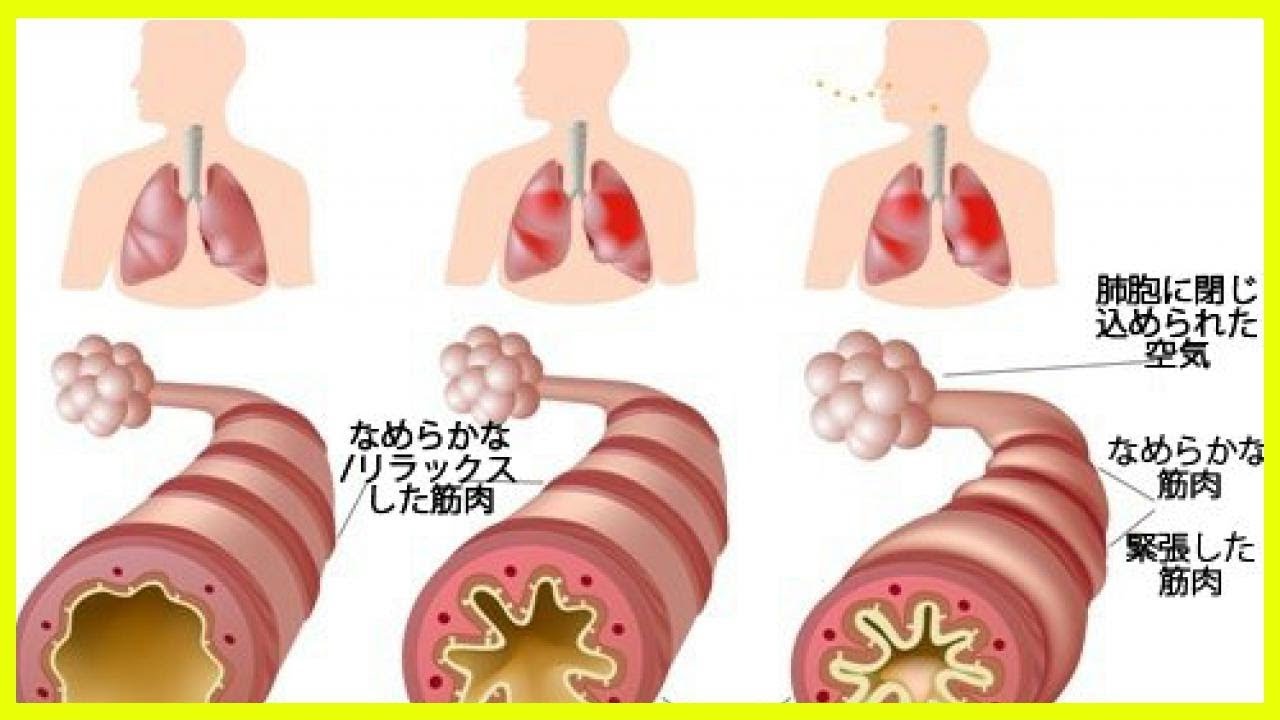 Синдром Stevens-Johnson, ассоциированный с M. pneumoniae, обычно развивается на 3-21 дни после начала проявлений респираторных симптомов, длится менее 14 дней и редко сопровождается серьезными осложнениями.
Синдром Stevens-Johnson, ассоциированный с M. pneumoniae, обычно развивается на 3-21 дни после начала проявлений респираторных симптомов, длится менее 14 дней и редко сопровождается серьезными осложнениями.
Слабовыраженный гемолиз с положительной пробой Кумбса или умеренный ретикулоцитоз появляются на 2-3 неделе от начала заболевания. Тяжелый гемолиз, который ассоциируется высокими титрами холодовых агглютининов (=1:512), тромбоцитопения и коагулопа-тия возникают редко.
Гастроинтестинальные осложнения: гепатит с умеренной активностью, панкреатит и протеин-теряющая гипертрофическая гастропатия, — встречаются редко.
Миокардит, перикардит и ревматоидный синдром
— редкие осложнения микоплазменной инфекции, но аритмии, изменения ST- сегмента и T-зубца, дилатация миокарда с сердечной недостаточностью, — чаще определяется у взрослых, чем у детей. Транзиторный моноартрит был описан у 1% пациентов.
Транзиторный моноартрит был описан у 1% пациентов.
Диагноз
Вследствие отсутствия специфических клинических, эпидемиологических и лабораторных данных точно диагностировать заболевание в начале клинических проявлений не представляется возможным. При наличии пневмонии у школьников и у взрослых молодого возраста, особенно если кашель является ведущим признаком, можно заподозрить микоплазменную этиологию [10,17,22].
Историческая справка и таксономическое положение
В 1942 г. Итону из мокроты больного удалось выделить агент размерами 180-250 нм, который пассировался при инокуляции на куриных эмбрионах. В 1963 г. этот агент был признан микоплазмой (Mycoplasma pneumoniae), которую отнесли к грамотрицательным бактериям. По существующей современной классификации микоплазмы относятся к микроорганизмам класса Mollicutes, который подразделяется на три порядка, 4 семейства, 6 родов и включает в себя около 100 видов.
Наиболее изучено на сегодняшний день семейс-твo Mycoplasmatacae, которое включает 2 рода: род Ureaplasma (3 вида) и род Mycoplasma (около 100 видов). Человек является естественным хозяином по крайней мере 12 видов микоплазм. Все известные подвижные микоплазмы патогенны для человека и животных. M. pneumoniae — возбудитель респираторного микоп-лазмоза, M. incognitis — генерализованного малоисследованного инфекционного процесса. M. fermentas играет определенную роль в развитии СПИДа. M. hominis, U.urealyticum являются возбудителями воспалительных заболеваний урогенитального тракта.
Микоплазмы — группа характерных по морфологии микроорганизмов способных к репликации на бескле-точных средах. Отличительными признаками микоплазм являются отсутствие клеточной стенки и способность персистировать на мембране клеток хозяина.
Все микоплазмы представлены клетками, ограниченными только трехслойной цитоплазматической мембраной. В цитоплазме клеток имеются нуклеотид, диффузно распределенный в виде нитей ДНК, рибосо-
В цитоплазме клеток имеются нуклеотид, диффузно распределенный в виде нитей ДНК, рибосо-
мы и иногда внутрицитоплазматические мембранные структуры. Клетки могут быть полиморфны по форме: глобулы, нитевидные, грушевидные и т.д. Встречаются и более мелкие структуры, приближающиеся по размерам к вирусам. Микоплазмы грамотрицательны, обладают крайне низкой чувствительностью к большинству красителей. Хотя по размеру микоплазмы очень близки к вирусам, они, как и бактерии, содержат обе нуклеиновые кислоты — РНК и ДНК, способны размножаться в условиях искусственных питательных сред.
Интересно отметить, что структура колоний микоплазм чрезвычайно разнообразна и по своей форме может быть представлена многочисленными элементами: мелкими палочками, коккоподобными клетками, шаровидными телами различной оптической плотности, нитевидными и ветвистыми структурами различной длины. Очевидно, благодаря разнообразию форм микоплазмы могут адсорбироваться практически на любых клетках эукариот, размножаться на их поверхности и в межклеточных пространствах. Прикрепляются микоплазмы к мембранам клеток организма хозяина с помощью актиноподобного белка. Способность мембраны микоплазм к тесному слиянию с мембраной клеток хозяина следует рассматривать как фактор патогенности, поскольку нарушается движение ресничек мерцательного эпителия, изменяется не только нормальная физиология клетки, но и архитектоника мембран [6,7].
Прикрепляются микоплазмы к мембранам клеток организма хозяина с помощью актиноподобного белка. Способность мембраны микоплазм к тесному слиянию с мембраной клеток хозяина следует рассматривать как фактор патогенности, поскольку нарушается движение ресничек мерцательного эпителия, изменяется не только нормальная физиология клетки, но и архитектоника мембран [6,7].
Микоплазмы могут длительно размножаться и пер-систировать в макроорганизме, изменять метаболизм инфицированных клеток, нарушать нормальные регуляторные механизмы стволовых, иммунокомпетентных и других клеток. Было доказано, что микоплазмы могут размножаться не только внеклеточно, но и внутрикле-точно. Микоплазмы являются факультативными мембранными паразитами.
Наиболее изученными с точки зрения эксперимента и клиники оказалась M. pneumoniae. В условиях эксперимента этот штамм вызывал инаппарантную инфекцию дыхательного эпителия. Однако появились работы, свидетельствующие о том, что штаммы M. pneumoniae были также обнаружены в цервикальном канале у женщин и их сексуальных партнеров, что свидетельствовало о половом, либо оральном пути передачи инфекции.
Однако появились работы, свидетельствующие о том, что штаммы M. pneumoniae были также обнаружены в цервикальном канале у женщин и их сексуальных партнеров, что свидетельствовало о половом, либо оральном пути передачи инфекции.
Наибольшей степенью патогенности, согласно С.
В. Прозоровскому (1995), обладают штаммы, способные вызывать пневмонии с явлениями перибронхита и продуктивного васкулита. При исследовании секционного материала новорожденных, умерших от микоп-лазменной инфекции, была выявлена генерализованная инфекция с поражением жизненно важных органов: центральной нервной системы, перикарда, почек, легких. В последние годы у трех видов микоплазм (M. pneumoniae, M. gallisepticum, M. laidlawii) выявлена самая высокая гемолитическая активность. Гемолизины обладают повреждающим действием на ткани и клетки реснитчатого эпителия. Прикрепляясь к эритроцитам, микоплазмы вызывают их гемолиз, что может приводить к нарушению микроциркуляции, васкулитам и тромбам.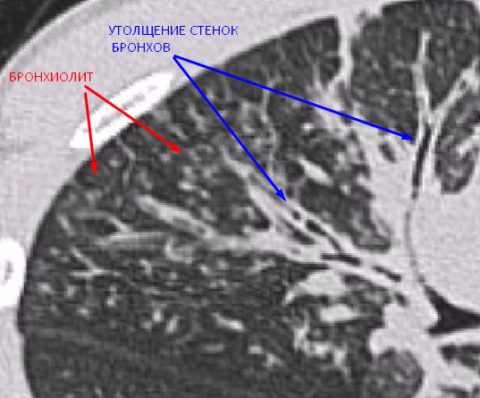 У M. pneumoniae и M. neurolyticum в культуральной жидкости были обнаружены нейротоксины.
У M. pneumoniae и M. neurolyticum в культуральной жидкости были обнаружены нейротоксины.
Антитела (АТ), связываясь с гомологичными тканевыми антигенами, образуют иммунные комплексы, присоединяют компоненты комплемента, обладая действием повреждающим мембраны клеток и вызывая местные и генерализованные иммунные реакции. Прикрепляясь к эритроцитам и вызывая их гемолиз, микоплазма обнажает скрытые антигены, к которым синтезируются
холодовые агглютинины. Агглютинация эритроцитов и гемолиз приводят к нарушениям микроциркуляции, образованию тромбов. В процессе участвуют также и циркулирующие иммунные комплексы способные прикрепляться к стенкам сосудов [7].
Диагностика
Благодаря многочисленным исследованиям, проведенным в течение последних десятилетий, удалось подробно изучить морфологию, антигенную структуру, особенности цикла развития и патогенные свойства внутриклеточных возбудителей. Прорыв в исследованиях хламидийной и микоплазменной инфекций произошел после внедрения в практику методов серологической диагностики, полимеразной цепной реакции (ПЦР) и гибридизации ДНК (дот-гибридизации). К сожалению, на практике эти методы исследования нашли свое применение преимущественно для диагностики урогенитального хламидиоза, передаваемого половым путем. Значительно реже, и в первую очередь по причине своей высокой стоимости, они применялись при бронхолегочной патологии у взрослых и реже — у детей. Прежде всего, недоступностью для широкой практики современных методов диагностики инфекций может быть объяснена сложившаяся ситуация, при которой такие важные вопросы, как реальная распространенность и последствия респираторных внутриклеточных заболеваний у детей, остаются не до конца изученными.
Прорыв в исследованиях хламидийной и микоплазменной инфекций произошел после внедрения в практику методов серологической диагностики, полимеразной цепной реакции (ПЦР) и гибридизации ДНК (дот-гибридизации). К сожалению, на практике эти методы исследования нашли свое применение преимущественно для диагностики урогенитального хламидиоза, передаваемого половым путем. Значительно реже, и в первую очередь по причине своей высокой стоимости, они применялись при бронхолегочной патологии у взрослых и реже — у детей. Прежде всего, недоступностью для широкой практики современных методов диагностики инфекций может быть объяснена сложившаяся ситуация, при которой такие важные вопросы, как реальная распространенность и последствия респираторных внутриклеточных заболеваний у детей, остаются не до конца изученными.
Перечисленные проблемы легли в основу исследования, проводимого Центром клинической фармакологии и фармакотерапии на протяжении 10 последних лет по изучению эпидемиологической структуры респираторных инфекций. За это время существенно менялись взгляды на возбудителей инфекций и постоянно совершенствовались методы лабораторной диагностики.
За это время существенно менялись взгляды на возбудителей инфекций и постоянно совершенствовались методы лабораторной диагностики.
Одной из задач, поставленных в настоящей работе, было определение реальной значимости возбудителей инфекций респираторного тракта, их чувствительности к противомикробным средствам, а также отбор клинических, лабораторных и функциональных методов для диагностики и контроля эффективности лечения инфекции респираторного тракта. Особое значение придавалось определению качества отечественных лабораторных тест-систем, которые появились и начали применяться на практике в последнее десятилетие.
Бактериологические исследования проводились в соответствии с установленными правилами [1-4,20]. Диагностика микоплазменной инфекции выполнялась с помощью реактивов ЗАО “Ниармедик-плюс” для M. pneumoniae (“МикопневмоФлюоскрин”). Культуральный метод диагностики микоплазмоза обеспечивался наборами диагностических сред, выпускаемых отечественными предприятиями. Наиболее полно объединил в себе возможности комплексной диагностики набор питательных сред для диагностики M. pneumoniae и определения чувствительности к антибиотикам, выпускаемый ООО НПО «Иммунотэкс» (Россия). В состав набора входят дифференциально-диагностическая среда для выделения и идентификации микоплазм (M. pneumoniae). Производителем предлагается возможность определения чувствительности микоплазм к достаточно широкому кругу антибактериальных средств: макролиды (эритромицин, азитромицин и кларитроми-цин), тетрациклины (доксициклин) и фторхинолоны (офлоксацин, ципрофлоксацин и левофлоксацин).
Наиболее полно объединил в себе возможности комплексной диагностики набор питательных сред для диагностики M. pneumoniae и определения чувствительности к антибиотикам, выпускаемый ООО НПО «Иммунотэкс» (Россия). В состав набора входят дифференциально-диагностическая среда для выделения и идентификации микоплазм (M. pneumoniae). Производителем предлагается возможность определения чувствительности микоплазм к достаточно широкому кругу антибактериальных средств: макролиды (эритромицин, азитромицин и кларитроми-цин), тетрациклины (доксициклин) и фторхинолоны (офлоксацин, ципрофлоксацин и левофлоксацин).
Результаты исследования еще раз подтвердили необходимость проведения микробиологической диагностики, направленной на выявление возбудителя в местах
колонизации. Оптимальным является исследование мазков из доступных мест (зев, конъюнктива, нос ит.д.) и мокроты с обязательным проведением культурального исследования. При сопоставлении результатов, полученных методом РИФ по выявлению АГ M. pneumoniae, с данными культурального исследования, выполненного с помощью коммерческих наборов НПО «Иммуно-тэкс», выявлено 98% совпадения результатов. Вместе с тем в 20% случаев выделение микоплазм с помощью питательных сред удавалось подтвердить методом РИФ только при изучении не менее 3-х мазков из материала пациента, что оказалось гораздо более трудоемким и затратным, чем культуральное исследование.
При сопоставлении результатов, полученных методом РИФ по выявлению АГ M. pneumoniae, с данными культурального исследования, выполненного с помощью коммерческих наборов НПО «Иммуно-тэкс», выявлено 98% совпадения результатов. Вместе с тем в 20% случаев выделение микоплазм с помощью питательных сред удавалось подтвердить методом РИФ только при изучении не менее 3-х мазков из материала пациента, что оказалось гораздо более трудоемким и затратным, чем культуральное исследование.
Применение современного комплекса клинических и лабораторных методов исследования позволило с высокой степенью достоверности верифицировать этиологию респираторных заболеваний и определить их реальную частоту при обследовании более чем 13000 пациентов. При рецидивирующих формах хронических тонзиллофарингитов (n-668) бактериологический диагноз подтвержден у 425 (63,6%) обследованных. Стрептококковый процесс выявлен у 53% пациентов, а в 24,5% выделены Mycoplasma pneumoniae. В ассоциациях с другими микроорганизмами идентифицированы Staphylococcus aureus и представители Enterobacteriaceae spp. Учитывая наличие определенных проблем с резистентностью к антибактериальным средствам у микоплазм, стафилококков и энтеробактерий, микробиологическая диагностика рассматривается в качестве обязательного элемента обследования при соответствующем диагнозе.
В ассоциациях с другими микроорганизмами идентифицированы Staphylococcus aureus и представители Enterobacteriaceae spp. Учитывая наличие определенных проблем с резистентностью к антибактериальным средствам у микоплазм, стафилококков и энтеробактерий, микробиологическая диагностика рассматривается в качестве обязательного элемента обследования при соответствующем диагнозе.
При синуситах (n-253) выявлены различия в составе выделенных возбудителей у пациентов разных возрастных групп. Результаты свидетельствуют, что основными возбудителями синуситов остаются Streptococcus pneumoniae и H.influenzae. Низкий уровень резистентности этих микроорганизмов к аминопенициллинам позволяет рекомендовать в качестве стартовой терапии синуситов в любом возрасте использование амокси-циллина. У лиц старшего возраста неэффективность при использовании препарата может быть связана с наличием ассоциации микроорганизмов, в том числе с M.pneumoniae.
При инфекционных заболеваниях нижних отделов респираторного тракта в амбулаторной практике (n-1531) структура выделяемых микроорганизмов зависела от установленного диагноза, возраста пациента, а также антибактериального анамнеза, предшествовавшего бактериологическому исследованию. Streptococcus pneumoniae и M. pneumoniae определялись в равных долях практически в 75% всех случаев внебольничной пневмонии (ВП) у взрослых пациентов. Гемофильные палочки в 2-3 раза чаще выделялись из мокроты больных с ХОБЛ и хроническим необструк-тивным бронхитом, но не с ВП. M. pneumoniae в 2-3 раза реже обнаруживалась в мокроте больных с хроническими формами патологии. С возрастом независимо от диагноза увеличивалась доля пневмококков, гемо-фильных палочек и различных представителей семейства Enterobacteriaceae, а роль M. pneumoniae значительно снижалась. Вместе с тем даже у пациентов старше 60 лет микоплазмы занимали существенную долю в общей структуре возбудителей (до 10%), что требует обязательного микробиологического мониторинга, особенно при ХОБЛ.
Streptococcus pneumoniae и M. pneumoniae определялись в равных долях практически в 75% всех случаев внебольничной пневмонии (ВП) у взрослых пациентов. Гемофильные палочки в 2-3 раза чаще выделялись из мокроты больных с ХОБЛ и хроническим необструк-тивным бронхитом, но не с ВП. M. pneumoniae в 2-3 раза реже обнаруживалась в мокроте больных с хроническими формами патологии. С возрастом независимо от диагноза увеличивалась доля пневмококков, гемо-фильных палочек и различных представителей семейства Enterobacteriaceae, а роль M. pneumoniae значительно снижалась. Вместе с тем даже у пациентов старше 60 лет микоплазмы занимали существенную долю в общей структуре возбудителей (до 10%), что требует обязательного микробиологического мониторинга, особенно при ХОБЛ.
Основными возбудителями внебольничных инфекций нижних отделов респираторного тракта у па-
циентов, поступавших в специализированные отделения стационаров г. Ставрополя и Ставропольского края (n-2540), являлись пневмококки и представители Enterobacteriaceae spp. У детей чаще находили M. pneumoniae (до 40%). Важно, что у взрослых общая структура возбудителей мало отличалась в различных ЛПУ г. Ставрополя и Ставропольского края. При пневмониях и ХОБЛ более чем в 15% случаев выделялись респираторные микоплазмы. При осложнениях хронического необструктивного бронхита в каждом десятом случае выявлены гемофильные палочки. Стафилококки чаще обнаруживались в мокроте пациентов с ХОБЛ. С возрастом независимо от диагноза снижается доля M. pneumoniae, но увеличивается число штаммов гемо-фильных палочек, Enterobacteriaceae spp. и Enterococcus faecalis.
Ставрополя и Ставропольского края (n-2540), являлись пневмококки и представители Enterobacteriaceae spp. У детей чаще находили M. pneumoniae (до 40%). Важно, что у взрослых общая структура возбудителей мало отличалась в различных ЛПУ г. Ставрополя и Ставропольского края. При пневмониях и ХОБЛ более чем в 15% случаев выделялись респираторные микоплазмы. При осложнениях хронического необструктивного бронхита в каждом десятом случае выявлены гемофильные палочки. Стафилококки чаще обнаруживались в мокроте пациентов с ХОБЛ. С возрастом независимо от диагноза снижается доля M. pneumoniae, но увеличивается число штаммов гемо-фильных палочек, Enterobacteriaceae spp. и Enterococcus faecalis.
Оценка чувствительности микроорганизмов, выделенных от госпитализированных с внебольничными формами инфекций пациентов, показала низкий уровень их резистентности к противомикробным средствам и идентичность показателей, полученных при изучении возбудителей в амбулаторных условиях.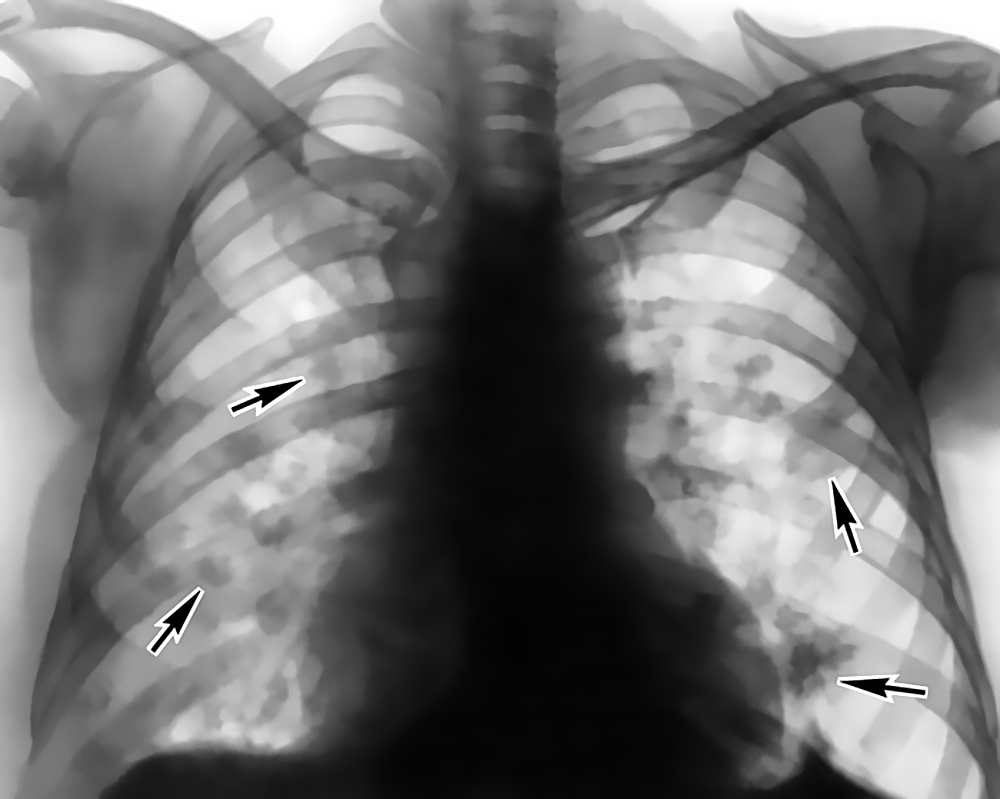
Таким образом, высокая доля M. pneumoniae, а у пациентов с предварительным использованием антибиотика — представителей семейства энтеробактерий с определенным профилем резистентности, делает необходимым обязательное проведение бактериологического исследования мокроты, в том числе с помощью наборов питательных сред для диагностики M. pneumoniae и определения чувствительности к антибиотикам, производства НПО «Иммунотэкс». Это тем более важно для коррекции проводимой терапии у пациентов, которые проходят диагностику из-за неэффективности предварительного применения этиотропных средств. Таких больных не менее трети от общего числа обследованных.
Другие методы диагностики
Наличие холодовых антител к эритроцитам в сыворотке крови у пациентов с атипичной пневмонией было подтверждено за 20 лет до установления M. pneumoniae в качестве этиопатогена [16]. Холодовые агглютинины
Холодовые агглютинины
— это IgM — антитела, направленные против I-антигена эритроцитов человека. Они появляются на 7 — 10 дни от начала симптомов, и их уровень быстро снижается после 2 — 3 недель заболевания. Они активны при низкой температуре тела; их определение проводят при 4°C. Холодовые агглютинины присутствуют в остром периоде заболевания приблизительно у 75% взрослых с микоплазменной пневмонией; титры антител 1:64 и выше высокоспецифичны. Выраженность вовлечения легких в патологический процесс отражается величиной титра антител. Так как тест недостаточно изучен у детей его точность в определении инфекции верхних дыхательных путей, вызванных M. pneumoniae, неизвестна; специфичность низкая, если титр антител <1:64, ряд респираторных патогенов провоцирует умеренное повышение титра холодовых агглютининов. Диагностическая значимость холодовых агглютининов при микоплазменных экстрапульмонарных заболеваниях низкая.
РСК — один из наиболее широко используемых серологических тестов для определения антител к M..jpg) pneumoniae. Показано, что титр антител =1:32 или четырехкратное повышение при РСК обнаруживаются у 90% из 674 пациентов с микоплазменной пневмонией [14]. Этот тест полезен для ретроспективного анализа, т.к. титры антител нарастают после нескольких недель
pneumoniae. Показано, что титр антител =1:32 или четырехкратное повышение при РСК обнаруживаются у 90% из 674 пациентов с микоплазменной пневмонией [14]. Этот тест полезен для ретроспективного анализа, т.к. титры антител нарастают после нескольких недель
от начала заболевания. Нарастание титра антител, выявляемое при РСК, следует интерпретировать с осторожностью у пациентов с нереспираторным заболеванием.
Имеются также диагностические коммерческие системы ИФА для определения антител кМ. pneumoniae. У них такие же ограничения, как и у РСК, и их специфичность не продемонстрирована.
При определении антигена M. pneumoniae используют различные методы: ИФА, ДНК-зонда, ПЦР и др. Метод ПЦР позволяет определять M. pneumoniae в большинстве заболеваний и синдромов, ассоциированных с M. pneumoniae. Чувствительность современных методов определения IgM к M. pneumoniae у детей с внебольничной пневмонией такая же высокая, как и у ПЦР [8,25].
pneumoniae у детей с внебольничной пневмонией такая же высокая, как и у ПЦР [8,25].
Таким образом, наиболее быстрым, доступным и удобным в использовании в условиях бактериологических лабораторий остается метод выявления жизнеспособных форм M. pneumoniae, дающий возможность получать воспроизводимые результаты в течение до 24 часов с определением чувствительности выделенных штаммов к противомикробным средствам.
Лечение внутриклеточных инфекций
Исследования на добровольцах показали облегчение симптомов после терапии антибиотиками, обладающими in vitro активностью против M. pneumoniae. Эритромицин и тетрациклины продемонстрировали клиническую эффективность при инфекциях нижних дыхательных путей, вызванных M. pneumoniae. Исследования, включавшие детей и подростков, показали большую эффективность в случае раннего начала лечения (в первые 3-4 дня) заболевания и у пациентов с более тяжелой пневмонией [10].
Микробиологическая и клиническая эффективность новых макролидов и азалидов такая же, как у эритромицина. У детей рекомендуется: эритромицин (30-40 мг/кг/сутки 4 раза в день), кларитромицин (15 мг/кг/сутки 2 раза в день) или азитромицин (10 мг/кг/ сутки 1 раз в день в первый день и 5 мг/кг/сутки 1 раз в день со 2 по 5-10 дни). Для подростков рекомендуются: эритромицин или тетрациклин (1-2 г/сутки разделенный на 4 приема), кларитромицин (1 г/сутки разделенный на 2 приема) или азитромицин (500 мг 1 раз в день в первый день и по 250 мг 1 раз в сутки в дальнейшем). Новые фторхинолоны (спарфлоксацин, левофлоксацин, моксифлоксацин и гатифлоксацин) активны в отношении M. pneumoniae in vitro.
Антибиотикотерапия респираторного микоплаз-моза имеет важные особенности, что заставляет увеличивать срок терапии. Во-первых, микроорганизм персистирует у большинства пациентов, несмотря на антибиотикотерапию; поэтому контагиозность сохраняется даже после лечения. Во-вторых, так как патоген персистирует, рецидивирующее течение заболевания предполагается у пациентов с повторными проявлениями симптомов. В регионах с широкой распространенностью макролидрезистентных пневмококков эти антибиотики должны осторожно использоваться для монотерапии внебольничной пневмонии.
Во-вторых, так как патоген персистирует, рецидивирующее течение заболевания предполагается у пациентов с повторными проявлениями симптомов. В регионах с широкой распространенностью макролидрезистентных пневмококков эти антибиотики должны осторожно использоваться для монотерапии внебольничной пневмонии.
Антибиотики следует назначать в зависимости от остроты и тяжести инфицирования в течение 14 дней. При наличии инфицированных родителей или сибсов, риск развития обострений заболевания у детей через 13 мес после окончания терапии значительно увеличивается. Последнее обстоятельство делает необходимым в случае выявления инфекции у ребенка обязательное обследование и лечение родителей. Лечение респиратор-
ных заболеваний без учета этиологии приводит лишь к кратковременному эффекту, увеличивает риск развития осложнений и способствует формированию рецидивирующего и хронического течения болезни.
Вопрос о продолжительности антибактериальной терапии респираторного микоплазмоза имеет принципиальное значение в связи с появившимися данными о терапевтической эффективности коротких курсов мак-ролидов (5-10 мг/кг азитромицина в течение 3-5 дней) для лечения острых и осложненных форм инфекционных заболеваний. Такой подход не может быть оправданным в отношении терапии респираторного мико-плазмоза. Наш опыт лечения свидетельствует о том, что в большинстве случаев приходится сталкиваться с обострением хронической инфекции или реинфицированием на фоне постоянного контакта больного с возбудителем. В этих ситуациях целесообразно применение более длительных, то есть 14-дневных курсов лечения с последующим проведением иммунокоррегирующей терапии, в том числе продленным назначением 14-членных макролидов.
Проведенное катамнестическое наблюдение за большой группой больных показало, что у многих из них основной причиной формирования хронического течения заболевания явились неадекватный контроль и недостаточно эффективное лечение заболевания на его ранних этапах, в том числе отсутствие должной диагностики и лечения инфицированных родителей, сиб-сов и окружающих лиц в замкнутых коллективах.
Таким образом, проведение всесторонней диагностики при респираторных заболеваниях, включая бактериологическое исследование с выявлением всех возможных возбудителей, следует признать обязательным на всех этапах оказания медицинской помощи — в поликлиниках, стационарах. Такой подход позволяет накапливать объективную информацию об эпидемиологии респираторных инфекций, а значит повышать эффективность и безопасность проводимой терапии.
Литература
1. Зубков, М.Н. Сбор, транспортировка биологического материала и трактовка результатов микробиологических исследований / М.Н. Зубков // Клин. микробиол. антимикроб. химиотер. 2004.- Т.6, №2.- С. 143-154.
2. Методические указания по определению чувствительности микроорганизмов к антибиотикам методом диффузии в агар с использованием дисков // МЗ СССР М. ; 1983.
; 1983.
3. Об унификации микробиологических методов исследования, применяемых в клинико-диагностических лабораториях лечебно-профилактических учреждений // Приказ №535 МЗ СССР от 22 апреля 1985 г.
4. Определение чувствительности микроорганизмов к антибактериальным препаратам (Методические указания МУК 4.2.1890-04) // Клин. микробиол. антимикроб. химиотер. 2004.- Т. 6, №4.- С. 306-357.
5. Покровский, В.И. Этиологическая диагностика и эти-отропная терапия острых пневмоний / В.И.Покровский,
С.В. Прозоровский, В.В. Малеев // М., 1995.
6. Прозоровский, С.В. Медицинская микоплазмология / С.В. Прозоровский, И.В. Раковская, Ю.В. Вульфович // М., 1995.
7. Раковская, И.В. Микоплазмы и микоплазмозы человека. Руководство для врачей. / И.В.Раковская // М., 1999.
Руководство для врачей. / И.В.Раковская // М., 1999.
8. Раковская, И.В. Лабораторная диагностика микоплазмо-
зов человека / И.В. Раковская, Л.Г. Горина // Клин. лаб. Диагностика. — 1999.- №11.- С. 6-7.
9. Чучалин, А.Г. Внебольничная пневмония у взрослых: практические рекомендации по диагностике, лечению и профилактике / А.Г. Чучалин, А.И. Синопальников, С.В. Яковлев // Инфекции и антимикробная химиотерапия. —
2003.- Т. 5, №4.- С. 99-118.
10. Current Pediatric Diagnosis & Treatment, 17th Edition / Eds by W.W.Hay, M.J.Levin, J.M.Sondheimer, R.R.Deterding // McGraw-Hill Education — Europe, 2005.- 429 p.
11. Dorigo-Zetsma, J.W. Results of molecular detection of Mycoplasma pneumoniae among patients with acute respiratory infection and in their household contacts reveals children as human reservoirs / J. W. Dorigo-Zetsma, B. Wilbrink, H. van der Nat // J Infect Dis — 2001. — Vol.183. — Р. 675.
W. Dorigo-Zetsma, B. Wilbrink, H. van der Nat // J Infect Dis — 2001. — Vol.183. — Р. 675.
12. Feikin, D.R. An outbreak of acute respiratory disease caused by Mycoplasma pneumoniae and adenovirus at a federal service training academy: New implications from an old scenario / D.R. Feikin, J.F. Moroney, D.F. Talkington // Clin Infect Dis
— 1999. — Vol. 29. — Р. 1545.
13. Foy, H.M. Infections caused by Mycoplasma pneumoniae and possible carrier state in different populations of patients / H.M. Foy // Clin Infect Dis — 1993. — Vol. 1. — S 37.
14. Kenny, G.E. Diagnosis of Mycoplasma pneumoniae pneumonia: Sensitivities and specificities of serology with lipid antigen and isolation of the organism on soy peptone medium for identification of infections / G.E. Kenny, G.G. Kaiser, M.K. Cooney, H.M. Foy // J Clin Microbiol — 1990. — Vol.28. — P. 2087.
Cooney, H.M. Foy // J Clin Microbiol — 1990. — Vol.28. — P. 2087.
15. Marc, E. Reduced lung diffusion capacity after Mycoplasma pneumoniae pneumonia / E. Marc, M. Chaussain, F. Moulin // Pediatr Infect Dis J — 2000. — Vol.19. — P. 706-10.
16. Marmion, B.P. Eaton agent—science and scientific acceptance: A historical commentary / B.P Marmion // Clin Infect Dis — 1990. — Vol. 12. — P. 338.
17. Mezarina, K.B. Outbreak of community-acquired pneumonia caused by Mycoplasma pneumoniae / K.B. Mezarina, A. Huffmire, J. Downing // Colorado, 2000. MMWR Morb Mortal Wkly Rep. — 2001. — Vol. 50. — P. 227-30.
18. Nagayama, Y. Clinical observations on lower respiratory tract infections with special reference to serum IgE levels / Y. Nagayama, N. Sakurai // Pediatr Pulmonol — 1991.- Vol.11. — P. 44.
44.
19. Nagayama, Y. Isolation of Mycoplasma pneumoniae from children with lower-respiratory-tract infections / Y. Nagayama, N. Sakurai, K. Yamamoto // J Infect Dis — 1988. — Vol. 157. — P. 911.
20. NCCLS Performance Standards for Antimicrobial Susceptibility Testing. Eleventh Informational Supplement, M100-S11 2001.- 21(1).
21. Prabhu, M.B. Bronchiolitis obliterans and Mycoplasma pneumoniae / M.B. Prabhu, D. Barber, D.W. Cockcroft // Respir Med — 1991. — Vol. 85. — P 535.
22. Schlossberg, D. Differential diagnosis of infections deseases / D.Schlossberg, J.A.Shulman // William & Willkins, 1996.
— 304 p.
23. Shulman, S.T. The unusual severity of mycoplasmal pneumonia in children with sickle-cell disease / S. T. Shulman, J. Bartlett, W.A. Clyde, E.M. Ayoub // N Engl J Med — 1972.
T. Shulman, J. Bartlett, W.A. Clyde, E.M. Ayoub // N Engl J Med — 1972.
— Vol.287. — P. 164.
24. Tay, Y.K. Mycoplasma pneumoniae infection is associated with Stevens-Johnson syndrome, not erythema multiforme (von Hebra) / Y.K. Tay, J.C. Huff, W.L Weston // J Am Acad Dermatol — 1996. — Vol. 35. — P. 757-60.
25. Waris, M.E. Diagnosis of Mycoplasma pneumoniae in children / M.E. Waris, P. Toikka, T. Saarinen // J Clin Microbiol
— 1998. — Vol. 36. — P 3155-61.
Бронхит: острый, обструктивный или хронический? | Здоровая жизнь | Здоровье
Рассказывает врач общей практики, преподаватель московского Медучилища № 13 Владимир Яшин.
Бронхит, как и следует из названия, – это воспаление бронхов. Бронхи, вопреки распространенному мнению, – это отнюдь не горло и не «то, что чуть ниже горла – трубочка такая». Чуть ниже горла – это трахея. Как мы помним из курса анатомии, трахея на подходе к легким раздваивается. «Трубочки» после этой развилки и называются бронхами. Дальше они ветвятся, становятся все мельче и мельче. Самые мелкие «трубочки» – бронхиолы – питают легкие кислородом.
Бронхи, вопреки распространенному мнению, – это отнюдь не горло и не «то, что чуть ниже горла – трубочка такая». Чуть ниже горла – это трахея. Как мы помним из курса анатомии, трахея на подходе к легким раздваивается. «Трубочки» после этой развилки и называются бронхами. Дальше они ветвятся, становятся все мельче и мельче. Самые мелкие «трубочки» – бронхиолы – питают легкие кислородом.
| Мокрота – это хорошо! | |
|---|---|
Показателем того, что ваш бронхит идет на поправку, служит наличие мокроты. Когда кашель сухой, то слизистая оболочка находится в состоянии отека, не производит достаточного количества защитной слизи и гной не отходит. А что такое гной? Это продукт распада наших защитных клеток – лейкоцитов. Они уничтожают бактерии, но сами при этом погибают. Эта масса и есть слизь с гноем. Поэтому когда появляются выделения – мокрота, это хороший знак. Значит, организм борется с инфекцией и человек выздоравливает.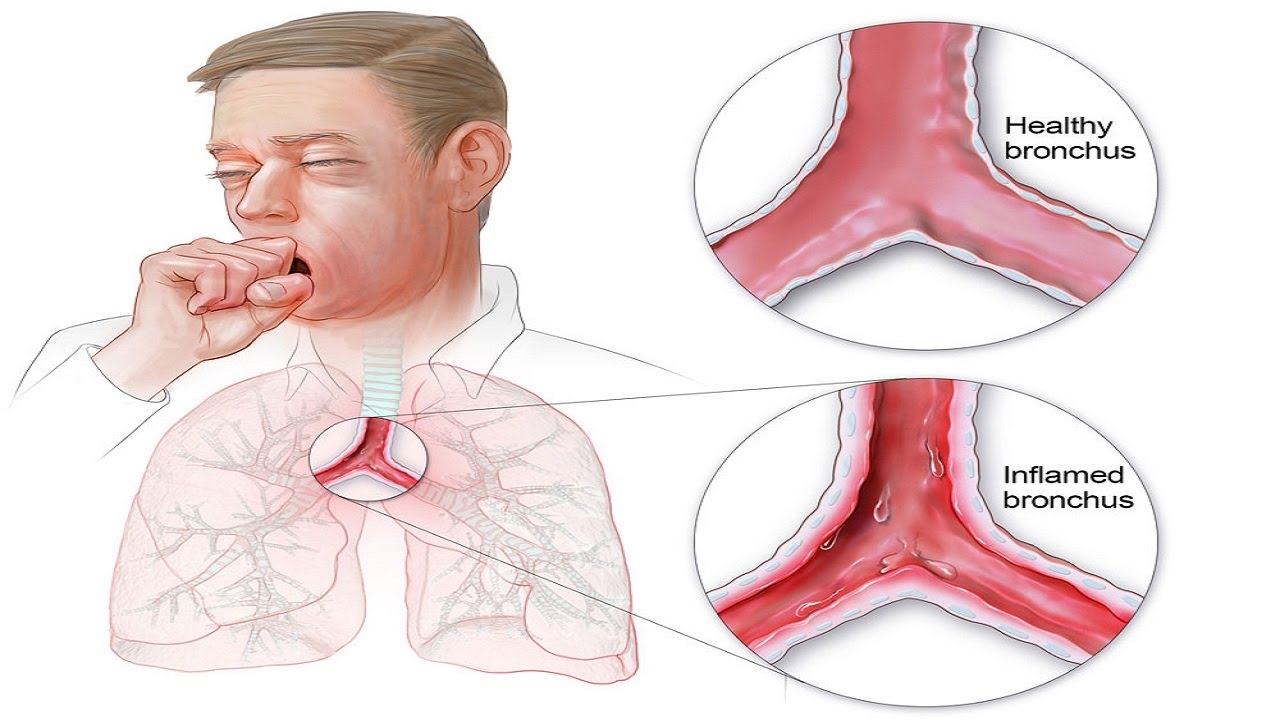 Чтобы усилить образование мокроты, используют препараты группы муколитиков. Чтобы усилить образование мокроты, используют препараты группы муколитиков. |
|
На фоне ОРЗ, ОРВИ и гриппа, как правило, развивается насморк, который может потом «опускаться» – воспаляется носоглотка и «трубочка чуть ниже», то есть трахея. Такое заболевание наиболее распространено, и называется оно трахеит. Бронхит – это явление более опасное, там до легких рукой подать. Как отличить трахеит от бронхита?
Диагностика с сомнением
Даже грамотный врач-терапевт при прослушивании не всегда отличит трахеит от бронхита. Поэтому есть универсальный диагноз: трахеобронхит. Благо оба заболевания лечатся примерно одинаково.
Основной симптом трахеита – сухой, надсадный кашель, который может продолжаться днями и ночами. Признаком бронхита может служить сильный сухой кашель в сочетании с одышкой и возрастающей слабостью. По мере распространения патологического процесса от крупных бронхов к мелким повышается температура тела, кашель становится влажным, отделяемая мокрота приобретает слизисто-гнойный характер.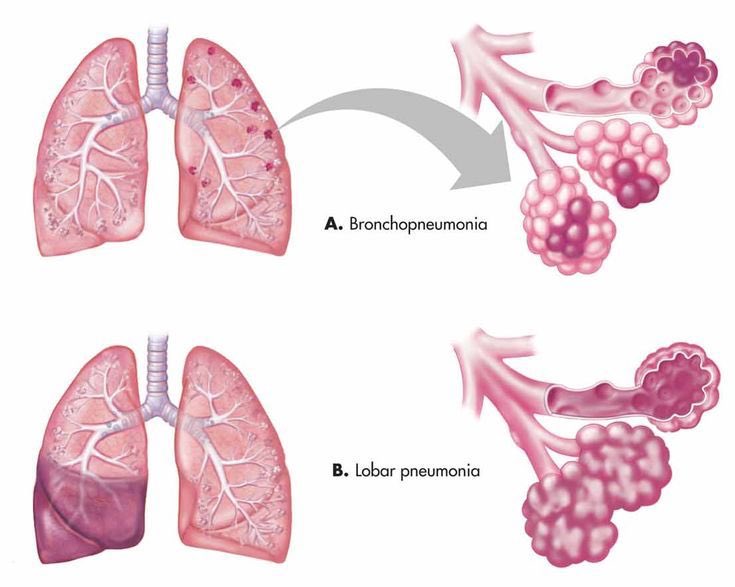 При эффективном лечении эти симптомы обычно исчезают через неделю.
При эффективном лечении эти симптомы обычно исчезают через неделю.
| Интересно! | |
|---|---|
| По данным Американского торакального общества, более чем в 40% случаев бронхит становится следствием насморка. Мужчины болеют бронхитом чаще, чем женщины. Однако ситуация меняется. Причина – пристрастие дам к табаку, одному из провокаторов болезни. | |
Хронь или не хронь?
Хронический бронхит может быть продолжением острого. А может и не быть! Когда врачи говорят о хроническом бронхите, нередко речь идет о самостоятельном заболевании, вызванном длительным раздражением дыхательных путей вредными агентами. Например, табачным дымом, пылью или химическими веществами, содержащимися во вдыхаемом воздухе. Типичными проявлениями хронического бронхита являются постоянный или периодический кашель с мокротой, продолжающийся не менее 3 месяцев в году в течение 2 и более лет подряд, а также прогрессирующая одышка.
Это странное слово «обструкция»
Если вы никогда не слышали словосочетание «обструктивный бронхит», вы счастливчик! Потому что это заболевание не просто докучает – оно всерьез пугает. При нем отекает слизистая бронхов, затрудняется отхождение мокроты, немного поднимается температура (37–37,5° С). Основной симптом, по которому можно узнать обструктивный бронхит, – шумный выдох со свистом. Опасен обструктивный бронхит возможными спазмами, которые полностью перекрывают дыхание. Обструктивный бронхит по «внешнему виду» похож на астму, и без серьезного обследования эти два заболевания могут перепутать даже врачи. Так что, если «засвистели», бегом в поликлинику искать причину.
Источник фото: Shutterstock.com
Лечим и вылечиваем
При остром бронхите больному показаны постельный режим, обильное теплое питье с медом, малиной, липовым цветом, подогретая щелочная минеральная вода. Из процедур, как правило, назначают горчичники на грудину и межлопаточную область, согревающие компрессы, ингаляции с отхаркивающими средствами.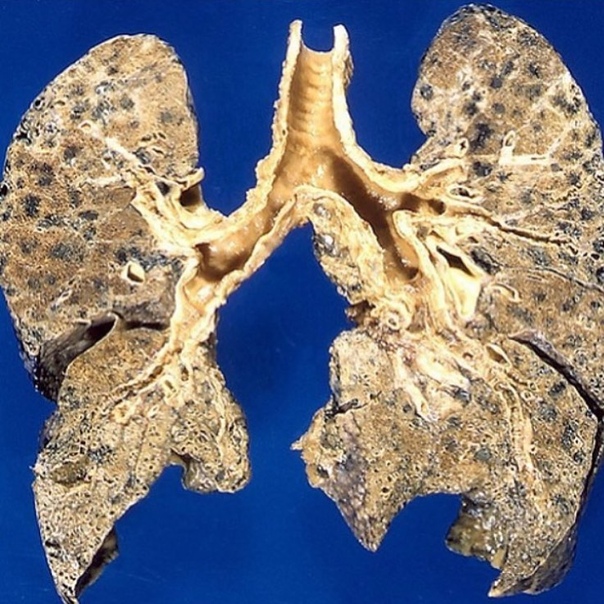 Из препаратов назначают поливитамины, а при выраженном сухом кашле – кодеин с гидрокарбонатом натрия или либексин.
Из препаратов назначают поливитамины, а при выраженном сухом кашле – кодеин с гидрокарбонатом натрия или либексин.
При лечении хронического бронхита в первую очередь следует устранить причины заболевания: отказаться от курения, исключить контакт с вредными примесями в воздухе (в частности, поменять работу, если на производстве есть вредные примеси в воздухе). В отличие от острого бронхита, при хроническом показаны антибиотики и бронхорасширяющие препараты.
Лечение травами
Хороший терапевтический эффект в лечении бронхита дают настои из различных лекарственных растений. Например, при остром и хроническом бронхитах рекомендуется использовать следующий сбор:
— Листья подорожника – 30 г
- Корень солодки – 30 г
- Трава фиалки – 20 г
- Листья мать-и-мачехи – 20 г
Одну столовую ложку сухого измельченного сырья залить стаканом кипятка, настаивать 20–25 минут, процедить и принимать в теплом виде по 1/3 стакана 3 раза в день перед едой.
Обратите внимание, что травяные настои не подходят для маленьких детей, у которых иммунная система еще не до конца сформирована. У них травы могут вызывать аллергическую реакцию, и в таком случае симптомы бронхита только усилятся. Так что по поводу «травяного» лечения детей лучше обращаться к фитотерапевтам.
Кроме того, имейте в виду, что травы максимально эффективно действуют на очищенный организм. Если последний год вы без перерыва травитесь антибиотиками по поводу и без, травы не подействуют.
Смотрите также:
Болезни легких
Бронхит (bronchitis). Бронхитом называется воспаление
слизистой оболочки бронхов, причем
воспалительный процесс в одних случаях
охватывает бронхи всех калибров
(диффузный
бронхит ), в других — только крупные бронхи
(макробронхит ), в третьих — только мелкие бронхи
(микробронхит ).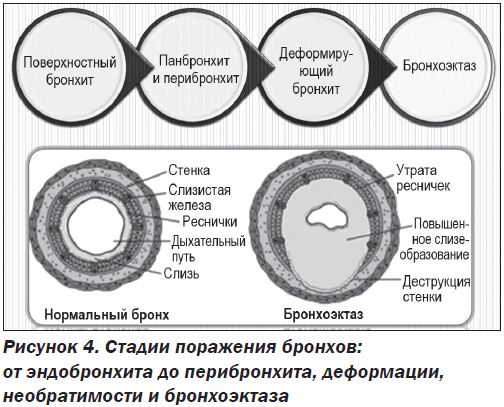
Бронхиты бывают первичные и вторичные . По течению болезни различают — острые и хронические .
Причиной первичного острого бронхита является главным образом простуда в холодное время года, особенно у охотничьих и розыскных собак (купание в холодной воде, длительное пребывание под дождем в холодную погоду). Бронхиты также возникают от непосредственного воздействия на слизистую оболочку бронхов горячего воздуха (при пожарах), дыма, различной пыли (угольной, металлической), ядовитых газов, случайного попадания в трахею лекарственных веществ. Таким образом, бронхит, как таковой, в чистом виде встречается редко. Это заболевание почти всегда сопровождается воспалением трахеи и гортани.
Вторичные
острые бронхиты возникают в результате
распространения воспаления с соседних
участков но продолжению, например, с
гортани и трахеи на крупные бронхи, или
воспаление, начавшееся в крупных бронхах,
переходит на мелкие (микробронхит), или
же воспаление на бронхи может перейти
с легочной ткани. Бронхит возникает и
при чуме.
Бронхит возникает и
при чуме.
Причинами хронического бронхита являются: повторные острые воспаления бронхов, хронические болезни сердца и почек. Наиболее часто хронический бронхит развивается у старых собак и у слабых, худых, сопротивляемость организма которых понижена. Хронический бронхит — частое явление при туберкулезе легких. Хронический бронхит сопровождается осложнениями (бронхоэктазией, ателектазом, эмфиземой), которые, в свою очередь, дают неоднократные рецидивы бронхита.
Клиническая
картина острого бронхита проявляется наличием
общей вялости животного, приступами
дрожи, болезненного сухого кашля,
учащением дыхания. Температура тела в
большинстве случаев повышена, иногда
на 1,5–2°. При аускультации грудной клетки
прослушиваются вначале отдельные и
редкие хрипы, а затем с обеих сторон
грудной клетки, по всему легочному полю,
сухие (поющие, свистящие). В последующие
дни кашель становится менее громким и
болезненным, влажным. Появляется
двустороннее носовое истечение вначале
серозное, слизистое, а затем и
слизисто-гнойное. При диффузных бронхитах
и бронхиолитах дыхание напряженное,
затрудненное; появляется смешанная
одышка. При аускультации прослушиваются
влажные смешанные, крупнопузырчатые
или мелкопузырчатые хрипы. Перкуссия
грудной клетки особых отклонений от
нормы не дает.
При диффузных бронхитах
и бронхиолитах дыхание напряженное,
затрудненное; появляется смешанная
одышка. При аускультации прослушиваются
влажные смешанные, крупнопузырчатые
или мелкопузырчатые хрипы. Перкуссия
грудной клетки особых отклонений от
нормы не дает.
При микробронхите наблюдается значительная одышка, болезненный тяжелый кашель, обильное истечение из ноздрей, иногда пенистое. Выделения из носа засыхают на носу и нередко закрывают носовые ходы. Собака при этом дышит через рот. Температура тела высокая (повышение на 1,5–2°). Эта форма бронхита часто осложняется заболеванием легких (бронхопневмония).
Клиническая
картина хронического бронхита
характеризуется наличием сухого,
болезненного, мучительного кашля, иногда
в виде приступов, а в других случаях
влажного, малоболезненного кашля с
обильным выделением слизисто-гнойного
истечения из носовых отверстии. Во
многих случаях отмечается одышка, а в
некоторых она появляется только при
физической нагрузке. Наибольшая степень
одышки проявляется при бронхитах,
которые вызвали такие осложнения, как
бронхоэктазия, эмфизема, ателектаз. При
перкуссии грудной клетки отклонений
от нормы установить не удается.
Аускультацией устанавливается наличие
разного рода хрипов в легких: сухие
(писки, жужжание, свистящие) или влажные,
крупно- или мелкопузырчатые. Хрипы не
отличаются постоянством и появляются
то в одном месте, то в другом, особенно
после кашля.
Наибольшая степень
одышки проявляется при бронхитах,
которые вызвали такие осложнения, как
бронхоэктазия, эмфизема, ателектаз. При
перкуссии грудной клетки отклонений
от нормы установить не удается.
Аускультацией устанавливается наличие
разного рода хрипов в легких: сухие
(писки, жужжание, свистящие) или влажные,
крупно- или мелкопузырчатые. Хрипы не
отличаются постоянством и появляются
то в одном месте, то в другом, особенно
после кашля.
Течение . Острый бронхит при своевременно принятых мерах заканчивается выздоровлением в течение 2–3 недель. Микро-бронхиты же могут осложняться бронхопневмонией в результате образования ателектических участков, перибронхитом — при переходе воспалительного процесса на перибронхиальную ткань. Перибронхит, в свою очередь, может вызвать образование бронхоэктазии и эмфиземы (при переходе в хроническую форму).
Хронический
бронхит может длиться многие недели,
месяцы и даже годы. Иногда в течении
болезни наблюдаются быстро проходящие
приступы повышения температуры,
сопровождающиеся понижением аппетита,
усилением кашля (в холодное сырое время). В периоды улучшения состояния животного
— температура в пределах нормы, аппетит
нормальный, кашель проявляется редко
(при резких изменениях окружающего
воздуха).
В периоды улучшения состояния животного
— температура в пределах нормы, аппетит
нормальный, кашель проявляется редко
(при резких изменениях окружающего
воздуха).
Диагноз на острый бронхит ставится на основании наличия болезненного кашля, возникшего недавно, вялости животного, хрипов при аускультации легких и отсутствии изменении перкуторного звука.
При постановке диагноза необходимо учитывать возможность возникновения бронхита при инфекционных заболеваниях.
Рентгенологическое исследование в начальный период каких-либо заметных изменений не дает. В более поздние сроки, когда слизистая оболочка бронхов набухает и особенно при наличии скопления эксудата в полости бронхов, отмечается некоторое усиление тени бронхов. Рентгенологическое исследование при бронхите необходимо для исключения туберкулеза легких.
Диагноз
на хронический бронхит ставится на
основании наличия давности заболевания,
периодических улучшений, кашля, одышки,
хрипов в легких при нормальной температуре
тела и неизмененном перкуторном звуке
или при наличии более громкого легочного
звука.
Для подтверждения диагноза необходимо рентгенологическое исследование грудной полости. При хроническом бронхите на экране или пленке обнаруживается усиление тени бронхиального рисунка. Тени бронхов хорошо заметны почти до диафрагмы (особенно при наличии перибронхита). Часто тень диафрагмы при вдохе перемещается назад незначительными толчками или делает мелкие волнообразные движения (нарушение нормальной вентиляции легких). При наличии эмфиземы легочное поле неравномерно или полностью повышенно светлое. На светлом легочном поле резко выступает сосудисто-бронхиальное дерево. Диафрагма в этом случае, в верхней своей части, выпячивается в сторону брюшной полости.
Лечение . При остром бронхите, сопровождающемся сухим болезненным кашлем, назначают наркотические лекарства, успокаивающие кашель: кодеин, морфий, дионин или героин по прописям, указанным в лечении острого ларингита.
При
кашле с наличием вязкого эксудата
применяют отхаркивающие средства для
более легкого освобождения бронхов от
секрета: порошок рвотного корня 0,03, сода
двууглекислая 0,3, сахарный порошок 0,5 —
по одному порошку 2 раза в день в течение
трех дней или настой рвотного корня 0,5
на 150,0, настойки опия 15 капель, сахарного
сиропа 15,0 — давать в зависимости от
величины собаки по столовой или чайной
ложке. Или давать по одному порошку 2
раза в день лекарство по прописи:
пяти-сернистая сурьма 0,2, доверов порошок
0,3, сахар порошком 0,5 — в течение трех
дней.
Или давать по одному порошку 2
раза в день лекарство по прописи:
пяти-сернистая сурьма 0,2, доверов порошок
0,3, сахар порошком 0,5 — в течение трех
дней.
Кроме того, назначают физиотерапевтические процедуры: прогревание грудной клетки лампой соллюкс с последующим теплым укутыванием. Глубокое прогревание легких коротковолновой диатермией или еще лучше УВЧ.
При хроническом бронхите лечебные средства остаются те же, что и при остром. При кашле наркотические отхаркивающие. При кашле, сопровождающемся спазмом гортани, назначают лекарство по прописи: кодеина фосфорнокислого 0,15, терпингидрита 3,0 — смешать, затем разделить на 10 порошков и давать по 3 порошка вдень. Для общего укрепления организма — процедуры физических методов лечения, ультрафиолетовое облучение, внутрь — облученный рыбий жир.
Катаральная
бронхопневмония (pneumonia catarrhalis). Катаральной бронхопневмонией
называется воспаление бронхов и отдельных
участков легкого. Это заболевание
встречается главным образом у щенков,
а нередко и у слабых анемичных, истощенных
взрослых собак, особенно же часто у
старых собак.
Это заболевание
встречается главным образом у щенков,
а нередко и у слабых анемичных, истощенных
взрослых собак, особенно же часто у
старых собак.
Причиной бронхопневмонии является обычно осложнение острого бронхита. Поэтому в большинстве случаев те этиологические факторы, которые вызывают бронхит, могут обусловить развитие катаральной бронхопневмонии. При наличии предрасполагающих моментов воспалительный процесс с бронхов переходит на легочную ткань. Наиболее часто бронхопневмония возникает таким путем при диффузных бронхитах и микробронхитах. Вначале воспалительный процесс охватывает легочную ткань отдельными участками. Позже эти участки сливаются в обширный воспалительный участок и получается бронхопневмония диффузного характера.
Бронхопневмония наблюдается также в результате попадания в легкие пищевых масс (при фарингите) и различных лекарственных веществ (при неправильной даче).
Вторичные
бронхопневмонии возникают при застревании
в глотке инородных тел, при чуме собак.
Клиническая картина . Общее состояние животного угнетенное. Время от времени короткий, глухой кашель. Из носовых отверстий значительное слизисто-гнойное истечение. Дыхание учащенное, поверхностное, затрудненное, с шумом сопения. Аппетит резко понижен или отсутствует совсем. Температура тела часто повышена на 1,5–2°, за время болезни то понижается, то снова повышается.
При перкуссии грудной клетки отмечается наличие отдельных участков притупления, чаще в нижних участках легочного поля. Над участками притупления перкуторный звук более громкий, чем в норме. При слиянии отдельных участков воспаления перкуссией обнаруживают обширный участок притупления с неровной и неясной верхней границей.
При
аускультации в одних участках
прослушивается ослабление или усиление
дыхательных шумов, в других — влажные
хрипы, в третьих — бронхиальное дыхание.
При наличии большого притупленного
участка в нижней части легочного поля
(сливная бронхопневмония) дыхательные
шумы полностью отсутствуют.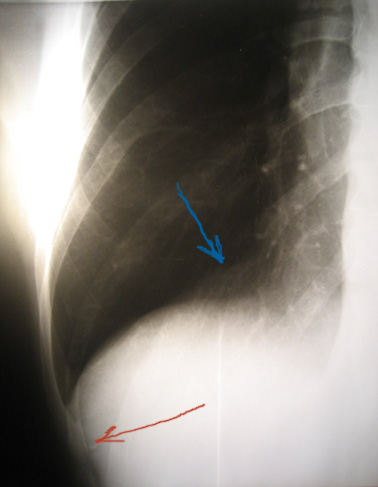 Такие
обширные участки получаются наиболее
часто при аспирационных бронхопневмониях.
В этих случаях быстро развивается
гнойно-некротический распад легочной
ткани, вследствие чего возникают
септические осложнения и гангрена
легкого. Истечения из носа при этих
осложнениях приобретают неприятный,
дурной запах.
Такие
обширные участки получаются наиболее
часто при аспирационных бронхопневмониях.
В этих случаях быстро развивается
гнойно-некротический распад легочной
ткани, вследствие чего возникают
септические осложнения и гангрена
легкого. Истечения из носа при этих
осложнениях приобретают неприятный,
дурной запах.
Течение и исход при катаральной бронхопневмонии различные. В одних случаях через 15–20 дней наступает выздоровление; в других, при неблагоприятных условиях, болезнь заканчивается смертью на 8–10-й день или даже раньше (особенно при аспирационной бронхопневмонии).
Диагноз на бронхопневмонию ставится: при
перкуссии легких на основании наличия
отдельных участков притупления или
одного обширного притупления с неровной
верхней границей; при аускультации
наблюдается пестрая картина дыхательных
шумов — хрипы в одних участках, отсутствие
или ослабление дыхания — в других,
усиленные дыхательные шумы — в третьих.
Необходимо также учитывать наличие
бронхиального дыхания и данные
рентгенологического исследования.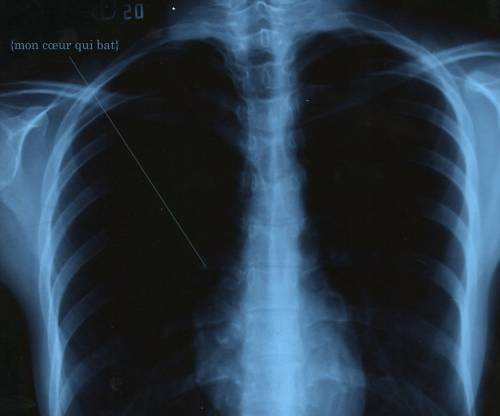
При рентгенологическом исследовании грудной полости обнаруживаются отдельные небольшие, с размытыми краями, места затемнения незначительной плотности на более светлом поле здоровых участков легких. Эти участки затемнения располагаются обычно в нижней половине легочного поля. При слиянии отдельных участков воспаления в более обширный, общий (сливная бронхопневмония) или при аспирационной бронхопневмонии, на рентгеновской картине в нижней части легочного ноля выступает обширное затемнение с нерезкой и неровной верхней границей.
Рис. 12. Участок затемнения небольшой плотности на светлом поле здоровых участков легких при бронхопневмонии
Лечение
мало чем отличается от острого катарального
бронхита. Сухой болезненный кашель
умеряют успокаивающими и отхаркивающими
средствами. Кроме прописей, приведенных
при бронхите, рекомендуется: хлористый
аммоний 6,0, рвотный камень 0,00, экстракт
солодкового корня 3,0, воды дистиллированной
до 200,0-по одной столовой ложке 3–4 раза
в день; или рвотного корня 0,03, соды
двууглекислой, сахарного песка по 0,5 —
на 6 порошков, по 1 порошку 2 раза в день.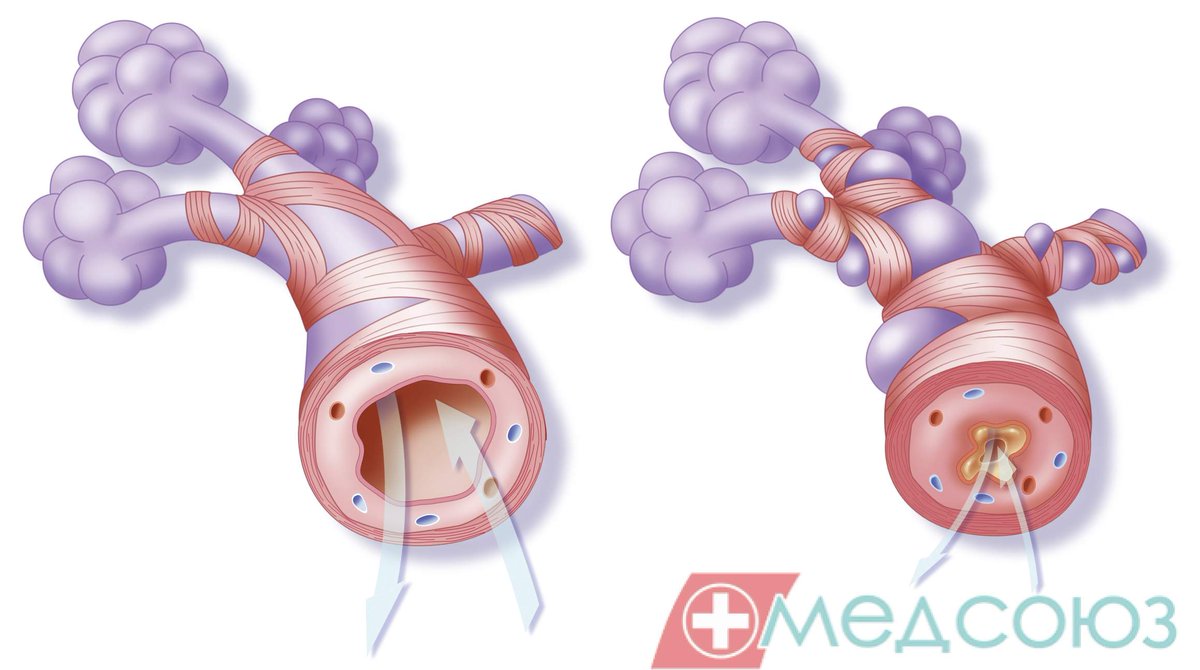 Для борьбы с инфекцией внутримышечно
пенициллин по 50 000 Е. Д. через 3–4 часа.
При наличии сердечной слабости под кожу
камфарное масло 1,0–2,0, кофеин по 0,1–0,3
на 1 мл дистиллированной воды. Из
процедур физического метода лечения —
теплое укутывание и согревающие компрессы
на грудную клетку. Прогревание лампой
соллюкс с теплым укутыванием. Глубокое
прогревание грудной полости аппаратом
УВЧ.
Для борьбы с инфекцией внутримышечно
пенициллин по 50 000 Е. Д. через 3–4 часа.
При наличии сердечной слабости под кожу
камфарное масло 1,0–2,0, кофеин по 0,1–0,3
на 1 мл дистиллированной воды. Из
процедур физического метода лечения —
теплое укутывание и согревающие компрессы
на грудную клетку. Прогревание лампой
соллюкс с теплым укутыванием. Глубокое
прогревание грудной полости аппаратом
УВЧ.
Крупозная пневмония (pneumonia crouposa). Крупозной пневмонией называется острое фибринозное воспаление легких, охватывающее сразу целую долю. Это заболевание у собак встречается очень редко.
Причиной крупозного воспаления легких чаще
всего является простудный фактор.
Поэтому заболевание чаще наблюдается
весной и осенью, редко зимой, главным
образом у охотничьих или служебных
собак (охота в болотах, на местности,
пересеченной ручьями, и т. д.). Крупозная
пневмония может возникнуть и при
чрезмерном утомлении и быстром охлаждении
разгоряченного животного.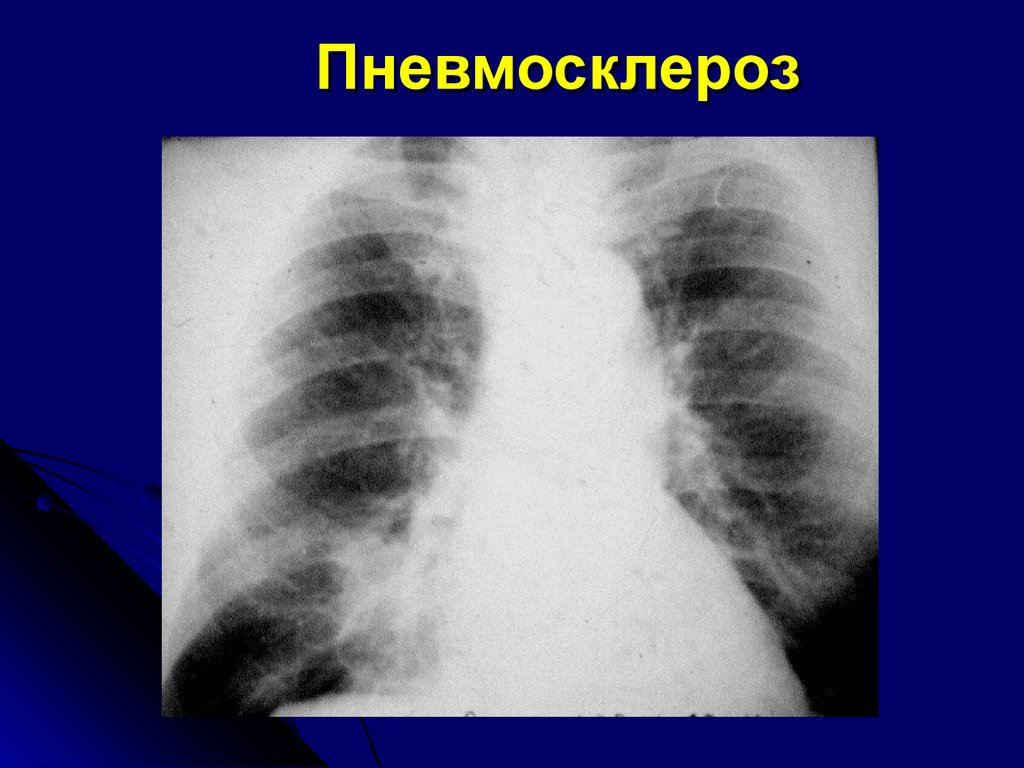 Микрофлора,
имеющаяся в бронхах, при ослаблении
защитных функций организма от указанных
выше причин свободно проникает в легочную
ткань и вызывает острый воспалительный
процесс.
Микрофлора,
имеющаяся в бронхах, при ослаблении
защитных функций организма от указанных
выше причин свободно проникает в легочную
ткань и вызывает острый воспалительный
процесс.
Клиническая картина . В отличие от бронхопневмонии болезнь обычно начинается внезапно. У животного отмечается резко угнетенное состояние, на окружающее больная собака реагирует вяло или совершенно не реагирует; аппетит отсутствует, отмечается сильная жажда. Температура тола высокая, слизистая оболочка глаз гиперемирована. Дыхание напряженное, несколько учащенное. Пульс учащенный, полный.
В дальнейшем проявляется короткий, болезненный, сухой кашель, дыхание становится более частым. При аускультации прослушиваются крепитирующие звуки. При перкуссии перкуторный звук громкий, без притупления. Перкуссия вызывает кашель.
Через
одни-двое суток появляется носовое
истечение сначала слизистое, а затем
ржавого цвета; наблюдается одышка,
глухой, болезненный, влажный кашель. При перкуссии обнаруживают притупление
обычно в нижнем участке легочного поля.
Границы притупления четко определены.
Над участком притупления легочный звук
громкий. При аускультации на участке
притупления дыхание ослаблено или
прослушиваются бронхиальное дыхание
и хрипы. Температура тела с небольшими
колебаниями держится на высоком уровне
(40° и выше).
При перкуссии обнаруживают притупление
обычно в нижнем участке легочного поля.
Границы притупления четко определены.
Над участком притупления легочный звук
громкий. При аускультации на участке
притупления дыхание ослаблено или
прослушиваются бронхиальное дыхание
и хрипы. Температура тела с небольшими
колебаниями держится на высоком уровне
(40° и выше).
При разрешении процесса воспаления (7–8-й день) состояние животного улучшается, появляется аппетит, общее состояние повышается. Температура тела быстро или постепенно снижается. Кашель влажный с мокротой. Носовое истечение снова усиливается, становится слизисто-гнойным, серого цвета. Притупление постепенно уменьшается и перкуторный звук становится снова громким. При аускультации слышны самые разнообразные хрипы, с преобладанием влажных.
Течение . При типичном течении заболевание
обычно заканчивается выздоровлением
через 14–15 дней. Причем первые 6–7 дней
идет нарастание клинических симптомов,
а затем наступает стадия разрешения
процесса.
В некоторых случаях наблюдается более удлиненное течение и выздоровление наступает в более поздние сроки, оставляя глубокие изменения в легких и сердечной мышце.
Крупозная пневмония может дать осложнения в виде плеврита, перикардита, нефрита, которые обычно приводят к гибели животного. Смерть животного может возникнуть и вследствие асфиксии при быстро развивающемся воспалительном процессе и поражении большей части легких. Смертельный исход возможен при этом и от резкого ослабления сердца.
Диагноз . Резкое угнетение и повышение температуры
тела, жажда и напряженное дыхание после
работы собаки (охота на болоте, плавание
в холодной воде осенью или весной) дают
подозрение на воспаление легких. Но
окончательный диагноз можно поставить
спустя один-два дня после заболевания,
когда признаки крупозной пневмонии
выражены более четко. Наличие характерного
истечения из носовых отверстий, хрипы
и притупление в легких, частое дыхание
дают основание поставить диагноз на
крупозное воспаление легких.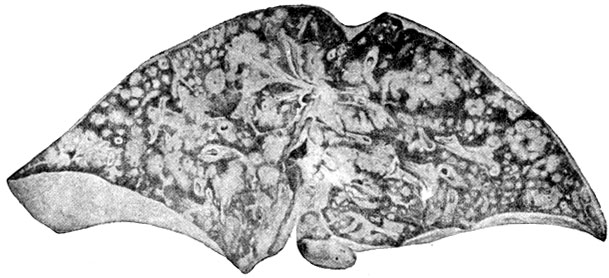
При постановке диагноза необходимо иметь в виду для дифференциации бронхопневмонию, серозный или серозно-фибринозный плеврит.
Бронхопневмонию отличить от крупозной можно по следующим признакам: бронхопневмония начинается обычно медленно вслед за бронхитом, который наблюдался раньше (бронхиолит). Притупление на грудной клетке ограничено небольшими участками, температура тела непостоянна.
При крупозной пневмонии отмечается внезапность заболевания, высокая постоянная температура, быстрое образование обширного участка притупления, ржавого цвета выделения из носа.
При плеврите, в отличие от крупозной пневмонии, отсутствуют истечение, хрипы в легких, отмечается горизонтальное притупление или неровное при серозно-фибринозном плеврите.
Существенную
помощь в постановке диагноза оказывает
рентгеновское исследование. При крупозной
пневмонии обнаруживается в той или иной
плоскости затемнение, обычно занимающее
нижний участок легочного поля
(сердечно-диафрагмальный треугольник
и выше) в зависимости от стадии и плотности
участка воспаления. Верхняя граница
затемнения резко отграничена, чем
отличается от сливной формы бронхопневмонии.
Легочный рисунок над затемненным
участком имеет повышенную прозрачность.
Верхняя граница
затемнения резко отграничена, чем
отличается от сливной формы бронхопневмонии.
Легочный рисунок над затемненным
участком имеет повышенную прозрачность.
Рис. 13. Затемнение в легком при крупозной пневмонии (начальная стадия)
При эксудативном плеврите затемненный участок дает более плотную тень и верхняя граница его имеет строго ровную горизонтальную линию. При дыхательных движениях верхняя граница тени волнообразно колышется. В случае наличия значительного количества жидкости или поражения большой части доли легкого тень сердца сливается с затемненным участком и поэтому не выделяется.
Лечение . Для борьбы с кашлем вначале дают
наркотические (кодеин, дионин, морфин)
как и при бронхите и бронхопневмонии.
Теплое укутывание грудной клетки. Для
поддержания сердечной деятельности —
под кожу камфарное масло 20 % по 1–2
мл. Для ограничения выпота эксудата
вначале и удаления токсических продуктов
в дальнейшем дают мочегонные — диуретин
по 0,2–0,5 2–3 раза в сутки; уксуснокислый
натрий по 0,3–1,0; уротропин по 0,5–1,0.
При появлении притупления — чередование прогревания грудной полости лампой соллюкс и аппаратом УВЧ с последующим теплым укутыванием грудной клетки. При наличии обильного носового истечения, обильных хрипов — отхаркивающие: рвотный корень, хлористый аммоний, терпипгидрат с содой (см. бронхиты).
Для предупреждения септических осложнений — внутримышечный пенициллин по 50 000 Е. Д. 4 раза в день.
Плеврит (plcuriiis). Плевритом называется воспаление
костальной и легочной плевры. Плевриты
бывают первичные и вторичные . По локализации — односторонние и двусторонние . По характеру эксудата — сухие и влажные . Влажные плевриты бывают серозные,
серозно-фибринозные, гнойные и гнилостные . Последние два вида влажного плеврита
обычно являются осложнением серозного
или серозно-фибринозного плеврита, а
также самостоятельно возникают при
проникающей ране грудной полости или
повреждении грудной части пищевода.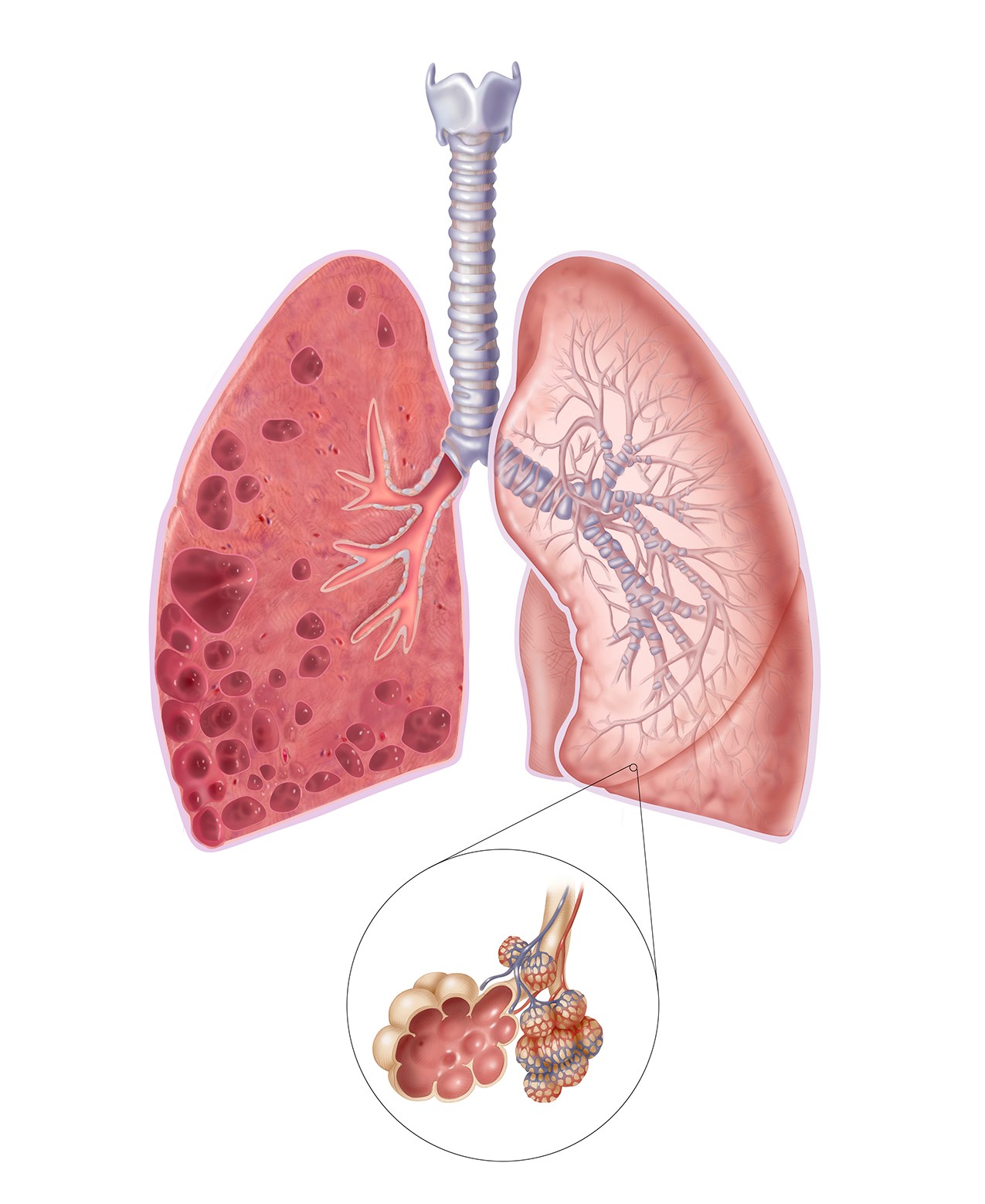
Причиной первичного плеврита является простуда, переохлаждение. Предрасполагающими моментами являются истощение, старость, хронические изнуряющие болезни и др.
Вторичные плевриты встречаются более часто как осложнение от других болезней: при проникающей ране грудной стенки, кариезе ребер и грудной кости, разрыве грудной части пищевода в результате его некроза, крупозной пневмонии, вскрытии абсцессов в грудную полость, при туберкулезе легких.
Клиническая картина . В начале заболевания отмечается вялость животного, понижение аппетита, температура тела повышена. Отмечается слабый болезненный сухой кашель.
При сухом или фибринозном плеврите дыхание поверхностное, прерывистое, учащенное, а иногда редкое, осторожное (вследствие болезненности). Дыхание абдоминального типа.
При
аускультации на пораженных участках
плевры отмечаются шумы трения плевры,
совпадающие с фазами дыхания.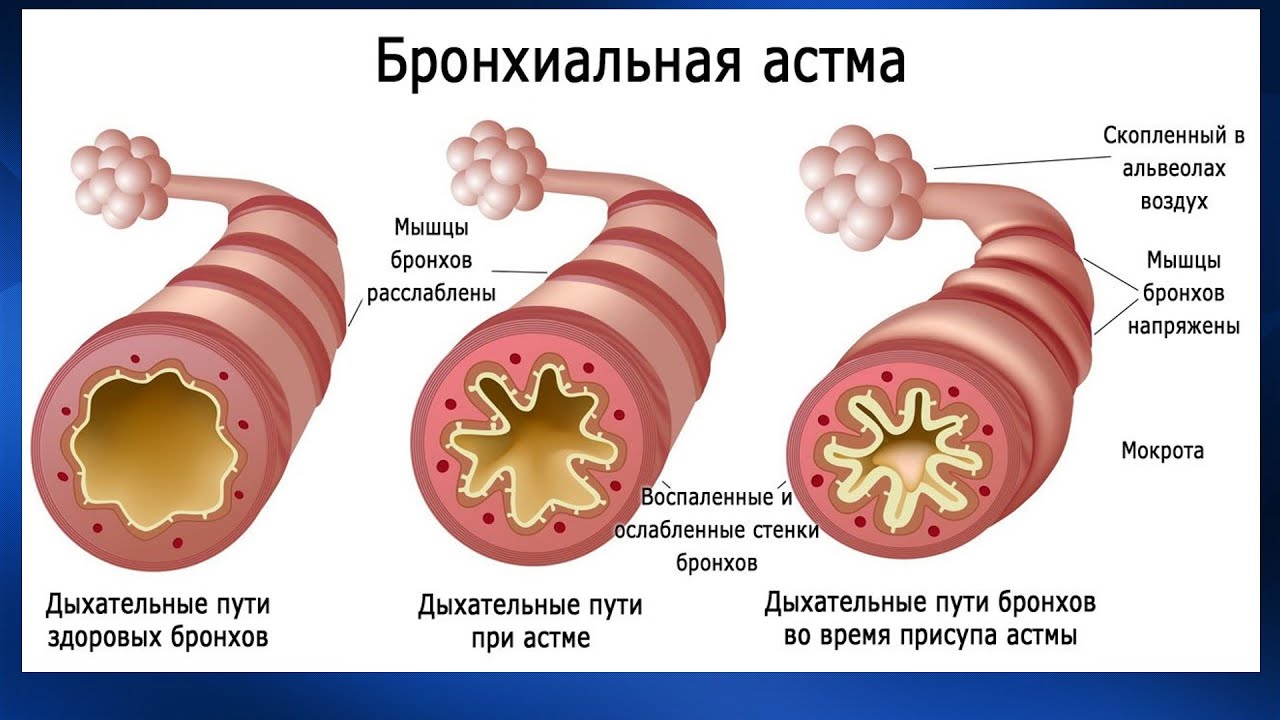 При
перкуссии грудной клетки отмечается
болезненность.
При
перкуссии грудной клетки отмечается
болезненность.
Легкие формы сухого плеврита заканчиваются быстрым выздоровлением животного.
При экссудативном плеврите скопление жидкости в грудной полости постепенно меняет клиническую картину. Дыхание вначале поверхностное, при скоплении эксудата становится менее частым, более глубоким. Болезненность грудной клетки постепенно уменьшается и может совсем исчезнуть. По мере накопления жидкости в дальнейшем дыхание снова учащается и появляется одышка.
При перкуссии обнаруживается, с одной или с обеих сторон грудной полости, в нижней ее части, притупление перкуторного звука или тупой перкуторный звук до определенного уровня с горизонтальной верхней линией. Над притуплением перкуторный звук, близкий к тимианическому.
При
аускультации в области притупления
дыхание прослушивается слабо, а при
большом скоплении эксудата может
отсутствовать совершенно. Над участком
притупления — усиленное или жесткое
везикулярное дыхание.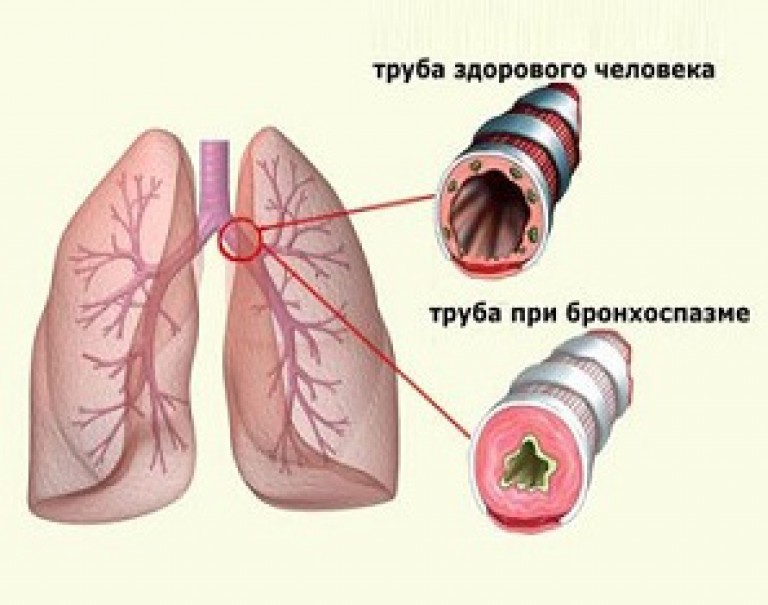
Пульс частый, малой волны и слабого наполнения. Сердечный толчок ослаблен, тоны сердца глухие. Температура тела непостоянная. Временами снижается до нормы, а затем снова повышается. При гнойных и гнилостных плевритах состояние животного весьма тяжелое. Температура тела постоянно высокая.
Течение зависит от вида плеврита, от степени поражения, причины, вызвавшей плеврит, а также от резистентности организма. Первичные плевриты заканчиваются выздоровлением в течение 2–3 недель. Вторичные плевриты могут протекать значительно дольше — месяцами, и выздоровление бывает неполным. Остаются сращение листков плевры, неполное рассасывание эксудата, возникают рецидивы. При большом скоплении эксудата может быть смертельный исход в течение первых двух недель от асфиксии или от слабости сердца. Гнойные и гнилостные плевриты в большинстве случаев заканчиваются смертью в течение первой или второй недели.
Диагноз . Сухой плеврит устанавливается по
наличию болезненности грудной клетки
и шумов трений плевры, связанных с фазами
дыхания, болезненного, осторожного
сухого кашля.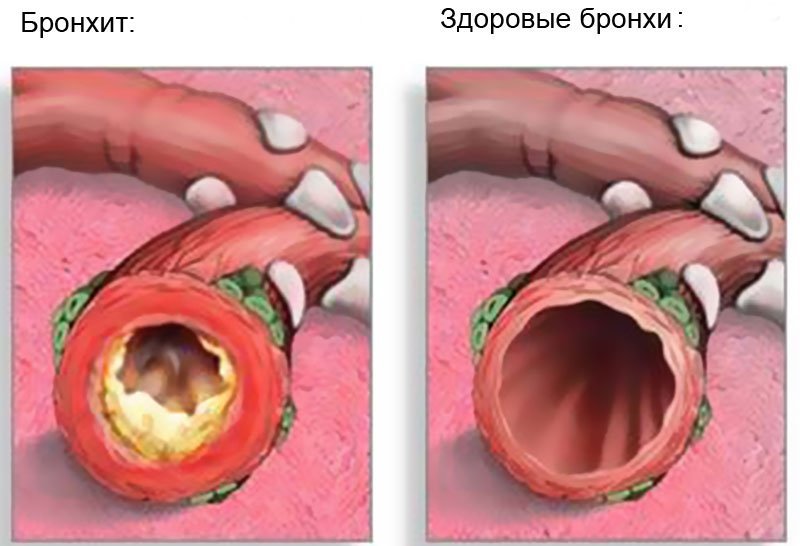
Эксудативный плеврит диагностируется при наличии одно- или двустороннего притупления в нижнем участке грудной клетки, горизонтальной линии верхней его границы, отсутствии хрипов в легких и истечения из носа.
Вид эксудативного плеврита уточняют путем пробного прокола грудной клетки. По характеру эксудата различают: плеврит серозный, серозно-фибринозный или гнойный . На основании прокола исключают гемоторакс и гидроторакс.
Транссудат при гидротораксе содержит 2–3% белка. Транссудат от эксудата можно отличить следующим образом: на 100 мл воды прибавляют 2 капли ледяной уксусной кислоты, затем в этот раствор капают по каплям полученную из грудной полости жидкость. Если это эксудат, то по ходу опускающейся капли будет тянуться беловато-голубоватое облачко (белок). При транссудате этого облака не будет. Жидкость будет прозрачной. К тому же гидроторакс — хроническое заболевание и протекает без температуры.
Для
подтверждения наличия жидкости в грудной
полости до пробного прокола грудной
клетки производят рентгенологическое
исследование.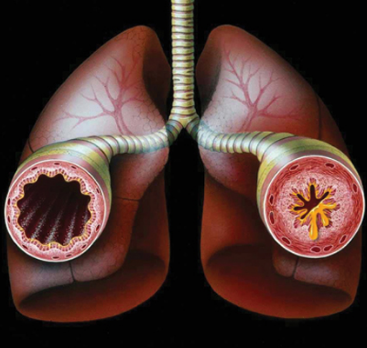 При рентгеноскопии в этом
случае обнаруживается плотное затемнение
в области притупления перкуторного
звука с горизонтальной верхней границей.
При изменении положения туловища
(исследование стоя и сидя) верхняя
граница тени сохраняет горизонтальное
положение.
При рентгеноскопии в этом
случае обнаруживается плотное затемнение
в области притупления перкуторного
звука с горизонтальной верхней границей.
При изменении положения туловища
(исследование стоя и сидя) верхняя
граница тени сохраняет горизонтальное
положение.
Рис. 14. Плотное затемнение при плеврите
Лечение . При сухом плеврите — согревающий компресс, сухое тепло в виде прогревания грудной полости лампой соллюкс, инфраруж с последующим теплым укутыванием. При болезненном кашле — кодеин, дионин (см. ларингит, бронхит).
При экссудативном плеврите — вначале у короткошерстных растирание скипидаром и теплое укутывание грудной клетки, сухое тепло. В дальнейшем давать уротропин по 0,5–1,0, диуретин по 0,1–0,3 внутрь, ограничение воды. Сердечные: кофеин по 0,1–0,3 под кожу, камфарное масло 20 % под кожу (в дозе 1–2 мл). При большом скоплении эксудата — прокол грудной клетки.
При
гнойном плеврите — пенициллин по 50 000
Е. Д. 3–4 раза в день внутримышечно. Прокол
грудной полости. Удаление гнойного
эксудата и введение туда пенициллина
по 100 000 Е. Д.
Д. 3–4 раза в день внутримышечно. Прокол
грудной полости. Удаление гнойного
эксудата и введение туда пенициллина
по 100 000 Е. Д.
Глубокое прогревание грудной полости при помощи аппарата УВЧ.
Эмфизема (emphysema). Эмфизема — это патологическое увеличение объема легких в результате чрезмерного расширения альвеол и потери ими эластичности, вследствие чего они не способны сокращаться при выдохе. У старых собак встречается довольно часто как вторичное заболевание. Эмфизема может быть диффузной или же захватывать отдельные участки легких . По течению подразделяют на острую и хроническую форму.
Причиной
возникновения острой эмфиземы служит
продолжительная напряженная работа
(быстрый бег на охоте, тяжелая езда),
особенно у старых животных; при
переболевании диффузным бронхитом,
микробронхитом в результате тяжелого
длительного кашля. Викарная (компенсаторная)
эмфизема отдельных участков легких
возникает при уменьшении дыхательной
поверхности легких, при сдавливании
части легкого экссудатом (плеврит),
одностороннем пневмотораксе и при
бронхопневмонии, захватывающей
значительные участки легких.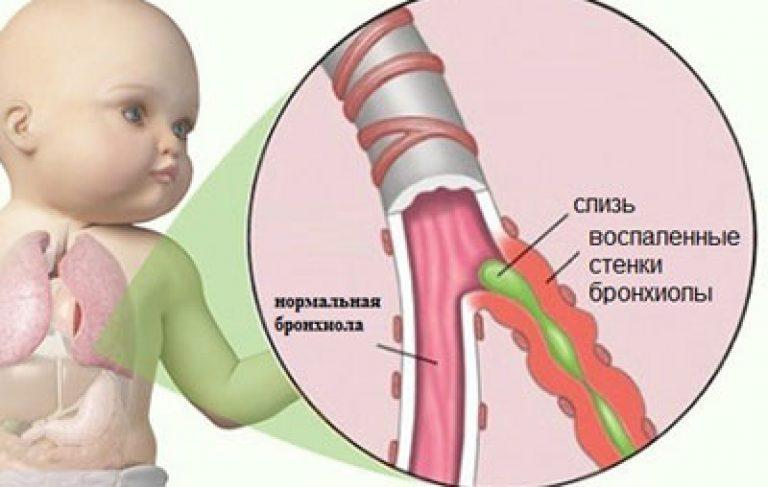
Причины хронической эмфиземы в основном те же, что и острой. Часто повторяющиеся причины, вызывающие острую эмфизему или длительное течение этих заболеваний, в конечном итоге вызывают хроническую альвеолярную эмфизему (хронический диффузный бронхит, перибронхиты, вызывающие стриктуры и скручивания бронхов и т. д.). В результате этого возникшая острая эмфизема постепенно переходит в хроническую.
Клиническая картина эмфиземы выражается учащенным, затрудненным дыханием и смешанной одышкой, припадками сухого кашля, доходящего иногда до приступов рвоты. При перкуссии слышен ясный, громкий звук с тимпаническим оттенком. Задние границы легких расширены. При аускультации прослушиваются сухие хрипы (поющие, свистящие), шумы дыхания ослаблены.
Наряду
с признаками собственно эмфиземы
обнаруживаются и признаки болезни,
вызвавшей эмфизему, в частности
хронического бронхита — сухие и влажные
хрипы в отдельных участках легких;
перибронхита — сухие, свистящие, шипящие,
поющие звуки, в результате образования
стриктур и скручиваний бронхов и сужения
их просвета; признаки пневмоторакса и
плеврита при викарной эмфиземе здорового
легкого.
Признаки хронической эмфиземы в основном те же, но необходимо указать, что хроническая альвеолярная эмфизема развивается постепенно и вначале признаки ее выступают слабо. У заболевшей собаки наблюдается быстрая утомляемость и слегка затрудненное дыхание при работе. Отмечается некоторое удлинение выдоха и большее участие брюшного пресса в эту фазу дыхания. По мере развития болезни эти признаки все более усиливаются. Одышка становится более выраженной, особенно выдыхательная, с более активным участком брюшных мышц. Выдох становится двойным: первый — короткий и резкий (активная работа выдыхательных мышц грудной клетки), второй — продолжительный, совпадающий с энергичным, более длительным сокращением брюшных мышц.
В результате увеличения объема легких грудная клетка может принять бочкообразную форму. Границы легких становятся увеличенными назад. Появляется глухой, слабый кашель.
Течение острой эмфиземы легких сравнительно
непродолжительное, при условии
своевременного устранения причины,
вызвавшей эмфизему, и излечения основного
заболевания.
Течение хронической эмфиземы, как правило, продолжительное. Она может продолжаться многие месяцы и годы. При этом периодически наступает улучшение. Не резко выраженная хроническая эмфизема при соответствующем лечении и надлежащих условиях ухода и кормления может не дать дальнейшего ухудшения состояния животного. При наличии же значительно выраженной эмфиземы легких болезнь постепенно утяжеляется в силу того, что возникшая эмфизема постоянно способствует развитию бронхита, который, в свою очередь, поддерживает и усиливает эмфизему. Поэтому хроническая эмфизема тянется до конца жизни животного, так как органические изменения в легких уже являются необратимыми.
Диагноз на острую альвеолярную эмфизему
становится при наличии одышки, которая
появилась вскоре после неоднократной
тяжелой работы или многократно
повторяющегося быстрого бега; данных
перкуссии, которая дает увеличение
задней границы легких и повышенный
легочный звук; данных аускультации, при
которой обнаруживаются сухие, поющие
звуки, а при наличии бронхита — и влажные
хрипы.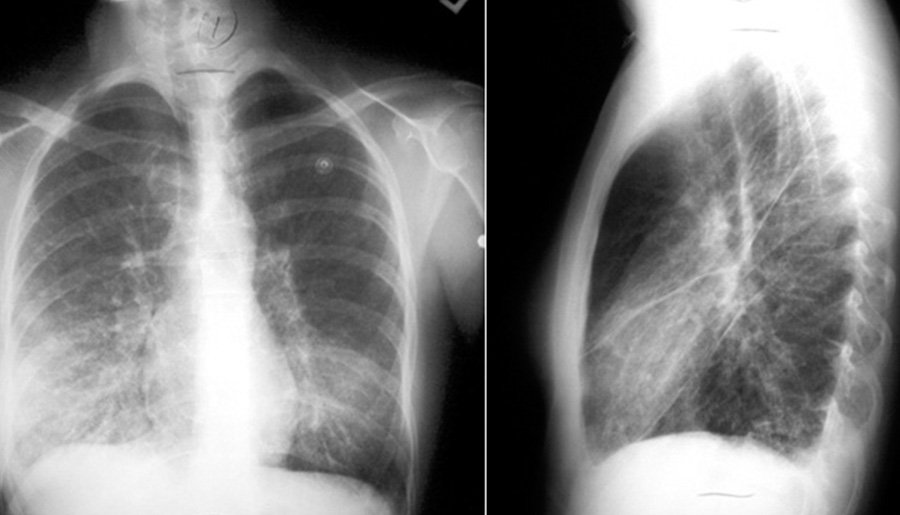
Диагноз на викарную эмфизему, возникающую при ателектазе, бронхопневмонии, экссудативном плеврите, становится на основании клинической картины, перкуссии и аускультации. При этих заболеваниях компенсаторная эмфизема имеет второстепенное значение и при излечении основного заболевания обнаруженная эмфизема здорового участка легкого исчезает бесследно.
Хроническая альвеолярная эмфизема легких диагностируется по следующим признакам: в анамнезе имеются данные о постепенном нарастании одышки, переболевании бронхитом или катаральной бронхопневмонией. При клиническом обследовании отмечается смешанная одышка с преобладанием экспираторной. Резкое усиление одышки при беге. Перкуссия грудной полости дает громкий, тимпанический звук. Границы легких увеличены. При аускультации прослушиваются сухие или при наличии бронхита — влажные или смешанные хрипы. Температура тела обычно в пределах нормы.
Внешняя
картина эмфиземы сходна с другими
заболеваниями легких, такими, как
пневмоторакс (спонтанный), эксудативный
плеврит, диафрагмальная грыжа с выпадением
части желудка и значительного количества
петель кишечника.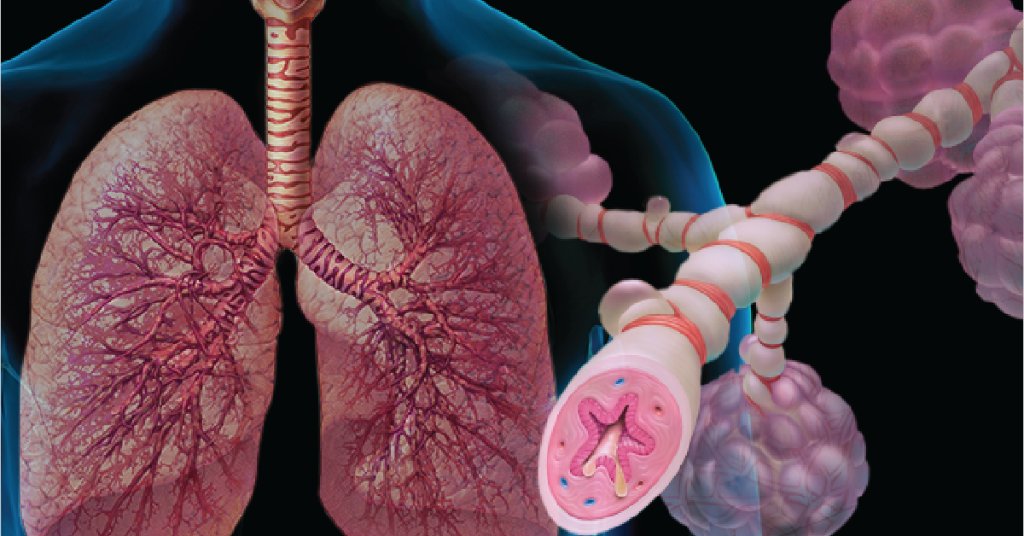
При дифференциации этих заболеваний исходят из того, что спонтанный (внутренний) пневмоторакс протекает обычно без температуры. При перкуссии отмечают повышенный коробочный звук в верхней части грудной клетки и притупленный — в нижних участках. При аускультации в верхней части дыхание совершенно отсутствует, а в нижней — ослаблено.
Эксудативный плеврит при перкуссии может дать сходные с пневмотораксом данные. При аускультации в верхних участках легких дыхательные шумы усилены, а в нижних могут полностью отсутствовать.
Обширная диафрагмальная грыжа обычно протекает без повышения общей температуры тела и в покое дает не особенно резко выраженную одышку. Перкуссия может дать незначительное притупление в нижних участках. При аускультации заметных изменений шумов дыхания не наблюдается.
Быстрый
дифференциальный диагноз устанавливают
рентгенологическим исследованием.
Острая альвеолярная эмфизема легких
характеризуется значительным просветлением
легочного поля (при диффузной эмфиземе)
или отдельных его участков.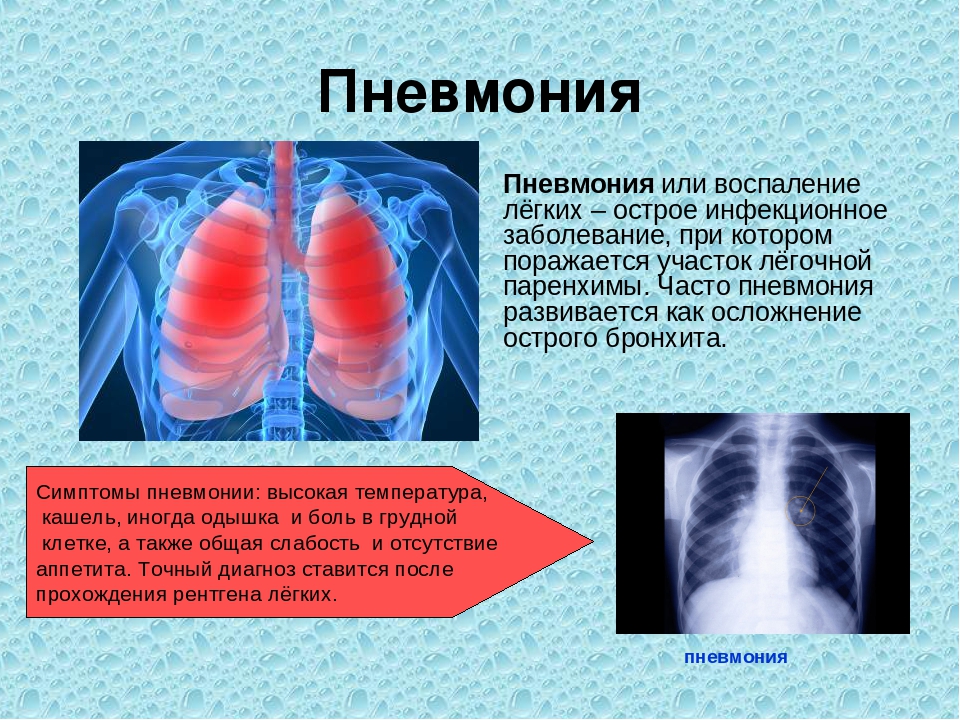
Хроническая альвеолярная эмфизема дает также картину повышенной воздушности легких, на фоне которого сосудисто-бронхиальный рисунок выделяется довольно резко и разветвления гилюсного рисунка просматриваются до самой линии диафрагмы.
При пневмотораксе в верхней части легочного поля имеется той или иной ширины светлая полоса, идущая вдоль позвоночника. Нижняя граница этого участка дугообразная. Остальное легочное поле более темное, на фоне которого просматривается сгущенный (в отжатом вниз легком) сосудисто-бронхиальный рисунок.
Эксудативный плеврит выявляется резким затемненным участком в нижней части легочного поля с горизонтальной верхней линией и с более светлым легочным полем над затемненным участком (см. плеврит).
Диафрагмальная
грыжа рентгенологически характеризуется
наличием в нижней части легочного поля
не особенно плотного (в отличие от
пневмонии и эксудативного плеврита)
затемнения с неравной верхней границей. Дача сернокислого бария внутрь дает
окончательное решение о диафрагмальной
грыже.
Дача сернокислого бария внутрь дает
окончательное решение о диафрагмальной
грыже.
Лечение . При острой эмфиземе, возникшей в результате перенапряжения и не связанной с другими заболеваниями легких, рекомендуются подкожные инъекции атропина в дозе 0,002–0,005; или эфедрин 0,02, сахара 0,3 — по 3 порошка в день внутрь и течение 3–4 дней; или платифилин 0,02, сахара 0,3 — по 3 порошка в день в течение 4 дней. Для поддержания сердечной деятельности под кожу камфарное масло в дозе 1–2 мл.
Викарная острая эмфизема обычно исчезает в процессе выздоровления от основной болезни, поэтому в этих случаях лечат основное заболевание — микробронхит, бронхиолит, катаральное воспаление легких и др.
Хроническая эмфизема практически неизлечима. Поэтому лечебные мероприятия в этом случае должны быть направлены на прекращение дальнейшего развития болезни и облегчение состояния животного.
Для
расслабления гладкой мускулатуры
бронхов дают атропин, эфедрин или
платифилин как и при острой эмфиземе. Если при даче указанных спазмолитических
средств в течение нескольких дней
наступает улучшение, необходимо дать
отхаркивающие для удаления секрета из
бронхов (см. бронхит, бронхопневмония).
При наличии приступов кашля —
наркотические.
Если при даче указанных спазмолитических
средств в течение нескольких дней
наступает улучшение, необходимо дать
отхаркивающие для удаления секрета из
бронхов (см. бронхит, бронхопневмония).
При наличии приступов кашля —
наркотические.
Кроме того, требуется производить прогревание грудной клетки лампой соллюкс или инфраруж с последующим теплым укутыванием в холодное время года; глубокое прогревание грудной полости аппаратом УВЧ.
(PDF) Рентгенологические картины грудной клетки позволяют прогнозировать продолжительность искусственной вентиляции легких у детей с RSV-инфекцией
, проведенной в специализированном специализированном центре, куда большинство из
пациентов, участвовавших в исследовании, которым требовался аппарат искусственной вентиляции легких
, были переведены извне
обращающиеся к больницам на уровне общины, где (1) либо рентгенограммы грудной клетки
до интубации не были отправлены в наше учреждение
как часть записей, и / или (2) значительному количеству этих пациентов
потребовалась неотложная помощь интубация дыхательных путей —
, основанная на клинической картине, при которой не хватило
времени для проведения прединтубационной рентгенографии грудной клетки —
график. Несмотря на то, что последняя модель в этом исследовании является значимой
Несмотря на то, что последняя модель в этом исследовании является значимой
, логистическая регрессия требует большего размера выборки
, чем обычная регрессия наименьших квадратов (линейная) для правильного вывода
. Возможно, небольшой размер выборки в нашем исследовании
повлиял на прогнозное моделирование. Это исследование также было ограничено
по своему объему, чтобы выяснить, повлияет ли другой метод вентиляции
или бактериальная коинфекция
на тип рентгенологического исследования грудной клетки у
этих пациентов.
Заключение
Рентгенологические картины грудной клетки на 1-й и 2-й день после интубации
могут помочь идентифицировать детей, которым потребуется длительная искусственная вентиляция легких
более 8 дней.
Знание этих радиологических паттернов на ранней стадии
течения болезни может помочь врачу
у постели больного направить семьи и персонал PICU к
, чтобы определить детей, у которых может быть длительная длительность искусственной вентиляции легких
.
Ссылки
1. Leader S, Kohlhase K (2003) Последние тенденции развития тяжелого респираторного вируса
синцитиального вируса (RSV) среди младенцев в США, 1997–2000 гг. J Pediatr
143: S127 – S132
2. Shay DK , Holman RC, Newman RD и др. (1999) Бронхиолит —
связанных госпитализаций среди детей в США, 1980–1996 гг.
JAMA 282: 1440–1446
3. Шей Д.К., Холман Р.К., Рузвельт Г.Е. и др. (2001) Бронхиолит
Смертность, связанная с, и оценки респираторно-синцитиального вируса
смертей среди детей в США, 1979–1997 гг.J Infect Dis
183: 16–22
4. Франкель Л.Р., Льюистон Нью-Джерси, Смит Д.В. и др. (1986) Клинические наблюдения
механической вентиляции легких при дыхательной недостаточности при бронхиолите
. Pediatr Pulmonol 2: 307–311
5. Van Steensel-Moll HA, Van der Voort E, Bos AP et al (1989)
Респираторно-синцитиальные вирусные инфекции у детей, госпитализированных в отделение интенсивной терапии
. Pediatrie 44: 583–588
Pediatrie 44: 583–588
6. Outwater KM, Crone RK (1984) Управление дыхательной недостаточностью
у младенцев с острым вирусным бронхиолитом.Am J Dis Child
138: 1071–1075
7. Tissing WJ, van Steensel-Moll HA, Offringa M (1993) Факторы риска
механической вентиляции при респираторно-синцитиальном вирусе
инфекции. Eur J Pediatr 152: 125–127
8. Stretton M, Ajizian SJ, Mitchell I et al (1992) Интенсивная терапия
Курс и исходы пациентов, инфицированных респираторным синцитиальным вирусом
. Pediatr Pulmonol 13: 143–150
9. Kneyber MC, Brandenburg AH, de Groot R et al (1998) Факторы риска
для респираторно-синцитиального вируса апноэ.Eur J
Pediatr 157: 331–335
10. Buckingham SC, Quasney MW, Bush AJ et al (2001) Респираторные
Синцитиальные вирусные инфекции в педиатрическом отделении интенсивной терапии:
клинические характеристики и факторы риска неблагоприятных исходов .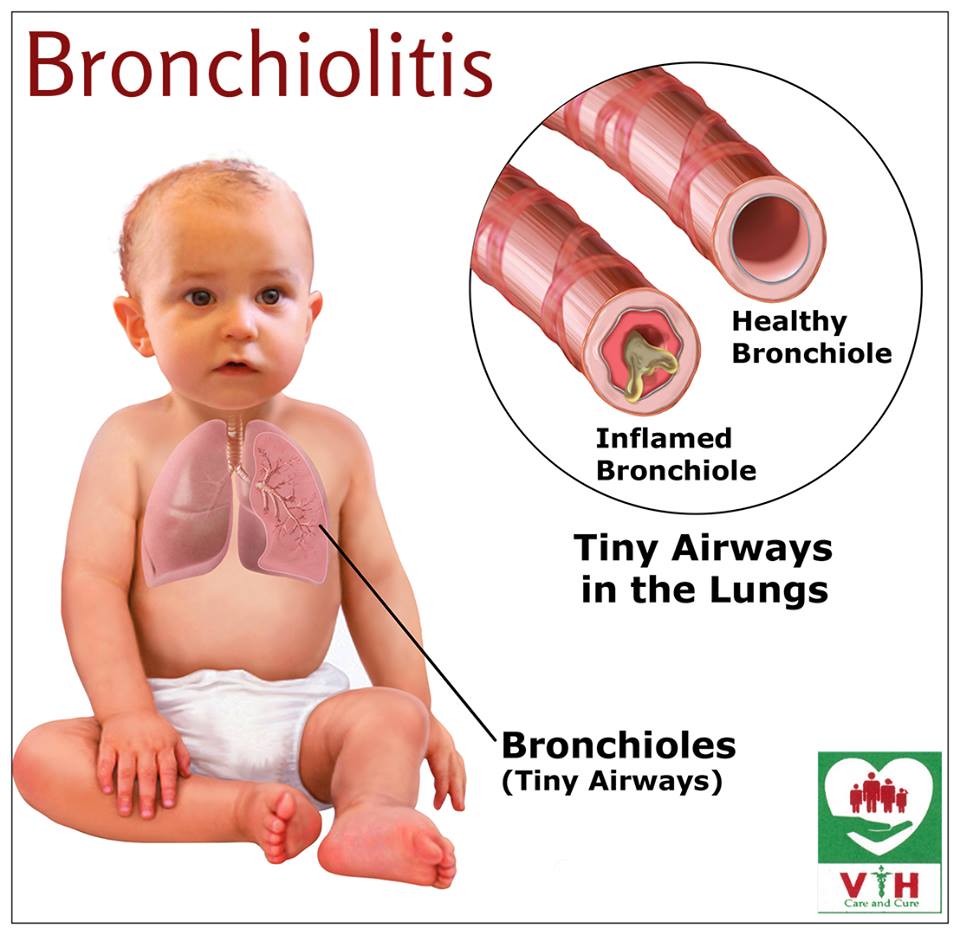
Pediatr Crit Care Med 2: 318–323
11. Leclerc F, Scalfaro P, Noizet O et al (2001) Механическая вентиляция
Поддержка младенцев с респираторно-синцитиальной вирусной инфекцией.
Pediatr Crit Care Med 2: 197–204
12.Martinello RA, Chen MD, Weibel C et al (2002) Корреляция
между генотипом респираторно-синцитиального вируса и тяжестью
болезни. J Infect Dis 186: 839–842
13. Chan PW, Lok FY, Khatijah SB (2002) Факторы риска
гипоксемии и дыхательной недостаточности при респираторно-синцитиальном вирусе
бронхиолит. Юго-Восточная Азия J Trop Med Public Health 33: 806–
810
14. Прайс Д., Шонфельд Т., Амир Дж; Израильский респираторно-синцитиальный вирус
Группа мониторинга(2003) Поступление в отделение интенсивной терапии для
Респираторно-синцитиальный вирусный бронхиолит: национальное обследование до применения паливизумаба
.Pediatrics 112: 548–552
15. Eisenhut M, Thorburn K, Ahmed T (2004) Уровни трансаминаз у
детей с респираторно-синцитиальным вирусным бронхиолитом на ИВЛ.
Intensive Care Med 30: 931–934
16. Purcell K, Fergie J (2004) Driscoll Children’s Hospital респираторный
База данных синцитиального вируса: факторы риска, лечение и больница
Курсу 3308 младенцев и детей раннего возраста, с 1991 по 2002. Pediatr
Infect Dis J 23: 418–423
17.Симпсон В., Хакинг П.М., Суд С.Д. и др. (1974) Радиологические результаты
при респираторно-синцитиальной вирусной инфекции у детей. II. Корреляция
радиологических категорий с клиническими и вирусологическими данными
. Pediatr Radiol 2: 155–160
18. Wilkesmann A, Ammann RA, Schildgen O et al; RSV Ped
Study Group (2007) Госпитализированные дети с респираторной инфекцией
синцитиального вируса и нервно-мышечными нарушениями сталкиваются с
повышенным риском осложненного течения.Pediatr Infect Dis J
26: 485–491
19. Eriksson J, Nordshus T, Carlsen KH et al (1986) Радиологические
находки у детей с респираторно-синцитиальной вирусной инфекцией:
взаимосвязь с клиническими и бактериологическими данными. Pediatr Radiol
Pediatr Radiol
16: 120–122
20. Фриис Б., Эйкен М., Хорнслет А. и др. (1990) Рентген грудной клетки
появления при пневмонии и бронхиолите. Корреляция с вирусологическим диагнозом
и данными секреторных бактерий.Acta
Paediatr Scand 79: 219–225
21. Ньюман Б., Юнис Э. (1995) Лобарная эмфизема, связанная с
респираторно-синцитиальной вирусной пневмонией. Pediatr Radiol 25: 646–648
22. Kern S, Uhl M, Berner R et al (2001) Респираторно-синцитиальный вирус
Инфекция нижних дыхательных путей: результаты радиологического исследования у
108 детей. Eur Radiol 11: 2581–2584
23. Фарах М.М., Паджетт Л.Pediatr Emerg Care 18: 333–336
24. Tasker RC, Gordon I, Kiff K (2000) Временной ход тяжелой
респираторно-синцитиальной вирусной инфекции у
младенцев с механической вентиляцией легких. Acta Paediatr 89: 938–941
25. Вилсон Д.Ф., Ландриган С.П., Хорн С.Д. и др. (2003) Осложнения у
младенцев, госпитализированных по поводу бронхиолита или респираторно-синцитиального вируса
пневмония. J Pediatr 143 (5 Suppl): S142 – S149
J Pediatr 143 (5 Suppl): S142 – S149
26. Lebel MH, Gauthier M, Lacroix J et al (1989) Дыхательная недостаточность
и ИВЛ при тяжелом бронхиолите.Arch Dis Child
64: 1431–1437
122 Pediatr Radiol (2009) 39: 117–123
| |
Добавка витамина А после неонатальной пневмонии Streptococcus pneumoniae подавляет прогрессирование экспериментальной астмы путем изменения субпопуляций CD4 + Т-клеток
Chawes, B.L. Низкая активность заболевания в раннем возрасте предшествует детской астме и аллергии. Дан. Med. Дж. 63 (2016).
Дан. Med. Дж. 63 (2016).
Piippo-Savolainen, E., Ремес, С., Каннисто, С., Корхонен, К. и Корппи, М. Ранние предикторы астмы у взрослых и нарушений функции легких у младенцев, госпитализированных по поводу бронхиолита: проспективное наблюдение в течение 18–20 лет. Allergy Asthma Proc. 27 , 341–349 (2006).
Артикул Google ученый
Sears, M. R. и др. . Лонгитюдное популяционное когортное исследование детской астмы с последующим переходом к взрослой жизни. N. Engl. J. Med. 349 , 1414–1422 (2003).
Артикул CAS Google ученый
.jpg)
фон М.Е. Педиатрическое происхождение заболеваний легких у взрослых. Грудь 56 , 153–157 (2001).
Артикул Google ученый
Лодж, К. Дж. И Дхармадж, С. С. Грудное вскармливание и перинатальное воздействие, а также риск астмы и аллергии. Curr. Мнение. Allergy Clin. Иммунол. 16 , 231–236 (2016).
Артикул CAS Google ученый
Бисгаард, Х. и др. . Детская астма после бактериальной колонизации дыхательных путей у новорожденных. N. Engl. J. Med. 357 , 1487–1495 (2007).
Артикул CAS Google ученый
Виссинг, Н.Х., Чос, Б. Л. и Бисгаард, Х. Повышенный риск пневмонии и бронхиолита после бактериальной колонизации дыхательных путей у новорожденных. Am. J. Respir. Крит. Care Med. 188 , 1246–1252 (2013).
Артикул Google ученый
Ян Б. и др. . Инфекция неонатального Streptococcus pneumoniae может усугубить аллергическое заболевание дыхательных путей у взрослых, связанное с IL-17A. PLoS One 10 , e0123010 (2015).
Артикул CAS PubMed PubMed Central Google ученый
Рестори, К. Х., МакДэниел, К. Л., Рэй, А. Е., Канторна, М. Т. и Росс, А. С. Пневмония, вызванная Streptococcus pneumoniae, и инфекция кишечника, вызванная Citrobacter rodentium, по-разному изменяют концентрации витамина А в легких и печени мышей. J. Nutr. 144 , 392–398 (2014).
J. Nutr. 144 , 392–398 (2014).
Артикул CAS PubMed PubMed Central Google ученый
Пневмококковая конъюгированная вакцина для детской иммунизации — позиционный документ ВОЗ. Wkly Epidemiol Rec 82 , 93–104 (2007).
Зоммер А. Переход от науки к программам общественного здравоохранения: уроки витамина А. Am. J. Clin. Nutr. 68 , 513S – 516S (1998).
Артикул CAS Google ученый
Соммер, А. Рахматулла, Л. Андервуд, Б. и др. .Возможные меры по профилактике детской пневмонии в развивающихся странах: метаанализ данных полевых испытаний для оценки воздействия добавок витамина А на заболеваемость и смертность от пневмонии. Рабочая группа по витамину А и пневмонии. Bull World Health Organ 73 , 609–619 (1995).
Рабочая группа по витамину А и пневмонии. Bull World Health Organ 73 , 609–619 (1995).
Рейес, Х. и др. . Частота и детерминанты дефицита витамина А у детей в возрасте до 5 лет с пневмонией. Arch.Med. Res. 33 , 180–185 (2002).
Артикул ОБЪЯВЛЕНИЯ Google ученый
Awasthi, S. et al. . Добавка витамина А с ретинолом каждые 6 месяцев для 1 миллиона детей дошкольного возраста на севере Индии: DEVTA, кластерное рандомизированное исследование. Ланцет 381 , 1469–1477 (2013).
Артикул CAS PubMed PubMed Central Google ученый
Из Центров по контролю и профилактике заболеваний. Дефицит витамина А у детей — Федеративные Штаты Микронезии, 2000. 286, 667 (2001).
Юлия В., Масия Л. и Домбрович Д. Влияние диеты на астму и аллергические заболевания. Нат. Rev. Immunol. 15 , 308–322 (2015).
Артикул CAS Google ученый
Нурматов У., Деверо Г. и Шейх А.Питательные вещества и продукты питания для первичной профилактики астмы и аллергии: систематический обзор и метаанализ. J. Allergy Clin. Иммунол. 127 (724–733), e1–30 (2011).
Google ученый
Луо, З. Х. и др. . Дефицит витамина А и хрипы. World J. Pediatr. 6 , 81–84 (2010).
Артикул CAS Google ученый
Вос, Т. и др. . Годы, прожитые с инвалидностью (YLD), из-за 1160 последствий 289 заболеваний и травм 1990–2010: систематический анализ для Глобального исследования бремени болезней 2010. Lancet 380 , 2163–2196 (2012).
Артикул PubMed PubMed Central Google ученый
Cabieses, B., Uphoff, E., Pinart, M., Antó, JM & Wright, J. Систематический обзор развития астмы и аллергических заболеваний в связи с международной иммиграцией: ведущая роль среда подтвердила. PLoS One 9 , e105347 (2014).
Артикул ОБЪЯВЛЕНИЯ CAS PubMed PubMed Central Google ученый
Дюшарм, Ф. М., Цзе, С. М. и Чаухан, Б. Диагностика, лечение и прогноз хрипов дошкольного возраста. Ланцет 383 , 1593–1604 (2014).
Артикул Google ученый
Кусель, М.М. и др. . Респираторные вирусные инфекции в раннем возрасте, атопическая сенсибилизация и риск последующего развития стойкой астмы. J. Allergy Clin. Иммунол. 119 , 1105–1110 (2007).
Артикул Google ученый
Webley, W. C. & Hahn, D. L. Инфекционно-опосредованная астма: этиология, механизмы и варианты лечения, с акцентом на Chlamydia pneumoniae и макролиды. Респир. Res. 18 , 98 (2017).
Артикул CAS PubMed PubMed Central Google ученый
Аль-Гарави, А. и др. . Грипп A способствует сенсибилизации к клещу домашней пыли у мышей, что приводит к фенотипу астмы во взрослом возрасте. Mucosal Immunol. 4 , 682–694 (2011).
Артикул CAS Google ученый
Росас-Салазар, К. и др. . Микробиом носоглотки при респираторно-синцитиальном вирусе напоминает профиль, связанный с повышенным риском детской астмы. Am. J. Respir. Крит. Care Med. 193 , 1180–1183 (2016).
Артикул CAS PubMed PubMed Central Google ученый
Бисгаард Х. и др. . Связь бактерий и вирусов с эпизодами свистящего дыхания у детей раннего возраста: проспективное когортное исследование при рождении. BMJ 341 , c4978 (2010).
Артикул PubMed PubMed Central Google ученый
Аннагюр А., Кендирли С. Г., Йилмаз М., Алтинтас Д. У. и Инал А. Есть ли какая-либо связь между астмой и приступом астмы у детей и атипичными бактериальными инфекциями; Chlamydia pneumoniae, Mycoplasma pneumoniae и Helicobacter pylori. J. Trop. Педиатр. 53 , 313–318 (2007).
Артикул Google ученый
Reibman, J. et al. . Астма обратно пропорциональна статусу Helicobacter pylori у городского населения. PLoS One 3 , e4060 (2008 г.).
Артикул ОБЪЯВЛЕНИЯ CAS PubMed PubMed Central Google ученый
Essilfie, A. T. et al. . Инфекция, вызванная Haemophilus influenzae, вызывает опосредованное IL-17 нейтрофильное аллергическое заболевание дыхательных путей. PLoS Pathog. 7 , e1002244 (2011).
Артикул CAS PubMed PubMed Central Google ученый
Kloepfer, K. M. et al. . Обнаружение патогенных бактерий при риновирусной инфекции связано с усилением респираторных симптомов и обострениями астмы. J. Allergy Clin. Иммунол. 133 (1301–1307), 1307.e1–3 (2014).
Google ученый
Стивенсен, С. Б. Витамин А, инфекции и иммунная функция. Annu. Rev. Nutr. 21 , 167–192 (2001).
Артикул CAS Google ученый
Веласкес-Мелендес, Г., Окани, Э. Т., Киертсман, Б. и Ронкада, М. Дж. Статус витамина А у детей с пневмонией. Eur. J. Clin. Nutr. 49 , 379–384 (1995).
CAS Google ученый
Jiang, Y. L. & Peng, D. H. Уровень витамина А в сыворотке у детей с пневмонией в возрасте до 3 лет. Чжунго Данг Дай Эр Кэ За Чжи 18 , 980–983 (2016).
Google ученый
Розалес, Ф.Дж., Риттер, С.Дж., Золфагари, Р., Смит, Дж. Э. и Росс, А.С. Влияние острого воспаления на ретинол плазмы, ретинол-связывающий белок и его мРНК в печени и почках витамина А -достаточно крыс. J. Lipid Res. 37 , 962–971 (1996).
CAS Google ученый
Райс, А. Л. и др. . Добавка материнского витамина А или бета-каротина кормящим женщинам из Бангладеш приносит пользу матерям и младенцам, но не предотвращает субклиническую недостаточность. J. Nutr. 129 , 356–365 (1999).
Артикул CAS PubMed PubMed Central Google ученый
Al, S.A. M. Уровни витамина А и бета-каротина в сыворотке крови у детей с астмой. J. Asthma 46 , 699–702 (2009).
Артикул CAS Google ученый
Арора П., Кумар В. и Батра С. Статус витамина А у детей с астмой. Pediatr. Allergy Immunol. 13 , 223–226 (2002).
Артикул PubMed PubMed Central Google ученый
Григер, Дж. А., Вуд, Л. Г. и Клифтон, В. Л. Улучшение астмы во время беременности с помощью диетических антиоксидантов: текущие данные. Питательные вещества 5 , 3212–3234 (2013).
Артикул CAS PubMed PubMed Central Google ученый
Coombes, J. L. et al. . Функционально специализированная популяция CD103 + DC слизистой оболочки индуцирует Foxp3 + регуляторные Т-клетки посредством TGF-бета и механизма, зависимого от ретиноевой кислоты. J. Exp. Med. 204 , 1757–1764 (2007).
Артикул CAS PubMed PubMed Central Google ученый
Yokota, A. et al. . GM-CSF и IL-4 синергетически запускают дендритные клетки для приобретения способности продуцировать ретиноевую кислоту. Внутр. Иммунол. 21 , 361–377 (2009).
Артикул CAS PubMed PubMed Central Google ученый
Накамото, А. и др. . Дефицит витамина А ухудшает индукцию пероральной толерантности у мышей. J. Nutr. Sci. Витаминол. 61 , 147–153 (2015).
Артикул CAS Google ученый
Браун, К. С. и др. . Ретиноевая кислота необходима для стабильности клонов клеток Th2 и предотвращает переход к программе клеток Th27. Immun. 42 , 499–511 (2015).
Артикул CAS Google ученый
Cui, W. и др. . Дефицит витамина А способствует воспалению за счет индукции цитокинов типа 2 на экспериментальной модели мыши с астмой, индуцированной овальбумином. Inflamm. 39 , 1798–1804 (2016).
Артикул CAS Google ученый
Муцида, Д. и др. . Реципрокная дифференцировка Th27 и регуляторных Т-клеток, опосредованная ретиноевой кислотой. Sci. 317 , 256–260 (2007).
Артикул ОБЪЯВЛЕНИЯ CAS Google ученый
Han, Y. Y. et al. . Диета и астма: доноры витаминов и метильных групп. Ланцет Респир. Med. 1 , 813–822 (2013).
Артикул CAS PubMed PubMed Central Google ученый
Thorburn, A. N., Macia, L. & Mackay, C. R. Диета, метаболиты и воспалительные заболевания «западного образа жизни». Immun. 40 , 833–842 (2014).
Артикул CAS Google ученый
Пайва, С. А. и Рассел, Р. М. Бета-каротин и другие каротиноиды в качестве антиоксидантов. J. Am. Coll. Nutr. 18 , 426–433 (1999).
Артикул CAS Google ученый
Мора, Дж. Р., Ивата, М. и фон, А. У. Х. Влияние витаминов на иммунную систему: витамины A и D занимают центральное место. Нат. Rev. Immunol. 8 , 685–698 (2008).
Артикул CAS PubMed PubMed Central Google ученый
Benson, MJ, Pino-Lagos, K., Rosemblatt, M. & Noelle, RJ All-trans-retinoic acid опосредует усиленный рост T reg-клеток, дифференцировку и возвращение в кишечник в условиях высоких уровней co -стимуляция. J. Exp. Med. 204 , 1765–1774 (2007).
Артикул CAS PubMed PubMed Central Google ученый
Сан, К. М. и др. . Дендритные клетки собственной пластинки тонкой кишки способствуют de novo генерации клеток Foxp3 T reg с помощью ретиноевой кислоты. J. Exp. Med. 204 , 1775–1785 (2007).
Артикул CAS PubMed PubMed Central Google ученый
Niu, C. et al. . Витамин А поддерживает эпителий дыхательных путей на мышиной модели астмы, подавляя вызванную глюкокортикоидами лейциновую молнию. Clin. Exp. Аллергия 46 , 848–860 (2016).
Артикул CAS Google ученый
Checkley, W. et al. . Добавки с витамином А в раннем возрасте и последующий риск астмы. Eur. Респир. J. 38 , 1310–1319 (2011).
Артикул CAS Google ученый
Милнер, Дж. Д., Стейн, Д.M., McCarter, R. & Moon, R.Y. Прием поливитаминных добавок в раннем возрасте связан с повышенным риском пищевой аллергии и астмы. Педиатрия 114 , 27–32 (2004).
Артикул Google ученый
Май, X. М., Лангхаммер, А., Чен, Ю. и Камарго, С. А. Потребление рыбьего жира и заболеваемость астмой у взрослых норвежцев — исследование HUNT. Грудь 68 , 25–30 (2013).
Артикул Google ученый
Mawson, A.R. Может ли бронхиальная астма быть эндогенным легочным проявлением ретиноидной интоксикации. Фронт. Biosci. 6 , D973–985 (2001).
CAS Google ученый
Торн, П. С., Хок, К., Калишевски, С. Д. и Гвини, П. Д. Неинвазивный анализ отека уха у мышей. I. Уточнения для определения слабых контактных сенсибилизаторов. Фундамент. Appl. Toxicol. 17 , 790–806 (1991).
Артикул CAS Google ученый
Ross, AC, Li, NQ & Wu, L. Компоненты VARA, комбинации питательных веществ и метаболитов витамина А и ретиноевой кислоты, эффективно действуют вместе и по отдельности, увеличивая количество ретиниловых эфиров в легких новорожденных крыс. . J. Nutr. 136 , 2803–2807 (2006).
Артикул CAS PubMed PubMed Central Google ученый
Джеймс, М. Л., Росс, А. С., Балджер, А., Филипс, Дж. Б. и Амбалаванан, Н. Витамин А и ретиноевая кислота действуют синергетически, повышая содержание ретиниловых эфиров в легких во время нормоксии и уменьшая гипероксическое повреждение легких у новорожденных мышей. Pediatr. Res. 67 , 591–597 (2010).
Артикул CAS PubMed PubMed Central Google ученый
Deng, Y. et al. . Противоастматический эффект вакцинации БЦЖ новорожденных не зависит от баланса Th27 / Th2, но IL-17 / IFN-γ на модели астмы у мышей BALB / c. J. Clin. Иммунол. 31 , 419–429 (2011).
Артикул CAS Google ученый
Zang, N. et al. . Опосредованное ресвератролом уменьшение гамма-интерферона предотвращает воспаление дыхательных путей и гиперреактивность дыхательных путей у мышей с иммунодефицитом, инфицированных респираторно-синцитиальным вирусом. J. Virol. 85 , 13061–13068 (2011).
Артикул CAS PubMed PubMed Central Google ученый
Zhang, L. и др. . Иммунизация младенцев 7-валентной пневмококковой конъюгированной вакциной изменяет субпопуляции CD4 (+) Т-лимфоцитов молодого взрослого на модели аллергического заболевания дыхательных путей на мышах. Вакцина 32 , 2079–2085 (2014).
Артикул CAS Google ученый
Myou, S. et al. . Блокада воспаления и гиперреактивности дыхательных путей у иммуносенсибилизированных мышей доминантно-отрицательной фосфоинозитидной 3-киназой-ТАТ. J. Exp. Med. 198 , 1573–1582 (2003).
Артикул CAS PubMed PubMed Central Google ученый
Коронавирусы человека HCoV-NL63 и HCoV-HKU1 у госпитализированных детей с острыми респираторными инфекциями в Пекине, Китай
Коронавирусы человека (HCoV) HCoV-NL63 и HCoV-HKU1 — это два недавно обнаруженных коронавируса, которые широко циркулируют. острые респираторные инфекции (ОРЗ).Мы обнаружили HCoV-NL63 и HCoV-HKU1 в образцах, собранных с мая 2008 г. по март 2010 г. у пациентов с ОРИ в возрасте <7,75 лет, посещающих Пекинскую детскую больницу. Тридцать два (8,4%) и 57 (14,9%) из 382 образцов дали положительный результат на HCoV-NL63 и HCoV-HKU1, соответственно, с помощью ОТ-ПЦР в реальном времени. Использование набора Luminex xTAG RVP Fast показало, что коинфекция респираторно-синцитиальным вирусом и вирусом парагриппа 3 была распространена среди пациентов, инфицированных любым типом вируса. У пациентов, инфицированных HCoV-HKU1, преобладающими клиническими симптомами были кашель, лихорадка и мокрота.У пациентов, инфицированных HCoV-NL63, наблюдались кашель, лихорадка и ринорея. Филогенетические исследования показали, что ген нуклеопротеина HCoV-HKU1 был относительно консервативным по сравнению с эталонными последовательностями NCBI, тогда как ген 1ab HCoV-NL63 показал большую вариабельность.
1. Введение
До вспышки тяжелого острого респираторного синдрома, вызванного коронавирусом SARS в 2003 году, коронавирусы человека (HCoV) не считались вредными респираторными патогенами. Вспышка SARS возобновила интерес к этому семейству вирусов и привела к идентификации двух дополнительных вирусов гепатита C, HCoV-NL63 и HCoV-HKU1.HCoV-NL63, член группы I коронавирусов, был впервые обнаружен у ребенка с бронхиолитом в Нидерландах в 2004 году [1]. HCoV-HKU1, вирус группы II, был обнаружен у взрослого человека с хроническим заболеванием легких в Гонконге в 2005 г. [2]. В настоящее время признано, что оба этих вируса циркулируют во всем мире и связаны с инфекциями дыхательных путей человека. В Китае несколько групп продемонстрировали существование HCoV-NL63 и HCoV-HKU1 в качестве потенциальных респираторных патогенов у младенцев и пожилых людей [3–5].Однако более точные данные об их эпидемиологии и генетических характеристиках в континентальном Китае отсутствуют. В этом исследовании мы проверили наличие HCoV-NL63 и HCoV-HKU1 у детей с острой респираторной инфекцией, госпитализированных в Пекинскую детскую больницу, чтобы лучше понять сезонность, эпидемиологию и генетическое разнообразие этих вирусов в город с населением более 22 миллионов человек.
2. Материалы и методы
2.1. Клинические образцы
Всего было собрано 382 назофарингеальных аспирата (НПА) госпитализированных детей с диагнозом пневмонит или бронхопневмония и температурой тела выше 38 ° C.Дети были госпитализированы в Пекинскую детскую больницу в период с мая 2008 г. по март 2010 г. (23 месяца). Родители всех детей, участвовавших в исследовании, дали информированное согласие на сбор образцов и тестирование. Средний возраст детей составлял 1,1 года (от 1 месяца до 7,75 лет). NPA собирали в транспортную среду для вирусов и хранили при -70 ° C перед тестированием.
2.2. Экстракция РНК и синтез кДНК
Нуклеиновую кислоту экстрагировали с использованием наборов QIAamp MinElute Virus Spin (Qiagen, Mississauga, Ontario, Canada) согласно инструкциям производителя.кДНК синтезировали из 10 мкл л РНК-элюата с использованием случайных гексамерных праймеров (TaKaRa, Далянь, Китай) и обратной транскриптазы SuperScript II (Invitrogen Carlsbad, Калифорния, США).
2.3. Анализы ОТ-ПЦР в реальном времени
Два анализа ОТ-ПЦР в реальном времени, нацеленные на консервативные области генов N и 1ab обоих вирусов, были разработаны и использовались параллельно. Последовательности праймера и зонда для HCoV-NL63 были следующими:
NL63-N прямой праймер 5′-AGGACCTTAAATTCAGACAACGTTCT-3 ‘; обратный праймер 5’-GATTACGTTTGCGATTACCAAGACT-3 ‘[6] ; Зонд TaqMan 5′-FAM-TAACAGTTTTAGCACCTTCCTTAGCAACCCAAACA-TAMRA-3 ‘.Прямой праймер NL63-1ab 5’-TGTTGTAGTAGGTGGTTGTGTAACATCT-3 ‘; обратный праймер 5’-AATTTTTGTGCACCAGTATCAAGTTT-3 ‘; Зонд TaqMan 5’-FAM-CAATTGTTAGTGAGAAAATTTCTGTTATGGA-TAMRA -3 ‘[7].
Праймеры и зонды для HCoV-HKU1 были следующими:
HKU-1-N прямой праймер 5′-AGTTCCCATTGCTTTCGGAGTA-3 ‘; обратный праймер 5’-CCGGCTGTGTCTATACCAATATCC-3 ‘; Зонд TaqMan-MGB, 5’-FAM-CCCCTTCTGAAGCAA-MGB-3 ‘[8]; Прямой праймер HKU-1-1ab 5’- CCATTACAAGCCATAAGAGAACAAAC-3 ‘; обратный праймер 5’-TATGTGTGGCGGTTGCTATTATGT-3 ‘; Зонд TaqMan 5’-FAM-TTGCATCACCACTGCTAGTACCACCAGG-TAMRA-3 ‘[9].
Для оценки чувствительности анализов ОТ-ПЦР в реальном времени ампликоны генов N и 1ab клонировали в векторы pET-9a (QIAGEN) и pGEM-T Easy (Promega Corporation, США), соответственно, за которыми следовали транскрипция in vitro с использованием крупномасштабной системы производства РНК T7 RiboMAX Express (Promega). Стандартные кривые для анализов генов N и 1ab были построены с использованием серийных логарифмических разведений (от 10 1 до 10 911 10 7 копий) транскрибированных фрагментов РНК.Нижний предел обнаружения каждого анализа ОТ ПЦР в реальном времени составлял 100 копий / 20 мкл л, с коэффициентами вариабельности внутри анализа (CV) от 0,45 до 1,02% (= 3) и CV между анализами от 0,68 до 2,24. %.
2.4. Обнаружение HCoV-NL63 и HCoV-HKU1 в клинических образцах
Образцы были протестированы на наличие HCoV-NL63 или HCoV-HKU1 с помощью ОТ-ПЦР в реальном времени с использованием набора TaqMan RNA-to-CT 1-Step (Applied Biosystems, США) и машину ABI Prism 7000 TaqMan (Applied Biosystems, США).10 4 копий транскриптов гена N и 1ab использовали в качестве положительного контроля в каждом опыте. Условия амплификации: 48 ° C в течение 15 минут, затем 40 циклов при 94 ° C в течение 15 секунд и 60 ° C в течение 15 секунд. Для каждого вируса, когда полученное значение C T было меньше 38, образец считался положительным. Когда значение C T было относительно высоким (38 ≤ C T < 40), образец повторно тестировали дважды и считали положительным, если значение C T любого повторного теста было меньше 40.
2,5. Обнаружение общих респираторных вирусов
Все образцы, положительные по HCoV-NL63 и HCoV-HKU1, были протестированы на другие респираторные вирусы с использованием быстрого теста luminex xTAG RVP (Luminex Trading, Шанхай, Китай) на приборе Biorad Bio-Plex 200 (BioRad, Hercules). , Калифорния, США) подвесная система.
2.6. Филогенетический анализ
Пятнадцать последовательностей (251 нуклеотид (нуклеотид)) гена полипротеина репликазы 1ab HCoV-NL63 и пять последовательностей (951 нуклеотид) гена нуклеопротеина (N) HCoV-HKU1 были получены из положительных образцов с использованием стандартной ПЦР и секвенирования. подвергнут филогенетическому анализу.Последовательности Genbank с наивысшей идентичностью (наименьшее ожидаемое значение (E)) при поиске по методу blastn были использованы в качестве ссылок для этого анализа вместе с последовательностями штамма общего типа HCoV. Последовательности Nt AY597011.2, AY56787.2 и DQ415910.1 использовали в качестве эталонов для анализа HCoV-NL63. Последовательности AY567487.2, AY518894.1, DQ445911.1, GU068568.1, DQ846901.1 и EF081296.1 были применены в анализе HCoV-HKU1. AF304460, представляющий последовательность HCoV-229E, также был включен. Множественное выравнивание последовательностей выполняли с помощью clustalW.Филогенетические деревья были построены с использованием Neighbor-Joining. Значения начальной загрузки были рассчитаны на 1000 повторов выровненных наборов данных.
3. Результаты
3.1. Заболеваемость и клинические симптомы, связанные с инфекциями HCoV-NL63 и HCoV-HKU1 у госпитализированных детей
Из 382 протестированных образцов 32 (8,4%) были положительными на HCoV-NL63 и 57 (14,9%) были положительными на HCoV-HKU1. Данные тестирования и клинические данные пациентов с этими инфекциями приведены в таблице 1.Большинство пациентов, инфицированных HCoV-NL63 (65,6%) или HCoV-HKU1 (77,2%), были младше 1 года на момент исследования. Оба вируса чаще выявлялись у мужчин (таблица 1). Четырьмя наиболее частыми клиническими симптомами обоих вирусов были кашель, лихорадка, ринорея и мокрота. Однако мокрота была более частым симптомом у пациентов, инфицированных HCoV-HKU1 (54,4 против 25,0%). Допущенный диагноз у более чем 80% детей — пневмония и бронхопневмония, независимо от того, был ли инфекционный вирус HCoV-NL63 или HCoV-HKU1.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
3,2. Эпидемиология инфекций HCoV-NL63 и HCoV-HKU1
Сезонные распределения HCoV-NL63 и HCoV-HKU1 с мая 2008 г. по конец марта 2010 г. респираторных инфекций снижалось (Рисунок 1).Пик заболеваемости обоими вирусами пришелся на лето 2009 года, но не на 2008 год. Увеличение числа случаев заражения HCoV-NL63 также было обнаружено осенью и зимой 2009 года, в отличие от 2008 года, когда зимой было выявлено лишь небольшое количество случаев. Аналогичное распределение произошло для HCoV-HKU1.
3.3. Коинфекция HCoV-NL63 и HCoV-HKU1 с другими респираторными вирусами
Тестирование HCoV-положительных образцов с помощью системы Luminex xTAG RVP Fast показало, что многие из них были коинфицированы другими распространенными респираторными вирусами (Таблица 2), в частности респираторно-синцитиальным вирусом (RSV ) и вируса парагриппа 3 типа.Также были обнаружены коинфекции с участием нескольких HCoV (таблица 2). Только 13 из 57 (14,0%) HCoV-HKU1-положительных пациентов и 8 из 32 (25%) HCoV-NL63-положительных пациентов дали отрицательный результат на другие респираторные вирусы.

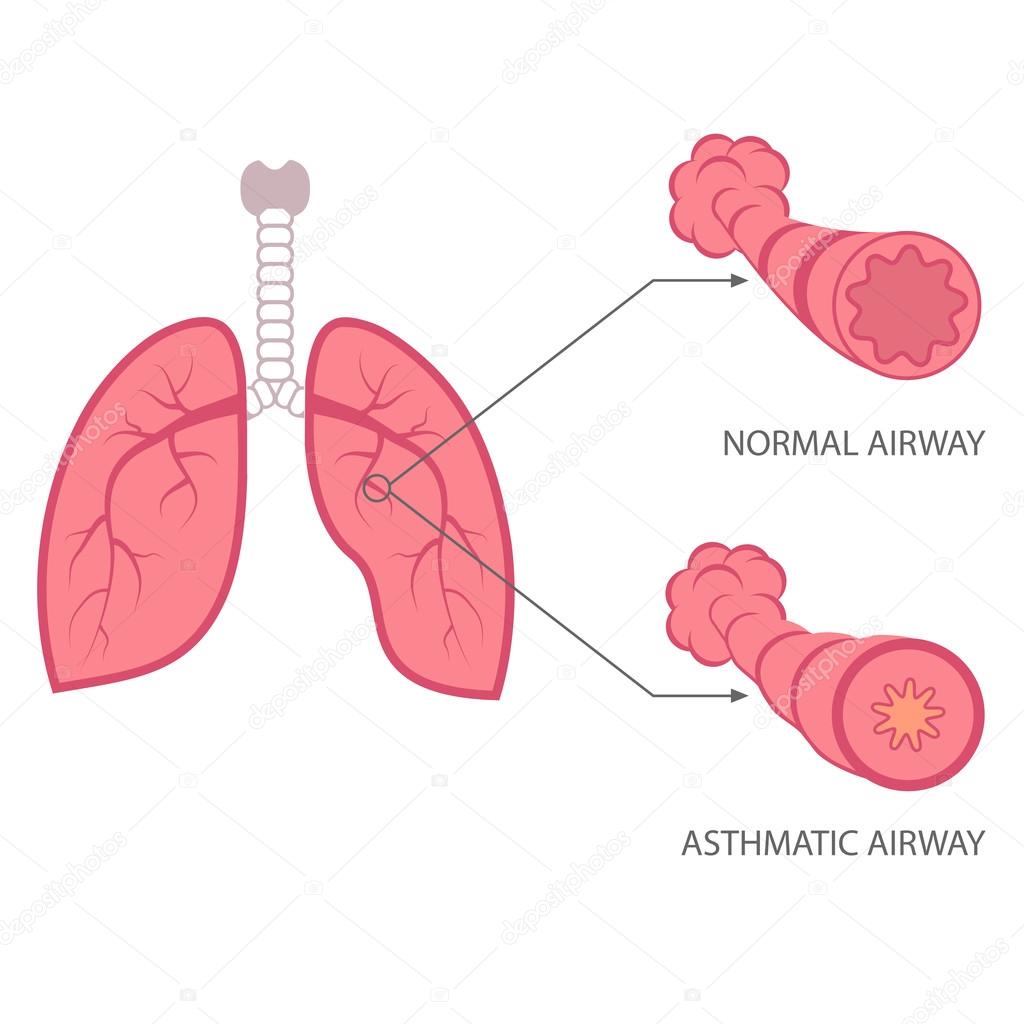

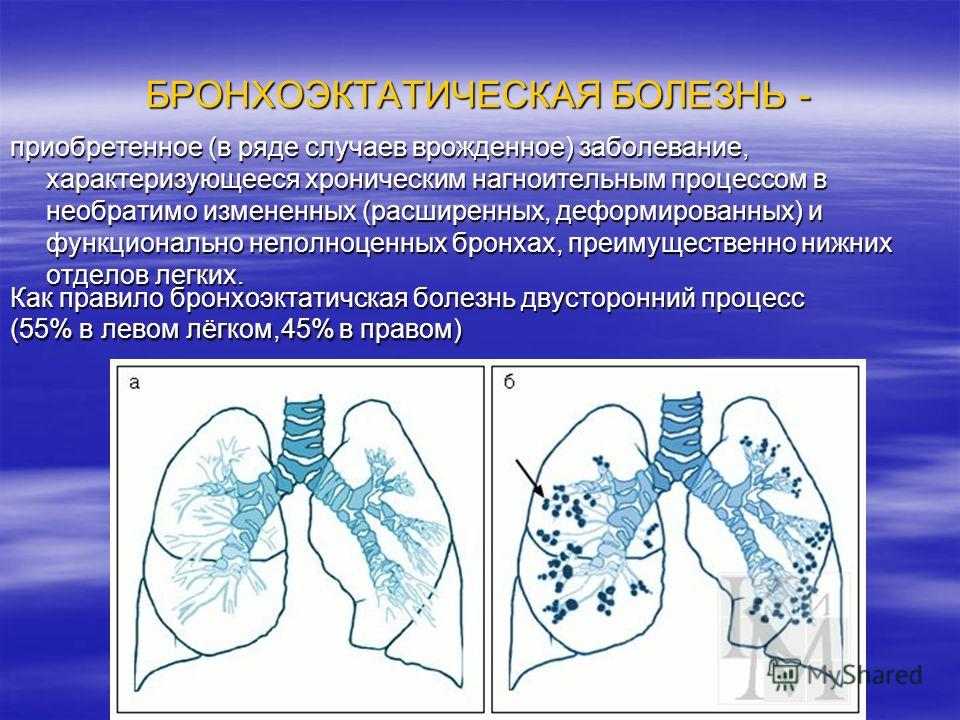
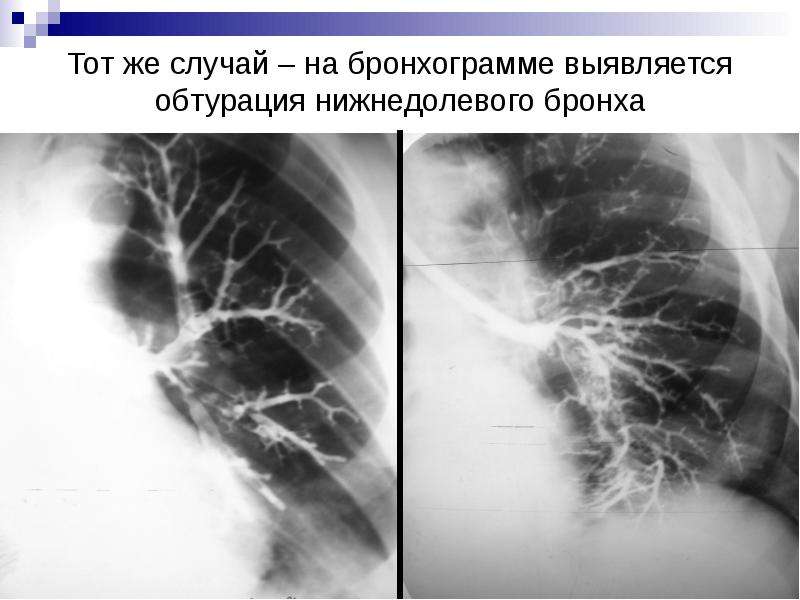
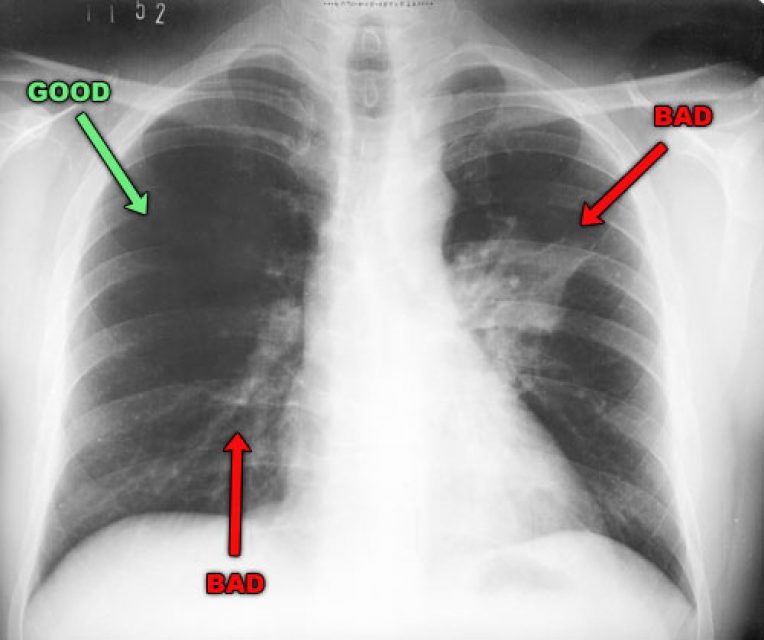 ) журнала Indian Pediatrics , состоящий из
четыре оригинальные статьи, истории болезни и обзор современной литературы.
Среди них мы решили рассмотреть статью под названием « Mycoplasma
pneumoniae у индийского ребенка.«В то время м.
pneumoniae была недавно открыта, и она произвела много
представляет интерес как возможная причина пневмонии. Впоследствии многое было
узнали об этом организме, и в этой статье мы рассмотрим прирост
представление об этом организме за последние 50 лет.
) журнала Indian Pediatrics , состоящий из
четыре оригинальные статьи, истории болезни и обзор современной литературы.
Среди них мы решили рассмотреть статью под названием « Mycoplasma
pneumoniae у индийского ребенка.«В то время м.
pneumoniae была недавно открыта, и она произвела много
представляет интерес как возможная причина пневмонии. Впоследствии многое было
узнали об этом организме, и в этой статье мы рассмотрим прирост
представление об этом организме за последние 50 лет.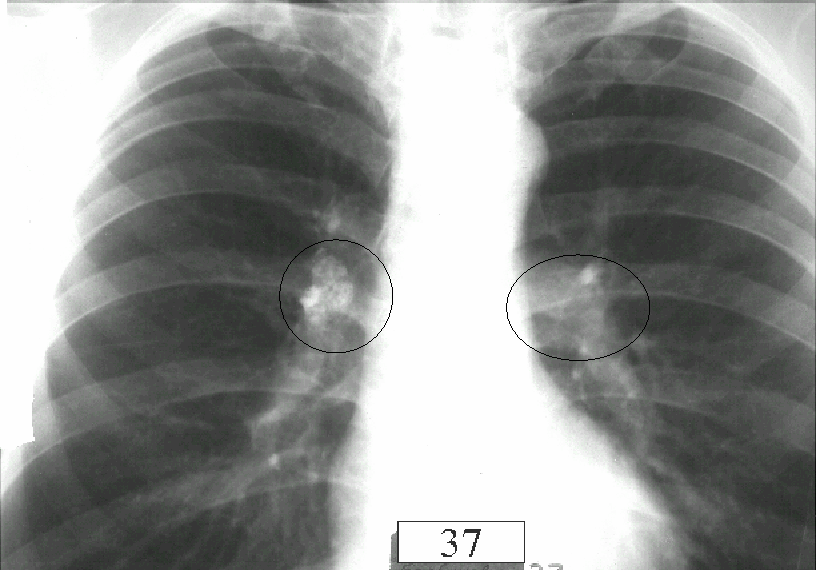 Исследования этого ребенка были поддержаны
Грант на исследования службы общественного здравоохранения США от National
Институт Здоровья. Сообщенный случай произошел с 23-месячной бенгальской девушкой,
одиннадцатый по порядку рождения! Она представила семидневную историю
лихорадка, насморк и прогрессирующий кашель, который был сильным ночью с некоторыми
случаи рвоты после кашля.В прошлом была история повторяющихся
инфекции верхних дыхательных путей. Ей сделали прививку только против мелких
оспа. При обследовании выявлено повышение температуры тела, тахикардия и тахипноэ. Ребенок
имели шейную и подмышечную лимфаденопатию, гиперемию слизистой оболочки носа и
миндалины и барабанная перепонка. Грудь была гиперинфлированной;
правая нижняя часть грудной клетки была тупой при перкуссии с затрудненным дыханием
звук. Изредка слышны хрипы на вдохе и выдохе.
пораженная зона.Кардиологическое обследование было нормальным; печень пальпируется 5
см и селезенка на 2 см ниже реберного края. Комод Х -луч
продемонстрировал сливное помутнение правой средней доли
соответствует альвеолярному пневмониту и перибронхиту справа
верхняя и нижняя доли.
Исследования этого ребенка были поддержаны
Грант на исследования службы общественного здравоохранения США от National
Институт Здоровья. Сообщенный случай произошел с 23-месячной бенгальской девушкой,
одиннадцатый по порядку рождения! Она представила семидневную историю
лихорадка, насморк и прогрессирующий кашель, который был сильным ночью с некоторыми
случаи рвоты после кашля.В прошлом была история повторяющихся
инфекции верхних дыхательных путей. Ей сделали прививку только против мелких
оспа. При обследовании выявлено повышение температуры тела, тахикардия и тахипноэ. Ребенок
имели шейную и подмышечную лимфаденопатию, гиперемию слизистой оболочки носа и
миндалины и барабанная перепонка. Грудь была гиперинфлированной;
правая нижняя часть грудной клетки была тупой при перкуссии с затрудненным дыханием
звук. Изредка слышны хрипы на вдохе и выдохе.
пораженная зона.Кардиологическое обследование было нормальным; печень пальпируется 5
см и селезенка на 2 см ниже реберного края. Комод Х -луч
продемонстрировал сливное помутнение правой средней доли
соответствует альвеолярному пневмониту и перибронхиту справа
верхняя и нижняя доли. В анализах крови выявлен нейтрофильный лейкоцитоз.
Туберкулиновая кожная проба была отрицательной, хлорид пота был нормальным.
В анализах крови выявлен нейтрофильный лейкоцитоз.
Туберкулиновая кожная проба была отрицательной, хлорид пота был нормальным. pneumoniae . Выделение M. pneumoniae из
аспират из горла и трахеи этого ребенка с пневмонией, у которого
обширные бактериальные и вирусные исследования не внесли вклад
указали этиологическую роль M.пневмония . Ребенок был
обработанный деметил-хлортетрациклином. Повтор Х -луч 3 мес.
позже были обнаружены стойкие инфильтраты средней доли, хотя ребенок был
бессимптомный.
pneumoniae . Выделение M. pneumoniae из
аспират из горла и трахеи этого ребенка с пневмонией, у которого
обширные бактериальные и вирусные исследования не внесли вклад
указали этиологическую роль M.пневмония . Ребенок был
обработанный деметил-хлортетрациклином. Повтор Х -луч 3 мес.
позже были обнаружены стойкие инфильтраты средней доли, хотя ребенок был
бессимптомный.  когда Мармион и Гудберн [6] описали его морфологически похожим
в PPLO. В конце концов, в 1962 году Чанок и др. [2] описал Eaton
возбудителем стать микоплазмой после успешного культивирования в бесклеточном
средства массовой информации.Вскоре после этого он предложил название Mycoplasma pneumoniae .
поскольку организм, зараженный добровольцами, вызывал пневмонию.
Kingston, et al. [7] установлена терапевтическая эффективность
деметилтетрациклина для M. pneumoniae пневмонии.
когда Мармион и Гудберн [6] описали его морфологически похожим
в PPLO. В конце концов, в 1962 году Чанок и др. [2] описал Eaton
возбудителем стать микоплазмой после успешного культивирования в бесклеточном
средства массовой информации.Вскоре после этого он предложил название Mycoplasma pneumoniae .
поскольку организм, зараженный добровольцами, вызывал пневмонию.
Kingston, et al. [7] установлена терапевтическая эффективность
деметилтетрациклина для M. pneumoniae пневмонии. M. pneumoniae в настоящее время
известны как самые маленькие свободно живущие вездесущие организмы. В
патогенность у человека объясняется явлениями цитоадгезии
на слизистой оболочке респираторного эпителия, нарушение мукоцилиарного
очищение и выработка цитотоксина, называемого токсином CARDS, который
повреждает респираторные реснитчатые эпителиальные клетки.Кроме того,
инфекция M. pneumoniae индуцирует образование
провоспалительные медиаторы и цитокины, которые еще больше усугубляют
болезненный процесс. Способность микоплазмы усваиваться и воспроизводиться
в альвеолярных макрофагах может привести к хронизации инфекции и
устойчивость к антибиотикам [9]. Известны рецидивы.
M. pneumoniae в настоящее время
известны как самые маленькие свободно живущие вездесущие организмы. В
патогенность у человека объясняется явлениями цитоадгезии
на слизистой оболочке респираторного эпителия, нарушение мукоцилиарного
очищение и выработка цитотоксина, называемого токсином CARDS, который
повреждает респираторные реснитчатые эпителиальные клетки.Кроме того,
инфекция M. pneumoniae индуцирует образование
провоспалительные медиаторы и цитокины, которые еще больше усугубляют
болезненный процесс. Способность микоплазмы усваиваться и воспроизводиться
в альвеолярных макрофагах может привести к хронизации инфекции и
устойчивость к антибиотикам [9]. Известны рецидивы. Предполагается, что он вызывает астму
обострения [10], и может привести к снижению легочного клиренса и
гиперчувствительность дыхательных путей даже после борьбы с инфекцией.
Предполагается, что он вызывает астму
обострения [10], и может привести к снижению легочного клиренса и
гиперчувствительность дыхательных путей даже после борьбы с инфекцией. Специфический IgM
и IgA-ответы необходимо сочетать с прямым обнаружением патогенов для
установление причинно-следственной связи. Полимеразная цепная реакция (ПЦР) с использованием множества
последовательности гена M. pneumoniae в качестве праймеров является высокочувствительным
и специальный тест для обнаружения M. pneumoniae в различных образцах
такие как респираторные выделения, кровь, спинномозговая жидкость и моча, но не подтверждены
и стандартизация. В этом контексте следует отметить, что авторы
эта история болезни может поставить диагноз M.пневмония инфекция
50 лет назад!
Специфический IgM
и IgA-ответы необходимо сочетать с прямым обнаружением патогенов для
установление причинно-следственной связи. Полимеразная цепная реакция (ПЦР) с использованием множества
последовательности гена M. pneumoniae в качестве праймеров является высокочувствительным
и специальный тест для обнаружения M. pneumoniae в различных образцах
такие как респираторные выделения, кровь, спинномозговая жидкость и моча, но не подтверждены
и стандартизация. В этом контексте следует отметить, что авторы
эта история болезни может поставить диагноз M.пневмония инфекция
50 лет назад! Хьюз-младший, Синха Д.П. Mycoplasma pneumoniae
инфекция у индийского ребенка. Indian Pediatr. 1966; 3: 52-9.
Хьюз-младший, Синха Д.П. Mycoplasma pneumoniae
инфекция у индийского ребенка. Indian Pediatr. 1966; 3: 52-9.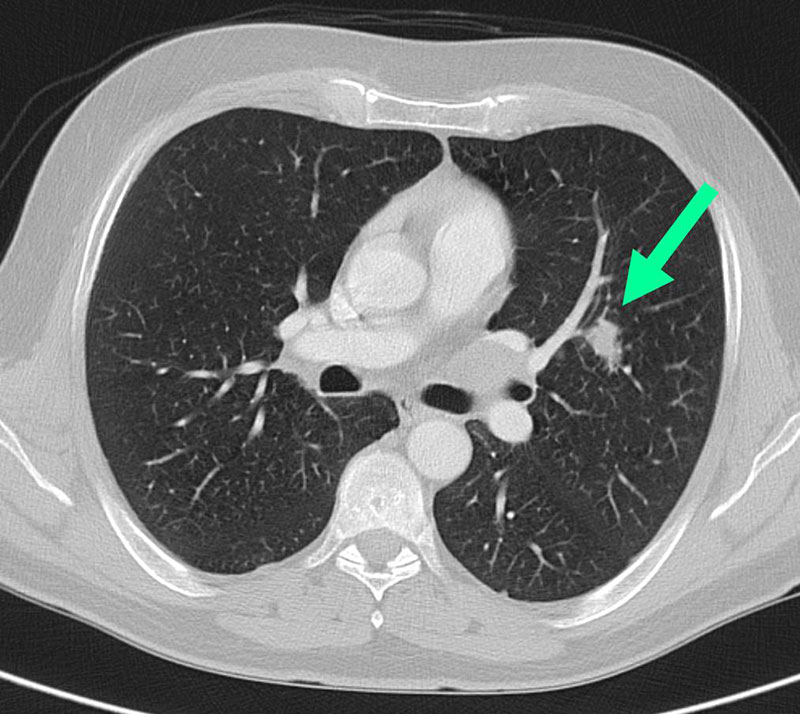 Д., Фокс Х.Н., и др. Возбудитель пневмонии Eaton.
JAMA.1961; 176: 118-23.
Д., Фокс Х.Н., и др. Возбудитель пневмонии Eaton.
JAMA.1961; 176: 118-23.